
- •1.Основные периоды детства (классификация по н.П. Гундобину).
- •2.Период новорождённости и его основная патология.
- •4. Оценка состояния ребенка при рождении.
- •5.Основные гнойно-септические заболевания новорожденных, тактика ведения.
- •6.Период грудного возраста и его основная патология.
- •8. Период младшего школьного возраста и его основная патология.
- •9.Период старшего школьного возраста и его основная патология.
- •10. Основные законы роста и развития в детском возрасте.
- •1) Спинальные сегментарные автоматизмы:
- •2) Оральные сегментарные автоматизмы:
- •3) Миелоэнцефальные позотонические рефлексы:
- •13. Морфофункциональные особенности и развитие центральной нервной системы у детей.
- •14. Основные этапы психомоторного развития детей на первом году.
- •15. Длина тела новорожденного и ее динамика на первом году жизни и в последующие годы.
- •0. Доношенный новорожденный:
- •3. Закон чередования направлений роста (штрац, 1903 г)
- •4. Закон половой специфичности роста
- •0. Внутриутробно:
- •1. 1Ого г. Жизни:
- •16. Масса тела новорожденного и ее динамика на первом году жизни и в последующие годы.
- •17. Анатомо-физиологические особенности кожи и её придатков у детей, клиническое значение в периоде новорожденности.
- •18. Физиологические изменения кожи в периоде новорожденности.
- •19. Анатомо-физиологические особенности подкожной жировой клетчатки у детей разного возраста, клиническое значение в грудном возрасте.
- •20. Анатомо-физиологические особенности периферических лимфатических узлов у детей и клиническое значение в различные периоды детства.
- •21. Анатомо-физиологические особенности костной системы у детей различного возраста.
- •22. Сроки прорезывания молочного и постоянного прикуса, специфические особенности и периоды молочного прикуса.
- •23. Сроки закрытия швов и родничков, семиотика изменений в грудном возрасте.
- •24. Анатомо-физиологические особенности мышечной системы у детей различного возраста, клиническое значение.
- •25. Анатомо-физиологические особенности носоглотки у детей различного возраста, клиническое значение.
- •26. Анатомо-физиологические особенности гортани и трахеи у детей различного возраста, клиническое значение.
- •27. Анатомо-физиологические особенности бронхов в различные периоды детства, механизмы бронхиальной обструкции. (Жидков)
- •28. Анатомо-физиологические особенности кольца Вальдейера-Пирогова у детей разного возраста, клиническое значение.
- •29. Анатомо-физиологические особенности легких в различные периоды детства, клиническое значение и возможная патология.
- •30. Виды кашля при различных заболеваниях у детей.
- •31. Внутриутробное формирование сердца, критические периоды пре и постнатально.
- •32.Анатомо-физиологические особенности сердца у новорожденного, особенности изменений в динамике роста и развития.
- •33.Особенности гемодинамики после рождения. Сроки закрытия экстра и интракардиальных шунтов после рождения.
- •34. Особенности аускультативной картины сердца у детей различного возраста
- •35. Причины и основные характеристики функциональных шумов в детском возрасте, дифференциальная диагностика с органическими шумами. Функциональные шумы - при отсутствии анатомических дефектов.
- •36. Семиотика жалоб и осмотра при заболеваниях сердечно-сосудистой системы у детей различного возраста, клиническое значение.
- •37. Анатомо-физиологические особенности полости рта у детей грудного возраста, физиологическое значение.
- •38. Анатомо-физиологические особенности пищевода и желудка у детей грудного возраста, физиологическое значение, наиболее частая патология.
- •40. Анатомо-физиологические и функциональные особенности тонкой кишки у детей в различные периоды детства, -физиологическое значение, наиболее частая патология.
- •41. Анатомо-физиологические особенности толстой кишки у детей различного возраста, клиническое значение.
- •42. Анатомо-физиологические особенности печени и желчевыводящих путей в различные периоды детства.
- •43. Анатомо-физиологические особенности поджелудочной железы на первом году и в последующие периоды детства.
- •44.Формирование микробиоты толстой кишки после рождения, особенности в зависимости от вида вскармливания.
- •45. Особенности периферической крови у новорожденных.
- •46. Особенности лейкограммы у детей первого года жизни и в последующие годы.
- •47. Особенности красной крови в периоде новорожденности и в последующие периоды детства.
- •3 Вида гемоглобина:
- •48. Семиотика железодефицитной анемии у детей.
- •49. Лимфаденопатия у детей различного возраста: критерии диагностики, причины развития.
- •50. Особенности системы гемостаза у новорожденных и в грудном возрасте.
- •51. Семиотика и диагностика основных типов геморрагического синдрома.
- •5. Ангиоматозный тип.
- •52. Семиотика заболеваний мочевыделительной системы у детей разного возраста по данным анамнеза и осмотра.
- •53. Анатомо-физиологические особенности почек у детей различного возраста, их клиническое значение.
- •54. Анатомо-физиологические особенности мочевыводящих путей у детей различного возраста, их клиническое значение.
- •55. Функциональные особенности почек в детском возрасте.
- •56. Гипертензионный синдром при заболеваниях почек у детей: патофизиология и клинические проявления.
- •57. Отечный синдром при патологии почек у детей: патофизиология, особенности проявлений, диагностика скрытых отеков.
- •58. Синдром нарушения мочевыделения: основные виды дизурических расстройств у детей.
- •60. Регуляция и сроки становления лактации, понятие лактационных кризов.
- •61. Срок прикладывания ребенка к груди, преимущества, противопоказания со стороны матери и ребенка.
- •62. Состав женского молока в зависимости от сроков лактации.
- •63. Понятие программирования питанием, эпигенетические свойства женского молока.
- •64. Преимущества естественного вскармливания для матери и ребенка.
- •1) Грудной ребенок:
- •2) Мать:
- •65. Противопоказания к естественному вскармливанию со стороны матери и ребенка.
- •66. Гипогалактия: классификация, критерии диагностики.
- •68. Искусственное вскармливание: правила проведения, расчет питания.
- •69. Смешанное вскармливание ребенка: показания, понятие докорма, правила введения, выбор заменителей грудного молока.
- •70. Прикормы: понятие, виды, правила введения
- •72. Основные принципы рационального питания детей
- •73.Правила формирования правильного пищевого поведения у детей различного возраста.
- •74. Основные типы нарушений аппетита и пищевого поведения
- •75. Половое развитие детей: сроки и последовательность появления вторичных половых признаков у мальчиков и девочек, стадии полового созревания по Таннеру.
- •76. Железодефицитная анемия у детей: стадии развития, этиология, клинические проявления, принципы лечения.
- •77. Гипо и апластические анемии у детей: классификация, этиология, патогенез, клинические проявления, лабораторно-инструментальная диагностика, принципы лечения.
- •78. Гемолитические анемии у детей: классификация, этиология, патогенез.
- •I. Наследственные (врожденные) формы гемолитической анемии
- •II. Другие гемолитические анемии
- •79. Гемолитические анемии у детей: клинические проявления, лабораторная диагностика, принципы лечения.
- •Дефицит активности глюкозо-6-фосфатдегидрогеназы.
- •Дефекты структуры и синтеза гемоглобина.
- •3.1 Талассемии
- •3.2 Серповидноклетогная анемия
- •80. Иммунная тромбоцитопеническая пурпура у детей: этиология, патогенез, клинические проявления, принципы диагностики и лечения.
- •81. Геморрагический васкулит у детей (болезнь Шенлейна — Геноха): этиология, патогенез, клинические проявления.
- •82. Геморрагический васкулит у детей (болезнь Шенлейна — Геноха): диагностические критерии, основные формы, лабораторная диагностика и лечение.
- •83. Гемофилия у детей (этиология, ведущие клинические проявления, критерии диагностики и методы лечения).
- •84. Дефицитные состояния у детей раннего возраста: понятие, основные факторы развития, общие проявления и клинические примеры.
- •85. Рахит (этиология и патогенез, клиническая картина по периодам).
- •86. Рахит (клинические проявления, лечение и профилактика).
- •1. Синдром остеомаляции
- •2.Сидром остеоидной гиперплазии
- •3. Синдром гипоплазии костной ткани
- •4.Изменение костей за счет мышечной гипотонии
- •87. Метаболизм витамина д в организме ребенка, факторы риска развития d-дефицитного рахита у детей.
- •88. Лабораторная диагностика недостаточности и дефицита витамина д по современным данным, внекостные проявления дефицита витамина д.
- •89. Клинические проявления синдромов поражения костной ткани при витамин д-дефицитном рахите у детей.
- •90. Белково-энергетическая недостаточность питания у детей (этиология, патогенез, классификация).
- •91. Белково-энергетическая недостаточность питания у детей: клиническая картина в зависимости от степени тяжести. (Жидков)
- •92. Основные направления лечения белково-энергетической недостаточности питания у детей, этапы диетотерапии в зависимости от степени тяжести.
- •93. Задержка внутриутробного развития: критерии диагностики, причины, классификация, проявления.
- •94. Семиотика избыточного веса у детей (диагностика паратрофии и ожирения).
- •95. Аллергический ринит у детей (классификация, клинические проявления, принципы диагностики и лечения).
- •96. Бронхиальная астма у детей: определение, патогенез, классификация.
- •97. Бронхиальная астма у детей: диагностические критерии у детей различного возраста, принципы лечения по gina-2020 и профилактика. (Жидков)
- •98. Острый бронхит у детей: этиология, патогенез, клинические проявления.
- •99. Острый бронхиолит у детей: этиология, патогенез, клинические проявления, лечение, профилактика.
- •100. Острый обструктивный бронхит у детей: этиология, патогенез, клиника, лечение и профилактика.
- •101. Пневмонии в детском возрасте : этиология, патогенез, классификация, критерии диагностики у детей различного возраста.
- •102. Внебольничная пневмония: определение, этиологическая классификация, клинические проявления типичной пневмонии, современные методы диагностики и лечения.
- •103. Внебольничная атипичная пневмония: определение, этиология, клинические проявления, методы диагностики и принципы рациональной антимикробной терапии.
- •104. Осложнения пневмоний: классификация, факторы риска и критерии диагностики основных осложнений, тактика ведения.
- •Патогенез:
- •108. Острая ревматическая лихорадка у детей: клинические проявления и критерии диагностики, тактика лечения и профилактики. Клиническая картина
- •Критерии диагностики
- •110. Этиология, патогенез, клиника острого постстрептококкового гломерулонефрита у детей.
- •111. Диагностика, принципы лечения, профилактика острого постстрептококкового гломерулонефрита у детей.
- •112. Классификация и патогенез хронического гломерулонефрита у детей.
- •113. Принципы лечения и профилактика хронического гломерулонефрита, прогноз и исходы.
- •114. Этиология и патогенез, классификация инфекции мочевыводящей системы, критерии диагностики, тактика ведения.
- •115. Клинические, лабораторные и рентгенологические методы диагностики пиелонефрита.
- •116. Классификация, этиология и патогенез пиелонефрита.
- •117. Нефротический синдром в детском возрасте: понятие, классификация, патогенез.
- •I. Клинические формы нс:
- •118. Нефротический синдром в детском возрасте: клиническая картина, дифференциальная диагностика, тактика ведения.
- •119. Острое повреждение почек у детей: определение, основные критерии диагностики.
- •120.Хроническая болезнь почек у детей: определение, стадии, особенности клинико-лабораторных проявлений .
- •121. Гастриты и гастродуодениты у детей: современная классификация, этиология, патогенез, клиническая картина.
- •4. Форма поражения желудка и двенадцатиперстной кишки:
- •126. Язвенная болезнь желудка и 12-перстной кишки у детей: этиология, патогенез, классификация.
- •127. Язвенная болезнь желудка и 12-перстной кишки у детей: клинические проявления, дифференциальная диагностика и лечение.
- •128. Болезнь Крона у детей: современная трактовка патогенеза, рабочая классификация, клинические проявления, лабораторно-инструментальное обследование больных.
- •129. Болезнь Крона у детей: кишечные и внекишечные проявления, патоморфологические изменения пищеварительного тракта, лечение и профилактика.
- •130. Язвенный колит у детей: современная трактовка патогенеза, рабочая классификация, клинические проявления, лабораторно-инструментальное обследование.
- •131. Язвенный колит у детей: кишечные и внекишечные проявления, патоморфологические изменения пищеварительного тракта, лечение и профилактика.
- •Результатах лабораторных и инструментальных исследований.
- •Немедикаментозное лечение
- •Медикаментозное лечение
- •Хирургическое лечение:
- •132.Острые панкреатиты у детей: этиология, патогенез, классификация, клиническая картина, план обследования больных, тактика ведения.
- •133. Дисфункции билиарного тракта у детей: классификация, этиология, патогенез, клинические проявления основных типов.
- •По гиперкинетическому типу характерны
- •По гипокинетическому типу:
- •139. Одышечно-цианостический приступ: этиология, патогенез, неотложная помощь.
- •140. Неотложная помощь при лихорадке у детей.
- •141. Судороги у детей: этиология, классификация.
- •142. Фебрильные судороги у детей: этиология, особенности проявлений, тактика ведения.
- •143.Спазмофильный синдром: этиология, тактика оказания неотложной помощи.
- •144.Неотложная помощь при стенозирующем ларинготрахеите.
- •145. Неотложная помощь при эпиглоттите у детей.
- •146. Неотложная помощь при приступе бронхиальной астмы.
- •147. Острая дыхательная недостаточность у детей: классификация.
- •148. Пароксизмальная тахикардия у детей: тактика оказания неотложной помощи.
- •1. Начать с рефлекторного воздействия на блуждающий нерв:
- •149. Синкопальные состояния у детей: определение, патофизиология, классификация
- •150. Классификация наследственных болезней, понятие орфанных заболеваний.
- •151. Коклюш у детей (этиопатогенез, классификация).
- •152. Коклюш у детей (опорно-диагностические признаки типичной формы).
- •153. Коклюш у детей: методы лечения и профилактики.
- •154. Дифференциальная диагностика синдрома бронхиальной обструкции у детей.
- •155. Грипп а у детей: эпидемиология, этиология, патогенез, опорно-диагностические признаки типичной формы.
- •5 Фаз патологического процесса:
- •156. Грипп а у детей: особенности течения тяжелых форм, осложнения, лечение и профилактика.
- •157. Аденовирусная инфекция у детей: эпидемиология, этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение.
- •2. Патогенетическая и симптоматическая терапия.
- •158. Респираторно-синцитиальная инфекция у детей: этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение.
- •159. Парагрипп у детей: этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение.
- •166. Скарлатина у детей: тактика лечения и диспансерного наблюдения.
- •167. Герпетическая инфекция: классификация, клинические проявления, принципы диагностики и лечения.
- •168. Инфекционный мононуклеоз: этиология, патогенез, основные симптомы типичной формы, лабораторная диагностика, лечение.
- •169. Локализованная дифтерия ротоглотки у детей: клиника, диагностика, лечение, тактика введения апдс, профилактика.
- •170. Токсическая дифтерия ротоглотки у детей: клиника, диагностика, лечение, тактика введения апдс, профилактика.
- •171. Осложнения дифтерии у детей.
- •172. Дифтерия гортани: классификация, основные периоды, их опорно-диагностические признаки, тактика введения апдс.
- •173. Новая коронавирусная инфекция (Covid-19) у детей: особенности проявлений и ведения.
- •174. Шигеллезы у детей (классификация, этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение).
- •175. Токсикоз при острых кишечных инфекциях у детей: степени тяжести, патогенетическая терапия основных синдромов.
- •176. Коли-инфекция у детей (этиология, патогенез, классификация диареегенных штаммов, диагностика, лечение, профилактика).
- •177. Энтеропатогенная коли-инфекция у детей (этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение, профилактика).
- •178. Энтеротоксигенная коли-инфекция у детей (этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение, профилактика).
- •179. Энтероинвазивная коли-инфекция у детей (этиология, патогенез, опорно-диагностические признаки типичной формы, диагностика, лечение, профилактика).
- •180. Сальмонеллез у детей (этиология, эпидемиология, клиника, диагностика, лечение, профилактика).
- •181. Ротавирусная инфекция у детей: эпидемиология, этиопатогенез, клинические проявления, методы лечения и профилактики.
- •182. Клинические проявления и степени тяжести дегидратации при кишечных инфекциях у детей.
- •183.Токсикоз при острых кишечных инфекциях у детей: клинико-лабораторные критерии по степеням тяжести.
- •184. Реалиментация и регидратация при острых кишечных инфекциях у детей в зависимости от степени эксикоза.
- •185. Эпидемиология и этиологическая классификация острых кишечных инфекций у детей, виды диарей.
- •190. Серозные менингиты вирусной этиологии у детей: особенности течения, лечение, профилактика.
- •191. Менингококковая инфекция (этиология, патогенез, классификация).
- •192. Корь (этиология, патогенез, эпидемиология, классификация, основные периоды типичной формы).
- •193. Клинические периоды кори. Осложнения, диагностика, лечение.
- •194. Профилактика кори: плановая и экстренная, виды вакцин.
- •195. Паротитная инфекция (этиология, эпидемиология, патогенез, классификация).
- •196. Клинические формы паротитной инфекции (диагностика, лечение, профилактика).
- •197. Краснуха у детей: этиология, эпидемиология, патогенез, классификация.
- •198. Краснуха у детей: опорно-диагностические признаки типичной формы, особенности экзантемы, специфические осложнения, лечения и профилактика.
- •199. Врожденная краснуха (клиническая картина большого и малого краснушного синдромов, принципы диагностики и профилактика).
- •200. Ветряная оспа (этиология, патогенез, эпидемиология, периоды типичной формы).
- •201. Ветряная оспа: классификация, специфические осложнения, лечение и профилактика.
- •202. Массовая и индивидуальная туберкулинодиагностика ( туберкулиновые пробы и их оценка). Критерии виража туберкулиновых проб и вакцинальная аллергия. (Жидков)
- •203. Туберкулез внутригрудных лимфоузлов у детей и подростков (основные формы, клиника, диагностика, лечение). Факторы риска по развитию туберкулеза. (Жидков)
- •204. Основные синдромы поражения печени при гепатитах у детей (клинические и биохимические маркеры). (Жидков)
- •205. Вирусный гепатит а у детей: эпидемиология, особенности этиологии и патогенеза, опорно-диагностические признаки и лабораторная диагностика типичной формы. (Жидков)
- •206. Вирусный гепатит а у детей: классификация, особенности течения, тактика ведения и профилактика. По типу: 1. Типичные формы 2. Атипичные формы: безжелтушная; стертая; латентная; бессимптомная.
- •207. Вирусный гепатит е у детей: особенности эпидемиологии, этиологии и патогенеза, клиническая картина, тактика лечения и профилактики.
- •208. Вирусный гепатит в у детей: особенности эпидемиологии, этиологии и патогенеза, течения, опорно-диагностические признаки и лабораторная диагностика периодов типичной формы.
- •209. Вирусный гепатит в у детей: тактика лечения, профилактика и диспансерное наблюдение.
- •210. Осложнения и исходы вирусных гепатитов у детей.
- •211. Клинические и лабораторные критерии тяжести гепатитов.
- •213. Фульминантная форма вирусного гепатита в у детей: причины развития, стадии, лабораторные маркеры, тактика ведения.
- •214. Вирусный гепатит d у детей: эпидемиология, патогенез, особенности течения, диагностика и тактика ведения.
- •215. Вирусный гепатит с у детей: эпидемиология, патогенез, клиническая картина типичной формы, лечение, диспансерное наблюдение.
- •215. Поражение нервной системы при эпидемическом паротите у детей: основные клинические формы, диагностика, лечение.
- •216. Клещевой боррелиоз у детей: эпидемиология, этиология, клинические проявления, лечение и профилактика.
- •217. Внутриутробные инфекции: этиология, эпидемиология, факторы риска, понятие torch-синдрома.
- •218. Внутриутробные инфекции: группы риска, клинические проявления в зависимости от сроков инфицирования, критерии диагностики, общие принципы лечения, профилактика.
- •219. Действующий Национальный календарь прививок, правила вакцинации, реакции на введение вакцин, поствакцинальные осложнения.
- •220. Менингококковая инфекция у детей: основные клинические синдромы, лабораторная и инструментальная диагностика, лечение и профилактика.
- •221. Атипичные формы кори: причины развития, особенности течения, тактика лечения, профилактика.
- •222. Осложнения кори: классификация, сроки развития, клинические проявления, тактика ведения.
- •223.Основные типы дегидратации у детей: клинико-лабораторные проявления.
- •224. Дифференциальная диагностика детских экзантем.
- •225. Дифференциальная диагностика острых тонзиллофарингитов у детей.
По гиперкинетическому типу характерны
периодические острые боли спастического характера («желчная колика»), возникающие на фоне стресса, сильных эмоциональных переживаний или физической нагрузки с повышением внутрибрюшного давления.
Боли обычно бывают кратковременными, имеют малую и среднюю интенсивность, чаще не иррадиируют, купируются самостоятельно или после приема спазмолитиков.
Во время приступа возможна тошнота, реже рвота.
Объективно обнаруживают болезненность в точке Кера.
Вне приступов колик на болевые ощущения пациенты обычно не жалуются.
Пальпация живота безболезненна или умеренно болезненна в правом подреберье, печень не увеличена. Характерны повышенное беспокойство больных, психоэмоциональные нарушения, признаки ВСД.
По гипокинетическому типу:
беспокоят боли дистензионного характера (постоянные, длительные, тупые, ноющие),
чувство распирания и тяжести в правом подреберье, появляющиеся или усиливающиеся после еды.
возможны ночные боли, связанные с переполнением желчью желчного пузыря из-за снижения его сократительной способности как после приема пищи, так и натощак.
Иногда отмечают иррадиацию болей в спину, в правую лопатку.
Интенсивность болевых ощущений может быть разной. При умеренном болевом синдроме нарушается повседневная деятельность ребенка, а при тяжелом необходима срочная медикаментозная терапия.
У пациентов с функциональной патологией желчевыводящих путей часто наблюдаются психогенные боли, когда периферические воздействия отсутствуют, либо играют роль пускового момента. Состояние психики человека оказывает на ощущение боли большое влияние, опосредованное эндогенной опиатной системой и ее рецепторным аппаратом, расположенным в окончаниях чувствительных нервов, в нейронах спинного мозга, в стволовых ядрах, в таламусе и лимбических структурах центральной нервной системы. Индуцируемое рецепторами выделение эндорфинов и энкефалинов, а также блокирование выделения субстанции Р приводит к снижению интенсивности болевых ощущений.
Уменьшению порога болевой чувствительности и усилению боли способствует понижение уровня серотонина и норадреналина.
Указанные виды болевого синдрома отличаются по характерным субъективным признакам, анализ которых позволяет иногда с большой точностью определить причину и особенности патологического процесса в регионе гепатобилиарной системы.
При анализе болевого синдрома необходимо учитывать его субъективный характер, остроту, длительность, периодичность, связь с приемом пищи, сочетание с другими симптомами, автономными вторичными эффектами, а также информацию о том, что купирует болевые ощущения – спазмолитики, антисекреторные средства, желчегонные препараты, антациды, анальгетики.
Висцеральный болевой синдром воспринимается чаще как тупая ноющая боль без четкой локализации. При поражении желчевыводящей системы висцерально обусловленные боли чаще локализуются в зоне эпигастрия по средней линии, и только при присоединении соматической компоненты (распространение процесса на париетальную брюшину, резкое перерастяжение органа, спазм мускулатуры) боли приобретают типичную локализацию – правое подреберье. Соматический болевой синдром значительно острее по силе и степени выраженности, чем висцеральный. Висцеральная боль длится обычно недолго, но ей свойственна периодичность и рецидивы.
Дистензионные боли чаще носят распирающий характер, ощущение тяжести, инородного тела, иногда приобретают жгучий характер (ощущение жжения, тепла и т.д.).
Спастические боли более острые (колики) – «режущие», «тянущие», «схватывающие».
Иррадиирующий болевой синдром часто может наблюдаться при патологии билиарной системы, как правило, когда процесс распространяется на париетальную брюшину, покрывающую желчный пузырь (перихолецистит), при раздражении нервных окончаний правого диафрагмального нерва (острый холецистит, обострение хронического холецистита). Отсутствие иррадиации более характерно для дискинезии желчевыводящих путей. Иррадиация свидетельствует о локализации и глубине процесса в стенке органа, а также об интенсивности поражения и раздражающих нервные рецепторы стимулов, что доказано экспериментально.
Пациентов также беспокоят признаки диспепсии:
снижение аппетита, горечь во рту,
отрыжка воздухом и пищей,
тошнота, рвота,
запоры.
после приема большого количества жирной пищи могут быть поносы, обусловленные поступлением в кишечник большого количества несвоевременно выделившейся желчи.
При пальпации живота обнаруживают болезненность в пузырной точке различной интенсивности. Иногда удается пропальпировать значительно увеличенный желчный пузырь. Печень бывает увеличена в размерах, имеет мягкоэластическую консистенцию, безболезненна при пальпации. Ее размеры быстро уменьшаются после приема холекинетиков, проведения «слепого» или дуоденального зондирования.
Дисфункция сфинктера Одди - комплекс функциональных расстройств, проявляющихся рецидивирующими приступами сильной или умеренной боли длительностью 20 мин и более.
Болевые ощущения могут иметь опоясывающий характер (сочетанный тип) или быть локализованы в эпигастрии или правом подреберье (билиарный тип), а также иррадиировать в левое подреберье, уменьшаясь при наклоне тела вперед (панкреатический тип). Боли провоцируются приемом пищи и сопровождаются тошнотой и/или рвотой.
При любом типе ДЖВП возможны симптомы холестаза: иктеричность кожи шеи и боковой поверхности живота, субъиктеричность склер.
К симптомам вегетативных дисфункций у детей с патологией гепатобилиарной системы относятся головные боли, головокружение, нарушения сна, повышенная утомляемость, снижение умственной и физической работоспособности, метеочувствительность, плохая переносимость холода, жары, душных помещений.
134. Дисфункции билиарного тракта у детей: данные объективного обследования детей, инструментальная диагностика, тактика лечения.
Острый холецистит острое воспаление желчного пузыря.
· внезапное повышение температуры тела до фебрильной;
· схваткообразные боли в правой половине, а иногда и по всему животу. Приступ болей может длиться от нескольких минут до нескольких часов. Боли усиливаются в положении на правом боку;
· тошнота и рвота;
· явления интоксикации: кожа бледная, влажная, губы и слизистые оболочки рта сухие, язык обложен, головная боль, отсутствие аппетита, задержка стула, тахикардия;
· возможно (в 50 % случаев) появление желтухи.
При осмотре живота отмечают некоторое его вздутие, отставание верхних отделов при дыхании. При пальпации находят ригидность мышц передней брюшной стенки справа, больше в верхних отделах и в подреберье. Как правило, положительны симптомы Менделя, Ортнера, Мерфи. Нередко положителен симптом Щеткина—Блюмберга. При анализе крови у больных выявляют лейкоцитоз с нейтрофилезом, увеличенную СОЭ. Течение острого холецистита у детей, как правило, доброкачественное, но в большинстве случаев острый холецистит является началом хронического холецистита.
Хронический холецистит - рецидивирующее воспалительное заболевание желчного пузыря. В отличие от билиарных дисфункций для клинических проявлений холецистита характерны стереотипность, наличие периодов обострений с выраженной интоксикацией, возможным субфебрилитетом.
Для хронического холецистита у детей характерны:
· правоподреберный болевой синдром;
· диспептический, воспалительно-интоксикационный, астеновегетативный, холестатический синдромы.
Из объективных симптомов холецистита у детей чаще всего находят следующие: резистентность мышц в правом подреберье, симптом Ортнера, симптом Мерфи, симптом Менделя, болезненность при пальпации в треугольнике Шоффара.
При лабораторных исследованиях при холецистите могут быть повышены показатели активности воспалительного процесса (гипергаммаглобулинемия, гиперфибриногенемия, повышение СОЭ, лейкоцитопения). При ультразвуковом исследовании аргументами в пользу холецистита являются обнаружение утолщенной (более 1,5 мм), слоистой, гиперэхогенной стенки желчного пузыря, а также неоднородность желчи. При тепловидении выявляют гипертермию в области проекции желчного пузыря. Диагностически значимо изменение состава желчи: снижение арахидоновой и олеиновой кислот, повышение пентадекано-вой и медистовой жирных кислот; увеличение концентрации иммуноглобулинов G и A, R-белков, С-реактивного протеина; повышение ферментов (5-нуклеотидазы и щелочной фосфатазы); снижение лизоцима. Возможно повышение в крови трансаминаз, билирубина и β-липопротеидов.
Диагностика. Основным методом верификации ДРБТ является ультрасонография желчевыводящих путей с использованием функциональной пробы с холекинетиками (неохолекс, яичный желток, сорбит). Динамическое наблюдение за изменениями объема желчного пузыря позволяет судить как о дисфункции сфинктеров, так и о скорости сокращения пузыря.
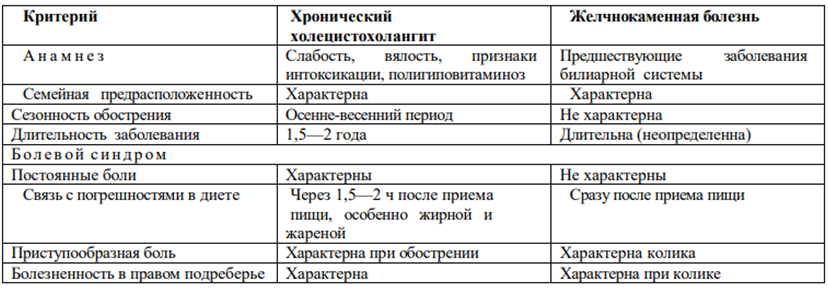
Дифференциальный диагноз с острым и хроническим холециститом (клиника воспаления, анализы крови, кала, УЗИ, рентген и т.д.) + ЖКБ.
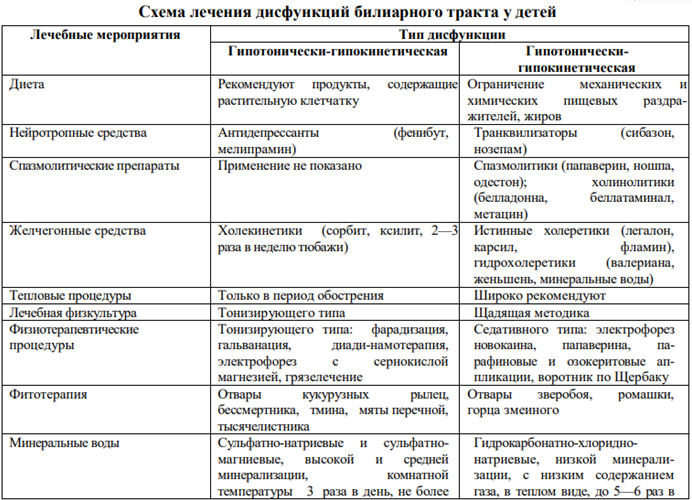
Лечение: Устранение провоцирующих факторов, 4—5-разовое питание с исключением жирной, жареной пищи и обогащением рациона клетчаткой, растительным маслом. Необходима коррекция нарушенных нейрогуморальных механизмов. При остром холецистите постельный режим, голод, обильное питье, антибиотики, спазмолитики и анальгезирующие препараты, инфузионная терапия, антиферментные препараты. Хирургическое вмешательство при подозрении на гнойный, флегмонозный или гангренозный холециститы, перфорацию стенки желчного пузыря. При хроническом холецистите наряду с диетой и симптоматической терапией, определяемой типом ДБТ, в период обострения назначают никодин или оксафенамид, циквалон, фуразолидон.
Обязательна витаминотерапия (в остром периоде витамины А, С, В1, В2, РР, а в дальнейшем — курсы витаминов В6 и В12, В15, В5, Е).
Диспансерное наблюдение при ДБТ осуществляют в течение 1 года. Необходимо соблюдение щадящей диеты, ограничение физических нагрузок, ЛФК. Показано лечение в местных санаториях, а через 3 месяца — на бальнеологических курортах с минеральными водами.
Недостаточность желчеотделения: Испражнения серого цвета, много жирных кислот, отсутствие реакции на стеркобилин.
![]()

135. Синдром мальабсорбции у детей: классификация и клинические проявления.
Мальабсорбция - синдром, объединяющий все виды патологии, обусловленной расстройством пищеварения или всасывания, приводящий к нарушению метаболизма. Синдром мальабсорбции может развиваться вследствие нарушения полостного пищеварения — внутриполостной тип (врожденная гипоплазия поджелудочной железы, муковисцидоз, дефицит энтерокиназы, хронический панкреатит). Существуют формы мальабсорбции (энтероцеллюлярный тип), обусловленные изолированным нарушением пристеночного пищеварения (дисахаридазная недостаточность) либо кишечного всасывания углеводов (мальабсорбция глюкозы-галактозы, мальабсорбция фруктозы), жиров (липопротеинемия), аминокислот (лизинурия, синдром Хартнапа и пр.) и минералов (энтеропатический акродерматит, хлоридная и натриевая диареи). Мальабсорбция может быть обусловлена сочетанным нарушением пищеварения и всасывания — целиакия, аллергическая и аутоиммунная энтеропатии, врожденные дефекты микроворсинок кишечника, болезнь Крона. Отдельно выделяют мальабсорбцию, обусловленную потерей компонентов плазмы через кишечную стенку, — постцеллюлярный тип (экссудативная энтеропатия). Существуют первичные формы мальабсорбции (муковисцидоз, врожденная глюкозо- галактозная мальабсорбция, первичная интестинальная лимфангиэктазия).
Вторичная мальабсорбция: синдром может быть связан с операциями на кишечнике (например, синдром короткой кишки после резекции значительной части тонкой кишки, образование межкишечных свищей), опухолевым поражением (диффузный лимфосаркоматоз, злокачественные лимфомы), воспалением (хронический энтероколит, хронический панкреатит с недостаточностью поджелудочной железы, болезнь Крона и др.), с длительным использованием антибиотиков (синдром раздраженной кишки), с острыми кишечными инфекциями.
Клиника разных форм мальабсорбции различается, но есть и общие черты, присущие большинству заболеваний этой группы. К ним относят: диарею, полифекалию, истощение, анемизацию, гиповитаминозы, задержку развития.
Для синдромов мальабсорбции характерна полифекалия (у детей количество кала превышает 2% от съеденной пищи и выпитой жидкости). Среди синдромов мальабсорбции наиболее часто наблюдается дисахаридазная недостаточность (лактазная и сахаразная), целиакия (непереносимость глютена-глиадина), непереносимость белков коровьего молока. У таких больных полифекалия нередко сопровождается расстройством стула, а иногда и синдромом дегидратации. Для дисахаридазной недостаточности характерен жидкий пенистый кал без патологических примесей, резко кислой реакции (pH менее 6). Для целиакии свойственна полифекалия. Фекалии гомогенны, без патологических примесей, светло-желтого цвета, как опара. Непереносимость белков коровьего молока наблюдается обычно у детей первого года жизни и клинически проявляется целиакоподобным синдромом. Полифекалия и расстройство стула при хронических панкреатитах обусловлены нарушением топографии полостного (дистантного) и мембранного пищеварения вследствие ферментативной недостаточности. + кишечные проявления муковисцидоза тоже вызывают мальабсорбцию.
136. Лактазная недостаточность у детей: патогенез, классификация, клинические проявления основных типов, диагностика, тактика ведения.
Лактазная недостаточность (непереносимость лактозы) - симптомокомплекс расстройств пищеварения, обусловленный нарушением гидролиза лактозы в тонкой кишке. ЛН является наиболее распространенной формой интестинальных энзимопатий.
Этиология. ЛН может быть наследственно обусловленной, т. е. первичной. ЛН часто развивается при различных инфекционно-воспалительных заболеваниях, дистрофических процессах, аллергических заболеваниях тонкой кишки, лямблиозе, медикаментозных воздействиях, а также всегда — при целиакии в сочетании с сахаразной и мальтазо-изомальтазной недостаточностью.
Патогенез. ЛН обусловлена нарушением гидролиза лактозы ферментом энтероцитов лактазой (a-галактозидазой) вследствие его дефектности (при ранних первичных формах), уменьшения его количества (при поздних первичных формах) или повреждения слизистой оболочки тонкой кишки (при вторичных формах). При употреблении молочной пищи нерасщепленная ферментами лактоза подвергается бактериальному гидролизу с образованием побочных продуктов: водорода, углекислого газа, пировиноградной и молочной кислот, с развитием метеоризма, диспепсии и интоксикации.
Классификация. Выделяют раннюю (врожденную) и позднюю формы первичной лактазной недостаточности, а также вторичную форму.
Клиника. Первичная ранняя форма ЛН проявляется с первых дней жизни беспокойством после кормлений, урчанием в животе, частым пенистым стулом с кислым запахом, низкими прибавками массы тела. Поздняя форма первичной ЛН формируется после завершения периода молочного вскармливания, в большинстве случаев после 3—5 лет. При этой форме интолерантность лактозы имеет частичный характер — ребенок может усвоить 100—200 мл молока, но большее количество вызывает появление резей в животе, урчание, послабление стула и умеренную интоксикацию. В Европе, ЛН встречается сравнительно редко, значительно чаще она отмечается у ряда народов Азии и Африки.
Вторичная ЛН проявляется тем, что через 1—1,5 ч после приема молочной пищи появляются рези, вздутие, урчание в животе и нередко интоксикация в виде подташнивания, слабости. Стул учащен, приобретает кислый запах. При исключении из рациона молочных продуктов диспепсические явления довольно быстро (в течение суток) ликвидируются, при повторном приеме молока рецидивируют.
Диагностика. Диагноз ЛН при манифестных формах заболевания устанавливают на основании данных анамнеза и подтверждают эффективностью безлактозной диеты. При субклинических формах ЛН для подтверждения диагноза наряду с анамнезом необходимы дополнительные исследования. Используют лактозотолерантный тест - гликемическая кривая в случае ЛН бывает уплощена. Проводят водородный дыхательный тест - после нагрузки лактозой при ЛН содержание водорода в выдыхаемом воздухе превышает 0,1 мл/мин; выполняют хроматографию лактозы в моче. Определяют появление лактозы в кале и моче после нагрузки. Дифференциальная диагностика проводится с непереносимостью белка коровьего молока, которая имеет обычно атопический характер, возникает при переводе ребенка на смешанное или искусственное вскармливание, сопровождается кожными высыпаниями и повышенным уровнем IgE. С другими видами дисахаридазной недостаточности (сахаразной, мальтазной, изомальтазной) ЛН дифференцируют, учитывая продукты, вызывающие диспепсические проявления.
Лечение ЛН основано на использовании низко- или безлактозной диеты. Однако при первичной ранней форме ЛН у детей, находящихся на естественном вскармливании, рекомендуют использовать препарат Лактаза или пищевую добавку Лактаза бэби (770—800 мг Лактазы или 1 капсулу Лактазы бэби на каждые 100 мл молока), добавляя их в каждое кормление со сцеженным грудным молоком в начале кормления, а затем докармливая ребенка из груди. У детей, находящихся на искусственном или смешанном вскармливании, следует подобрать питание с максимальным количеством лактозы, которое не вызывает появления клинической симптоматики и повышения углеводов в кале. Индивидуальный подбор диеты осуществляют путем комбинации безлактозной смеси (Алсой, Нутри-соя, Прособи, Фрисосой и др.) и стандартной адаптированной смеси в соотношении 2 : 1, 1 : 1 или 1 : 2. При первичной поздней ЛН вполне достаточно ограничения молока и лактозосодержащих продуктов с адекватной заменой их другими продуктами. При вторичной ЛН необходимо выявление и лечение основного заболевания, временное ограничение молочных продуктов с заменой их кисломолочными или низколактозными. Профилактика ранней первичной формы ЛН состоит в предупреждении патологии беременности. Профилактика вторичных форм ЛН предполагает предупреждение, раннее выявление и своевременное лечение заболеваний кишечника.
137. Целиакия у детей: патогенез, клинические проявления, лабораторно-инструментальное обследование, тактика ведения.
Целиакия (глютеновая энтеропатия, нетропическая спру, болезнь Ги—Гертера — Гейбнера,) — хроническая аутоиммунная генетически детерминированная энтеропатия, характеризующаяся стойкой непереносимостью специфических белков злаковых культур с развитием обратимой гиперрегенераторной атрофии слизистой оболочки тонкой кишки и связанного с ней синдрома мальабсорбции.
Этиология. Причиной заболевания генетически детерминированная пожизненная непереносимость белков некоторых злаков: пшеницы, ржи, ячменя (из-за наличия в них глютена). Ген, кодирующий синтез антигенов системы HLA, расположен на коротком плече 6-й хромосомы. Целиакия - полигенное заболевание.
Патогенез. Стартовым моментом является употребление в пищу глютенсодержащих продуктов. В щеточной кайме энтероцитов у предрасположенных к целиакии лиц повышена активностьтканевой трансглутаминазы (тТГ). Под действием этого фермента: происходит частичное расщепление глютена, его пептиды связываются с антигенами системы HLA-DQ2/DQ8 с образованием токсичных комплексов, повреждающих слизистую оболочку кишечника с повышением ее проницаемости; нарушается распознавание фрагментов глютена приводящее к срыву иммунологической толерантности; антиогенпрезентация\активация и все вот это вот сопровождается повреждением энтероцитов цитотоксичными лимфоцитами, выбросом провоспалительных цитокинов, активацией естественных киллеров и развитием иммунного воспаления в слизистой оболочке кишечника; Т2-лимфоциты активируют В-клетки к выработке антител к глютену, а также к тканям кишки: ретикулиту, эндомизию, трансглутаминазе. Так как трансглутаминаза содержится практически во всех органах и тканях (эндотелии, макрофагах, фибробластах, гладкомышечных клетках и т. д.), внекишечные проявления целиакии могут быть обусловлены воздействием таких антител; наряду с атрофией слизистой оболочки кишечника при целиакии отмечают гиперплазию D-клеток, продуцирующих соматостатин, который подавляет продукцию энтеральных гормонов и СТГ, экскреторную функцию поджелудочной железы. Развивается нарушение полостного, пристеночного пищеварения и всасывания. Морфологическим субстратом целиакии является уменьшение толщины гликокаликса, снижение количества абсорбтивных клеток, уплощение или исчезновение ворсинок, значительное увеличение числа пролиферирующих недифференцированных клеток крипт, удлинение крипт, ускорение по сравнению с нормой обновления и миграции клеток.
Классификация. Указывают форму (типичная, атипичная, латентная), период (обострение, ремиссия) и тяжесть заболевания. Клиника целиакии может проявиться в любом возрасте. У детей заболевание чаще развивается после введения продуктов, содержащих глютен, в возрасте между 9 и 24 мес. жизни, у взрослых — чаще всего после 30 лет. К типичным проявлениям целиакии относят симптомы, обусловленные поражением кишечника и связанной с ним мальабсорбцией. Ведущими симптомами типичной целиакии являются:
· полифекалия - обильный стул, превышающий 5 % массы съеденной пищи;
· стеаторея - зловонный, с гнилостным запахом, сероватый с характерным жирным блеском стул, значительное увеличение в копрограмме нейтрального жира и, особенно, жирных кислот;
· значительное исхудание
генерализованное отсутствие подкожной жировой клетчатки, особенно в области груди, конечностей, ягодиц;
· псевдоасцит Дельбе - контрастирующий с исхуданием большой, вздутый живот вследствие скопления жидкости в атонически расширенных петлях кишечника и гепатомегалии.
· На нижних конечностях - безбелковые отеки;
· задержка роста при длительном течении заболевания;
· изменение характера больного: дети становятся угрюмыми, раздражительными, неадекватными, капризными и эгоистичными невропатами - «синдром несчастного ребенка»;
· симптомы поливитаминной недостаточности - сухость кожи, атрофический глоссит, ангулярный стоматит; анемии (дефицит железа и витаминов);
· рахит; дистрофические изменения зубов, ногтей, волос; могут возникать спонтанные переломы (дефицит кальция и витамина D).
Типичные формы в общей структуре цилиакии составляют 10—15 %. Атипичной считают целиакию, при которой, несмотря на наличие атрофии слизистой оболочки кишечника, кишечные симптомы не выражены, но имеются какие-либо внекишечные проявления: герпетиформный дерматит, аутоиммунный тиреоидит, сахарный диабет I типа, аутоиммунный гепатит, задержка роста и полового развития, селективный дефицит IgA, алопеция, васкулит, IgA-нефропатия и др. Для латентной формы целиакии характерны при отсутствии симптоматики наличие генетической предрасположенности (антигены HLA DQ2, DQ8), положительные серологические тесты. Течение заболевания волнообразное, с ремиссиями от нескольких месяцев до нескольких лет. Диагностика начинается с клинического скрининга, особенно при отягозеном анамнезе.
I этап диагностики может быть проведено исследование DQ2 и DQ8 (генетический скрининг).
II этап диагностики серологическое обследование для определения наличия антител к тТГ и к эндомизию (ЭМА).
III этап морфологическое исследование при положительных серологических пробах. Один биоптат слизистой оболочки получают при ФЭГДС из луковицы и по 2 биоптата - из средней и нисходящей частей двенадцатиперстной кишки. Для целиакии типично наличие атрофии слизистой оболочки: укорочение ворсин, гиперплазия (углубление) крипт, IgA в слизистой.
IV этапом диагностики (завершающим) является наблюдение на фоне диетотерапии в течение 6—12 мес. При отчетливой положительной динамике симптомов и снижении титра антител целиакия считается доказанной, а диагноз окончательным. При отсутствии положительной динамики симптомов на фоне строгого (!) соблюдения диеты производят анализ всех этапов диагностики, проводят контрольное серологическое и морфологическое исследование.
При достоверно установленном диагнозе он является пожизненным, и любые провокации глютенсодержащими продуктами категорически противопоказаны и опасны. В особых случаях при обоснованных сомнениях в диагнозе проведение провокационной пробы допускается под тщательным медицинским контролем (нежелательно у детей до 5 лет и в пубертатном периоде). Отсутствие клинических симптомов и повышения антител при наблюдении за ребенком не менее 2 лет говорит о необходимости отмены диагноза целиакии. Дифференциальный диагноз проводят с другими формами мальабсорбции.
Лечение. В терапии больных целиакией особое место принадлежит диете: строгому пожизненному исключению из рациона больных продуктов, содержащих глютен (манная, перловая, ячневая, пшеничная крупы, пшеничная, ржаная, ячменная мука и ржаные отруби, толокно, макароны, рожки, вермишель, лапша, все виды пшеничного и ржаного хлеба, баранки, сушки, сухари, соломка, хлебные палочки, сдобные булочки, печенье, вафли, торты, пирожные); обеспечению физиологических потребностей ребенка в основных пищевых веществах и энергии за счет продуктов, не содержащих глютен. В активном периоде целиакии с заместительной целью назначают ферментные препараты: креон, панцитрат. Целесообразно назначение витаминов группы В, С, D, препаратов кальция, применение парентеральных препаратов железа. У многих больных (20—70 %) вследствие явлений гипоспленизма возможны пневмококковые и менингококковые инфекции. В этой связи имеются показания для вакцинации больных против пневмококка. При несоблюдении аглютеновой диеты у 9—19 % больных в дальнейшем развивается опухоль кишки — лимфома. Профилактика целиакии у детей состоит в позднем (после 12 мес. жизни) введении в питание манной и пшенной каш, профилактика обострений — в постоянном соблюдении аглютеновой диеты. Диспансерное наблюдение проводят пожизненно. Корригируют диету и заместительную терапию, контролируют динамику роста и массы тела, оценивают копрограмму, проводят массаж, ЛФК.
138. Острая сердечная недостаточность в детском возрасте: причины, клиника и неотложная терапия.
Сердечная недостаточность — это неспособность сердца обеспечивать сердечный выброс, достаточный для метаболических потребностей тканей.
Общепринятой классификации ОСН у детей нет.
По степени выраженности А.В. Папаян и Э.К. Цыбулькин (1984) выделяют 3 степени острой сердечной недостаточности:
Острая сердечная недостаточность I степени характеризуется тахикардией и одышкой. Самым важным симптомом является изменение соотношения между частотой сердечных сокращений и дыхания. У детей до 1 года отношение частоты пульса к частоте дыхания будет свыше 3,5; у детей старше 1 года - 4,5. Имеются признаки поражения сердца: глухость тонов, расширение границ относительной сердечной тупости.
Острую сердечную недостаточность II степени в зависимости от тяжести можно подразделить на 2 состояния: с преобладанием декомпенсации только в одном круге кровообращения или с тотальной недостаточностью кровообращения.
При недостаточности II А степени, если преобладают явления застоя в большом круге, у больного увеличиваются размеры печени, могут быть периорбитальные отеки. ЦВД повышается только в том случае, если декомпенсация развивается быстро, в течение минут или нескольких часов. Если недостаточность нарастает постепенно в течение 1-2 сут., то ЦВД может оставаться нормальным на фоне прогрессивного набухания печени. Печень в этих случаях играет роль буфера. Обязательна приглушенность тонов сердца, возможно расширение границ относительной сердечной тупости. Если преобладают явления застоя в малом круге кровообращения, помимо относительной тахикардии, усиливается цианоз, степень которого не уменьшается под влиянием оксигенотерапии. В легких появляются рассеянные мелкопузырчатые хрипы, определяется акцент II тона на легочной артерии.
При недостаточности II Б степени к перечисленным признакам присоединяются олигурия, периферические отеки, возможен отек легких.
Острая сердечная недостаточность III степени - гипосистолическая форма сердечной недостаточности с развитием артериальной гипотензии на фоне клиники перегрузки малого круга кровообращения.
Этиология.
· Врожденные пороки сердца, особенно с большим сбросом крови слева направо или обструкцией выносящего тракта левого или правого желудочка.
· Приобретенные заболевания сердца — кардиты, кардиомиопатии, острое или хроническое поражение сердца при ревматизме.
· Нарушения ритма и проводимости — пароксизмальная тахикардия, мерцательная аритмия, трепетание предсердий, полная АВ-блокада и др.
· Ятрогенные факторы — повреждение сердца во время хирургического вмешательства, перегрузка объемом, медикаментозное лечение и др.
· Внесердечные причины — тиреотоксикоз, артериовенозные фистулы, острые и хронические заболевания легких, гликогенозы, диффузные заболевания соединительной ткани, нервно[1]мышечные заболевания, гипоксия, артериальная гипертензия и др.
Лечение
Кардиогенный шок
Оказание скорой медицинской помощи должно начинаться с мероприятий по устранению причин кардиогенного шока.
1. Обеспечить свободную проходимость дыхательных путей.
2. Кислородотерапия.
3. Обеспечить доступ к вене, т.к. иные пути введения лекарственных препаратов вследствие нарушений микроциркуляции неэффективны.
4. Ввести в/в капельно реополиглюкин 5-8 мл/кг, 10% раствор глюкозы и 0,9% раствор хлорида натрия в соотношении 2:1 в дозе 50 мл/кг, кокарбоксилазу 100-200 мг, 7,5% раствор хлорида калия в дозе 0,5 мл/кг.
5. Ввести в/в гидрокортизон 10-15 мг/кг или преднизолон в/в струйно в дозе 2-5 мг/кг.
6. При выраженном болевом синдроме в/в струйно промедол 1% раствор 0,1 мл/год жизни или баралгин 0,1-0,2 мл/год жизни или анальгин 50% раствор 0,1-0,2 мл/год жизни.
7 При наличии психомоторного возбуждения - диазепам (седуксен, реланиум, сибазон) 0,5% раствор 0,1-0,3 мг/кг в/в струйно или дроперидол 0,25% раствор 0,05 мл/кг в/в.
Госпитализация обязательна во всех случаях развития кардиогенного шока.
Острая застойная сердечная недостаточность:
при I стадии ОСН:
· - положение больного с опущенными ногами;
· - сосудорасширяющие препараты - папаверин;
· - лазикс 2-4 мг/кг;
· - доставка в стационар.
при II стадии ОСН:
· - положение больного с опущенными ногами;
· - доступ свежего воздуха;
· - лазикс 2-4 мг/кг;
· - вызов специализированной бригады скорой медицинской помощи.
при III стадии ОСН:
· - положение больного с опущенными ногами;
· - доступ свежего воздуха;
· - преднизолон 5 мг/кг;
· - вызов специализированной бригады скорой медицинской помощи.
