
- •1. Аллергические пробы in vivo и in vitro, их сущность, применение.
- •2. Анатоксины. Получение, применение. Антитоксический иммунитет
- •3. Антибактериальные препараты. Классификация. Механизмы антибактериального действия. Механизмы возникновения и распространения устойчивости.
- •Классификация, которую Козлова указала у себя в презентации:
- •3)По типу взаимодействия с микробной клеткой:
- •4)По кислотоустойчивости антимикробные препараты классифицируются на:
- •5. Бактериологический метод диагностики. Требования к выращиванию бактерий в искусственных условиях.
- •6. Бактериоскопический метод диагностики, его задачи и возможности. Методы микроскопии и их применение.
- •7. Бактериофаги. Взаимодействие фага с бактериальной клеткой. Умеренные и вирулентные бактериофаги. Лизогения.
- •8. Бактериофаги. Получение, титрование. Практическое применение в диагностике, профилактике и лечение
- •9. Вакцины Вакцинопрофилактика и вакцинотерапия
- •10. Внутривидовое типирование бактерий. Методы. Использование в практике
- •11. Врожденный иммунитет. Фагоцитоз. Показатели фагоцитоза
- •14 Грибы. Строение клетки. Классификация грибов по морфологии таллома.
- •15. Действие физических и химических факторов на микроорганизмы. Использование в практике.
- •16. Дисбиозы. Препараты для восстановления микробиоты
- •17 Иммунодиагностика (серодиагностика) инфекционных заболеваний. Принципы и диагностические критерии.
- •18. Иммунопрофилактика, иммунотерапия. Осложнения: анафилактический шок, сывороточная болезнь. Их предупреждение
- •19. Иммуноферментный анализ, иммуноблоттинг. Принципы методов, используемые реагенты и оборудование, применение.
- •20. История микробиологии. Этапы развития. Современные задачи.
- •21. Культивирование бактерий in vitro. Требования к условиям культивирования. Питательные среды, их классификация. Требования, предъявляемые к питательным средам
- •Условия культивирования бактерий:
- •Требования к питательным средам:
- •Классификация
- •Примеры сред
- •22. Методы культивирования вирусов. Вирусологический метод, основные этапы.
- •23. Методы микроскопического исследования (световая, люминесцентная, темнопольная, фазово-контрастная, электронная микроскопия)
- •24. Методы определения чувствительности бактерий к антибиотикам. Мпк (мик) и мбк. Критерии определения бактериальных изолятов как чувствительные, устойчивые, умеренно чувствительные
- •Достоинства метода
- •Недостатки метода
- •28. Механизмы формирования и распространения устойчивости к антибактериальным препаратам бактерий – возбудителей инфекционных болезней
- •29. Микробиота желудочно-кишечного тракта человека
- •30. Микробиота урогенитального тракта человека
- •31. Моноклональные антитела. Получение. Использование
- •32. Морфология микроорганизмов. Морфологические группы бактерий
- •33. Нагрузочные серологические реакции. Реакции непрямой гемагглютинации. Компоненты. Применение
- •34. Наследственность и изменчивость у бактерий. Механизмы обеспечения и передачи дочерним клеткам генетической информации. Механизмы изменчивости
- •35. Органеллы бактериальной клетки. Функциональное назначение органелл
- •Особенности клеточной стенки грамположительных бактерий
- •Особенности клеточной стенки грамотрицательных бактерий
- •5. Жгутики
- •36. Особенности биологии вирусов. Принципы классификации вирусов
- •37. Особенности противовирусного иммунитета
- •38. Отличительные черты риккетсий. Методы культивирования. Риккетсиозы, общая характеристика.
- •39. Патогенность и вирулентность бактерий. Факторы вирулентности. Генетические основы распространения факторов вирулентности среди бактерий.
- •40. Понятие о морфологических свойствах микроорганизмов. Морфологические группы бактерий.
- •41.Понятие об инфекции. 3 участника инфекционного процесса. 3 звена эпидемической цепи
- •3 Участника инфекционного процесса:
- •3 Звена эпидемической цепи:
- •42. Предмет и задачи медицинской микробиологии и иммунологии. Вклад российских ученых в развитии микробиологии и иммунологии.
- •43. Предмет и современные задачи санитарной микробиологии. Санитарно-показательные микроорганизмы. Их значение для оценки безопасности объектов окружающей среды и продуктов питания
- •44. Принципы классификации инфекционных заболеваний.
- •45. Противогрибковые препараты.
- •46. Различия в строении микроорганизмов прокариот и эукариот
- •47. Реакция агглютинации. Компоненты, механизм, способы постановки. Применение.
- •48. Реакция иммунофлюоресценции. Механизм, типы, компоненты, применение для индикации антигенов и иммунодиагностики
- •49. Реакция нейтрализации токсина антитоксином. Механизм. Способы постановки, применение
- •51.Роль врожденного и приобретенного иммунитета в развитии инфекции
- •52. Рост и размножение бактерий в искусственных условиях. Фазы размножения
- •53. Спирохеты. Характеристика. Особенности строения. Роль в патологии человека
- •54. Стерилизация, способы, аппаратура
- •Физические:
- •Химические:
- •Механические:
- •55. Строение бактериального генома. Хромосомные и внехромосомные элементы. Подвижные элементы. Умеренные бактериофаги и их роль в изменчивости генома
- •56. Структура и функции клеточной стенки бактерий. Особенности строения клеточной стенки грамположительных и грамотрицательных бактерий.
- •57. Тинкториальные свойства бактерий. Цели и методы окраски
- •Источник: Mikrobiologia_Zverev, khoroshie_lektsii_po_mikre
- •58. Типы и механизмы питания бактерий. Классификация бактерий по используемым источникам углерода и энергии. Прототрофы и ауксотрофы
- •59. Токсины бактерий, их природа и свойства. Получение и применение экзо- и эндотоксинов.
- •60. Транспорт веществ в бактериальную клетку. Экскреция высокомолекулярных соединений из бактериальной клетки
- •Секреция продуктов жизнедеятельности бактериальной клеткой
- •61. Ферменты бактерий. Роль ферментов в патогенности бактерий Идентификация бактерий по ферментативной активности
- •62. Чистые культуры микроорганизмов. Принципы и методы выделения
- •63. Энергетический метаболизм у бактерий. Типы энергетического метаболизма. Типы дыхания.
- •64. Этапы взаимодействия вирусов с чувствительными клетками и факторы, способные их нарушить. Формы вирусной инфекции.
- •1. Аденовирусная инфекция. Характеристика возбудителей. Лабораторная диагностика.
- •4. Вирусы герпеса. Классификация, значение в патологии человека. Профилактика
- •5. Вирусы экхо и Коксаки, вызываемые ими заболевания. Лабораторная диагностика энтеровирусных инфекций.
- •Коксаки Coxsackievirus
- •Экхо есно (Enteric Cytopathic Human Orphan)
- •7. Возбудители анаэробной газовой инфекции. Характеристика. Лабораторная диагностика. Специфическая и неспецифическая профилактика. Принципы лечения
- •Характеристика возбудителей
- •C. Septicum (палочка Гона-Сакса)
- •Эпидемиология
- •Патогенез
- •Клиника
- •Иммунитет
- •Лабораторная диагностика
- •Профилактика
- •Лечение
- •8. Возбудители бруцеллеза. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •9.Возбудители брюшного тифа и паратифов. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •10. Возбудители возвратных тифов. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения
- •11. Возбудители гнойно-септических инфекций. Принципы лабораторной диагностики.
- •Возбудители гси
- •Принципы лабораторной диагностики гси, вызванных аэробными и факультативно-анаэробными бактериями
- •Лабораторная диагностика анаэробных инфекций
- •Аэробные грамположительные кокки
- •12.Возбудители гриппа. Характеристика. Лабораторная диагностика. Специфическая профилактика.
- •Характеристика
- •Вирус гриппа а
- •1.Геном.
- •2.Морфология
- •5.Методы культивирования.
- •6.Резистентность
- •Лабороторная диагностика.
- •Специфическая профилактика
- •Вирус гриппа в
- •Вирус гриппа с
- •13. Возбудители кишечного иерсиниоза и псевдотуберкулеза. Характеристика. Лабораторная диагностика. Профилактика
- •14. Возбудители коклюша и паракоклюша. Характеристика. Лабораторная диагностика. Специфическая профилактика
- •15. Возбудители микобактериозов. Морфология, особенности строения микобактериальной клетки). Распространенность. Лабораторная диагностика
- •16. Возбудители микозов кожи и ее придатков
- •Дерматофиты
- •Возбудители разноцветного лишая и других поверхностных микозов
- •17. Возбудители орви. Общая характеристика. Принципы диагностики, профилактики и лечения.
- •18. Возбудители пищевых токсикоинфекций. Лабораторная диагностик.
- •19. Возбудители сальмонеллезных гастроэнтеритов. Характеристика возбудителей. Лабораторная диагностика. Профилактика. Принципы лечения
- •20. Возбудители пищевых токсикоинфекций. Лабораторная диагностика.
- •21. Возбудители туберкулеза. Классификация. Особенности микобактериальной клетки. Распространенность.
- •22. Возбудители хламидиозов. Характеристика. Лабораторная диагностика. Принципы лечения
- •23. Возбудители шигеллезов. Характеристика. Лабораторная диагностика. Специфическая профилактика и принципы лечения
- •24. Возбудители эшерихиозов. Характеристика. Лабораторная диагностика эшерихиозов
- •25. Возбудитель бешенства. Характеристика. Патогенез. Специфическая профилактика.
- •26. Возбудитель ботулизма. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •Источник: лекции 21 года и Коваленко
- •28. Возбудитель кампилобактериоза. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения.
- •29. Возбудитель клещевого энцефалита. Характеристика
- •30. Возбудитель кори. Характеристика. Лабораторная диагностика. Специфическая профилактика
- •Профилактика. Для профилактики кори используют вакцины:
- •31. Возбудитель краснухи. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •32. Возбудитель Ку-лихорадки. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •33. Возбудитель паротита. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •34. Возбудитель сибирской язвы. Характеристика. Лабораторная диагностика. Специфическая профилактика Принципы лечения
- •35. Возбудитель сифилиса. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения.
- •38. Возбудитель чумы. Характеристика. Лабораторная диагностика. Специфическая профилактика Принципы лечения
- •39. Гонококки. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения
- •40. Классификация микозов по локализации инфекционного процесса
- •41. Криптококкоз. Возбудители. Лабораторная диагностика криптококкоза
- •43. Микологический метод диагностики микозов. Методы идентификации дрожжей и нитчатых грибов.
- •44. Микоплазмы. Биологические свойства, особенности строения. Роль в патологии человека. Принципы диагностики и лечения
- •Возбудители урогенитальных микоплазмозов и уреаплазмоза.
- •45. Микоплазмы. Биологические свойства, особенности строения. Роль в патологии человека. Принципы диагностики и лечения.
- •46. Общая характеристика рода Candida. Методы и критерии диагностики.
- •Основные свойства грибов рода Candida:
- •Лабораторная диагностика
- •47. Патогенные и условно-патогенные грибы. Классификация грибов по группам патогенности.
- •49 Стафилококки.Характеристика. Лабораторнаядиагностика стафилококковых инфекций. Стафилококковое носительство
- •50. Стрептококки. Характеристика. Лабораторная диагностика стрептококковых инфекций.
- •1. Назовите возбудителя гриппа.
- •2. Таксономическое положение возбудителя.
- •3. Какова морфология возбудителя?
- •4. Эпидемиология гриппа (источник инфекции, механизм, пути передачи инфекции).
- •5. Каковы основные звенья патогенеза гриппа?
- •Задача 2
- •Задача 3.
- •1. Назовите возбудителя коклюша.
- •2. Назовите факторы вирулентности возбудителя коклюша.
- •3. Эпидемиология коклюша (источник инфекции, механизм, пути передачи инфекции).
- •4. Какие периоды болезни выделяют и какие методы диагностики будут эффективны в каждом? Периоды болезни.
- •5. Профилактика коклюша
- •Задача 4.
- •Задача 5.
- •1. Назовите возбудителя сифилиса. К какой морфологической группе относится возбудитель сифилиса?
- •2. Как называется первичный аффект при сифилисе и место его локализации.
- •3. Опишите морфологические, тинкториальные и культуральные свойства возбудителя сифилиса.
- •4. Эпидемиология сифилиса: источник инфекции, механизм и пути передачи инфекции.
- •Задача 6.
- •Задача 7.
- •1. Кто из обследованных сотрудников хирургического отделения является носителем патогенного стафилококка?
- •2. По каким признакам проводится идентификация s.Aureus?
- •3. С какой целью проводилось фаготипирование s.Aureus?
- •4. Кто из обследованных лиц мог быть источником послеоперационных осложнений у больных?
- •5. Какие меры необходимо срочно принять для прекращения распространения данной внутрибольничной инфекции?
- •Задача 8.
- •Задача 9.
- •1. Какой микроорганизм чаще всего вызывает данное заболевание?
- •3. Основной метод диагностики гси? Какой материал может использоваться для исследования?
- •4. Какие препараты помимо антибиотиков можно применять для специфической терапии?
- •5. Какие другие заболевания еще может вызывать данный возбудитель: специфические и неспецифические?
- •Задача 10.
- •Задача 11.
- •Задача 12.
- •1. Назовите возбудителя названного заболевания, его таксономическое положение, морфологические и тинкториальные свойства.
- •2. Эпидемиология менингита: источник инфекции, входные ворота, механизм, факторы и пути передачи инфекции.
- •3. Какие формы инфекции существуют и их эпидемиологическое значение?
- •4. Какой материал нужно взять для микробиологического исследования? Основные методы микробиологического исследования?
- •5. Проводится ли специфическая профилактика названного заболевания?
- •Задача 13.
- •1. Назовите род и вид основного возбудителя туберкулеза у человека.
- •2. Морфологические и тинкториальные свойства возбудителя туберкулеза.
- •3. В чем особенность строения клеточной стенки возбудителя туберкулеза, и какую они играют роль в диагностических приемах?
- •4. Какой метод окраски применяется для выделения возбудителя туберкулеза?
- •5. Профилактика туберкулеза.
- •Задача 14
- •Задача 15.
- •Задача 16
- •Задача 17.
- •1. К какой группе микробов относится возбудитель краснухи?
- •2. К чему приводит заражение женщин в первые 4 месяца беременности?
- •3. Эпидемиология краснухи (источник инфекции, механизм, пути передачи инфекции).
- •4. Методы лабораторной диагностики краснухи и характер исследуемого материала.
- •5. Специфическая профилактика краснухи.
- •Задача 18.
- •Задача 19
- •1. Назовите возбудителя и инфекционного паротита.
- •2. Какое лабораторное исследование было назначено?
- •3. Эпидемиология данного заболевания (источник инфекции, механизм, пути передачи инфекции).
- •4. Какие осложнения данного заболевания?
- •5. Какова профилактика данного заболевания?
- •Задача 20.
- •1. Какое/ие инфекционное заболевание можно предположить в данном случае?
- •2. С чем необходимо дифференцировать заболевание?
- •3. Какие дополнительные исследования следует провести для уточнения этиологического диагноза?
- •4. Нужно ли в данном случае назначить антифунгальные препараты?
- •5. Нужна ли изоляция больного для предотвращения распространения инфекции?
- •Задача 22. (эту задачу я еще уточню у преподавателя)
- •5. Каковы принципы лечения инфекции?
- •Задача 23.
- •Задача 24.
- •Задача 25.
- •1. Назовите возбудителя/лей газовой гангрены
- •2. Особенности биологии возбудителя.
- •3. Какова причина возникновения подобного осложнения?
- •4. Какие факторы способствуют развитию газовой гангрены?
- •5. Какой материал необходимо взять на исследование и какие лабораторные методы могут применяться для диагностики данного заболевания?
- •Задача 26.
- •1. Как называется группа микроорганизмов, в норме населяющих тело человека?
- •2. При каких условиях микроорганизмы данной группы могут вызывать заболевания у человека?
- •3. Какой главный критерий диагностики при выделении данных микроорганизмов?
- •4. Какова роль микроорганизмов этой группы в возникновении внутрибольничных инфекций?
- •5. Какими особенностями обладают госпитальные штаммы микроорганизмов?
- •Задача 27
- •Задача 28.
- •1. Назовите возбудителя скарлатины?
- •2. Факторы вирулентности данного микроорганизма, чем он отличается от представителей того же вида?
- •3. Каковы основные осложнения нелеченой скарлатины?
- •4. Каковы принципы лечения скарлатины?
- •5. Назовите основные методы диагностики скарлатины.
- •Задача 29.
- •Задача 30.
- •1. Что содержится в препарате?
- •2. Как получен препарат?
- •3. Показания к применению и способ применения.
- •4. Механизм противовирусного действия препарата.
- •5. Клинический эффект от применения препарата.
- •Задача 31.
- •Задача 32.
- •1. Что содержится в препарате?
- •2. Как получают нистатин?
- •3. Показания и способ применения
- •4. Механизм действия
- •5.Клинический эффект применения нистатина
- •Задача 33.
- •1. К какой группе относится препарат флуконазол?
- •2. Как получают флуконазол?
- •3. Механизм действия флуконазола на клетки грибов.
- •4. Показания и способы применения препарата
- •5. Клинический эффект от применения препарата.
- •Задача 34.
- •1. Что содержит препарат?
- •2. Как получен биопрепарат?
- •3. Что означает адсорбированный?
- •4. Для чего используется данный препарат?
- •Задача 35.
- •Задача 36.
- •Задача 37.
- •1. Для чего он используется препарат? Что он содержит?
- •2. Как получен биопрепарат?
- •3. Механизм действия препарата.
- •4. Дайте характеристику иммунитета при введении данного препарата.
- •5. Схема введения вакцины?
- •Задача 38.
- •5. О чем говорит отрицательный, положительный и гиперергический результат пробы?
- •Задача 39.
- •Задача 40.
- •Задача 41
- •Задача 42.
- •Действующее вещество:
- •5. Объясните достигаемый эффект после введения препарата.
- •Задача 43
- •Задача 44
- •1. К какой группе относится данный препарат?
- •2. Что содержит препарат?
- •3. Каков механизм действия препарата?
- •4. Как применяют препарат?
- •5. Укажите противопоказания к применению препарата
- •2. При нарушении функции почек
- •Задача 45.
- •5. Опишите достигаемый эффект после введения препарата.
- •Задача 48.
- •Задача 49.
- •Задача 50.
- •Задача 51.
- •Задача 52
- •Задача 53.
- •1. К какой группе относится данный препарат?
- •2. Что содержит данный препарат?
- •3. Как получен данный препарат?
- •4. Какова причина, по Вашему мнению, состояния больного?
- •5. В чем состоит профилактика последствий подобных травм?
- •Задача 54.
- •Задача 55.
- •1. Какой препарат следует назначить для коррекции данного дисбиотического состояния? к какой группе он относится?
- •2. Что содержит данный препарат?
- •3. Как получен и как применяется данный препарат?
- •4. Объясните предполагаемый механизм действия препарата.
- •5. Какие еще группы препаратов могут применяться при коррекции дисбиозов?
- •Задача 56.
- •Задача 57.
- •1. К какой группе относится данный биопрепарат?
- •2. Что содержит данный биопрепарат?
- •3. Как получен данный препарат?
- •4. Кому рекомендуют вакцинацию «Пневмо – 23»?
- •5. Дайте характеристику иммунитета, возникающего после введения данной вакцины.
- •Задача 58.
- •1. К какой группе относится данный препарат?
- •2. Что содержит данный препарат?
- •3. Как получен препарат?
- •4. Каковы показания для вакцинации, схема вакцинации?
- •Задача 59.
- •Задача 60.
- •Задача 61.
- •Задача 62.
- •1. К какой группе относится данный биопрепарат?
- •2. Что содержит биопрепарат?
- •3. Как получен биопрепарат?
- •4. Для чего применяется препарат?
- •5. Схема использования и учета результата
- •Задача 63
- •1)К какой группе относится препарат «интести-бактериофаг»?
- •2)Что содержит препарат«интести-бактериофаг»?
- •3)Как получен«интести-бактериофаг»?
- •4)Для чего используется «интести-бактериофаг»?
- •5)Возможный способ введения препарата?
- •Задача 64.
- •Задача 65.
- •Задача 66
- •Задача 67.
- •1. Какой (какие) возбудитель(и) при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя?
- •3. Какой материал, помимо мокроты, можно взять для исследования?
- •Задача 68.
- •Задача 69
- •1. Какой (какие) возбудитель(и) при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя.
- •3. Особенности подготовки мокроты для микроскопии.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика данной инфекции
- •Задача 70.
- •1. Какой возбудитель, кроме мбт, при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя.
- •3. Особенности подготовки мокроты для микроскопии.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика данной инфекции
- •Задача 71.
- •Задача 72.
- •Задача 73.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика туберкулеза
- •Задача 74.
- •Задача 75.
- •Задача 76.
- •1. Какие методы лабораторного исследования следует применить для подтверждения диагноза?
- •2. Каковы меры профилактики заболевания у контактных с ним детей?
- •3. Каковы особенности эпидемиологии гепатита а?
- •4. Существует ли специфическая профилактика гепатита а?
- •5. Какой еще гепатит может передаваться таким же механизмом?
- •Задача 77
- •Задача 78
- •1. Какой возбудитель при данной патологии Вы предполагаете?
- •2. Какой диагностический материал может быть исследован в этом случае?
- •3. Факторы вирулентности данного возбудителя.
- •4. Методы лабораторной диагностики.
- •5. Какие осложнения, кроме гломерулонефрита, может вызвать данный возбудитель?
41. Криптококкоз. Возбудители. Лабораторная диагностика криптококкоза
Возбудитель криптококкоза
Возбудителем криптококкоза (европейский бластомикоз, болезнь Буссе-Бушке) является дрожжевой гриб Cryptococcus neoformans. Телеоморфа С. neoformans находится в отделе Basidiomycota. Выделяют два биовара возбудителя: С. neoformans var. neoformans и С. neoformans var. gattii, имеющих разные телеоморфы.
Экология и эпидемиология.
Заболевание распространено повсеместно, но случаи криптококкоза, вызванного С. neoformans var. gattii, встречаются, в основном, в субтропическом и тропическом климате Африки и Юго-Восточной Азии.
Природный источник С. neoformans var. neoformans - почва, содержащая помет голубей, реже гниющие овощи, фрукты, растения. Заболевание встречается у грызунов, домашнего скота, кошек, собак. Птицы не болеют криптококкозом, возможно из-за более высокой температуры тела. С. neoformans var. gattii не выделяется из почвы или помета птиц. Заболевание встречается в тех областях с жарким и влажным климатом, где растут деревья красного эвкалипта.
Заражение происходит при вдыхании содержащихся в пыли мелких клеток гриба, лишенных капсулы, а возможно и базидиоспор совершенной формы. Возможно заражение и другими путями: через поврежденную кожу или слизистые оболочки. Надежного скринингового теста для диагностики криптококкоза нет, поэтому точные сведения о заболеваемости криптококкозом, с учетом стертых форм, отсутствуют.
Морфология и физиология
На агаре Сабуро в стандартных условиях С. neoformans растет медленно, созревает в течение недели. При температуре 30-37oС многие штаммы созревают за 3-4 сут. Колонии С. neoformans плоские или слегка выпуклые, влажные, блестящие, с гладкими краями, вначале кремовые, затем светло-коричневые.
При микроскопии обнаруживают круглые, дрожжевидные почкующиеся клетки. Морфология исследуется на кукурузном агаре, где обнаруживают круглые, размером 4-8 мкм, почкующиеся клетки С. neoformans с толстыми темными стенками.
Для рода Cryptococcus характерны следующие признаки: образование капсулы, отсутствие мицелия, способность ассимилировать инозитол и уреазная активность. Cryptococcus spp. не ферментируют сахара.
Факторы патогенности.
Главным фактором патогенности является мукополисахаридная капсула. С ее помощью возбудитель противостоит фагоцитозу, и подавляет образование ряда цитокинов, в частности фактора некроза опухолей. Кроме того, С. neoformans образует фермент, которого нет у всех остальных болезнетворных грибов: фенолоксидазу, также считаемую фактором патогенности.
Патогенез и иммунитет
Больных криптококкозом можно разделить на две группы: с иммунодефицитом (в основном это ВИЧ-инфекция) и внешне здоровые лица. У последних заболевание часто протекает благоприятно, имеет стертую клиническую картину. Криптококкоз считается СПИД-индикаторным заболеванием.
Защита организма от криптококковой инфекции представлена прежде всего клеточным иммунитетом (Т-лимфоциты и макрофаги). Поэтому тяжелые и диссеминированные формы криптококкоза встречаются у больных с клеточным иммунодефицитом: при ВИЧ-инфекции, и у пациентов, получающих кортикостероидные и цитостатические препараты, при лимфомах, саркоидозе, аутоиммунных заболеваниях.
В начале заболевания происходит инвазия легких, с развитием пневмонии. Обычно пневмония характеризуется благоприятным течением и проходит самостоятельно, но у больных с иммунодефицитом нередко развивается хроническое поражение легких, или происходит гематогенная диссеминация возбудителя, чаще всего в головной мозг, иногда в кожу или кости, еще реже - другие органы. Характерным для поражения ЦНС является длительно протекающий менингит. При отсутствии терапии больные умирают от отека мозга через несколько месяцев.
Лабораторная диагностика
Материалом для исследования служат цереброспинальная жидкость, мокрота и бронхиальные смывы, кровь, моча, экссудат из кожных очагов, биопсированная ткань. Диагноз криптококкоза ставится при обнаружении окруженных капсулой дрожжевых клеток в патологическом материале или ткани, при выделении возбудителя из любой локализации. Цереброспинальную и другие жидкости, мокроту и экссудат окрашивают тушью или нигрозином, чтобы обнаружить капсулу гриба. Перед исследованием мокроты или гноя их следует обработать в 10 % растворе едкого кали. Обнаруживают круглые или овальные, окруженные толстой, толще, чем сами клетки, капсулой. При обычной окраске капсулу можно не заметить из-за ее прозрачности.
Чтобы отличить С. neoformans от других видов Cryptococcus при выделении культуры, а также в целях быстрой идентификации выявляют фенолоксидазную активность на средах с птичьим кормом или кофеиновой кислотой. Для идентификации С. neoformans разработан метод, использующий гибридизацию ДНК. Для дифференцирования С. neoformans var. neoformans от С. neoformans var. gattii, используют среду с L-канаванином-глицином и бромтимолом, а также способность С.neoformans var. gattii ассимилировать D-пролин и образовать продолговатые сигаровидные клетки.
Иммунологическая диагностика.
Иммунологическая диагностика криптококкоза основывается на обнаружении полисахаридного (глюкуроксилманнанового) антигена капсулы, поскольку антитела к криптококкам обнаруживаются только на ранней стадии заболевания. Для обнаружения антигена исследуют спинномозговую жидкость и кровь, а также мочу. Используются тесты латекс-агглютинации и иммуноферментный.
Лечение и профилактика.
В лечении криптококкоза используют амфотерицин В (в том числе его липосомальную форму «амбизом»), флуконазол, флуцитозин, итраконазол и различные комбинации этих препаратов.
42. Лекарственная устойчивость микобактерий туберкулеза. Эпидемиология. Механизмы действия основных противотуберкулезных препаратов и механизмы возникновения устойчивости к ним. Лабораторная диагностика
Лекарственная устойчивость микобактерий – актуальная проблема нынешнего времени. В связи с широким использованием АБ препаратов в терапии у микобактерий развивается к ним резистентность.
Эпидемиология.
Туберкулез распространен повсеместно. Основной источник – больной человек. При туберкулезе легких в 50% случаев отмечается выделение возбудителя во внешнюю среду. Заражение чаще всего происходит при прямом, длительном и тесном контакте здорового человека с больным. Основным механизмом заражения является аэрогенный, а входными воротами – органы дыхания. Пути заражения туберкулезом - воздушно-капельный и воздушно-пылевой. Иногда наблюдается заражение контактно-бытовым путем через поврежденные кожные покровы и слизистые оболочки при использовании предметов больного человека.
Резистентность: высокая, за счет особенностей клеточной стенки – большое содержание липидов и восковой слой. В мокроте – до пяти месяцев. На предметах больного сохраняются также в течение нескольких месяцев. Сохраняются в почве и в воде, при кипячении погибают через 5-7 минут. В пыли пребывают до нескольких дней (до 10). Солнечный свет вызывает их гибель через 1,5 часа, УФЛ – через 2-3 минуты. Устойчивы к действию низких температур, обычных дезинфицирующих средств.
Основным механизмом формирования лекарственной резистентности является селекция мутантов и их адаптация. Резистентность может носить как хромосомный, так и плазмидный характер. Устойчивость также может определяться действием инсерционных (IS) последовательностей. Такие последовательности не несут дополнительной информации, кроме той, которая необходима для их транспозиции. Перемещаясь, они могут изменять функционирование гена, «включать» или «выключать» последовательности, координировать действие других подвижных генетических элементов.
Биохимические механизмы являют собою:
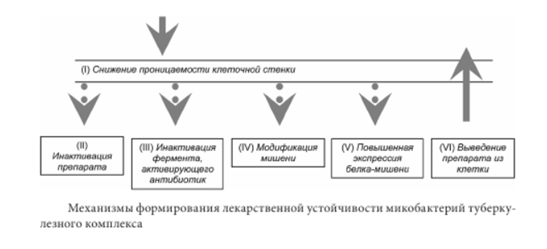
Различают следующие виды лекарственной резистентности у микобактерий:
· Монорезистентность – устойчивость к одному из противотуберкулезных препаратов;
· Полирезистентность – устойчивость к двум и более препаратам;
множественная лекарственная устойчивость (МЛУ) – устойчивость к изониазиду и рифампицину одновременно, независимо от наличия устойчивости к другим препаратам;
· Суперустойчивость (XDR) – множественная лекарственная устойчивость в сочетании с устойчивостью к фторхинолонам и одному из инъекционных препаратов (канамицин, амикацин, капреомицин)
· Перекрестная устойчивость – возникновение устойчивости к одному препарату влечет за собой устойчивость к другим препаратам внутри одной группы.
По происхождению различают первичную и приобретенную лекарственные резистентности: первичной считаются штаммы, выделенные от пациентов, не получавших лечения в течение месяца или более, приобретенной же, соответственно – резистентность, развившаяся на фоне проводимой терапии продолжительностью менее месяца.
Лечение.
1. Препараты первого ряда – изониазид, рифампицин, стрептомицин, пиразинамид, этамбутол. Это препараты выбора, используемые в первую очередь.
2. Препараты второго ряда – этионамид, циклосерин, капреомицин, канамицин, офлоксацин, ципрофлоксацин, амикацин, протионамид. Используются при лекарственной резистентности
3. Резервные препараты – рифабутин, клофазимид, кларитромицин, амоксициллин, фтивазид, флуренизид, тиацитазон.
Самой высокой активностью обладают изониазид и рифампицин
Изониазид - ингибирует синтез миколовых кислот, важного компонента клеточной стенки обеспечивающего патогенность микобактерий),
Рифампицин (антибиотик, ингибирующий РНК-полимеразу (ингибирование транскрипции РНК))
Стрептомицин ингибирует синтез белков, присоединяясь к 30S субъединице рибосом.
Этамбутол, пиразинамид – бактериостатическое действие, (Видаль их механизмов не ведает)
Для уменьшения вероятности возникновения лекарственной резистентности применяют четырех- и пятикомпонентные схемы лечения, включающие препараты с разными механизмами действия. Общими механизмами действия при этом считаются действие на клеточную стенку, на синтез АТФ и белка.
Диагностика.
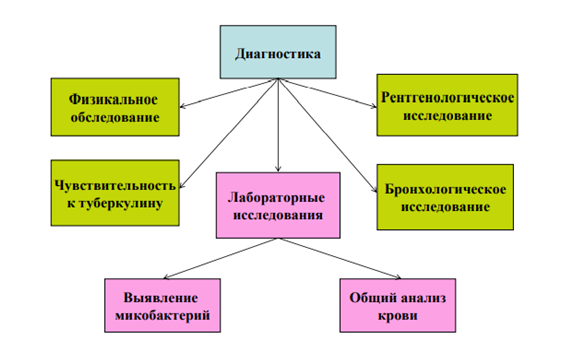
Для лабораторной диагностики туберкулеза применяют практически все доступные методы исследования.
Основными методами диагностики туберкулеза являются:
- бактериоскопический метод (световая и люминесцентная микроскопия);
- бактериологический метод.
Дополнительными методами диагностики туберкулеза являются:
- биологический метод;
- серологический метод;
- кожные аллергические пробы;
- ПЦР
Материал для исследования: мокрота, отделяемое из бронхов, свищей, спинномозговая жидкость (СМЖ), моча, испражнения.
Бактериоскопический метод: готовятся мазки, которые окрашивают по методу Циля-Нильсена или флюорохромом, для дальнейшего люминесцентного микроскопирования.В результате исследования в препаратах обнаруживают единичные кислотоустойчивые бактерии. Если концентрация бактерий невеликатогда для их обнаружения используют методы обогащения: центрифугирование и флотацию. Метод центрифугирования подразумевает обработку щелочью с последующим центрифугированием, осадок же микроскопируют. Метод флотации: также начинается с обработки (смесью щелочи и бензола). Пробу встряхивают, а образующаяся пена выносит микобактерии на поверхность. Готовят препарат из пены. При микроскопии неоходимо проводить количественный учет результатов, т.к. количество видимых бактерий прямо соотносится с тяжестью заболевания.
Используется также метод люминесцентной микроскопии. В окуляре микроскопа – светящиеся бактерии, похожие на мицелий грибов
Бактериологический метод: микобактерии весьма требовательны к средам. Для их роста необходимы глицерин, сыворотка крови, яичный желток, факторы роста (витамины группы Б), электролиты.
Материал обрабатывают раствором кислоты, отмывают, высевают на плотные питательные среды и выращивают в течение 2-12 недель.
Опасность культуры определяется по наличию корд-фактора – фактора патогенности микобактерий, являющегося по совместительству миколовой кислотой и компонетом клеточной стенки. При наличии оного при микроскопировании обнаруживаются «жгуты» бактерий.
Существует ускоренный метод культивирования, метод по Прайсу. Материал также обрабатывают, промывают и высеивают на среду с кровью, где культивируют 3-4 дня и окрашивают по Цилю-Нильсену. В окуляре – красные жгуты
Для выращивания микобактерий рекомендуются яичные среды Левенштейна-Йенсена и Финна-2 (шороховатые плотные неровные колонии цвета слоновой кости), а также глицериновые агаровые среды Миддлбрука.
Биологический метод – введение обработанного материала лабораторным животным, тем же морским свинкам, и наблюдение за развитием симптомов туберкулеза.
Аллергические пробы: применяются для определения повышенной чувствительности к туберкулину, возникающей в случае инфицирования или после специфической вакцины.
Из микобактерий туберкулеза получают т.н. сухой очищенный туберкулин, PPD (белковый очищенный дериват). Вводят накожно, внутрикожно в зависимости от реакции
В настоящее время в основном используется проба Манту. Туберкулин вводят внутрикожно, и через 24-72 часа смотрят реакцию. При положительном результате на месте введения образуется небольшой очаг воспаления из-за скопления лимфоцитов, уже сенсибилизированных возбудителем туберкулеза.
Также, из недавнего – диаскинтест, в этом случае внутрикожно вводятся рекомбинантные белки.
Серологические методы: (НЕ ОСНОВНОЙ МЕТОД ДИАГНОСТИКИ) включают:
- РСК, РА, РПГА, РНГА;
- ИФА;
- РИФ с моноклональными антителами.
Также может использоваться ПЦР-реакция.
