
- •1. Аллергические пробы in vivo и in vitro, их сущность, применение.
- •2. Анатоксины. Получение, применение. Антитоксический иммунитет
- •3. Антибактериальные препараты. Классификация. Механизмы антибактериального действия. Механизмы возникновения и распространения устойчивости.
- •Классификация, которую Козлова указала у себя в презентации:
- •3)По типу взаимодействия с микробной клеткой:
- •4)По кислотоустойчивости антимикробные препараты классифицируются на:
- •5. Бактериологический метод диагностики. Требования к выращиванию бактерий в искусственных условиях.
- •6. Бактериоскопический метод диагностики, его задачи и возможности. Методы микроскопии и их применение.
- •7. Бактериофаги. Взаимодействие фага с бактериальной клеткой. Умеренные и вирулентные бактериофаги. Лизогения.
- •8. Бактериофаги. Получение, титрование. Практическое применение в диагностике, профилактике и лечение
- •9. Вакцины Вакцинопрофилактика и вакцинотерапия
- •10. Внутривидовое типирование бактерий. Методы. Использование в практике
- •11. Врожденный иммунитет. Фагоцитоз. Показатели фагоцитоза
- •14 Грибы. Строение клетки. Классификация грибов по морфологии таллома.
- •15. Действие физических и химических факторов на микроорганизмы. Использование в практике.
- •16. Дисбиозы. Препараты для восстановления микробиоты
- •17 Иммунодиагностика (серодиагностика) инфекционных заболеваний. Принципы и диагностические критерии.
- •18. Иммунопрофилактика, иммунотерапия. Осложнения: анафилактический шок, сывороточная болезнь. Их предупреждение
- •19. Иммуноферментный анализ, иммуноблоттинг. Принципы методов, используемые реагенты и оборудование, применение.
- •20. История микробиологии. Этапы развития. Современные задачи.
- •21. Культивирование бактерий in vitro. Требования к условиям культивирования. Питательные среды, их классификация. Требования, предъявляемые к питательным средам
- •Условия культивирования бактерий:
- •Требования к питательным средам:
- •Классификация
- •Примеры сред
- •22. Методы культивирования вирусов. Вирусологический метод, основные этапы.
- •23. Методы микроскопического исследования (световая, люминесцентная, темнопольная, фазово-контрастная, электронная микроскопия)
- •24. Методы определения чувствительности бактерий к антибиотикам. Мпк (мик) и мбк. Критерии определения бактериальных изолятов как чувствительные, устойчивые, умеренно чувствительные
- •Достоинства метода
- •Недостатки метода
- •28. Механизмы формирования и распространения устойчивости к антибактериальным препаратам бактерий – возбудителей инфекционных болезней
- •29. Микробиота желудочно-кишечного тракта человека
- •30. Микробиота урогенитального тракта человека
- •31. Моноклональные антитела. Получение. Использование
- •32. Морфология микроорганизмов. Морфологические группы бактерий
- •33. Нагрузочные серологические реакции. Реакции непрямой гемагглютинации. Компоненты. Применение
- •34. Наследственность и изменчивость у бактерий. Механизмы обеспечения и передачи дочерним клеткам генетической информации. Механизмы изменчивости
- •35. Органеллы бактериальной клетки. Функциональное назначение органелл
- •Особенности клеточной стенки грамположительных бактерий
- •Особенности клеточной стенки грамотрицательных бактерий
- •5. Жгутики
- •36. Особенности биологии вирусов. Принципы классификации вирусов
- •37. Особенности противовирусного иммунитета
- •38. Отличительные черты риккетсий. Методы культивирования. Риккетсиозы, общая характеристика.
- •39. Патогенность и вирулентность бактерий. Факторы вирулентности. Генетические основы распространения факторов вирулентности среди бактерий.
- •40. Понятие о морфологических свойствах микроорганизмов. Морфологические группы бактерий.
- •41.Понятие об инфекции. 3 участника инфекционного процесса. 3 звена эпидемической цепи
- •3 Участника инфекционного процесса:
- •3 Звена эпидемической цепи:
- •42. Предмет и задачи медицинской микробиологии и иммунологии. Вклад российских ученых в развитии микробиологии и иммунологии.
- •43. Предмет и современные задачи санитарной микробиологии. Санитарно-показательные микроорганизмы. Их значение для оценки безопасности объектов окружающей среды и продуктов питания
- •44. Принципы классификации инфекционных заболеваний.
- •45. Противогрибковые препараты.
- •46. Различия в строении микроорганизмов прокариот и эукариот
- •47. Реакция агглютинации. Компоненты, механизм, способы постановки. Применение.
- •48. Реакция иммунофлюоресценции. Механизм, типы, компоненты, применение для индикации антигенов и иммунодиагностики
- •49. Реакция нейтрализации токсина антитоксином. Механизм. Способы постановки, применение
- •51.Роль врожденного и приобретенного иммунитета в развитии инфекции
- •52. Рост и размножение бактерий в искусственных условиях. Фазы размножения
- •53. Спирохеты. Характеристика. Особенности строения. Роль в патологии человека
- •54. Стерилизация, способы, аппаратура
- •Физические:
- •Химические:
- •Механические:
- •55. Строение бактериального генома. Хромосомные и внехромосомные элементы. Подвижные элементы. Умеренные бактериофаги и их роль в изменчивости генома
- •56. Структура и функции клеточной стенки бактерий. Особенности строения клеточной стенки грамположительных и грамотрицательных бактерий.
- •57. Тинкториальные свойства бактерий. Цели и методы окраски
- •Источник: Mikrobiologia_Zverev, khoroshie_lektsii_po_mikre
- •58. Типы и механизмы питания бактерий. Классификация бактерий по используемым источникам углерода и энергии. Прототрофы и ауксотрофы
- •59. Токсины бактерий, их природа и свойства. Получение и применение экзо- и эндотоксинов.
- •60. Транспорт веществ в бактериальную клетку. Экскреция высокомолекулярных соединений из бактериальной клетки
- •Секреция продуктов жизнедеятельности бактериальной клеткой
- •61. Ферменты бактерий. Роль ферментов в патогенности бактерий Идентификация бактерий по ферментативной активности
- •62. Чистые культуры микроорганизмов. Принципы и методы выделения
- •63. Энергетический метаболизм у бактерий. Типы энергетического метаболизма. Типы дыхания.
- •64. Этапы взаимодействия вирусов с чувствительными клетками и факторы, способные их нарушить. Формы вирусной инфекции.
- •1. Аденовирусная инфекция. Характеристика возбудителей. Лабораторная диагностика.
- •4. Вирусы герпеса. Классификация, значение в патологии человека. Профилактика
- •5. Вирусы экхо и Коксаки, вызываемые ими заболевания. Лабораторная диагностика энтеровирусных инфекций.
- •Коксаки Coxsackievirus
- •Экхо есно (Enteric Cytopathic Human Orphan)
- •7. Возбудители анаэробной газовой инфекции. Характеристика. Лабораторная диагностика. Специфическая и неспецифическая профилактика. Принципы лечения
- •Характеристика возбудителей
- •C. Septicum (палочка Гона-Сакса)
- •Эпидемиология
- •Патогенез
- •Клиника
- •Иммунитет
- •Лабораторная диагностика
- •Профилактика
- •Лечение
- •8. Возбудители бруцеллеза. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •9.Возбудители брюшного тифа и паратифов. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •10. Возбудители возвратных тифов. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения
- •11. Возбудители гнойно-септических инфекций. Принципы лабораторной диагностики.
- •Возбудители гси
- •Принципы лабораторной диагностики гси, вызванных аэробными и факультативно-анаэробными бактериями
- •Лабораторная диагностика анаэробных инфекций
- •Аэробные грамположительные кокки
- •12.Возбудители гриппа. Характеристика. Лабораторная диагностика. Специфическая профилактика.
- •Характеристика
- •Вирус гриппа а
- •1.Геном.
- •2.Морфология
- •5.Методы культивирования.
- •6.Резистентность
- •Лабороторная диагностика.
- •Специфическая профилактика
- •Вирус гриппа в
- •Вирус гриппа с
- •13. Возбудители кишечного иерсиниоза и псевдотуберкулеза. Характеристика. Лабораторная диагностика. Профилактика
- •14. Возбудители коклюша и паракоклюша. Характеристика. Лабораторная диагностика. Специфическая профилактика
- •15. Возбудители микобактериозов. Морфология, особенности строения микобактериальной клетки). Распространенность. Лабораторная диагностика
- •16. Возбудители микозов кожи и ее придатков
- •Дерматофиты
- •Возбудители разноцветного лишая и других поверхностных микозов
- •17. Возбудители орви. Общая характеристика. Принципы диагностики, профилактики и лечения.
- •18. Возбудители пищевых токсикоинфекций. Лабораторная диагностик.
- •19. Возбудители сальмонеллезных гастроэнтеритов. Характеристика возбудителей. Лабораторная диагностика. Профилактика. Принципы лечения
- •20. Возбудители пищевых токсикоинфекций. Лабораторная диагностика.
- •21. Возбудители туберкулеза. Классификация. Особенности микобактериальной клетки. Распространенность.
- •22. Возбудители хламидиозов. Характеристика. Лабораторная диагностика. Принципы лечения
- •23. Возбудители шигеллезов. Характеристика. Лабораторная диагностика. Специфическая профилактика и принципы лечения
- •24. Возбудители эшерихиозов. Характеристика. Лабораторная диагностика эшерихиозов
- •25. Возбудитель бешенства. Характеристика. Патогенез. Специфическая профилактика.
- •26. Возбудитель ботулизма. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •Источник: лекции 21 года и Коваленко
- •28. Возбудитель кампилобактериоза. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения.
- •29. Возбудитель клещевого энцефалита. Характеристика
- •30. Возбудитель кори. Характеристика. Лабораторная диагностика. Специфическая профилактика
- •Профилактика. Для профилактики кори используют вакцины:
- •31. Возбудитель краснухи. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •32. Возбудитель Ку-лихорадки. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения
- •33. Возбудитель паротита. Характеристика. Лабораторная диагностика. Специфическая профилактика. Принципы лечения.
- •34. Возбудитель сибирской язвы. Характеристика. Лабораторная диагностика. Специфическая профилактика Принципы лечения
- •35. Возбудитель сифилиса. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения.
- •38. Возбудитель чумы. Характеристика. Лабораторная диагностика. Специфическая профилактика Принципы лечения
- •39. Гонококки. Характеристика. Лабораторная диагностика. Профилактика. Принципы лечения
- •40. Классификация микозов по локализации инфекционного процесса
- •41. Криптококкоз. Возбудители. Лабораторная диагностика криптококкоза
- •43. Микологический метод диагностики микозов. Методы идентификации дрожжей и нитчатых грибов.
- •44. Микоплазмы. Биологические свойства, особенности строения. Роль в патологии человека. Принципы диагностики и лечения
- •Возбудители урогенитальных микоплазмозов и уреаплазмоза.
- •45. Микоплазмы. Биологические свойства, особенности строения. Роль в патологии человека. Принципы диагностики и лечения.
- •46. Общая характеристика рода Candida. Методы и критерии диагностики.
- •Основные свойства грибов рода Candida:
- •Лабораторная диагностика
- •47. Патогенные и условно-патогенные грибы. Классификация грибов по группам патогенности.
- •49 Стафилококки.Характеристика. Лабораторнаядиагностика стафилококковых инфекций. Стафилококковое носительство
- •50. Стрептококки. Характеристика. Лабораторная диагностика стрептококковых инфекций.
- •1. Назовите возбудителя гриппа.
- •2. Таксономическое положение возбудителя.
- •3. Какова морфология возбудителя?
- •4. Эпидемиология гриппа (источник инфекции, механизм, пути передачи инфекции).
- •5. Каковы основные звенья патогенеза гриппа?
- •Задача 2
- •Задача 3.
- •1. Назовите возбудителя коклюша.
- •2. Назовите факторы вирулентности возбудителя коклюша.
- •3. Эпидемиология коклюша (источник инфекции, механизм, пути передачи инфекции).
- •4. Какие периоды болезни выделяют и какие методы диагностики будут эффективны в каждом? Периоды болезни.
- •5. Профилактика коклюша
- •Задача 4.
- •Задача 5.
- •1. Назовите возбудителя сифилиса. К какой морфологической группе относится возбудитель сифилиса?
- •2. Как называется первичный аффект при сифилисе и место его локализации.
- •3. Опишите морфологические, тинкториальные и культуральные свойства возбудителя сифилиса.
- •4. Эпидемиология сифилиса: источник инфекции, механизм и пути передачи инфекции.
- •Задача 6.
- •Задача 7.
- •1. Кто из обследованных сотрудников хирургического отделения является носителем патогенного стафилококка?
- •2. По каким признакам проводится идентификация s.Aureus?
- •3. С какой целью проводилось фаготипирование s.Aureus?
- •4. Кто из обследованных лиц мог быть источником послеоперационных осложнений у больных?
- •5. Какие меры необходимо срочно принять для прекращения распространения данной внутрибольничной инфекции?
- •Задача 8.
- •Задача 9.
- •1. Какой микроорганизм чаще всего вызывает данное заболевание?
- •3. Основной метод диагностики гси? Какой материал может использоваться для исследования?
- •4. Какие препараты помимо антибиотиков можно применять для специфической терапии?
- •5. Какие другие заболевания еще может вызывать данный возбудитель: специфические и неспецифические?
- •Задача 10.
- •Задача 11.
- •Задача 12.
- •1. Назовите возбудителя названного заболевания, его таксономическое положение, морфологические и тинкториальные свойства.
- •2. Эпидемиология менингита: источник инфекции, входные ворота, механизм, факторы и пути передачи инфекции.
- •3. Какие формы инфекции существуют и их эпидемиологическое значение?
- •4. Какой материал нужно взять для микробиологического исследования? Основные методы микробиологического исследования?
- •5. Проводится ли специфическая профилактика названного заболевания?
- •Задача 13.
- •1. Назовите род и вид основного возбудителя туберкулеза у человека.
- •2. Морфологические и тинкториальные свойства возбудителя туберкулеза.
- •3. В чем особенность строения клеточной стенки возбудителя туберкулеза, и какую они играют роль в диагностических приемах?
- •4. Какой метод окраски применяется для выделения возбудителя туберкулеза?
- •5. Профилактика туберкулеза.
- •Задача 14
- •Задача 15.
- •Задача 16
- •Задача 17.
- •1. К какой группе микробов относится возбудитель краснухи?
- •2. К чему приводит заражение женщин в первые 4 месяца беременности?
- •3. Эпидемиология краснухи (источник инфекции, механизм, пути передачи инфекции).
- •4. Методы лабораторной диагностики краснухи и характер исследуемого материала.
- •5. Специфическая профилактика краснухи.
- •Задача 18.
- •Задача 19
- •1. Назовите возбудителя и инфекционного паротита.
- •2. Какое лабораторное исследование было назначено?
- •3. Эпидемиология данного заболевания (источник инфекции, механизм, пути передачи инфекции).
- •4. Какие осложнения данного заболевания?
- •5. Какова профилактика данного заболевания?
- •Задача 20.
- •1. Какое/ие инфекционное заболевание можно предположить в данном случае?
- •2. С чем необходимо дифференцировать заболевание?
- •3. Какие дополнительные исследования следует провести для уточнения этиологического диагноза?
- •4. Нужно ли в данном случае назначить антифунгальные препараты?
- •5. Нужна ли изоляция больного для предотвращения распространения инфекции?
- •Задача 22. (эту задачу я еще уточню у преподавателя)
- •5. Каковы принципы лечения инфекции?
- •Задача 23.
- •Задача 24.
- •Задача 25.
- •1. Назовите возбудителя/лей газовой гангрены
- •2. Особенности биологии возбудителя.
- •3. Какова причина возникновения подобного осложнения?
- •4. Какие факторы способствуют развитию газовой гангрены?
- •5. Какой материал необходимо взять на исследование и какие лабораторные методы могут применяться для диагностики данного заболевания?
- •Задача 26.
- •1. Как называется группа микроорганизмов, в норме населяющих тело человека?
- •2. При каких условиях микроорганизмы данной группы могут вызывать заболевания у человека?
- •3. Какой главный критерий диагностики при выделении данных микроорганизмов?
- •4. Какова роль микроорганизмов этой группы в возникновении внутрибольничных инфекций?
- •5. Какими особенностями обладают госпитальные штаммы микроорганизмов?
- •Задача 27
- •Задача 28.
- •1. Назовите возбудителя скарлатины?
- •2. Факторы вирулентности данного микроорганизма, чем он отличается от представителей того же вида?
- •3. Каковы основные осложнения нелеченой скарлатины?
- •4. Каковы принципы лечения скарлатины?
- •5. Назовите основные методы диагностики скарлатины.
- •Задача 29.
- •Задача 30.
- •1. Что содержится в препарате?
- •2. Как получен препарат?
- •3. Показания к применению и способ применения.
- •4. Механизм противовирусного действия препарата.
- •5. Клинический эффект от применения препарата.
- •Задача 31.
- •Задача 32.
- •1. Что содержится в препарате?
- •2. Как получают нистатин?
- •3. Показания и способ применения
- •4. Механизм действия
- •5.Клинический эффект применения нистатина
- •Задача 33.
- •1. К какой группе относится препарат флуконазол?
- •2. Как получают флуконазол?
- •3. Механизм действия флуконазола на клетки грибов.
- •4. Показания и способы применения препарата
- •5. Клинический эффект от применения препарата.
- •Задача 34.
- •1. Что содержит препарат?
- •2. Как получен биопрепарат?
- •3. Что означает адсорбированный?
- •4. Для чего используется данный препарат?
- •Задача 35.
- •Задача 36.
- •Задача 37.
- •1. Для чего он используется препарат? Что он содержит?
- •2. Как получен биопрепарат?
- •3. Механизм действия препарата.
- •4. Дайте характеристику иммунитета при введении данного препарата.
- •5. Схема введения вакцины?
- •Задача 38.
- •5. О чем говорит отрицательный, положительный и гиперергический результат пробы?
- •Задача 39.
- •Задача 40.
- •Задача 41
- •Задача 42.
- •Действующее вещество:
- •5. Объясните достигаемый эффект после введения препарата.
- •Задача 43
- •Задача 44
- •1. К какой группе относится данный препарат?
- •2. Что содержит препарат?
- •3. Каков механизм действия препарата?
- •4. Как применяют препарат?
- •5. Укажите противопоказания к применению препарата
- •2. При нарушении функции почек
- •Задача 45.
- •5. Опишите достигаемый эффект после введения препарата.
- •Задача 48.
- •Задача 49.
- •Задача 50.
- •Задача 51.
- •Задача 52
- •Задача 53.
- •1. К какой группе относится данный препарат?
- •2. Что содержит данный препарат?
- •3. Как получен данный препарат?
- •4. Какова причина, по Вашему мнению, состояния больного?
- •5. В чем состоит профилактика последствий подобных травм?
- •Задача 54.
- •Задача 55.
- •1. Какой препарат следует назначить для коррекции данного дисбиотического состояния? к какой группе он относится?
- •2. Что содержит данный препарат?
- •3. Как получен и как применяется данный препарат?
- •4. Объясните предполагаемый механизм действия препарата.
- •5. Какие еще группы препаратов могут применяться при коррекции дисбиозов?
- •Задача 56.
- •Задача 57.
- •1. К какой группе относится данный биопрепарат?
- •2. Что содержит данный биопрепарат?
- •3. Как получен данный препарат?
- •4. Кому рекомендуют вакцинацию «Пневмо – 23»?
- •5. Дайте характеристику иммунитета, возникающего после введения данной вакцины.
- •Задача 58.
- •1. К какой группе относится данный препарат?
- •2. Что содержит данный препарат?
- •3. Как получен препарат?
- •4. Каковы показания для вакцинации, схема вакцинации?
- •Задача 59.
- •Задача 60.
- •Задача 61.
- •Задача 62.
- •1. К какой группе относится данный биопрепарат?
- •2. Что содержит биопрепарат?
- •3. Как получен биопрепарат?
- •4. Для чего применяется препарат?
- •5. Схема использования и учета результата
- •Задача 63
- •1)К какой группе относится препарат «интести-бактериофаг»?
- •2)Что содержит препарат«интести-бактериофаг»?
- •3)Как получен«интести-бактериофаг»?
- •4)Для чего используется «интести-бактериофаг»?
- •5)Возможный способ введения препарата?
- •Задача 64.
- •Задача 65.
- •Задача 66
- •Задача 67.
- •1. Какой (какие) возбудитель(и) при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя?
- •3. Какой материал, помимо мокроты, можно взять для исследования?
- •Задача 68.
- •Задача 69
- •1. Какой (какие) возбудитель(и) при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя.
- •3. Особенности подготовки мокроты для микроскопии.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика данной инфекции
- •Задача 70.
- •1. Какой возбудитель, кроме мбт, при данной патологии Вы предполагаете?
- •2. Факторы вирулентности возбудителя.
- •3. Особенности подготовки мокроты для микроскопии.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика данной инфекции
- •Задача 71.
- •Задача 72.
- •Задача 73.
- •4. Какие лабораторные методы исследования должны применяться в этом случае?
- •5. Профилактика туберкулеза
- •Задача 74.
- •Задача 75.
- •Задача 76.
- •1. Какие методы лабораторного исследования следует применить для подтверждения диагноза?
- •2. Каковы меры профилактики заболевания у контактных с ним детей?
- •3. Каковы особенности эпидемиологии гепатита а?
- •4. Существует ли специфическая профилактика гепатита а?
- •5. Какой еще гепатит может передаваться таким же механизмом?
- •Задача 77
- •Задача 78
- •1. Какой возбудитель при данной патологии Вы предполагаете?
- •2. Какой диагностический материал может быть исследован в этом случае?
- •3. Факторы вирулентности данного возбудителя.
- •4. Методы лабораторной диагностики.
- •5. Какие осложнения, кроме гломерулонефрита, может вызвать данный возбудитель?
1. Аденовирусная инфекция. Характеристика возбудителей. Лабораторная диагностика.
Семейство Adenoviridae включает пять родов:
· Mastadenivirus (вирусы млекопитающих) – только они имеют медицинское значение, остальные так для интереса.
· Aviadenovirus (вирусы птиц), Atadenovirus (геном этих вирусов обогащен А-Т-парами)
· Siadenovirus (содержит ген сиалидазы)
· Ichtadenovirus (вирусы рыб)
Известно более 100 серотипов, из которых около 50 патогенны для людей. Наиболее типично субклиническое и инаппарантное течение аденовирусной инфекции, связанное с поражением респираторной, гастроинтестинальной и зрительной систем.
Вирион аденовирусов имеет форму икосаэдра (диаметр 90 нм). Оболочки нет. Капсид заключает двунитевую линейную ДНК, связанную с белками. Капсид состоит из 252 капсомеров, из них 240 (гексоны) образуют грани, 12 (пентоны) образуют вершины капсида; От каждого пентона отходит гликопротеиновая нить (фибрилла), которая является прикрепительным белком и гемагглютинином. Аденовирусы человека делят на шесть групп (A–F).
Антигенная структура:
• нуклеокапсид – комплементсвязывающий антиген, идентичный у всех сероваров;
• А-антиген (гексоны) – группоспецифический антиген;
• В-антиген (пентоны) – антиген подгрупп (всего 3);
• С-антиген (фибры) – типоспецифический (определяет серовар).
Репродукция. Прикрепляются к рецепторам поверхности клетки с помощью гликопротеиновых фибрилл. Проникает в клетку клатринопосредованным эндоцитозом. Депротеинизация вирионов начинается в цитоплазме и заканчивается в ядре клетки. Репликация вирусной ДНК происходит в ядре клетки. Белки капсида образуются в цитоплазме и затем транспортируются в ядро, где собираются вирионы. Вирус выходит из клетки в результате ее дегенерации и лизиса. Возможна латентная инфекция (в лимфоидных клетках).
Жизненный цикл (по порядку):
ü адсорбция с помощью фибров
ü проникновение
ü депротеинизация НК у ядерной мембраны и проникновение в ядро
ü синтез мРНК РНК-полимеразой
ü синтез ранних вирусоспецифических белков
ü репликация вирусной ДНК
ü репликация поздних мРНК
ü синтез поздних вирусных белков
ü выход из клетки с ее лизисом
Эпидемиология. Источником инфекции являются больные люди с острой или латентной формой заболевания. Чаще болеют дети до 14 лет. Механизмы распространения — респираторный и контактный. Кишечные аденовирусы имеют фекально-оральный механизм передачи. Заболеваемость характеризуется осенне-зимней сезонностью. Отмечаются вспышки и спорадическая заболеваемость.
В окружающей среде аденовирусы более устойчивы, чем большинство других вирусов человека. Они инактивируются при 56 qС в течение 30 мин; сохраняют активность в течение 7 сут при 36–37 qС, сохраняются при лиофилизации; устойчивы при рН 5,0–9,0.
Инкубационный период составляет 4–5 суток. Первичная репродукция аденовирусов происходит в эпителиальных клетках слизистой оболочки дыхательных путей и кишечника, в конъюнктиве глаза и в лимфоидной ткани (миндалины и мезентериальные узлы). После появления первых симптомов возникает короткая вирусемия.
По типу поражений клеток различают:
· продуктивная инфекция сопровождается гибелью клетки после выхода из нее до 1 млн вирионов (у некоторых хозяев наблюдается низкий выход вирионов — низкопродуктивная инфекция, либо абортивная инфекция);
· персистирующая инфекция (протекающая хронически, бессимптомно) возможна при замедленной скорости репродукции вируса, что позволяет клеткам исправлять повреждения, наносимые вирусом;
· трансформирующая инфекция возникает при заражении аденовирусами человека новорожденных мышей, крыс, хомяков; у них возникают опухоли.
Клиника: Аденовирусы — одни из возбудителей ОРВИ, катаральные проявления, фарингоконъюнктивиты, возможно тяжелое воспаление роговицы с потерей зрения. У детей младшего возраста могут развиваться гастроэнтериты. В закрытых организованных коллективах (школьники, военнослужащие) возможны эпидемические вспышки с тяжелыми осложнениями (пневмония, энцефалит). К редким аденовирусным инфекциям относятся менингоэнцефалиты и геморрагические циститы. Иммунитет — типоспецифический, клеточно-гуморальный, стойкий.
Диагностика: В зависимости от клинической формы болезни исследуют отделяемое носоглотки, зева, конъюнктивы и фекалии. Возможно выделение аденовирусов на культуре эпителиальных клеток человека (ЦПД, внутриядерные включения) и идентификация с помощью РИФ (экспресс метод), ИФА, РСК, РН, ИФМ. Серологический метод: с помощью РСК, РН, РНГА определяют нарастание титра антител в сыворотке крови. Молекулярно-генетический метод: ДНК вируса выявляют с помощью ПЦР. Специфическая идентификация по РТГА и РН.
Лечение симптоматическое, возможно применение рибавирина, интерферона и его индукторов. Разработаны пероральные живые тривалентные вакцины, назначаются по эпидпоказаниям.
2. Актиномицеты. Актиномикозы, диагностика и принципы лечения
Морфология. Род Actynomyces Ветвящиеся бактерии.
Ветвящиеся грамположительные некислотоустойчивые неспорообразующие бактерии. Они полиморфны и могут быть палочковидной неправильной формы, прямыми или слегка изогнутыми с утолщениями на концах.
В мазках располагаются одиночно, парами Y-, V-образно или в виде палисада. Часто образуют нити длиной 10–50 мкм и хорошо развитый истинный несептированный мицелий (у одних видов — длинный редко ветвящийся, у других — короткий и сильноветвящийся).
Не содержат в клеточной стенке хитина, стенка имеет строение грамположительных бактерий. Мицелий имеет вид тонких прямых палочек, образуют нити.
Все морфологические формы способны к истинному ветвлению, особенно на тиогликолевой полужидкой среде. По Граму окрашиваются плохо, часто образуют зернистые либо четкообразные формы; некислотоустойчивы.
Типовой вид — Actinomyces bovis.
Культуральные свойства: Облигатные и факультативные анаэробы. Капнофилы (6–10% СО2). Для хорошего роста необходимы среды, содержащие витамин K3, гемин, 5% СО2. Растут на тиогликолевой среде, сердечно-мозговом бульоне, агаре Шелдона. Растут медленно, посевы следует культивировать 7 сут. Температурный оптимум роста 37 С. Некоторые штаммы дают α-β-гемолиз на средах с кровью. Некоторые виды формируют нитчатые микроколонии, напоминающие мицелий, на 7е сутки образуют S-формы колоний, иногда окрашенные в желтый/красный цвет. A odontolyticus на кровяном агаре образует красные колонии с зоной β-гемолиза.
Биохимическая активность. Хемоорганотрофы. Ферментируют углеводы образованием кислоты без газа, продукты ферментации — уксусная, муравьиная, молочная и янтарная кислоты. Наличие каталазы и способность восстанавливать нитраты в нитриты, индол не образуют.
Антигенная структура. В ИФА выделяют 6 cepoгpyпп: A, B, C, D, E и F
Чувствительность к антимикробным препаратам. Чувствительны к пенициллинам, тетрациклину, эритромицину, но резистентны к антимикотикам. Чувствительны к действию обычно применяемых антисептиков и дезинфектантов.
Эпидемиология: Источник инфекции — почва. Механизм передачи — контактный, а путь передачи — раневой. Наиболее часто отмечается эндогенный путь инфекции. Характерна множественность механизмов, путей и факторов передачи. Восприимчивость к актиномицетам, как ко всем условно-патогенным микробам, низкая. Колонизируют слизистую оболочку полости рта человека и млекопитающих.
Патогенез. Вызывают оппортунистическую инфекцию. Наиболее частым возбудителем которой является A. israelii.
Вокруг возбудителя формируются уплотнения, которые постепенно размягчаются с образованием множественных абсцессов, сливающихся между собой. В гное и тканях образуются «серные» гранулы (тельца Боллингера) — сферические бледно-желтые шаровидные частицы диаметром 1–2 мм, содержащие друзы микроба. Характерно распространение воспалительного процесса по направлению к поверхности кожи с образованием свищей. Одновременно отмечается фиброз. В образовании нагноений также играет роль присоединение вторичной, преимущественно стафилококковой инфекции. Антигены актиномицетов приводят к специфической сенсибилизации и аллергической перестройке организма.
Клиника. Актиномикоз.
Актиномицеты вызывают актиномикоз — хроническое гнойно-воспалительное заболевание с образованием гранулем.
Микробиологическая диагностика: Материал для исследования - мокрота, ликвор, гной из свищей, биопсия тканей.
Для диагностики используют бактериоскопический, бактериологический, серологический и аллергологический методы.
По обнаружению в исследуемом материале друз актиномицетов, имеющих вид мелких желтоватых или серовато-белых зернышек с зеленоватым отливом. По Граму споры окрашиваются в темно-фиолетовый, мицелий — в фиолетовый, а друзы — в розовый цвет.
Для подавления роста сопутствующей микрофлоры гной и мокроту перед посевом центрифугируют в растворе пенициллина и стрептомицина. Засевают на питательные среды (сахарный агар) и культивируют в аэробных и анаэробных условиях. У выделенных культур определяют способность сворачивать и пептонизировать молоко — признак, характерный для актиномицетов. Выделение анаэробных видов подтверждает диагноз актиномикоза.
Для серодиагностики ставят РСК с актинолизатом. Реакция недостаточно специфична, поскольку положительные результаты могут отмечаться при раке легкого и тяжелых нагноительных процессах. Применение в качестве АГ вместо актинолизата внеклеточных белков актиномицетов повышает чувствительность РСК. Этот же АГ можно использовать и для постановки РИГА. Аллергическую пробу проводят с актинолизатом. Диагностическое значение имеют положительные пробы.
Лечение. Лучшие результаты дает сочетание этиотропной терапии (антибиотики) и иммунотерапии актинолизатом. Применение пенициллина, тетрациклина, эритромицина, клиндамицина.
Профилактика. Специфическая профилактика - нет. Неспецифическая - повышение иммунного статуса.
Источники: Mkb_-_teoriaA.pdf, Уч. Микробиология _Зверев
3. Аспергиллез. Морфология возбудителей. Методы и критерии диагностики.
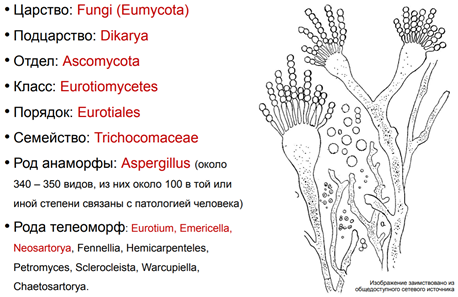
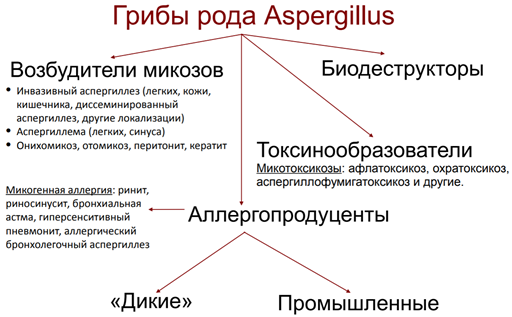
К возбудителям аспергиллеза относят несколько видов несовершенных плесневых грибов из рода Aspergillus. Наиболее часто ими являются следующие виды Aspergillus: A. fumigatus, реже A. flavus, A. niger, A. terreus, еще реже A. glaucus, A. nidulans и другие, всего 15 условно патогенных для человека видов.
Экология и эпидемиология. Все аспергиллы – космополиты, сапрофиты, обитающие в почве, споры этих грибов всегда можно обнаружить в окружающем воздухе, в домашней и строительной пыли. Заболевание распространено повсеместно. Механизм инфицирования аэрогенный, споры гриба попадают на слизистые оболочки дыхательных путей. Гораздо реже заражение происходит в результате травматической имплантации возбудителя – в том числе и при инфицировании мест инъекций, при хирургических вмешательствах. Внутрибольничные вспышки аспергиллеза возникают, как правило, там, где рядом с больницей или внутри нее проводятся строительные работы, во время которых вместе со строительной пылью в воздух высвобождается огромное количество спор. Описаны внутрибольничные вспышки, причиной которых было загрязнение аспергиллами систем вентиляции, кондиционеров. С грибами рода Aspergillus встречаются чаще люди следующих профессий: сельскохозяйственные рабочие, птицеводы, строители, мусорщики, работники хлопкоочистительных и ткацких фабрик, ферментных производств.
Морфология и физиология. Грибы рода Aspergillus растут очень быстро, их колонии созревают за 3–4 сут. Типичные колонии вначале светлые, а затем темнеют. Колонии A. fumigatus имеют серые с зеленоватым или синеватым оттенком, A. flavus – желтые, A. niger – черные при созревании конидий.
Характерным для всего рода Aspergillus является конидиальная головка. Конидиеносец располагается на особой клетке-ножке. Верхушка конидиеносца утолщена, на ней в один или несколько рядов располагаются конидиогенные клетки-фиалиды, а на них образуются округлые конидии. Виды Aspergillus различают по особенностям взаиморасположения фиалид и конидий.
Aspergillus fumigatus и многие другие аспергиллы – термотолерантные грибы, способные расти при 40(С более высоких температурах. Для идентификации аспергилл используется специальная синтетическая среда Чапека-Докса.
Факторы патогенности. Среди факторов патогенности аспергилл выделяют инвазивный рост, способность выживать во внутренней среде человека и наличие ферментов-протеиназ, в частности – кератиназ и эластазы, способной разрушать эластические волокна легких. A. flavus является токсигенным, выделяя экзотоксины (афлотоксины, или флавотоксины)
Патогенез и иммунитет. Попадание спор Aspergillus на слизистые оболочки дыхательных путей само не приводит к разрушению тканей. Прорастание спор контролируется макрофагами, и локальная недостаточность их функции позволяет колонизацию слизистой. При СПИД описана особая изолированная форма инфекции – аспергиллез бронхов. Нейтропения различного происхождения – основная причина развития инвазивных и диссеминированных форм аспергиллеза. При достаточном числе нейтрофилов проникшие грибы Aspergillus могут колонизировать, без инвазии, поверхности измененных в результате предшествовавшего патологического процесса тканей, а также существующие (придаточные пазухи носа), или сформировавшиеся в результате другого заболевания полости. Так развивается аспергиллема. Контакт с антигенами Aspergillus может привести к развитию аллергии – инфекционно-зависимой бронхиальной астме (реакции гиперчувствительности I типа), экзогенному аллергическому альвеолиту (реакции IV типа) и аллергическому бронхолегочному аспергиллезу (реакции I и III, а возможно, и IV типа).
Гифы Aspergillus обладают свойством прорастать стенки сосудов, вызывая тромбозы, кровотечения. В части случаев инвазивного аспергиллеза легких наступает гематогенная диссеминация – в головной мозг, почки, сердце, кости, кожу и другие органы. Диссеминация может возникать не только из очагов в легких, но и при травматической имплантации возбудителя – через кожу, роговицу глаза, при оперативных вмешательствах. Грибы рода Aspergillus вызывают также кератомикозы, возникающие вследствие травмы глаза, и отомикозы – поражения наружного слухового прохода.
Лабораторная диагностика. Материалом для исследования служат: при легочном аспергиллезе – мокрота, смывы с бронхов; при диссеминированных поражениях – кровь, биоптаты, а также моча и спинномозговая жидкость. Можно использовать также смывы из пазух носа, соскобы с некротических поражений кожи. Выделенный в культуре гриб, принадлежащий к роду Aspergillus, не всегда означает лабораторное подтверждение диагноза аспергиллеза, поскольку грибы рода Aspergillus являются самыми распространенными контаминантами культуры. Культура гриба, полученная при посеве материала из стерильных сред (кровь, ликвор), обычно является результатом загрязнения из воздуха. Диагностическое значение имеет обнаружение или выделение Aspergillus spp. из мокроты пациента с выраженной нейтропенией, входящего в группу риска (больные лейкозами, получающие цитостатическую и кортикостероидную терапию), в этом случае немедленно назначается лечение.
ЗВЕРЕВ

РЯБИНИН

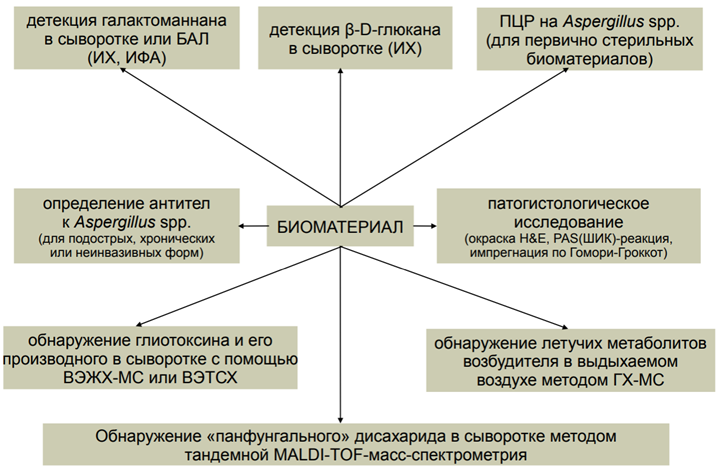
Иммунологическая диагностика. В диагностике инвазивных и аллергических форм аспергиллемы, используется обнаружение антител методом иммунопреципитации: иммунодиффузии в агаре и иммуноэлектрофореза. В диагностике инвазивных и диссеминированных форм аспергиллеза, на фоне нейтропении используют тест на обнаружение растворимого галактоманнанового антигена клеточной стенки Aspergillus, латекс-агглютинации, или иммуноферментный. Кожные пробы с антигенами Aspergillus используются в диагностике аллергических форм. В настоящее время для диагностики аспергиллеза разработана и внедряется методика ПЦР.
Лечение и профилактика. В лечении аспергиллеза используются два препарата: амфотерицин В и итраконазол. Предпочтение отдают новым липидным формам амфотерицина («амбизом»). Проходит испытания каспофунгин («кандикас»). Профилактическое назначение амфотерицина проводят предрасположенным больным при нейтропении. Внутрибольничное инфицирование предупреждается контролем стерильности оборудования и чистоты воздуха.
