
- •1. Основные этапы развития физиологии в мире и в нашей стране. Вклад и.М. Сеченова, и.П. Павлова, а.А. Ухтомского, л.А. Орбели, а.М. Уголева.
- •2. Раздражимость и возбудимость. Возбудимые ткани. Порог возбуждения. Классификация раздражителей. Кривая «силы – длительности. Реобаза и хронаксия. Хронаксиметрия, ее значение для клиники.
- •3. Строение и функции клеточных мембран. Ионные каналы, их классификация. Мембранные рецепторы. Ионные насосы. Вторичные посредники (мессенджеры).
- •4. Транспорт веществ через клеточную мембрану: активный, пассивный. Особенности транспорта водо-и жирорастворимых веществ.
- •7. Потенциал действия и его фазы. Изменение возбудимости в процессе возбуждения. Рефрактерность, ее виды и причины.
- •Билет №11 Гладкие мышцы: структурные и функциональные особенности, классификация, механизм сокращения. Регуляторные белки в гладкомышечных клетках, их функции.
- •Билет №12 Строение и функции нервов. Классификация нервных волокон, их характеристика. Законы проведения возбуждения по нервам. Аксонный транспорт, его физиологическое значение.
- •Билет №13 Механизм проведения возбуждения по безмиелиновым и миелиновым нервным волокнам. Роль перехватов Ранвье. Скорость проведения возбуждения по нервным волокнам.
- •Билет №15 Рецепторы: классификации, свойства. Механизм формирования рецепторного потенциала. Кодирование информации в рецепторах и нервных волокнах.
- •16. Гематоэнцефалический барьер: структура, функции, значение, результаты нарушения целостности. Глия: структура и функции.
- •1) Макроглия
- •2) Микроглия
- •17. Нейрон как структурно-функциональная единица цнс. Виды нейронов. Интегративная функция нейрона.
- •18. Синапсы в цнс: классификация и свойства. Возбуждающий постсинаптический потенциал, его свойства и значение. Возбуждающие медиаторы (нейротрансмиттеры) в цнс.
- •19. Торможение в цнс: виды и механизмы. Роль и.М. Сеченова. Тормозной постсинаптический потенциал, его свойства, значение.
- •1) Пресинаптическое торможение
- •2) Постсинаптическое торможение
- •3)Торможение, не связанное с функцией тормозных синапсов:
- •20. Свойства нервных центров: суммация, трансформация ритма, дивергенция, конвергенция, иррадиация и др. Доминанта, значение работ а.А. Ухтомского.
- •21.Центральное торможение. Тормозные медиаторы цнс, механизмы их действия. Вторичное торможение, его виды и физиологическое значение.
- •22.Координационная деятельность цнс. Рефлекс. Классификация рефлексов. Структура рефлекторной дуги соматической и вегетативной нервной системы. Обратная связь.
- •23.Спинальные рефлексы: классификация, механизмы контроля мышечного тонуса и фазных движений. Спинальный шок, механизм его развития. Проприорецепторы скелетных мышц и их роль в координации рефлексов.
- •24.Спинальные двигательные рефлексы: классификация, характеристика. Сухожильные рефлексы человека и методы их оценки. Реципрокный механизм регуляции движений.
- •26. Мозжечок: афферентные и эфферентные связи, участие в регуляции движений. Методы оценки функций мозжечка.
- •28. Роль среднего мозга в регуляции движений. Рефлексы поддержания позы. Статические и статокинетические рефлексы. Ориентировочные рефлексы.
- •29. Автономная (вегетативная) нервная система: отделы и высшие центры, взаимодействие отделов, тонус центров.
- •30. Симпатический отдел автономной (вегетативной) нервной системы: особенности строения, медиаторы (нейротрансмиттеры), роль в регуляции функций организма.
- •31. Парасимпатический отдел автономной (вегетативной) нервной системы: особенности строения, медиаторы (нейротрансмиттеры), роль в регуляции функций организма.
- •33. Гормоны: классификация, цикл жизни гормона. Обратная связь (определение, значение). Особенности отрицательной и положительной обратных связей (примеры).
- •34. Гипоталамо-гипофизарная система. Рилизинг-гормоны. Гормоны аденогипофиза: химическая природа, классификация, клетки-мишени, эффекты.
- •35. Нейрогипофиз, его связь с гипоталамусом. Гормоны нейрогипофиза: химическая природа, клетки-мишени, эффекты. Регуляция секреции нейрогипофиза.
- •36. Щитовидная железа. Роль йодсодержащих гормонов в организме. Регуляция секреции гормонов щитовидной железы. Основные проявления гипо- и гипертиреоза.
- •37. Гормональный контроль уровня Ca в крови. Роль паратгормона, кальцитонина и производных витамина d.
- •38. Гормоны поджелудочной железы: синтез, химическая природа, эффекты. Регуляция эндокринной функции поджелудочной железы.
- •39. Гормональный контроль уровня глюкозы в крови.
- •40. Гормональный контроль уровня натрия в крови.
- •41. Гормоны коры надпочечников: классификация, химическая природа, эффекты. Регуляция секреции гормонов коры надпочечников.
- •42. Мозговое вещество надпочечников. Симпато-адреналовая система. Регуляция секреции гормонов мозгового вещества надпочечников.
- •43. Мужские половые гормоны: синтез, химическая природа, эффекты. Регуляция секреции мужских половых гормонов.
- •44. Женские половые гормоны: классификация, химическая природа, синтез, эффекты. Женский половой цикл. Регуляция секреции женских половых гормонов. Физиологические основы контрацепции.
- •45. Гормональная регуляция беременности, родов, лактации.
- •46. Система крови. Кровь: количество, состав, функции. Гематокрит. Депо крови и их значение. Методы исследования крови.
- •47. Плазма крови: количество, состав, физико-химические свойства: плотность, осмотическое и онкотическое давления, реакция крови (pH), вязкость.
- •48. Системы групп крови: ab0, Rh и другие. Принцип метода определения групповой принадлежности крови. Принципы переливания крови, кровезамещающие растворы.
- •49. Эритроциты: строение, количество, функции. Гемолиз и его виды. Соэ. Цветовой показатель. Регуляция эритропоэза.
- •50. Лейкоциты: виды, количество, функции. Лейкоцитарная формула. Лейкоцитоз, его виды и значение. Регуляция лейкопоэза.
- •51. Гемоглобин: структура, виды, количество, свойства, соединения, функции. Кривая диссоциации оксигемоглобина и факторы, на нее влияющие.
- •52. Свертывание крови. Факторы, участвующие в свертывании крови. Сосудисто-тромбоцитарный гемостаз.
- •53. Свертывание крови. Факторы, участвующие в свертывании крови. Коагуляционный гемостаз.
- •54. Свертывающая и противосвертывающая системы крови: состав, роль, регуляция и возможные нарушения.
- •55. Свойства сердечной мышцы. Особенности строения клеток проводящей системы и рабочих кардиомиоцитов. Автоматия, градиент автоматии.
- •56. Изменение возбудимости сердечной мышцы в сердечном цикле. Экстрасистола и компенсаторная пауза, механизмы их возникновения. Значение рефрактерности сердца для обеспечения насосной функции.
- •1. Возбудимость миокарда
- •1) Фаза абсолютной рефрактерности
- •2. Значение рефрактерности
- •3. Экстрасистола
- •4. Пояснение компенсаторной паузы
- •57. Свойства сердечной мышцы. Проводящая система сердца: скорость проведения на различных ее участках. Значение для клиники.
- •2) Значение для клиники
- •58. Электрическая активность клеток миокарда. Особенности потенциалов действия клеток проводящей системы и рабочих кардиомиоцитов.
- •59. Электрокардиография: отведения, интервалы, зубцы и сегменты, их происхождение. Электрическая ось сердца. Значение в оценке функций сердца.
- •61. Сердечный цикл и его фазы. Давление крови в камерах сердца в различные фазы. Минутный объем крови в покое и при физической нагрузке.
- •Диастола желудочков
- •62. Клапаны сердца: классификация, значение, положение в разные фазы сердечного цикла. Давление крови в камерах сердца в эти фазы.
- •63. Звуковые явления во время сердечной деятельности. Происхождение тонов сердца. Фонокардиография. Значение для клиники.
- •64. Внутрисердечные регуляторные механизмы: гетеро- и гомеометрический механизмы, внутрисердечные периферические рефлексы.
- •65. Нервная регуляция работы сердца: роль блуждающего и симпатического нервов, их тонус. Влияния на сердце с экстеро- и интерорецепторов. Рефлексогенные зоны. Условно-рефлекторная регуляция сердца.
- •67. Отделы сосудистого русла: функциональная классификация. Давление крови в различных участках сосудистого русла. Факторы, обеспечивающие движение крови и непрерывность кровотока.
- •68. Артериальное давление; факторы, его определяющие. Формула Пуазейля. Давление: систолическое, диастолическое, пульсовое и среднее. Методы определения.
- •69. Артериальный пульс: происхождение, параметры. Методы регистрации (сфигмография). Скорость распространения пульсовой волны по центральным и периферическим артериям.
- •70. Механизмы поддержания артериального давления: нервные и гуморальные; кратковременного, промежуточного и длительного действия. Значение для клиники.
- •1. Кратковременный механизм;
- •2. Промежуточный механизм;
- •3. Длительный механизм.
- •Сопряженные рефлексы
- •2. Понижение фильтрационного давления;
- •3. Стимуляцию процесса реабсорбции;
- •1. Уменьшение сосудистой регуляции и работы сердца;
- •2. Уменьшение объема циркулирующей крови;
- •3. Изменение уровня белка и форменных элементов.
- •71. Особенность движения крови в венах разного калибра, давление крови в венах.
- •72. Основные показатели гемодинамики:
- •73. Особенности кровообращения в:
- •74. Лимфа: состав, механизмы образования, физиологическая роль.
- •75. Микроциркуляция.
- •76. Дыхание: этапы; механизмы вдоха и выдоха. Значение дыхательных мышц в обеспечении внешнего дыхания. Эластическая тяга легких, факторы, ее определяющие. Сурфактант, его значение.
- •81. Транспорт двуокиси углерода кровью: роль эритроцитов и плазмы.
- •82. Регуляция дыхания при физических нагрузках. Роль механо-, проприо- и хеморецепторов; роль дыхательного центра ствола мозга и коры больших полушарий.
- •83. Дыхание в измененных условиях газовой среды (недостаток о2, избыток со2, пониженное и повышенное барометрическое давление). Постоянство состава альвеолярного воздуха.
- •84. Система пищеварения: структура и назначение ее частей. Типы пищеварения (полостное, внутриклеточное, контактное). Пищеварительный конвейер. Методы изучения функций пищеварительного тракта.
- •87. Пищеварение в тонкой кишке: полостное и пристеночное (мембранное). Значение работ а.М.Уголева.
- •88. Кишечный сок: состав и роль в пищеварении (обработка белков, жиров и углеводов). Методы исследования кишечной секреции.
- •89. Моторная функция пищеварительного тракта. Виды моторики. Нарушения моторной функции кишки.
- •90. Регуляция секреции и моторики тонкой кишки: нервная и гуморальная. Всасывание в тонкой кишке. Методы исследования функций тонкой кишки.
- •91. Кишечник как орган внутренней секреции: кишечные гормоны и их роль в регуляции пищевого поведения и пищеварения. Микрофлора толстой кишки и ее значение для организма.
- •92. Панкреатический сок: состав, свойства и роль в пищеварении (обработка белков, жиров и углеводов). Регуляция панкреатической секреции: нервные и гуморальные механизмы.
- •93. Жёлчь: состав, свойства, роль в пищеварении. Жёлчеобразование и жёлчевыделение, их регуляция.
- •94. Моторная функция желудка. Нервные и гуморальные влияния на моторику желудка. Методы исследования. Регуляция перехода химуса из желудка в двенадцатиперстную кишку.
- •95. Моторика тонкой и толстой кишки: виды сокращений, их роль в пищеварении, регуляция моторики, нарушения моторики.
- •96. Голод и насыщение: мозговые центры, нервные и гуморальные воздействия на них, исходящие из желудочно-кишечного тракта. Пищевое поведение.
- •97. Обмен липидов и его нарушения. Регуляция массы тела и ее нарушения: избыточная масса и ожирение. Механизмы похудания.
- •98. Гомеотермия. Терморецепция и роль гипоталамического термостата. Термогенез сократительный и несократительный. Теплоотдача: механизмы, эффективность, регуляция. Гипо- и гипертермия. Лихорадка.
- •100. Требования к пищевому рациону человека. Пластическая и энергетическая роль питательных веществ. Калорический коэффициент питательных веществ. Правило изодинамии, ограниченность его применения.
- •101.Основы рационального питания: роль белков, жиров и углеводов, макро- и микроэлементов, витаминов, пищевых волокон и воды в обмене веществ.
- •102. Выделение. Органы выделения. Функции почек. Методы исследования функций почек.
- •103.Структура нефрона. Процесс мочеобразования: клубочковая фильтрация, канальцевая реабсорбция, канальцевая секреция. Механизмы концентрирования мочи.
- •104.Роль почки в поддержании гомеостаза (изоволюмия, изотония, изоосмия, кислотно-основной баланс). Ренин-ангиотензин-альдостероновая система.
- •105. Регуляция мочеобразования: роль осмо- и волюморецепторов, роль гормонов и механизм их действия. Регуляция мочевыделения.
- •106. Сенсорные системы (анализаторы). Структура: периферический, проводниковый и корковый отделы. Механизмы кодирования информации. Локализация сенсорных функций в коре больших полушарий.
- •107. Зрительная сенсорная система, ее структура. Восприятие света. Цветное зрение и формы его нарушения. Бинокулярное зрение и его значение.
- •108. Слуховая сенсорная система. Роль наружного, среднего и внутреннего уха. Восприятие интенсивности и высоты звуков. Бинауральный слух и его значение.
- •109.Вестибулярная сенсорная система: строение, свойства, функции.
- •2.Проводниковый отдел:
- •3.Центральный (корковый) отдел
- •110. Тактильная и температурная чувствительность (кожный анализатор): рецепторы, проводящие пути, мозговые центры.
- •2) Проводниковый отдел:
- •3) Корковый отдел
- •1)Периферический отдел
- •2) Проводниковый отдел
- •3) Корковый отдел
- •111. Ноцицептивная и антиноцицептивная системы. Теории боли. Виды боли. Принципы обезболивания.
- •112. Распределение функций между правым и левым полушариями мозга. Функциональная асимметрия: сенсорная, моторная. Локализация центров речи.
- •114. Условное торможение, его виды. Механизмы формирования условного торможения. Динамический стереотип, его физиологическая сущность, значение для научения и приобретения трудовых навыков.
- •115. Научение и память. Память кратковременная и долговременная: характеристики и механизмы. Структуры головного мозга, участвующие в формировании долговременной памяти.
- •116. Мышление, сознание, речь: физиологические основы и возможные нарушения. Критерии оценки сознания в клинике.
- •118. Бодрствование и сон. Теории сна. Сон быстрый и медленный, значение фазы rem. Участие структур мозга в поддержании состояния бодрствования и сна. Нарушения сна.
- •119. Эмоции: значение, классификация, механизм формирования. Роль подкорковых образований и коры головного мозга. Вегетативный и моторный компонент эмоций.
- •120. Учение п.К. Анохина о функциональных системах. Функциональная система поведенческого акта. Потребности, мотивации, поведение.
76. Дыхание: этапы; механизмы вдоха и выдоха. Значение дыхательных мышц в обеспечении внешнего дыхания. Эластическая тяга легких, факторы, ее определяющие. Сурфактант, его значение.
Дыхание- это физиологический процесс, обеспечивающий обмен кислородом и углекислым газом между окружающей средой и организмом.
Стадии дыхания:
Внешнее дыхание - обмен кислородом и углекислым газом между окружающей средой и кровью легочных капилляров
Легочная вентиляция – обмен между внешней средой и альвеолами – конвекция (на далекие расстояния, процесс активный с затратой энергии)
Легочная диффузия – газообмен между кровью организма и газовой смесью в легких (на короткие расстояния, менее чем на 0,1 м, процесс пассивный.)
Транспорт газов кровью – путём конвекции;
Тканевая диффузия – обмен кислородом и углекислым газом
Тканевое дыхание – потребление кислорода и выделение углекислого газа
Механизм вдоха:
Возбуждение -> сокращение респираторных мышц;
Сокращение диафрагмы, увеличение вертикального объема грудной клетки (ДО70%);
Диафрагма опускается на 1 см;
Объём лёгких увеличивается;
Внутрилегочное давление уменьшается до -1 мм.рт.ст. – меньше атмосферного;
Воздух по градиенту поступает в альвеолы.
Механизм выдоха:
Расслабление испираторных мышц;
Диафрагма поднимается;
Объём грудной клетки уменьшается;
Объём лёгких уменьшается;
Внутрилегочное давление повышается до +1мм.рт.ст – больше атмосферного.;
Воздух по градиенту выходит из лёгких.
Дыхательные мышцы:
Инспираторные (обеспечивают увеличение объема грудной клетки и легких -> вдох):
Основные: диафрагма, наружные межреберные и межхрящевые;
Вспомогательные: большие и малые грудные, лестничные, ГКС, зубчатые.
Экспираторные (обеспечивают уменьшение грудной клетки и легких -> выдох): внутренние межреберные и мышцы передней брюшной стенки.
Эластическая тяга легких — сила, с которой ткань легкого противодействует атмосферному давлению и обеспечивает спадение альвеол (обусловлена наличием в стенке альвеол большого количества эластических волокон и поверхностным натяжением пленки жидкости, покрывающей внутреннюю поверхность альвеол), т. е. это сила, с которой легкие стремятся сжаться.
Эластическая тяга легких обусловлена 3 факторами:
1.Поверхностным натяжением пленки жидкости, покрывающей внутреннюю поверхность альвеол – сурфактанта;
2.Упругостью ткани стенок альвеол (содержат эластические волокна).
3.Тонусом бронхиальных мышц.
Важным фактором, влияющим на эластические свойства и растяжимость легких, является поверхностное натяжение жидкости в альвеолах. Спадению альвеол препятствует сурфактант, выстилающий внутреннюю поверхность альвеол, препятствующий их спадению, а также выходу жидкости на поверхность альвеол из плазмы капилляров легкого. На любой поверхности раздела между воздухом и жидкостью действуют силы межмолекулярного сцепления, стремящиеся уменьшить величину этой поверхности (силы поверхностного натяжения). Под влиянием этих сил альвеолы стремятся сократиться. Поверхностное натяжение альвеол в 10 раз меньше теоретически рассчитанного натяжения для соответствующей водной поверхности.
Силы поверхностного натяжения создают 2/3 эластической тяги легких. Если заполнить легкие водой, поверхностное натяжение увеличится в 5–8 раз. Следовательно, в состав жидкости, покрывающей внутреннюю поверхность альвеол, входит вещество, снижающее поверхностное натяжение, — сурфактант.
Он представляет собой мономолекулярный слой строго ориентированных молекул поверхностно-активных веществ — липопротеин (90 % составляют липиды, преимущественно фосфолипиды, дипальмитоилфосфатидилхолин — 45 %, фосфатидилхолин — 25 %, фосфатидилглицерол — 5 %, остальные фосфолипиды — 5 %, другие липиды (холестерин, триглицериды, ненасыщенные жирные кислоты, сфигномиелин) — 10 %). Оставшиеся 10 % приходятся на долю белковой фракции, которая представлена белками-апопротеинами.
Сурфактант синтезируется альвеолоцитами 2-го типа, отработанные сурфактанты поглощаются альвеолярными макрофагами и альвеолоцитами 3-го типа. Слой сурфактанта имеет толщину 20–100 нм. Когда легкие растягиваются, пленка сурфактанта становится менее плотной и в меньшей степени уменьшает поверхностное натяжение. При уменьшении размеров альвеол поверхностное натяжение, напротив, уменьшается, что препятствует их спаданию. Нарушение образования или действия сурфактанта сопровождается спадением большого количества альвеол, в результате чего возникает ателектаз (ateles (греч.) — неполный, ektasis (греч.) — расширение) — состояние, при котором обширные участки легких не вентилируются.
Синтез и замена поверхностно-активного вещества — сурфактанта происходит довольно быстро, поэтому нарушение кровотока в легких, воспаление и отеки, курение, острая кислородная недостаточность (гипоксия) или избыток кислорода (гипероксия), а также различные токсические вещества, в том числе некоторые фармакологические препараты (жирорастворимые анестетики), могут снизить его запасы и увеличить поверхностное натяжение жидкости в альвеолах. Все это ведет к их ателектазу, или спадению. В профилактике и лечении ателектазов определенное значение имеют аэрозольные ингаляции лекарственных средств, содержащих фосфолипидный компонент, например лецитин, который способствует восстановлению сурфактанта.
Функции сурфактанта:
обеспечивает расправление легких при первом вдохе новорожденного,
в 10 раз уменьшает силу поверхностного натяжения,
стабилизирует размеры альвеол,
способствует переключению дыхания с одних альвеол на другие,
уменьшает энергозатраты на дыхание,
регулирует водный баланс (влияет на интенсивность испарения воды с альвеолярной поверхности),
способствует сохранению сухой поверхности альвеол,
облегчает диффузию кислорода из альвеол в кровь, обладает бактериостатическим действием (опсонизация бактерий),
оказывает противоотечное, антиокислительное действие,
способствует активизации фагоцитоза альвеолярными макрофагами.
Эластическая тяга грудной клетки создается за счет эластичности межреберных хрящей, мышц, париетальной плевры, структур соединительной ткани, способных сжиматься и расширяться. Благодаря эластической тяге давление в плевральной полости (Рpl) ниже давления в альвеолах (Ра) на величину, ей создаваемую. Поэтому транспульмональное давление (Рt), представляющее собой разность Ра-Рpl , стремится расправить легкие. При вдохе, когда Рpl, как указывалось выше, становится более отрицательным, Рt возрастает. Вследствие этого объем легких увеличивается, а давление в них уменьшается. Когда Ра становистся ниже атмосферного, воздух устремляется в легкие.
Дополнительно:
Неэластическая тяга- сила трения внутри воздушной струи и между потоком воздуха и стенкой дыхательных путей и аэродинамическим сопротивлением.
Величина аэродинамического сопротивления зависит от :
Трения между молекулами газовых смесей;
Вязкости газов;
Длины воздухоносных путей.
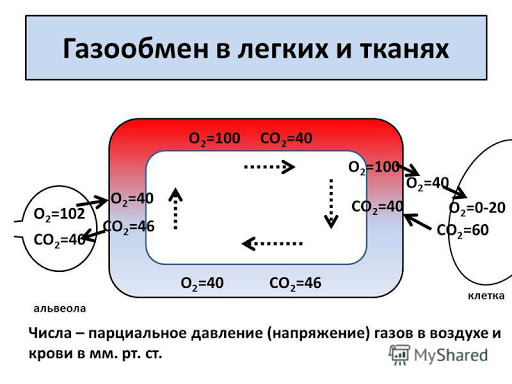
77. Газообмен в легких. Состав атмосферного и альвеолярного воздуха. Диффузия газов в легких. Факторы, определяющие объем диффузии. Напряжение газов в артериальной и венозной крови, тканях. Кислородная емкость крови. Коэффициент утилизации кислорода.
Альвеолярная вентиляция (МВЛ) характеризует газообмен, эффективность внешнего дыхания.
МВЛ=( ДО-АМП) х ЧД
3,5-4,5
л/мин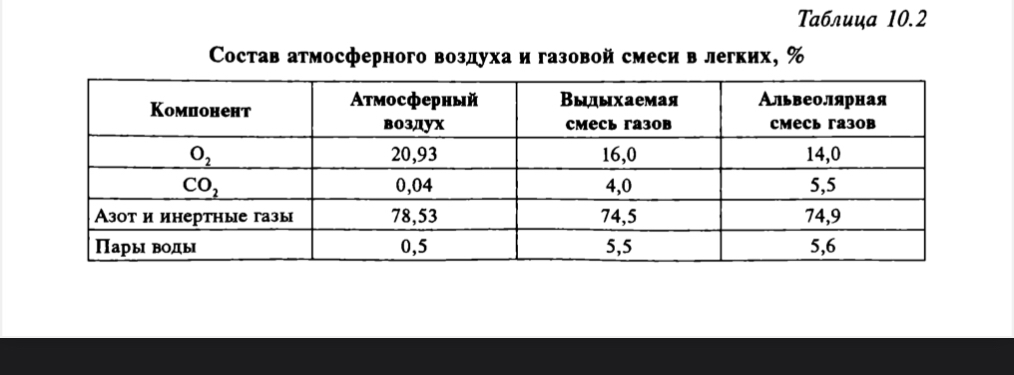
Легочная диффузия – пассивный процесс.
Факторы, способствующие диффузии в тканях лёгких:
Движущая сила, обеспечивающая давление, это градиент парциального давлени.
Большая скорость диффузии (выравнивания парциального давления кислорода в альвеолах и в крови лёгких происходит за 0,25с, кровь в капиллярах находится 0,5 секунд, то есть в 2 раба больше. Скорость диффузии углекислого газа в 20 раз больше таковой кислорода, так как он быстрее диффундирует, что обусловленно его лучшей растворимостью.)
Свойства газа. (Углекислый газ в 20-25 раз диффундирует быстрее, чем кислород, что обусловлено лучшей его растворимостью в жидкости и в мембранах.)
Большая диффузионная поверхность ( контакта легочных капилляров и альвеол 60-120м*2)
Корреляция между кровотоком в данном участке легкого (Q) и его вентиляцией (V).( Если участокплохо вентилируется, то кровеносные сосуды в этой области суживаются и закрываются, это осуществляется с помощью механизмов местной саморегуляции. Благодаря этому поддерживается отношение объема вентиляции лёгких к объёму кровотоков них в норме = 0,8-0,9.
Интенсивность вентиляции и кровообращения различных отделов легких, которая зависит от положения тела : в вертикальном положении лучше вентилируются нижние отделы, в горизонтальном – отделы легких, находящиеся внизу, в положение на спине – дорсальные. Примерно также изменяется кровообращение легких.
Скорость диффузии прямо пропорциальна площади поверхности барьера и градиенту парциального давления газа и обратно пропорциональна толщине барьера.

Кислородная ёмкость крови – это количество кислорода, которое может быть связано с гемоглобином у муж – 180-200мл/л; у жён – на 10-20% меньше.
Главный фактор связывания кислорода с гемоглобином – высокое парциальное давление кислорода в альвеолах – 100 мм рт.ст, в венозной крови парциальное давление = 40 мм рт ст, а в артериальной как в альвеолах.
Вспомогательные факторы: отщепление от карбогемоглобина углекислого газа и удаление его; понижение температуры в легких, увеличение рН крови.
Коэффициент утилизации кислорода – это процентное отношение доли кислорода, использованной тканями (разности концентраций кислорода в артериальной и венозной
Крови в % об.), к его концентрации в артериальной крови (в % об.).
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
.Каждый литр крови, содержащий 180-200 мл кислорода, отдаёт тканям 45мл кислорода – артериовенозная разницапо кислороду. Количество поглощенного кислорода – коэффициент использования кислорода.
78. Показатели внешнего дыхания: легочные объемы и емкости. Методы исследования внешнего дыхания у человека. Типы нарушения вентиляции легких: обструктивный и рестриктивный. Изменения показателей внешнего дыхания при нарушениях вентиляции легких.
Показатели внешнего дыхания:
Легочных объёмы:
Дыхательный объем (ДО) – количество воздуха, который человек вдыхает и выдыхает при спокойном дыхании(500 мл).
•Резервный объем вдоха (Рвд)– количество воздуха, которое человек может дополнительно вдохнуть после спокойного вдоха ( 1500-2500 мл).
•Резервный объем выдоха (Рвыд) – количество воздуха, которое человек может дополнительно выдохнуть после спокойного выдоха ( 1200-1500 мл).
Легочных ёмкости:
Жизненная емкость легких – наибольшее количество воздуха, которое человек может выдохнуть после максимального вдоха
3500-5000 мл
ЖЕЛ= ДО+РОвдоха+Ровыдоха
Функциональная остаточная емкость – количество воздуха, остающееся в легких после спокойного выдоха (2000-3000 мл.).
Это «буфер» между атмосферным и альвеолярным воздухом. Предотвращает выраженные колебания Р о2 и Р со2 в альвеолярном воздухе в течении дыхательного цикла
Емкость вдоха (Ев) – максимальное количество воздуха, которое можно вдохнуть после спокойного выдоха (2000-3000 мл).
Общая емкость легких (ОЕЛ) – количество воздуха, содержащееся в легких после максимального вдоха (4000-6000 мл.)
Остаточный объем (ОО)– количество воздуха, остающееся в легких после максимального выдоха (1000-1500 мл).
Методы исследования внешнего дыхания:
Спирометрия – регистрация легочных объемов (ДО, Ровд и выд, ЖЕЛ)
Спирография – графическая регистрация объемов воздуха, проходящих через легкие (ДО, МОД, МВЛ, ЖЕЛ, РО вд и выд, ИТ);
Пневмотахография – оценка объемной скорости дыхания.
Пнёвмография – графическая регистрация движения грудной клетки во время дыхания (не позволяет оценить легочные объемы)
Типы нарушений легочной вентиляции.
Рестриктивный тип - снижение дыхательных экскурсий легких (разница обхвата легких при вдохе и выдохе).
Причины:поражения легочной паренхимы (фиброз легких, пневмокониоз).
Признак: снижение ЖЕЛ, МВЛ
Обструктивный тип - сужение воздухоносных путей, повышение их аэродинамического сопротивления.
Причины:накопление в дыхательных путях слизи, набухание слизистой оболочки дыхательных путей, спазм бронхиальных мышц.
Признак: снижение индекса Тиффно, МВЛ
Показатели, их характеризующие.
Тест Тиффно- объём форсированного выдоха за секунду.
Индекс Тиффно = ОФВ1/ ЖЕЛ*100%.
В норме ИТ= 70-80%
Показатели: ЧД, МОД, МВЛ.
79. Регуляция внешнего дыхания: дыхательный центр, его структура. Роль периферических и центральных хеморецепторов, рецепторов растяжения легких, ирритантных, юкстакапиллярных рецепторов и мышечных веретен в регуляции параметров дыхания.
Дыхательный центр - совокупность взаимно связанных нейронов ЦНС, обеспечивающих координированную ритмическую деятельность дыхательных мышц и постоянное приспособление внешнего дыхания к изменяющимся условиям внутренней и внешней среды.
• Структуры, ответственные за процесс вдоха и выдоха, находятся в бульбопонтийной области мозга.
Дыхательный центр выполняет две основные функции в системе дыхания:
⎯ моторную, или двигательную, регулирующую сокращения дыхательных мышц
⎯ гомеостатическую, изменяющую характер дыхания при сдвигах содержания О2 и СО2 во внутренней среде организма.
Выделяют следующие части дыхательного центра.
1. Высшие отделы, расположенные выше ствола головного мозга, организуют взаимодействие нижележащих частей дыхательного центра, управляют произвольным дыханием и организуют взаимодействие системы дыхания с другими системами.
2. Пневмотаксический центр переднего моста (с апнейстическим центром) организует взаимодействие двух других структур следующего, нижнего уровня.
3. Медуллярные инспираторный и экспираторный центры (центры вдоха и выдоха), в соответствии с названием, посредством пейсмекернойритмической активности обеспечивают чередование вдоха и выдоха. Это происходит путем организации взаимодействия элементов нижележащего уровня (иерархии структур) дыхательного центра.
4. Мотонейроны спинного мозга, аксоны которых образуют нервы, идущие к дыхательным мышцам. Сами по себе мотонейроны не обладают способностью к осуществлению целостных актов дыхания. Дыхание возможно только при наличии связей совокупности мотонейронов спинного мозга, по крайней мере, с инспираторным и экспираторным центрами продолговатого мозга. При нарушении связей с отделами, расположенными выше продолговатого мозга, ухудшаются приспособительные возможности дыхания. Причем, чем выше локализация нарушения, тем более тонкие адаптационные возможности дыхания утрачиваются.
Центральные хеморецепторы расположены на вентральной поверхности продолговатого мозга и чувствительны к уровню углекислого газа и водородных ионов спинномозговой жидкости. Обеспечивают возбуждение дыхательных нейронов, т.к. поддерживают постоянный афферентный поток и участвуют в регуляции частоты и глубины дыхания при изменении газового состава спинномозговой жидкости.
Периферические рецепторы локализованы в области бифуркации сонной артерии и дуги аорты в специальных гломусах (клубочках). Афферентные волокна идут в составе блуждающего и языкоглоточного нервов в дыхательный центр. Реагируют на снижение напряжения кислорода, повышение уровня углекислого газа и водородных ионов в плазме крови.
Значение: обеспечивают рефлекторное усиление дыхания при изменении газового состава крови.
Вторичночувствующие рецепторы, сосудистые, неадаптирующиеся, всегда активны, увеличивается при изменениях.
Особенно сильным стимулом для хеморецепторов является сочетание гиперкапнии и гипоксемии. Это естественные сдвиги газового состава крови при физической нагрузке, которые приводят к рефлекторному увеличению легочной вентиляции.
Гиперкапния — повышение напряжения углекислого газа в плазме крови.
Гипоксемия — понижение напряжения кислорода в плазме крови.
При гипоксемии рост [H+] в ткани гломусов снижает проницаемость К-каналов мембраны рецепторов → деполяризация → открытие потенциалзависимых Са-каналов и диффузия ионов Сa внутрь клетки.
Са → экзоцитоз ДОФА. В области контакта мембраны рецептора с окончанием чувствительного нервного волокна → активность в волокнах синокаротидного нерва (нерв Геринга — часть языкоглоточного) → к ДЦ через нейроны ядер одиночного пути → рост вентиляции легких.
Рецепторы растяжения легких локализованы в гладкомышечном слое воздухоносных путей (трахея, бронхи), связаны толстыми афферентными миелиновыми волокнами с нейронами дыхательного центра, проходят в составе блуждающего нерва. При вдохе легкие растягиваются и активируются рецепторы растяжения легких, импульсы идут в дыхательный центр, вдох тормозится, а выдох стимулируется. Если перерезать блуждающие нервы, дыхание становится более редким и глубоким.
Значение: регулируют частоту и глубину дыхания, при спокойном дыхании не активны; низкопороговые.
Мощной рефлексогенной зоной является паренхима легких, обеспечивающая не только альвеолярное дыхание, но и рефлекторную регуляцию внешнего дыхания.
Основные типы легочных вагусных афферентов включают: медленноадаптирующиеся рецепторы растяжения альвеол, быстроадаптирующиеся рецепторы, С-волокна.
Важная роль в рефлекторной регуляции дыхания отводится проприорецепторам суставов грудной клетки, межреберных мышц, диафрагмы, сухожильным рецепторам. Недостаточное укорочение инспираторных или экспираторных мышц усиливает импульсацию от мышечных веретен, которая через α-мотонейроны повышает активность α-мотонейронов и дозирует таким образом мышечное усилие.
В регуляции активности бульбарного дыхательного центра и внешнего дыхания принимает участие и афферентация с висцеральных рецепторов и рецепторов кожи, о чем свидетельствует развитие гипервентиляции легких при болевом и термическом раздражении.
B эпителии и субэпителиальном слое воздухоносных путей располагаются рецепторы, получившие название ирритантных. Особенно их много в области корней легких.
Для них характерными являются свойства как механорецепторов, так и хеморецепторов.
Возбуждаются они при очень сильных изменениях (увеличении или уменьшении) объема легких. Порог возбуждения них выше, чем всех остальных рецепторов. Импульсы в афферентных волокнах ирритантныхрецепторов возникают пачками только в течение короткого времени во время изменения объема легких, но часть из них возбуждается и при обычном вдохе и выдохе.
В качестве раздражителей ирритантных рецепторов могут быть:
· пылевые частицы;
· слизь;
· пары едких веществ (табачный дым, аммиак и др.);
· биологически активные вещества, образующиеся в стенках воздухоносных путей (гистамин).
· Они могут сильно раздражаться при ряде заболеваний (отек легких, пневмотораксе, бронхиальной астме и др.).
Раздражение ирритантных рецепторов приводит к:
· возникновению кашля;
· неприятным ощущениям типа жжения или першения;
· усилению инспираторной активности;
· укорачению фазы выдоха;
· увеличению частоты дыхания;
· рефлекторной бронхоконстрикции
J-рецепторы (юкстакапиллярные, юкстаальвеолярные) располагаются вблизи капилляров малого круга кровообращения в интерстициальной ткани альвеол. Афферентные волокна от них относятся к типу С. Точный механизм их участия в регуляции дыхания пока не ясен. Но, полагают, что основным раздражителем I-рецепторов является увеличение объема интерстициальной жидкости в легочной ткани.
Высокая активность J-рецепторов отмечается при:
· пневмониях;
· отеке легких;
· эмболии мелких сосудов легких;
· застое крови в малом круге кровообращения.
Раздражение J-рецепторов приводит к частому и поверхностному дыханию (тахипноэ - одышка) и бронхоконстрикции. В этих процессах наряду с J-рецепторами принимают участие и ирритантные рецепторы.
80. Транспорт кислорода кровью: роль эритроцитов и плазмы, кислородная емкость крови, коэффициент утилизации кислорода. Кривая диссоциации оксигемоглобина; факторы, влияющие на степень диссоциации оксигемоглобина.v
Транспорт О2 осуществляется в физически растворенном и химически связанном виде.
Физические процессы, т. е. растворение газа, не могут обеспечить запросы организма в О2.
Наиболее оптимальным является механизм транспорта О2 в химически связанном виде.
Согласно закону Фика, газообмен О2 между альвеолярным воздухом и кровью происходит благодаря наличию концентрационного градиента О2 между этими средами.
В альвеолах легких парциальное давление О2 составляет 100 мм рт.ст., а в притекающей к легким венозной крови парциальное напряжение О2 составляет примерно 40 мм рт.ст.
Давление газов в воде или в тканях организма обозначают термином «напряжение газов» и обозначают символами Ро2, Рсo2. Градиент О2 на альвеолярно-капиллярной мембране, равный в среднем 60 мм рт.ст., является одним из важнейших, но не единственным, согласно закону Фика, факторов начальной стадии диффузии этого газа из альвеол в кровь.
Транспорт О2 начинается в капиллярах легких после его химического связывания с гемоглобином.
Гемоглобин (Нb) способен избирательно связывать О2 и образовывать оксигемоглобин (НbО2) в зоне высокой концентрации О2 в легких и освобождать молекулярный О2 в области пониженного содержания О2 в тканях. При этом свойства гемоглобина не изменяются, и он может выполнять свою функцию на протяжении длительного времени.
Гемоглобин переносит О2 от легких к тканям.
Эта функция зависит от двух свойств гемоглобина:
1) способности изменяться от восстановленной формы, которая называется дезоксигемоглобином, до окисленной (Нb + О2 à НbО2) с высокой скоростью (полупериод 0,01 с и менее) при нормальном Рог в альвеолярном воздухе;
2) способности отдавать О2 в тканях (НbО2 à Нb + О2) в зависимости от метаболических потребностей клеток организма.
Кислородная емкость крови - это количество кислорода, связанного с гемоглобином, находящимся в 100 мл крови, при его полном насыщении кислородом.
Кислородную емкость крови определяют по концентрации Нb с двухвалентным железом (Fe2+). Максимально 1 моль гемоглобина может присоединить 4 моля О2 к своим 4 молям железа гема.
КУО2 -это процентное отношение доли кислорода, используемой тканями (разности концентраций кислорода в артериальной и венозной крови), к общему содержанию его в артериальной крови:
КУО2 = VO2а- VO2в / VO2а x 100 %
Скорость доставки кислорода в нормальных условиях значительно превышает его потребление, в результате чего лишь малая доля доступного кислорода извлекается из капиллярной крови в обычном состоянии (в покое КУО2 = 25-35%). Это позволяет тканям приспосабливаться к снижению доставки кислорода
Зависимость степени оксигенации гемоглобина от парциального давления Огв альвеолярном воздухе графически представляется в виде кривой диссоциации оксигемоглобина, или сатурационной кривой. Плато кривой диссоциации характерно для насыщенной О2 (сатурированной) артериальной крови, а крутая нисходящая часть кривой — венозной, или десатурированной, крови в тканях.


На сродство кислорода к гемоглобину влияют различные метаболические факторы, что выражается в виде смещения кривой диссоциации влево или вправо.
Сродство гемоглобина к кислороду регулируется важнейшими факторами метаболизма тканей: Ро2 pH, температурой и внутриклеточной концентрацией 2,3-дифосфоглицерата.
Величина рН и содержание СО2 в любой части организма закономерно изменяют сродство гемоглобина к О2: уменьшение рН крови вызывает сдвиг кривой диссоциации соответственно вправо (уменьшается сродство гемоглобина к О2), а увеличение рН крови — сдвиг кривой диссоциации влево (повышается сродство гемоглобина к О2) (см. рис. 8.7, А). Например, рН в эритроцитах на 0,2 единицы ниже, чем в плазме крови. В тканях вследствие повышенного содержания СО2 рН также меньше, чем в плазме крови. Влияние рН на кривую диссоциации оксигемоглобина называется «эффектом Бора».
Рост температуры уменьшает сродство гемоглобина к О2. В работающих мышцах увеличение температуры способствует освобождению О2. Уменьшение температуры тканей или содержания 2,3-дифосфоглицерата вызывает сдвиг влево кривой диссоциации оксигемоглобина.
Метаболические факторы являются основными регуляторами связывания О2 с гемоглобином в капиллярах легких, когда уровень O2, рН и СО2 в крови повышает сродство гемоглобина к О2 по ходу легочных капилляров. В условиях тканей организма эти же факторы метаболизма понижают сродство гемоглобина к О2 и способствуют переходу оксигемоглобина в его восстановленную форму — дезоксигемоглобин. В результате О2 по концентрационному градиенту поступает из крови тканевых капилляров в ткани организма.
Оксид углерода (II) — СО, способен соединяться с атомом железа гемоглобина, изменяя его свойства и реакцию с О2. Очень высокое сродство СО к Нb (в 200 раз выше, чем у О2) блокируют один или более атомов железа в молекуле гема, изменяя сродство Нb к О2.
