
- •Кафедра патофизиология, клиническая патофизиология, 3курс, лечебный факультет, перечень экзаменационных вопросов
- •1. Патофизиология как теоретическая и методологическая база медицины. Предмет и задачи патофизиологии. Основные особенности патофизиологии как научной и учебной дисциплины. Роль эксперимента в развитии патофизиологии и медицины.
- •2. Здоровье и болезнь – основные понятия нозологии. Переходные состояния организма между здоровьем и болезнью (предболезнь).
- •3. Болезнь как диалектическое единство повреждения и адаптивных реакций организма.
- •4. Этиология. Роль причин и условий в возникновении болезней, их диалектическая взаимосвязь. Понятие о внешних и внутренних причинах и факторах риска.
- •5. Патогенез. Причинно-следственные связи в развитии болезни. Понятие о порочном круге патогенеза. Единство функциональных и структурных изменений в патогенезе заболевания.
- •6. Повреждение как начальное звено патогенеза. Проявления повреждения на разных уровнях интеграции организма. Защитные, компенсаторные и восстановительные реакции организма.
- •7. Болезнетворное воздействие факторов внешней среды: действие электрического тока на организм человека.
- •10. Гипоксия. Определение, общая характеристика, классификация гипоксических состояний. Этиология и патогенез различных видов гипоксии.
- •https://docs.google.com/file/d/1L1k9VNrYG_6Rpq-KfVDVvRuDf0T11oxo/edit?filetype=msword
- •11. Защитно-приспособительные реакции при гипоксии. Механизмы срочной и долговременной адаптации к гипоксии. Нарушение обмена веществ и физиологических функций при гипоксии.
- •13. Молекулярные наследственные болезни углеводного и аминокислотного, белкового обмена. Галактоземия, гликогенозы. Фенилкетонурия, альбинизм.
- •15. Нарушение периферического кровообращения. Артериальная гиперемия. Причины, виды, механизмы развития, последствия.
- •16. Нарушение периферического кровообращения. Венозная гиперемия. Причины, виды, механизмы развития, последствия.
- •19. Воспаление. Сущность явления. Причины воспаления. Защитная роль воспаления. Теории воспаления.
- •20. Воспаление. Первичная и вторичная альтерация. Молекулярные механизмы повреждения.
- •22. Воспаление. Сосудистые реакции при воспалении. Экссудация, механизмы развития, роль медиаторов. Значение экссудации.
- •23. Сравнительная патология воспаления (И.И. Мечников). Эмиграция лейкоцитов (L) в очаг воспаления. Фагоцитоз.
- •24. Диалектика защиты и повреждения в процессе развития воспаления.
- •26. Характеристика понятия «ответ острой фазы». Основные цитокины РООФ, их происхождение и биологические эффекты.
- •27. Лихорадка как типовая патологическая реакция. Этиология, патогенез. Изменение теплопродукции и теплоотдачи в разные стадии лихорадки.
- •28. Лихорадка как компонент РООФ. Классификация пирогенов. Механизм реализации эндопирогенов. Биологическое значение лихорадки.
- •29. Отличие лихорадки от экзогенного перегревания и других видов гипертермий.
- •30. Тромботический синдром. Причины, механизмы развития, последствия (тромбоэмболическая болезнь). Патогенез тромбофилий.
- •Причины:
- ••Повреждение стенок сосудов и сердца, приводящее к снижению ее тромборезистентности.
- •Механизмы развития:
- •Механизм тромбофилии состоит в нарушении фибрин-опосредованной активации плазминогена (точнее, усиления его активации тканевым плазминоген-активирующим фактором).
- •К основным механизмам развития тромбофилии относят:
- •Последствия гиперкоагуляции и тромбоза:
- •Патогенез тромбофилий:
- •31. Геморрагический синдром: ангиопатии. Виды, причины, механизмы развития, последствия.
- •33. Геморрагический синдром: коагулопатии. Нарушения свертывания крови в 1,2,3 фазе коагуляции Причины, механизмы развития, последствия.
- •34. Синдром диссеминированного внутрисосудистого свертывания (синдром ДВС). Причины, механизмы развития, стадии, последствия. Принципы патогенетической терапии.
- •35. Гипо- и гипергликемии. Виды, причины, и механизмы развития, последствия.
- •36. Этиология и патогенез сахарного диабета I и II типа. Экспериментальный сахарный диабет. Патогенез острых и хронических осложнений сахарного диабета.
- •37. Метаболический синдром и его характеристика. Общее ожирение. Виды, причины и механизмы развития. Последствия.
- •38. Энергетический обмен организма в состояниях положительного энергетического баланса. Энергетический обмен организма в состояниях отрицательного энергетического баланса.
- •39. Голодание. Виды голодания, стадии полного голодания. Гормоно-субстратные изменения в разные периоды полного голодания.
- •41. Нарушения водно-солевого обмена. Обезвоживание. Причины, механизмы развития, последствия. Роль профессиональных факторов в развитии обезвоживания.
- •42. Гипергидратация. Виды. Патогенез отеков при сердечной недостаточности.
- •43. Отеки. Патогенетические механизмы развития отеков. Патогенез токсического, голодного и почечного отеков.
- •44. Гипо- и гиперволемии. Причины, механизмы развития, последствия.
- •45. Респираторный ацидоз. Причины, механизмы развития. Роль буферных систем и органов в компенсации. Изменение показателей КОБ. Характеристика нарушений при некомпенсированной форме ацидоза.
- •49. Этиология опухолевого процесса. Виды канцерогенов. Эндо- и экзогенные канцерогены (физические, химические, биологические). Механизмы их воздействия.
- •50. Онковирусы. Их классификация. Роль вирусов в канцерогенезе.
- •51. Молекулярные механизмы канцерогенеза. Значение онкогенов в канцерогенезе.
- •52. Механизмы активации протоонкогенов. Роль онкобелков в канцерогенезе. Классификация онкобелков.
- •53. Опухолевый процесс. Определение понятия. Виды опухолей, признаки малигинизации. Понятие о предопухолевом состоянии.
- •54. Атипизм опухолевой ткани. Морфологический, биохимический, функциональный атипизм.
- •55. Механизмы антиканцерогенеза. Механизмы противоопухолевой резистентности организма.
- •56. Механизмы взаимодействия опухоли и организма. Опухолевая кахексия. Паранеопластические синдромы.
- •57. Молекулярные механизмы атеросклероза. Атерогенные дислипопротеидемии. Роль рецепторов к липопротеидам в регуляции обмена холестерина и в атерогенезе.
- •58. Атеросклероз. Значение нарушений нейроэндокринной регуляции в этиологии и патогенезе атеросклероза. Роль социальных факторов в развитии атеросклероза.
- •59. Нейрогенная теория атеросклероза (П.С. Хомуло). Этиология и патогенез. Эмоциональная реакции и эмоциональный стресс. Влияние эмоционального стресса на атерогенез.
- •60. Общая патология нервной системы. Формирование генератора патологически усиленного возбуждения как основной механизм патологической функциональной системы.
- •61. Функциональные нарушения высшей нервной деятельности. Экспериментальные неврозы. Значение типов нервных систем в возникновении неврозов (И.П. Павлов).
- •62. Эмоции и эмоциональные расстройства. Роль психоэмоционального напряжения в развитии соматической патологии.
- •65. Патология щитовидной железы. Классификация функциональных состояний. Эутиреоидное состояние щитовидной железы . Гипо- и гиперфункция щитовидной железы. Причины, признаки, механизмы развития.
- •66. Патология коры надпочечников. Гипо- и гиперфункция. Первичный и вторичный альдостеронизм. Причины, признаки, механизмы развития.
- •68. Значение и механизмы формирования срочной и долговременной адаптации.
- •69. Общий адаптационный синдром. Роль желез внутренней секреции в развитии общего адаптационного синдрома. Стадии стресса.
- •70. Стресс-факторы, стресс-реализующие системы. Механизмы стрессогенного повреждения различных органов и систем.
- •71. Адаптивные и дизадаптивные эффекты гормонов стресса (катехоламины, глюкокортикоиды). Болезни адаптации.
- •72. Стресс-лимитирующие системы. Виды, эффекты.
- •73. Понятие психоэмоционального стресса. Определение, причины, механизмы развития, роль в патогенезе психосоматических заболеваний.
- •74. Иммунодефицитные состояния и аллергия как типовые иммунопатологические процессы. Взаимосвязь аллергии и воспаления, аллергии и иммунитета.
- •75. Первичные (наследственные и врожденные) иммунодефициты. Виды, патогенез, проявления, последствия. Вторичные (приобретенные) иммунодефицитные состояния. Этиология, патогенез, последствия. СПИД, этиология, пути инфицирования, патогенез.
- •76. Аллергия и иммунитет. Общность и различия. Классификация аллергических реакций.
- •2. Патогенная роль реакций цитотоксического типа - реакция из иммунной переходит в аллергическую, повреждает и разрушает ткани, если направлена против клеток, которые стали аутоантигенными.
- •82. Лекарственная аллергия. Условия и механизмы развития.
- •83. Сердечная недостаточность. Определение, причины, классификация, механизмы развития. Интракардиальные механизмы компенсации сердечной недостаточности.
- •84. Недостаточность системы кровообращения. Определение, виды. Гемодинамическая характеристика видов недостаточности кровообращения.
- •85. Компенсаторные механизмы сердца. Понятие о гиперфункциях, виды, механизмы развития. Физическая нагрузка и гиперфункция сердца.
- •86. Острая левожелудочковая сердечная недостаточность. Клинические проявления. Виды, причины, механизмы развития.
- •87. Хроническая сердечная недостаточность. Клинические признаки и механизмы. Механизмы развития сердечной недостаточности при мио-, эндо- и перикардитах. Механизмы развития сердечной недостаточности при эндокринопатиях.
- •88. Коронарная недостаточность. Определение, классификация, причины, клинические проявления.
- •89. Инфаркт миокарда. Причины, механизмы развития, осложнения. ИБС. Определение. Стенокардия, классификация по патогенезу, механизмы развития.
- •93. Хроническая сосудистая недостаточность, гипотоническая болезнь. Определение, классификация, причины, механизмы развития.
- •95. Дизэритропоэтические анемии (железодефицитная, апластическая, сидероахрестическая). Причины, механизмы развития, картина крови.
- •96. Гемолитические анемии. Принципы классификации. Приобретенные и наследственные гемолитические анемии. Причины, механизмы развития, картина крови.
- •97. Острая кровопотеря. Механизмы компенсации. Постгеморрагические анемии (острые, хронические), механизмы развития, картина крови.
- •98. Лейкоцитозы. Классификация. Причины, механизмы развития. Сдвиги лейкоцитарной формулы.
- •99. Лейкемоидные реакции. Виды, этиология, патогенез. Отличие от лейкоза. Значение для организма.
- •100. Лейкозы. Классификации. Этиопатогенез, картина костного мозга и крови при острых и хронических лейкозах.
- •101. Лейкопении. Виды, причины, механизмы развития. Изменения в лейкоцитарной формуле (процентное содержание различных форм к общему числу лейкоцитов).
- •102. Патология внешнего дыхания. Механизм компенсации при нарушении внешнего дыхания. Одышка. Виды. Периодическое и терминальное дыхание. Причины, виды, механизмы развития.
- •103. Хроническая обструктивная болезнь легких (ХОБЛ). Эмфизема легких. Виды. Патогенез нарушения внешнего дыхания при эмфиземе.
- •104. Рестриктивные причины нарушения внешнего дыхания. Пневмоторакс. Виды. Патогенез нарушений внешнего дыхания при пневмотораксе.
- •105. Обструктивные причины нарушения внешнего дыхания. Ателектаз. Виды. Патогенез нарушений внешнего дыхания при ателектазе.
- •106. Нарушение секреторной и моторной функции желудка. Причины, механизмы развития, последствия.
- •107. Нарушение пищеварения в тонком кишечнике. Пристеночное пищеварение и его нарушения. Причины, механизмы развития, последствия.
- •Характеристика билирубинового обмена
- •113. Нефротический синдром. Причины, механизмы развития, последствия, профилактика.
- •114. Острая почечная недостаточность. Формы, этиология, механизмы развития, последствия.
- •115. Хроническая почечная недостаточность. Причины, стадии, механизмы развития. Уремия.
- •116. Гломерулонефриты. Патогенетическая классификация. Клинические проявления, принципы лечения.
- •118. Кома. Виды комы. Этиология, патогенез. Нарушение функций организма при коматозных состояниях.
- •Патогенез и нарушение функции
- •Задача №20
- •Задача №26
- •Задача №44
- •Задача №54
- •Задача №55
Эндопирогены дают такой же биологический эффект, как и экзопирогены, повышая защитные свойства организма:
●усиливают фагоцитоз,
●усиливают выработку глюкокортикоидов,
●усиливают регенерацию тканей, которая ведет к образованию нежных рубцов (применяется при повреждении ЦНС для предотвращения осложнений (эпилепсии, парезов, параличей),
●усиливают дезинтоксикационную функцию печени,
●улучшают процессы микроциркуляции
Значение лихорадки. Лихорадка — адаптивный процесс, который при определенных условиях может сопровождаться патологическими эффектами.
Адаптивные эффекты лихорадки:
1.Прямые: бактериостатический и бактерицидный эффекты — коагуляция чужеродных белков и уменьшение активности микробов.
2.Опосредованные эффекты: потенцирование специфических и неспецифических факторов иммунокомпетентной системы, инициация стресса.
Патогенные эффекты лихорадки:
1.Прямое повреждающее действие высокой температуры заключается в коагуляции собственных белков, увеличении свободнорадикального окисления липидов.
2.Опосредованное повреждающее действие: функциональная перегрузка органов и систем может привести к развитию патологических реакций.
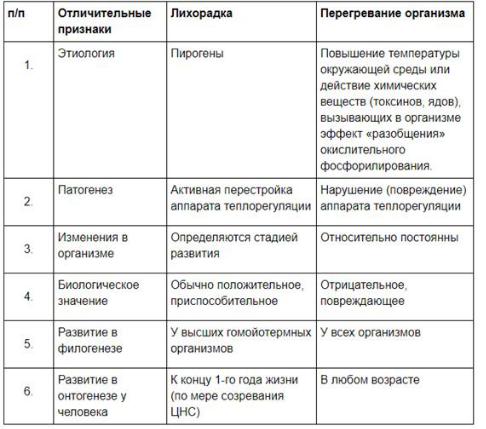
29.Отличие лихорадки от экзогенного перегревания и других видов гипертермий.
Гипертермические реакции проявляются временным повышением температуры тела за счет преходящего преобладания теплопродукции над теплоотдачей при сохранении механизмов терморегуляции.
По происхождению различают гипертермические реакции (ГР) эндогенные и экзогенные. Эндогенные гипертермические реакции подразделяют на психогенные, нейрогенные и эндокринные:
– психогенные ГР развиваются при сильном стрессе и психопатологических состояниях;
– нейрогенные ГР подразделяют на центрогенные и рефлекторные. ГР Центрогенные ГР развиваются при непосредственном раздражении нейронов центра терморегуляции, отвечающих за теплопродукцию. Рефлекторные ГР возникают при сильном раздражении различных органов и тканей: желчных ходов печени и желчевыводящих путей, лоханок почек и мочевыводящих путей при прохождении по ним конкрементов;
– эндокринные ГР развиваются в результате гиперпродукции катехоламинов (феохромоцитома) или гормонов щитовидной железы (при гипертиреоидных состояниях).
Экзогенные гипертермические реакции подразделяют на лекарственные и нелекарственные:
– лекарственные ГР обусловлены лекарственными средствами, оказывающими разобщающий эффект — симпатомиметиками (кофеин, эфедрин, дофамин), Са2+-содержащими препаратами;
– нелекарственные ГР вызывают вещества, обладающие термогенным действием — 2,4-динитрофенол, цианидин, амитах. Эти вещества активируют симпатикоадреналовую и тиреоидную системы.
В течении лихорадки выделяют 3 стадии, в перегревания 2 ст (компенсация/декомпенсация)
30. Тромботический синдром. Причины, механизмы развития, последствия (тромбоэмболическая болезнь). Патогенез тромбофилий.
Тромботический синдром, или тромбофилия — состояние, характеризующееся чрезмерной (неадекватной) коагуляцией крови и тромбообразованием, обусловленному нарушением регуляции системы гемостаза или изменением функционирования и свойств отдельных ее звеньев, ведущими к ишемии тканей и органов.
Причины:
•Повреждение стенок сосудов и сердца, приводящее к снижению ее тромборезистентности.
•Патология форменных элементов крови.
•Образованию тромбозов способствуют нарушения гемодинамики, в частности, снижение скорости кровотока.
•Патология факторов системы гемостаза.
-Абсолютное или относительное преобладание эффектов прокоагулянтных факторов.
-Одним из основных факторов тромбообразования является активация коагуляционного (вторичного) гемостаза.
-К тромбообразованию может привести ослабление противосвертывающей системы крови.
-Недостаточность антикоагулянтных и фибринолитических факторов (например, при системном атеросклерозе, СД, гипертонической болезни, эндотоксинемиях, шоковых состояниях).
-Тромбообразование может быть обусловлено активацией адгезивно агрегационной функции тромбоцитов, как первичной (при болезни Вакеза), так и вторичной (при массивных травмах тканей, хирургических операциях и т.д.).
Механизмы развития:
Механизм тромбофилии состоит в нарушении фибрин-опосредованной активации плазминогена (точнее, усиления его активации тканевым плазминоген-активирующим фактором).
В основе дисфункции лежат мутации, число которых, согласно одной из последних баз данных, достигает 330. Тип наследования, за редким исключением, аутосомно-доминантный. В большинстве случаев дисфибриногенемия протекает бессимптомно. Однако иногда бывают случаи геморрагического диатеза или тромбофилии; возможно сочетание кровотечений и тромбоэмболии.
К основным механизмам развития тромбофилии относят:
-Тромбоцитозы и возрастные функциональной активности тромбоцитов;
-Увеличение прокоагулянтной активности крови;
-Уменьшение антикоагулянтной активности крови;
-Снижение активности крови;
-Изменение тромборезистентности и тромбогенной активности стенки сосудов.
Последствия гиперкоагуляции и тромбоза:
•Нарушения центральной, органно тканевой и микрогемоциркуляции с исходом в инфаркт. При этом характер и тяжесть нарушений кровообращения определяются видом сосуда, поражённого тромбозом.
•Расстройства кровообращения, не завершающиеся инфарктом. Они обусловливают гипоксию тканей и органов (первично циркулярного типа), развитие дистрофических изменений и снижение их функций, гипотрофию и гипоплазию тканевых и клеточных элементов, сдавление ткани дистальнее места пристеночного венозного тромба (расширенной веной и отёчной тканью), образование тромбоэмболов (чаще в связи с разрушением венозного тромба).
Патогенез тромбофилий:
В артериях, обладающих более высокой тромборезистентностью, но и более высокой активностью тромботического процесса, тромб (чаще белый) быстро растет по направлению к оси сосуда. Однако, для артериальных тромбов характерен короткий период фиксации к сосудистой стенке. В венах с более низкой скоростью кровотока больше выражена АДФ и тромбин-индуцированная агрегация с образованием красных тромбов с большой площадью сечения.
В артериях, обладающих высокой скоростью кровотока, причиной тромбоза может стать: 1. Повреждение стенки сосуда атеросклеротическим процессом. 2. Ангиоспазм. 3. Изменение соотношения между простациклином и тромбоксаном А2 в пользу последнего с последующей активацией ААФТ. Таким образом, в основе тромбоза в артериальных сосудах лежит преимущественно активация сосудистотромбоцитарного (первичного) гемостаза.
В венах с медленным током крови тромбоз может быть обусловлен следующими причинами: 1. Замедлением скорости кровотока, особенно в области клапанов. 2. Повышением вязкости крови. 3. Преобладанием активности свертывающей системы вследствие, в частности, повышения уровня тромбина, что объясняется недостаточным его инактивированием тромбомодулином эндотелия из-за замедленного тока крови.
31.Геморрагический синдром: ангиопатии. Виды, причины, механизмы развития, последствия.
Эта форма геморрагических диатезов связана с нарушением сосудистого звена гемостаза, с повышением проницаемости сосудов.
Ангиопатии делятся на приобретенные и наследственные.
К приобретенным ангиопатиям относятся: авитаминоз С, старческая и стероидная пурпура, васкулиты. Авитаминоз С (цинга, скорбут) проявляется кровоточивостью десен, возникновением геморрагической сыпи в области волосяных фоликулов, подкожными, внутримышечными, внутрисуставными кровоизлияниями, чаще на нижних конечностях. В тяжелых случаях могут возникать кровотечения во внутренних органах.
Недостаток аскорбиновой кислоты вызывает увеличение активности гиалуронидазы сосудистой стенки, что обуславливает дезорганизацию основного вещества и повышение проницаемости — кровоточивость.
Наибольший интерес представляет группа васкулитов, в основном аутоиммунного характера, протекающих по II, III и IV типу аллергических реакций. К васкулитам относятся: инфекционный васкулит (II тип), ревматоидный артрит (III тип), поражение сосудов при сывороточной болезни (III тип), гломерулонефрит (II, III, IV тип), узелковый периартрит (IV тип), болезнь Шенлейна– Геноха. Болезнь Шенлейна–Геноха (геморрагический васкулит, или капилляротоксикоз) – остро развивающееся инфекционно-аллергическое заболевание с преимущественным поражением микроциркуляторного русла кожи, суставов, ЖКТ и почек. Встречается как самостоятельное заболевание и как синдром при инфекционных, ревматических и гематологических заболеваниях Патогенез Микробный или другой причинный фактор приводит к сенсибилизации организма, на фоне которой при
воздействии разрешающего фактора развивается аллергическая реакция III типа с образованием иммунных комплексов. Воспалительные изменения и повышение проницаемости сосудистой стенки усугубляется накоплением вазоактивных аминов — гистамина, серотонина, кининов. Происходит нарушение свертывающей системы крови, проявляющееся в виде внутрисосудистой гиперкоагуляции
— повышения тромбообразования, нарастания концентрации фибриногена, активации фибринолитической системы. Итогом поражения сосудистой стенки являются выраженные микроциркуляторные нарушения 35 с образованием геморрагий в тяжелых случаях доходящие до образования очагов некроза.
Типичными клиническими проявлениями являются: кожный, геморрагический (тип кровоточивости — васкулитно-пурпурный), суставной, абдоминальный и почечный. Характерна сыпь, представленная мелкоточечными кровоизлияниями, петехиями, иногда уртикарными и пятнисто-папулезными элементами, превращающимися в динамике в геморрагическое пятно. Высыпания располагаются ассиметрично на стопах, голенях, бедрах, разгибательной поверхности предплечий и плеч. Геморрагический васкулит часто трансформируется в ДВС-синдром.
Примером наследственной ангиопатии может служить болезнь Рандю–Ослера (геморрагический ангиоматоз или телеангиоэктазия). Заболевание наследуется по аутосомно-доминантному типу и характеризуется очаговым истончением стенок сосудов вследствие недоразвития субэндотелия и снижение содержания в сосудах коллагена и других тромбогенных факторов, что ведет к снижению коагуляции, адгезии и агрегации тромбоцитов, а истончение участков сосудистой стенки к образованию аневризм, повышению проницаемости и кровоточивости. При повышении артериального давления может произойти разрыв этих аневризм и возникают кровотечения.
32.Геморрагический синдром: тромбоцитопении. Виды, причины, механизмы развития. Причины,
механизмы развития, последствия.
Геморрагический синдром – это типовая форма патологии системы гемостаза, характеризующиеся повышенной кровоточивостью в результате недостаточности одного или нескольких элементов и эффектов этой системы.
Тромбоцитопения – типовая форма патологии системы тромбоцитов, характеризующаяся уменьшением количества тромбоцитов в единице объема крови ниже нормы (как правило, менее 150*10^9/л). Природа факторов, вызывающего тромбоцитопению:
Физическая (напр., действие высокой дозы проникающей радиации, что подавляет и тромбоцитарный гемопоэз); Химическая (напр., влияние алкилирующих агентов и цитостатиков);
Биологическая (напр., экзо- и эндотоксины м/о, высокая концентрация фибриногена (активирует массированную агрегацию и агглютинацию тромбоцитов), недостаток тромбопоэтина, наследственные мутации в гематопоэтических стволовых клетках, повышенное разрушение тромбоцитов аутоагрессивными Ig и/или иммуноцитами).
Механизмы развития тромбоцитопении (реализация одного или нескольких процессов):
1)Подавление тромбоцитарного ростка гемопоэза;
2)Избыточное разрушение тромбоцитов;
3)Вовлечение тромбоцитов в процесс генерализованного тромбообразования;
4)Повышенное депонирование тромбоцитов в селезенке.
Проявления:
Со стороны костного мозга:
·гипоплазия ткани (пациенты с гемобластозами, лучевой болезнью, метастазами опухолей, которые не относятся к гемобластозам, в костный мозг);
·гиперплазия ткани (повышенное разрушение или генерализованное «потребление» тромбоцитов);
·снижение содержания гликогена и активности ряда ферментов (напр., Г-6-ФД, ЛДГ) в
мегакариобластах и мегакариоцитах, что приводит к снижению продолжительности жизни тромбоцитов.
Со стороны периферической крови:
·уменьшение числа тромбоцитов (обычно при нормальном количестве эритроцитов, гемоглобина, лейкоцитов);
·изменение (увеличение/уменьшение) размеров тромбоцитов, но не всегда, напр., при иммуногенной тромбоцитопении размер не меняется;
·анемия при длительном и/или выраженном геморрагическом синдроме.
Со стороны системы гемостаза:
·снижение концентрации и/или активности тромбоцитарных факторов свертывания;
·увеличение длительности кровотечения;
·снижение степени ретракции сгустка крови;
·геморрагический синдром.
Патогенетическая классификация тромбоцитопений:
1)тромбоцитопения распределения (отражает степень секвестрации тромбоцитов в увеличенной селезенке);
2)тромбоцитопения потребления (иммунная тромбоцитопеническая пурпура, ДВС-синдром, гемолитико-уремический синдром), причиной развития которой являются ускоренная утилизация тромбоцитов и сокращение периода полужизни;
3)продуктивная тромбоцитопения (при апластической анемии, остром лейкозе, лучевой терапии, дефиците витамина В12 и фолиевой кислоты), которая наблюдается тогда, когда костный мозг не в состоянии поставить тромбоциты в количестве, необходимом для нормального кругооборота;
4)тромбоцитопения разведения (развивается при возмещении ОЦК после сильных кровотечений растворами плазмы).
Иммунная тромбоцитопения потребления (ИТП)
Наиболее часто встречаются аутоиммунные тромбоцитопении (аутоиммунная тромбоцитопеническая пурпура), которые возникают в результате сенсибилизации аутореактивными антитромбоцитарными антителами (IgG) против компонентов тромбоцитарной мембраны. Сенсибилизация тромбоцитов (определяется у 90% больных) IgG приводит к существенному сокращению времени их жизни вследствие опосредованного Fс-рецепторами фагоцитоза селезеночными макрофагами. В основе патогенеза большинства аутоиммунных тромбоцитопений лежит срыв иммунологической толерантности. Одна из возможных причин этого срыва — снижение функции Т-супрессоров. Увеличение количества мегакариоцитов и продукции тромбоцитов обусловлено повышением синтеза тромбоцитопоэтинов в ответ на снижение количества тромбоцитов. Основным местом выработки антитромбоцитарных тел является селезенка, которая может чрезвычайно активно элиминировать тромбоциты, покрытые антителами. Однако развитие спленомегалии не типично для ИТП.
Болезнь Верльгофа (идиопатическая тромбоцитопеническая пурпура) — хроническое, волнообразно протекающее заболевание, обусловленное количественной и качественной недостаточностью тромбоцитарного звена гемостаза. Характеризуется элиминативной тромбоцитопенией, наличием гигантских тромбоцитов в кровотоке, мегакариоцитозом в костном мозге и обязательным присутствием антитромбоцитарных аутоантител.
Болезнь Виллебранда («наследственная псевдогемофилия») – геморрагический диатез, сходный как с тромбоцитовазопатией (удлинение времени кровотечения), так и с гемофилией (отличающийся от нее по наследованию и некоторым клиническим проявлениям). Болезнь Виллебранда относится к наиболее распространенным видам врожденных геморрагических диатезов, передается аутосомно-доминантным путем, характеризуется количественной или качественной патологией комплекса «фактор Виллебранда
