
- •Кафедра патофизиология, клиническая патофизиология, 3курс, лечебный факультет, перечень экзаменационных вопросов
- •1. Патофизиология как теоретическая и методологическая база медицины. Предмет и задачи патофизиологии. Основные особенности патофизиологии как научной и учебной дисциплины. Роль эксперимента в развитии патофизиологии и медицины.
- •2. Здоровье и болезнь – основные понятия нозологии. Переходные состояния организма между здоровьем и болезнью (предболезнь).
- •3. Болезнь как диалектическое единство повреждения и адаптивных реакций организма.
- •4. Этиология. Роль причин и условий в возникновении болезней, их диалектическая взаимосвязь. Понятие о внешних и внутренних причинах и факторах риска.
- •5. Патогенез. Причинно-следственные связи в развитии болезни. Понятие о порочном круге патогенеза. Единство функциональных и структурных изменений в патогенезе заболевания.
- •6. Повреждение как начальное звено патогенеза. Проявления повреждения на разных уровнях интеграции организма. Защитные, компенсаторные и восстановительные реакции организма.
- •7. Болезнетворное воздействие факторов внешней среды: действие электрического тока на организм человека.
- •10. Гипоксия. Определение, общая характеристика, классификация гипоксических состояний. Этиология и патогенез различных видов гипоксии.
- •https://docs.google.com/file/d/1L1k9VNrYG_6Rpq-KfVDVvRuDf0T11oxo/edit?filetype=msword
- •11. Защитно-приспособительные реакции при гипоксии. Механизмы срочной и долговременной адаптации к гипоксии. Нарушение обмена веществ и физиологических функций при гипоксии.
- •13. Молекулярные наследственные болезни углеводного и аминокислотного, белкового обмена. Галактоземия, гликогенозы. Фенилкетонурия, альбинизм.
- •15. Нарушение периферического кровообращения. Артериальная гиперемия. Причины, виды, механизмы развития, последствия.
- •16. Нарушение периферического кровообращения. Венозная гиперемия. Причины, виды, механизмы развития, последствия.
- •19. Воспаление. Сущность явления. Причины воспаления. Защитная роль воспаления. Теории воспаления.
- •20. Воспаление. Первичная и вторичная альтерация. Молекулярные механизмы повреждения.
- •22. Воспаление. Сосудистые реакции при воспалении. Экссудация, механизмы развития, роль медиаторов. Значение экссудации.
- •23. Сравнительная патология воспаления (И.И. Мечников). Эмиграция лейкоцитов (L) в очаг воспаления. Фагоцитоз.
- •24. Диалектика защиты и повреждения в процессе развития воспаления.
- •26. Характеристика понятия «ответ острой фазы». Основные цитокины РООФ, их происхождение и биологические эффекты.
- •27. Лихорадка как типовая патологическая реакция. Этиология, патогенез. Изменение теплопродукции и теплоотдачи в разные стадии лихорадки.
- •28. Лихорадка как компонент РООФ. Классификация пирогенов. Механизм реализации эндопирогенов. Биологическое значение лихорадки.
- •29. Отличие лихорадки от экзогенного перегревания и других видов гипертермий.
- •30. Тромботический синдром. Причины, механизмы развития, последствия (тромбоэмболическая болезнь). Патогенез тромбофилий.
- •Причины:
- ••Повреждение стенок сосудов и сердца, приводящее к снижению ее тромборезистентности.
- •Механизмы развития:
- •Механизм тромбофилии состоит в нарушении фибрин-опосредованной активации плазминогена (точнее, усиления его активации тканевым плазминоген-активирующим фактором).
- •К основным механизмам развития тромбофилии относят:
- •Последствия гиперкоагуляции и тромбоза:
- •Патогенез тромбофилий:
- •31. Геморрагический синдром: ангиопатии. Виды, причины, механизмы развития, последствия.
- •33. Геморрагический синдром: коагулопатии. Нарушения свертывания крови в 1,2,3 фазе коагуляции Причины, механизмы развития, последствия.
- •34. Синдром диссеминированного внутрисосудистого свертывания (синдром ДВС). Причины, механизмы развития, стадии, последствия. Принципы патогенетической терапии.
- •35. Гипо- и гипергликемии. Виды, причины, и механизмы развития, последствия.
- •36. Этиология и патогенез сахарного диабета I и II типа. Экспериментальный сахарный диабет. Патогенез острых и хронических осложнений сахарного диабета.
- •37. Метаболический синдром и его характеристика. Общее ожирение. Виды, причины и механизмы развития. Последствия.
- •38. Энергетический обмен организма в состояниях положительного энергетического баланса. Энергетический обмен организма в состояниях отрицательного энергетического баланса.
- •39. Голодание. Виды голодания, стадии полного голодания. Гормоно-субстратные изменения в разные периоды полного голодания.
- •41. Нарушения водно-солевого обмена. Обезвоживание. Причины, механизмы развития, последствия. Роль профессиональных факторов в развитии обезвоживания.
- •42. Гипергидратация. Виды. Патогенез отеков при сердечной недостаточности.
- •43. Отеки. Патогенетические механизмы развития отеков. Патогенез токсического, голодного и почечного отеков.
- •44. Гипо- и гиперволемии. Причины, механизмы развития, последствия.
- •45. Респираторный ацидоз. Причины, механизмы развития. Роль буферных систем и органов в компенсации. Изменение показателей КОБ. Характеристика нарушений при некомпенсированной форме ацидоза.
- •49. Этиология опухолевого процесса. Виды канцерогенов. Эндо- и экзогенные канцерогены (физические, химические, биологические). Механизмы их воздействия.
- •50. Онковирусы. Их классификация. Роль вирусов в канцерогенезе.
- •51. Молекулярные механизмы канцерогенеза. Значение онкогенов в канцерогенезе.
- •52. Механизмы активации протоонкогенов. Роль онкобелков в канцерогенезе. Классификация онкобелков.
- •53. Опухолевый процесс. Определение понятия. Виды опухолей, признаки малигинизации. Понятие о предопухолевом состоянии.
- •54. Атипизм опухолевой ткани. Морфологический, биохимический, функциональный атипизм.
- •55. Механизмы антиканцерогенеза. Механизмы противоопухолевой резистентности организма.
- •56. Механизмы взаимодействия опухоли и организма. Опухолевая кахексия. Паранеопластические синдромы.
- •57. Молекулярные механизмы атеросклероза. Атерогенные дислипопротеидемии. Роль рецепторов к липопротеидам в регуляции обмена холестерина и в атерогенезе.
- •58. Атеросклероз. Значение нарушений нейроэндокринной регуляции в этиологии и патогенезе атеросклероза. Роль социальных факторов в развитии атеросклероза.
- •59. Нейрогенная теория атеросклероза (П.С. Хомуло). Этиология и патогенез. Эмоциональная реакции и эмоциональный стресс. Влияние эмоционального стресса на атерогенез.
- •60. Общая патология нервной системы. Формирование генератора патологически усиленного возбуждения как основной механизм патологической функциональной системы.
- •61. Функциональные нарушения высшей нервной деятельности. Экспериментальные неврозы. Значение типов нервных систем в возникновении неврозов (И.П. Павлов).
- •62. Эмоции и эмоциональные расстройства. Роль психоэмоционального напряжения в развитии соматической патологии.
- •65. Патология щитовидной железы. Классификация функциональных состояний. Эутиреоидное состояние щитовидной железы . Гипо- и гиперфункция щитовидной железы. Причины, признаки, механизмы развития.
- •66. Патология коры надпочечников. Гипо- и гиперфункция. Первичный и вторичный альдостеронизм. Причины, признаки, механизмы развития.
- •68. Значение и механизмы формирования срочной и долговременной адаптации.
- •69. Общий адаптационный синдром. Роль желез внутренней секреции в развитии общего адаптационного синдрома. Стадии стресса.
- •70. Стресс-факторы, стресс-реализующие системы. Механизмы стрессогенного повреждения различных органов и систем.
- •71. Адаптивные и дизадаптивные эффекты гормонов стресса (катехоламины, глюкокортикоиды). Болезни адаптации.
- •72. Стресс-лимитирующие системы. Виды, эффекты.
- •73. Понятие психоэмоционального стресса. Определение, причины, механизмы развития, роль в патогенезе психосоматических заболеваний.
- •74. Иммунодефицитные состояния и аллергия как типовые иммунопатологические процессы. Взаимосвязь аллергии и воспаления, аллергии и иммунитета.
- •75. Первичные (наследственные и врожденные) иммунодефициты. Виды, патогенез, проявления, последствия. Вторичные (приобретенные) иммунодефицитные состояния. Этиология, патогенез, последствия. СПИД, этиология, пути инфицирования, патогенез.
- •76. Аллергия и иммунитет. Общность и различия. Классификация аллергических реакций.
- •2. Патогенная роль реакций цитотоксического типа - реакция из иммунной переходит в аллергическую, повреждает и разрушает ткани, если направлена против клеток, которые стали аутоантигенными.
- •82. Лекарственная аллергия. Условия и механизмы развития.
- •83. Сердечная недостаточность. Определение, причины, классификация, механизмы развития. Интракардиальные механизмы компенсации сердечной недостаточности.
- •84. Недостаточность системы кровообращения. Определение, виды. Гемодинамическая характеристика видов недостаточности кровообращения.
- •85. Компенсаторные механизмы сердца. Понятие о гиперфункциях, виды, механизмы развития. Физическая нагрузка и гиперфункция сердца.
- •86. Острая левожелудочковая сердечная недостаточность. Клинические проявления. Виды, причины, механизмы развития.
- •87. Хроническая сердечная недостаточность. Клинические признаки и механизмы. Механизмы развития сердечной недостаточности при мио-, эндо- и перикардитах. Механизмы развития сердечной недостаточности при эндокринопатиях.
- •88. Коронарная недостаточность. Определение, классификация, причины, клинические проявления.
- •89. Инфаркт миокарда. Причины, механизмы развития, осложнения. ИБС. Определение. Стенокардия, классификация по патогенезу, механизмы развития.
- •93. Хроническая сосудистая недостаточность, гипотоническая болезнь. Определение, классификация, причины, механизмы развития.
- •95. Дизэритропоэтические анемии (железодефицитная, апластическая, сидероахрестическая). Причины, механизмы развития, картина крови.
- •96. Гемолитические анемии. Принципы классификации. Приобретенные и наследственные гемолитические анемии. Причины, механизмы развития, картина крови.
- •97. Острая кровопотеря. Механизмы компенсации. Постгеморрагические анемии (острые, хронические), механизмы развития, картина крови.
- •98. Лейкоцитозы. Классификация. Причины, механизмы развития. Сдвиги лейкоцитарной формулы.
- •99. Лейкемоидные реакции. Виды, этиология, патогенез. Отличие от лейкоза. Значение для организма.
- •100. Лейкозы. Классификации. Этиопатогенез, картина костного мозга и крови при острых и хронических лейкозах.
- •101. Лейкопении. Виды, причины, механизмы развития. Изменения в лейкоцитарной формуле (процентное содержание различных форм к общему числу лейкоцитов).
- •102. Патология внешнего дыхания. Механизм компенсации при нарушении внешнего дыхания. Одышка. Виды. Периодическое и терминальное дыхание. Причины, виды, механизмы развития.
- •103. Хроническая обструктивная болезнь легких (ХОБЛ). Эмфизема легких. Виды. Патогенез нарушения внешнего дыхания при эмфиземе.
- •104. Рестриктивные причины нарушения внешнего дыхания. Пневмоторакс. Виды. Патогенез нарушений внешнего дыхания при пневмотораксе.
- •105. Обструктивные причины нарушения внешнего дыхания. Ателектаз. Виды. Патогенез нарушений внешнего дыхания при ателектазе.
- •106. Нарушение секреторной и моторной функции желудка. Причины, механизмы развития, последствия.
- •107. Нарушение пищеварения в тонком кишечнике. Пристеночное пищеварение и его нарушения. Причины, механизмы развития, последствия.
- •Характеристика билирубинового обмена
- •113. Нефротический синдром. Причины, механизмы развития, последствия, профилактика.
- •114. Острая почечная недостаточность. Формы, этиология, механизмы развития, последствия.
- •115. Хроническая почечная недостаточность. Причины, стадии, механизмы развития. Уремия.
- •116. Гломерулонефриты. Патогенетическая классификация. Клинические проявления, принципы лечения.
- •118. Кома. Виды комы. Этиология, патогенез. Нарушение функций организма при коматозных состояниях.
- •Патогенез и нарушение функции
- •Задача №20
- •Задача №26
- •Задача №44
- •Задача №54
- •Задача №55
Увеличение осмотического давления (гиперосмия): а) результат катаболических процессов — расщепление крупных молекул на более мелкие; б) увеличение концентрации ионов К+, Са2+ (гипериония); в) дисиония — изменение соотношения между отдельными ионами, К+ высвобождается из гибнущих клеток.
Последствия: гипергидратация очага воспаления, стимуляция эмиграции лейкоцитов, изменение тонуса стенок сосудов, формирование чувства боли.
Гиперонкия — увеличение концентрации белка в очаге воспаления, альбумины выходят в ткань вместе с экссудатом. Это ведет к развитию отека.
Изменение поверхностного заряда клеток (как правило, снижение). Обусловлено нарушением водно-электролитного баланса в воспаленной ткани.
♦Механизмы развития: нарушение энергообеспечения трансмембранного переноса ионов и развитие электролитного дисбаланса.
♦Последствия: изменение порога возбудимости клеток, потенцирование миграции фагоцитов за счёт электрокинеза; стимуляция кооперации клеток в связи со снижением величины отрицательного поверхностного их заряда, нейтрализацией его или даже перезарядкой.
Изменения коллоидного состояния межклеточного вещества и гиалоплазмы клеток в очаге воспаления.
♦ Механизмы развития:
- Ферментативный и неферментативный гидролиз макромолекул (гликозаминогликанов, белков, протеогликанов).
-Фазовые изменения микрофиламентов, облегчающие переход их состояния из геля в золь и наоборот.
+♦ Последствия (основное): увеличение тканевой проницаемости.
Уменьшение поверхностного натяжения клеточных мембран. Обусловлено изменениями структуры молекул плазмолеммы.
♦Механизмы развития: воздействие на клеточные мембраны значительного количества поверхностноактивных веществ (фосфолипидов, ВЖК, К+, Са2+).
♦Последствия: облегчение подвижности клетки и потенцирование адгезии клеток при фагоцитозе.
22.Воспаление. Сосудистые реакции при воспалении. Экссудация, механизмы развития, роль медиаторов. Значение экссудации.
Экссудация — компонент воспаления, включающий в себя сосудистые и клеточные реакции.
Этот компонент воспаления включает в себя:
•сосудистые реакции и изменения кровообращения в очаге воспаления;
•выход жидкой части крови из сосудов (экстравазация);
•выход лейкоцитов в очаг воспаления (эмиграция лейкоцитов);
•развитие фагоцитоза.
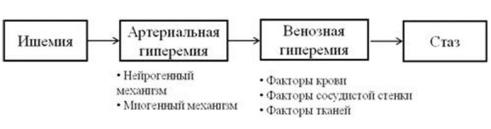
Спазм возникает рефлекторно в ответ на действие флогогена.
Атрериальная гиперемия — результат действия медиаторов воспаления, снижения рН и увеличения осмолярности ткани в очаге повреждения, что ведет к увеличению притока артериальной крови, увеличению скорости кровотока, увеличению гидростатического давления в капиллярах и открытию ранее не функционировавших сосудов.
Венозная гиперемия — результат сдавления венозных сосудов жидкостью, вышедшей в ткань (экссудатом), это ведет к микротромбозу вен и лимфатических сосудов, набуханию эндотелия, краевому стоянию лейкоцитов, сладжированию крови, развитию толчкообразного и маятникообразного кровотока, и в итоге развивается венозный стаз — полная остановка кровотока. Формируется барьер, ограничение очага воспаления.
Непосредственно экссудация — выход жидкой части крови, электролитов, белков и форменных элементов крови из сосудов в очаг воспаления. Жидкость, которая выходит из сосудов (экссудат) формирует отек.
Выход клеток в очаг воспаления — эмиграция. Развитию эмиграции способствуют следующие условия:
–увеличение проницаемости сосудистой стенки;
–выход белка в ткань (гиперонкия);
–увеличение осмотического давления в очаге повреждения;
–увеличение гидростатического давления внутри сосудов.
С момента венозной гиперемии создаются благоприятные условия для выхода клеток во внесосудистое пространство и развития клеточных реакций в очаге воспаления. Замедление скорости кровотока при венозной гиперемии ведет к развитию феномена краевого стояния лейкоцитов (маргинация) и прилипанию их к эндотелию (адгезия), через 2–4 часа сосудистая стенка покрывается слоем лейкоцитов и приобретает вид «булыжной мостовой», а еще через 1–3 часа начинается массивный выход лейкоцитов в ткань (эмиграция).
Место выхода — посткапиллярные венулы.
Медиаторы воспаления и цитокины (С5а, ЛТ В4, ФАТ, ИЛ-1, ИЛ-8, γ-интерферон, ФНО-α) воздействуют на клетки эндотелия, вызывая экспрессию на мембране этих клеток особых молекул адгезии и начинается процесс взаимодействия эндотелиальных клеток с лейкоцитами. Молекулы адгезии — лиганд-рецепторы для межклеточных взамодействий.
1. Селектины — лектиновые молекулы, трансмембранные белки, концевой домен этих белков способен связывать олигосахариды (т.е. белок-лектин). Селектины опосредуют раннюю стадию маргинации — обратимую адгезию клеток.
2.Интегрины — димерные трансмембранные белки, отвечают за поздние стадии адгезии лейкоцитов и тромбоцитов к эндотелию и частично за диапедез клеток, контактные взаимодействия лейкоцитов и тромбоцитов в очаге воспаления.
3.Семейство иммуноглобулинов — являются трансмембранными
белками с пятью доменами, экспрессируются преимущественно эндотелием после активации цитокинами (ИЛ-1, ИЛ-8, γ-интерферон, ФНО-α), они обеспечивают отсроченную адгезию, прохождение лейкоцитов через сосудистую стенку.
4. Адресины — белки клеток внутренней выстилки высокоэндотелиальных венул (сосуды лимфоидных органов), они играют роль при развитии хронического воспаления, когда происходит усиленный ангиогенез и формируются окна усиленной миграции лейкоцитов (например, в суставы при аутоиммунном воспалении).
Хемоаттрактанты (липополисахариды бактериальной стенки Гр (-), ЛТ В4, ФАТ, ИЛ-8, С5а) — вызывают хемотаксис, активное перемещение лейкоцитов в направлении наибольшей концентрации этих веществ. Последовательность выхода лейкоцитов в очаг воспаления — через 2 часа (максимум через 4–6 часов) — нейтрофилы, моноциты — через 16–24 часа.
Значение
Смысл выхода лейкоцитов в очаг воспаления — осуществление фагоцитоза (поглощение и нейтрализация чужеродного агента).
23. Сравнительная патология воспаления (И.И. Мечников). Эмиграция лейкоцитов (L) в очаг воспаления. Фагоцитоз.
Классическое описание сравнительной патологии воспаления дал И. И. Мечников, показав, что
воспаление всегда представляет собой активную реакцию организма, на какой бы ступени эволюционного развития он ни находился.
Воспаление встречается в различных формах у всех представителей животного мира. Усложнение организации животного сопровождается усложнением воспалительной реакции. Как и другие патологические процессы, воспаление эволюционирует с эволюцией животных видов. У животных, лишенных кровеносных сосудов (губки, кишечнополостные, иглокожие), воспаление выражается в скоплении амебоидных соединительнотканных клеток (амебоциты) вокруг места повреждения. И. И. Мечников вводил шип розы в прозрачный колокол медузы и наблюдал скопление амебоцитов вокруг поврежденного участка ткани. Эта реакция и представляла собой воспаление.
У высших беспозвоночных (ракообразные, насекомые), имеющих кровеносную систему открытого типа, воспаление также выражается в скоплении кровяных клеток - лимфогематоцитов - в месте повреждения. Изменения кровообращения в воспаленной ткани, характерные для позвоночных животных и человека, у беспозвоночных не возникают.
Развитие кровеносной системы и ее нервной регуляции у позвоночных животных и у человека значительно усложнило воспалительную реакцию. Расстройства кровообращения в воспаленной ткани являются важнейшими выражениями воспаления. Кроме того, существенное значение в развитии воспаления приобрела нервная система. Участие кровяных клеток в воспалении у высших животных и у человека проявляется выходом лейкоцитов в воспаленную ткань. Кроме того, наблюдается размножение местных соединительнотканных клеток (гистиоцитов, фибробластов) в очаге воспаленной ткани.
Эмиграция лейкоцитов в очаг воспаления – в фазу ВГ; место выхода – посткапиллярные венулы Стадии миграции: маргинация, адгезия, эмиграция Первыми эмигрируют нейтрофилы → моноциты (через 24-28 ч) → лимфоциты и др. (через 72 ч и более)
Медиаторы воспаления → экспрессия на эндотелиоцитах молекул адгезии (селектины, интегрины, молекулы, относящиеся к семейству Ig) → взаимодействие эндотелиоцитов с L → взаимодействие L с межклеточным матриксом → накопление L в очаге воспаления
Стадия адгезии опосредуется селектинами: среди селектинов выделяют L-селектин (экспресс. постоянно на пов-ти всех L), E-селектин (экспресс. на мембранах эндотелиоцитов после их активации цитокинами), Р-селектин (синтезируется в эндотелиаоцитах постоянно и накапливается в секреторных тельцах)
Медиаторы воспаления (гистамин, ИЛ-1, ФНО, ЛПС м/о) → появление Р-селектина на поверхности клеток → взаимодействие с лигандами на пов. L → первоначальное замедление и rolling L – «качение» по эндотелию (позже в процесс вмешивается L-селектин) → ↑ t контакта L с эндотелием → ↑ вероятности активации L медиаторами воспаления → появление на поверхности L интегринов, которые обеспечивают более плотное прикрепление L к эндотелию (лиганды интегринов – ICAM-1, ICAM-2, VCAM-1 на поверхности эндотелиоцитов) → миграция L во внесосудистом пространстве (L «цепляются» с помощью интегринов за элементы межклеточного матрикса: фибронектин, ламинин, коллаген) → проникновение в очаг воспаления → фагоцитоз
Особую роль в процессе эмиграции L играют хемоаттрактанты (ХА):
·активируют L
·мобилизуют внутриклеточные органеллы L и вызывают хемотаксис (активное перемещение
внаправлении наибольшей [ХА])
Наиболее сильные ХА, воздействующие на разные формы L:
·ЛПС м/о (входят в состав клеточной оболочки Грбактерий)
·фрагменты комплемента С5а-С9
·ЛТ В4 (а вообще большинство ЛТ)
·фактор активации тромбоцитов
Хемокины – ХА, воздействующие преимущественно на специальные подтипы L (низкомолекулярные белки, которые секретируются различными участвующими в воспалительном ответе клетками)
·ИЛ-8 (ХА для нейтрофилов)
·MCP-1 (ХА для моноцитов)
·лимфотактин (ХА для лимфоцитов и NK)
·эотаксин (ХА для эозинофилов)
ХА → специфические R на пов-ти L → ↑ [Ca2+] в цитоплазме → активация микротубулярной системы (образующей внутренний скелет) → появление псевдоподий + активация ФЛ А2 (ПКа, ПКс) → арахидоновая кис-та → образование Pg и ЛТ (участвуют в воспалении)
Фагоцитоз – процесс узнавания, активного захвата и поглощения микроорганизмов, разрушенных клеток и инородных частиц специализированными клетками иммунной системы Облигатные фагоциты: макрофаги (моноциты, МФ), микрофаги (нейтрофилы, эозинофилы, базофилы)
Стадии фагоцитоза: прилипание, поглощение, внутриклеточное разрушение
Прилипание – обусловлено существованием на мембране фагоцитов R для молекул (входящий в состав микробной клетки/появляющихся на поверхности собственной погибающей клетки), но в большинстве случаев прилипание фагоцитов осуществляется при участии опсонинов Опсонины – сывороточные фак-ры, попадающие в очаг воспаления в составе воспалительного экссудата (Ig, фрагмент C3b, некоторые плазменные белки)
Молекулы опсонинов располагают двумя участками, один из которых связывается с поверхностью атакуемой частички, а другой — с мембраной фагоцита (например, IgG связывается Fab-фрагментом с АГ м/о, а Fc-фрагментом – с мембраной фагоцитов, на которой есть R для Fc-фрагмента) Поглощение: образование псевдоподий фагоцитом → окружение объекта → объект оказывается
«внутри мешка» - фагосомы → внутриклеточное разрушение
При незавершенном фагоцитозе, гибели L, разрушении мембраны фагосомы → выход содержимого гранул и активных метаболитов кислорода → гибель объекта атаки + повреждение тканей организма
Доп. инфа про бактерицидные системы: https://docs.google.com/document/d/1Sm9h24vqZPWpgY7dOmXMVqb3TK9l1q4DCuDOgZHL23Q/edit
24. Диалектика защиты и повреждения в процессе развития воспаления.
Как и всякий патологический процесс, воспаление по своей сущности процесс противоречивый. В нем сочетаются и мобилизация защитных сил организма, и явления повреждения («полом»). Возникнув в филогенезе как явление приспособительное, воспаление сохранило это свойство и у высших животных. Организм защищается от воздействия чуждых и вредных ему факторов путем отграничения воспалительного очага от всего организма. Такое действие предотвращает распространение и генерализацию воспалительного процесса, сосредоточивая борьбу с вредным агентом в одном очаге. Воспаленная зона не только фиксирует все, что происходит в ней, но и поглощает токсические вещества, циркулирующие в крови. Это объясняется формированием вокруг очага воспаления своеобразного барьера с односторонней проницаемостью. Вначале такой барьер создается путем закупорки отводящих лимфатических и кровеносных сосудов и блокады внесосудистого тканевого транспорта. Далее он окончательно формируется вследствие размножения соединительнотканных клеток на границе между здоровой и пораженной тканью. Защитная роль воспалительного барьера наглядно демонстрируется в эксперименте со стрихнином, смертельная доза которого не приводит к гибели животного, если ее ввести в воспалительный очаг.
В очаге воспаления создаются неблагоприятные условия для жизни микроорганизмов. В этом отношении главную роль играют фагоциты и специфические антитела, а также ферменты и основные белки. Целебные свойства воспаления особенно отчетливо проявляются в стадии пролиферации и регенерации. Однако все изложенное выше отражает только одну (положительную) сторону воспаления. Вторая, противоположная, заключается в том, что воспаление всегда несет в себе элемент разрушения. Борьба с «агрессором» в зоне воспаления неизбежно сочетается с гибелью собственных клеток. В некоторых случаях начинает преобладать альтерация, что приводит к гибели ткани или целого органа. Экссудация может вызвать нарушение питания ткани, ее ферментативное расплавление, гипоксию и общую интоксикацию. И. И. Мечников отмечал, что «целительная сила природы, главный элемент которой составляет воспалительная реакция, вовсе не есть еще приспособление, достигшее совершенства».
Представление о воспалении, как о патологическом процессе, в котором «защитительное» и «собственно патологическое» находятся в единстве и борьбе, соответствует действительности.
25. Локализация и генерализация повреждения. Местные и общие реакции на
повреждение. Их взаимосвязь.
Альтерация (повреждение) – касается всех структур ткани, попавших под воздействие повреждающего фактора (флогогена), вызывающего необратимые и обратимые изменения клеток, межклеточного вещества, нервных окончаний, сосудов.
Повреждающие факторы (флогогены) → повреждение → комплексная интегративная реакция, включающая в себя:
1)Местный типовой процесс – воспаление
