
- •ОГЛАВЛЕНИЕ
- •ОБСТРУКТИВНЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ
- •Хроническая обструктивная болезнь легких (ХОБЛ)
- •Бронхиальная астма (БА)
- •Вопросы для самоконтроля
- •Воспалительные и нагноительные заболевания легких
- •Пневмонии
- •Госпитальная пневмония
- •Вопросы для самоконтроля
- •НЕФРОЛОГИЯ
- •Иммунные заболевания почек
- •Гломерулонефриты
- •Инфекционно-воспалительные заболевания почек
- •Пиелонефрит
- •Хроническая болезнь почек (ХБП)
- •Вопросы для самоконтроля
- •Железодефицитная анемия
- •Меголобластные анемии
- •Гемолитические анемии
- •Наследственные гемолитические анемии, обусловленные изменениями мембраны эритроцитов. Болезнь Минковского-Шоффара
- •Пароксизмальная ночная гемоглобинурия (болезнь Маркиафавы-Микели)
- •Апластическая анемия
- •Вопросы для самоконтроля
- •Острые лейкозы
- •Острые лейкозы
- •Вопросы для самоконтроля
- •Хронические лейкозы
- •Хронический лимфолейкоз
- •Миелопролиферативные заболевания
- •Хронический миелолейкоз
- •Хронический идиопатический миелофиброз
- •Истинная полицитемия
- •Вопросы для самоконтроля
- •Парапротеинемические гемобластозы
- •Общие вопросы
- •Множественная миелома
- •Вопросы для самоконтроля
- •Лимфомы
- •Общие вопросы
- •Лимфогранулематоз
- •Неходжкинские злокачественные лимфомы
- •Вопросы для самоконтроля
- •Геморрагические диатезы
- •Общие вопросы
- •Болезнь Рандю-Ослера-Вебера (наследственная телеангиоэктазия)
- •Болезнь Шенлейн-Геноха (Геморрагический васкулит)
- •Болезнь Верльгофа (Идиопатическая тромбоцитопеническая пурпура, аутоиммунная тромбоцитопения)
- •Гемофилия
- •Вопросы для самоконтроля
- •Ревматоидный артрит (РА)
- •Остеоартроз (ОА)
- •Подагра
- •Реактивный артрит (РеА)
- •Псориатический артрит (ПсА)
- •Анкилозирующий спондилоартрит (болезнь Бехтерева)
- •Системные болезни соединительной ткани
- •Системная красная волчанка (СКВ)
- •Системная склеродермия
- •Дерматомиозит
- •Системные васкулиты
- •Классификация
- •Болезнь Хортона
- •Болезнь Кавасаки
- •Гранулематоз Вегенера
- •Синдром Чарга-Стросса
- •Микроскопический полиангиит
- •Вопросы для самоконтроля
- •Ахалазия кардии
- •Гастроэзофагеальная рефлюксная болезнь
- •Хронический гастрит
- •Язвенная болезнь желудка и двенадцатиперстной кишки
- •Воспалительные заболевания кишечника Болезнь Крона
- •Болезнь Уиппла
- •Неспецифический язвенный колит
- •Вопросы для самоконтроля
- •Заболевания желудочно-кишечного тракта: желчного пузыря, печени и поджелудочной железы
- •Хронический бескаменный холецистит
- •Хронический гепатит
- •Аутоиммунный гепатит
- •Алкогольная болезнь печени (АБП)
- •Цирроз печени.
- •Гемохроматоз
- •Болезнь Коновалова - Вильсона
- •Лекарственные поражение печени
- •Цирроз печени
- •Хронический панкреатит
- •Вопросы для самоконтроля
A.Иммуноэлектрофорез сыворотки крови и мочи;
B.Гистологическое исследование костного мозга;
C.Иммунофенотипирование костного мозга;
D.Цитологическое исследование;
E.Определение уровня лактатдегидрогеназы в сыворотке крови.
36.Какая схема химиотерапии используется для лечения острого лимфобластного лейкоза с благоприятным прогнозом?
A. Комбинация винкристина, преднизолона;
B. Комбинация монохимиотерапии с облучением головы; C. Схема Хельцера;
D. Монотерапия антрациклиновыми антибиотиками; E. Схема «7+3».
37.Каким способом вводятся препараты для профилактики нейролейкемии?
A.Внутривенно;
B.Внутриартериально;
C.Интратекально;
D.Внутрикостно;
E.Внутрибрюшинно.
38.Какая схема химиотерапии используется для лечения острого промиелоцитарного
лейкоза?
A. Монотерапия цитозаром;
B. Монотерапия аспарагиназой;
C. Комбинация производных ретиноевой кислоты и курса "7 + 3"; D. Курсы "7 + 3" или "5 + 2";
E. Тотальное облучение всего тела.
39.Какие препараты используются для профилактики нейролейкемии?
A.Винкристин, аспарагиназа;
B.Циклофосфан, мелфалан;
C.Метатрексат, цитозар;
D.Вепезид, циклофосфан;
E.Тиогуанин, сульфасалазин.
Ответы на вопросы для самоконтроля:
1-D, 2-C, 3-C, 4-В, 5-А, 6-C, 7-B, 8-C, 9-E, 10-А, 11-C, 12- E, 13-А, 14-А, 15-A, 16-E, 17-D, 18- B, 19-C, 20-C, 21-C, 22-C, 23-C, 24-C, 25-D, 26-A, 27-D, 28-D, 29-C, 30-E, 31-B, 32-C, 33-B, 34-C, 35-C, 36-C, 37-C, 38-C, 39-C
Хронические лейкозы
Хронический лимфолейкоз
Определение. Хронический лимфолейкоз (ХЛЛ) – злокачественная опухоль кроветворной ткани с первичной локализацией в костном мозге, субстратом которой являются зрелые лимфоциты.
87
Эпидемиология. Это наиболее часто встречающаяся форма среди гемобластозов. Он распространен в Европе и Северной Америке и составляет 30% от всех форм лейкозов. Крайне редко встречается в Азии. Средний возраст больных при диагностике ХЛЛ – 65 лет. Мужчины болеют чаще женщин. Ежегодно данной формой лейкоза заболевают 3-3,5 человека на 100 000 населения.
Этиология заболевания не установлена. Это один из немногих лейкозов взрослых, происхождение которого не обусловлено воздействием химических веществ, ионизирующей радиации или лекарственных препаратов, а также единственная форма, которая этиологически не связана с атомными взрывами. У большинства больных имеются цитогенетические аномалии (см. цитогенетическое исследование).
Патогенез и иммунология. Все лимфоциты делятся на В- и Т-клетки. Термин В-клетки происходит от латинского названия фабрициевой сумки (bursa Fabricius) – органа, необходимого для созревания В-клеток у птиц. Аналогичного органа у человека нет; созревание В-клеток у него происходит в основном в костном мозге.
Развитие В-клеток начинается с дифференцировки полипотентной стволовой клетки в недифференцированные предшественники В-клеток. Из них образуются пре-В и недифференцированные (так называемые малые) В-клетки. Затем происходит их дифференцировка с образованием плазматических клеток, которые способны продуцировать иммуноглобулины.
Т-лимфоциты играют ключевую роль в клеточном иммунитете. Этот иммунитет обеспечивает уничтожение различных клеток непосредственно цитотоксическими Т- клетками. Развитие их аналогично В-клетками. Незрелые протимоциты мигрируют из костного мозга и «заселяют» субкапсулярный кортикальный слой селезенки. Важнейшая функция селезенки в развитии Т-клеток состоит в ликвидации аутореактивных Т-клеток, которые способны распознавать антигены других нормальных клеток организма. Образовавшись из стволовых клеток костного мозга, Т-клетки обязательно проходят стадию развития в тимусе, в результате чего генерируются зрелые, функционально полноценные Т- лимфоциты.
Морфологическим субстратом ХЛЛ чаще всего являются малые В-лимфоциты (промежуточные клетки между пре-В и зрелыми лимфоцитами), которые экспрессируют большинство поверхностных антигенов, представленных на зрелых В-клетках в норме. Основной отличительной фенотипической чертой клеток при ХЛЛ является коэкспрессия CD5+. Главное свойство CD5+В-клеток заключается в их способности продуцировать аффинные (родственные) полиреактивные иммуноглобулины, которые распознают ряд аутоантигенов и имеют перекрестную реакцию с бактериальными антигенами. Повышенное содержание этих клеток обнаруживается также у больных с аутоиммунными заболеваниями (ревматоидный артрит, СКВ и другие). Особенностью лимфоцитов при ХЛЛ является их функциональная неполноценность, нарушение механизма антителообразования, что способствует возникновению у больных различных инфекционных процессов. Нарушение иммунологического гомеостаза вызывает различные аутоиммунные конфликты (аутоиммунную гемолитическую анемию, тромбоцитопению). Функционально инертные лимфоциты имеют длинный жизненный цикл, связанный с нарушением апоптоза, накапливаются в паренхиматозных органах и органах кроветворения, нарушая их функцию.
Клиника.
1. Основным клиническим проявлением является локализованная или генерализованная лимфаденопатия (рис. 5.1.). Размеры увеличенных л/у в различных областях могут колебаться в широких пределах от 1-2 см до 10-15 см в диаметре. Л/у как
88
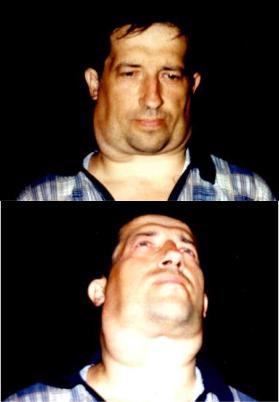
правило имеют тестоватую консистенцию, безболезненные, подвижные, не спаянные с подкожной клетчаткой и кожей, кожа над ними не изменена. Они могут локализоваться на шее, в подмышечных впадинах, в паху, средостении, брюшной полости и забрюшинном пространстве.
Рис. 5.1. Лимфоаденопатия у больного хроническим лимфолейкозом.
2.В 30-40% случаев - спленомегалия
3.В 20% случаев - гепатомегалия
4.Высокая активность CD5+клеток приводит к подверженности больных осложнениям аутоиммунного характера, например, аутоиммунной гемолитической анемии (почти у 50% больных), аутоиммунной тромбоцитопении (2-3%) или васкулитам.
5.Бактериальные, вирусные и грибковые инфекции характерны для ХЛЛ, особенно на поздних стадиях болезни у 70-80% пациентов. Возникновение рецидивирующих инфекций, особенно, пневмоний и опоясывающего герпеса связывают с
а) гипогаммаглобулинемией, которая является одним из ведущих признаков ХЛЛ и обусловлена снижением количества нормальных В-лимфоцитов.
б) с неспособностью лейкемических лимфоцитов продуцировать специфические антитела.
в) со снижением количества нормальных В-лимфоцитов, продуцирующих иммуноглобулины.
6.С нарушениями «иммунологического надзора» при ХЛЛ связывают также возможность развития второго или даже третьего онкологического заболевания.
7.При ХЛЛ возможно развитие геморрагического и/или анемического синдрома.
8.Неспецифические высыпания на коже – опоясывающий лишай, крапивница, эритема, опухолевидные разрастания.
9.Неспецифические В-симптомы - потливость, усталость, потеря веса
89
Классификация. В настоящее время при оценке и сопоставлении результатов терапии широко используются две классификации, отражающие стадийность течения болезни, - по
Rai и Binet.
Классификация по Rai: |
|
|
|
|
|
Стадия |
|
|
|
|
|
0 |
Только лимфоцитоз >15х109в крови и >30% в костном мозге |
|
|||
I |
Лимфоцитоз+лимфаденопатия |
|
|
|
|
II |
Лимфоцитоз+спленомегалия |
и/или |
гепатомегалия |
(независимо |
от |
лимфаденопатии) |
|
|
|
|
|
III |
Лимфоцитоз+анемия (снижение Hb<110 г/л) (независимо от увеличения |
||||
размеров л/у, селезенки, печени) |
|
|
|
|
|
IV |
Лимфоцитоз+тромбоцитопения |
<100х109/л (независимо |
от наличия других |
||
признаков) |
|
|
|
|
|
Классификация по Binet: |
|
|
|
|
|
Стадия |
|
|
|
|
|
А |
Увеличение л/у в 1-2 областях, Нв>100 г/л, Тр>100х109/л (0-II стадия по Rai). |
|
|||
B |
Увеличение л/у в 3-х областях и более, Нв>100 г/л, Тр>100х109/л (I-II стадия |
||||
по Rai) |
|
|
|
|
|
С |
Содержание Нв<100 г/л, Тр<100х109/л при любом количестве увеличенных |
||||
л/у, независимо от увеличения печени или селезенки (III-IV стадия по Rai) Выделяют также следующие варианты течения типичного В-ХЛЛ:
1.Медленно текущий – отличается стабильным течением с длительным сохранением 0 или А стадий, отсутствием инфекционных осложнений. Данный вариант болезни нередко имеет медиану выживаемости 25 лет.
2.Прогрессирующий – быстрое возрастание стадий заболевания. Такой вариант часто связан с атипичной морфологией лейкемических клеток, высоким лимфоцитозом в крови и диффузной опухолевой инфильтрацией костного мозга.
3.Трансформация ХЛЛ в крупноклеточную лимфому (синдром Рихтера) или пролимфоцитарный лейкоз.
А) Синдром Рихтера сопровождается клиническими признаками генерализации опухолевого процесса, прогрессированием анемии и тромбоцитопении, появлением в крови пролимфоцитов, тяжелыми аутоиммунными и инфекционными нарушениями, развитием кахексии и резистентности к терапии.
Б) Морфологическим субстратом пролимфоцитарного лейкоза являются крупные клетки с большим круглым ядром и выделяющимися ядрышками. В клинической картине превалирует спленомегалия; размеры печени также увеличены, умеренно выраженная лимфаденопатия; у 25% больных обнаруживаются кожные проявления. В лейкоцитарной формуле преобладают пролимфоциты (до 90%), выражен лейкоцитоз, анемия, тромбоцитопения. Иммунофенотип опухолевых клеток характеризуется экспрессией маркеров В-клеточной линии. Нередкой цитогенетической находкой при этом варианте является 14q+, которая обнаруживается у 60% больных.
По особенностям клинических проявлений, наряду с типичным вариантом выделяют Т-клеточный, опухолевый, костномозговой, селезеночный и волосатоклеточный варианты ХЛЛ.
1.Т-клеточный вариант характеризуется значительной спленомегалией, гепатомегалией, более частым вовлечением висцеральных л/у. По иммунологическим параметрам они чаще всего имеют фенотип CD4+, CD18-
2.При опухолевом варианте, как правило, невысокий лимфоцитоз в крови, л/у достигают больших размеров, преимущественно в брюшной полости, выраженная гепато- и
90

спленомегалия. Обнаруживается лейкозная инфильтрация различных органов с нарушением их функции
3.Костномозговой вариант характеризуется отсутствием увеличения л/у, печени
иселезенки и глубокой анемией в связи с диффузной инфильтрацией костного мозга лимфоцитами.
4.При селезеночном варианте – большая селезенка без увеличения л/у.
5.Волосатоклеточный лейкоз – для него характерна выраженная спленомегалия, анемия и (в отличие от типичной формы ХЛЛ) лейкопения с лимфоцитозом, а также тромбоцитопения.
Морфологической особенностью этой формы является выявление в костном мозге характерных патологических лимфоцитов с ворсинчатой цитоплазмой (не менее 10-15%), эксцентричным бобообразным ядром, с бледно-голубой или базофильной цитоплазмой (рис. 5.2.). Пункция костного мозга не всегда удачна из-за фиброзных изменений. Основная роль в развитии панцитопении при ВКЛ отводится гиперспленизму и фиброзу костного мозга, а также лейкемической инфильтрации миелоидной ткани с резким сужением плацдарма нормального гемопоэза.
90% лимфоцитов имеют иммунофенотип зрелых В-клеток. Наиболее специфичным маркером для ворсинчатых клеток является антиген CD103. Характерно отсутствие типичного для ХЛЛ антигена CD5.
Специфических хромосомных аномалий не выявлено, хотя примерно у 30% пациентов происходит инверсия хромосомы 5, в которой обнаруживаются изменения в длинном плече.
Рис. 5.2. Морфологическая картина костного мозга при волосатоклеточном лейкозе
Дополнительные методы исследования
I. Общий клинический анализ крови: увеличение уровня лейкоцитов, лимфоцитов, наличие промежуточных клеток лимфоидного рядя (пролимфоцитов), тени БоткинаГумпрехта – полуразрушенные ядра лейкоцитов (образовавшиеся при приготовлении мазков крови). Возможно наличие анемии и тромбоцитопении.
II. Миелограмма: более 30% лимфоцитов (рис. 5.3.)
III. Иммунофенотипирование: в клеточном клоне лейкемических лимфоцитов при В-
ХЛЛ обнаруживаются СD5+, CD19, CD20, CD21, CD23и CD24.
IV. Цитогенетическое исследование: специфические хромосомные аномалии при ХЛЛ не обнаружены. В то же время различные генетические нарушения удается выявить более чем у 80% пациентов. Наиболее частым цитогентическим отклонением при ХЛЛ является делеция 13q, которая отмечается у 55% больных.
5. Для уточнения размеров поражения л/у - ультразвуковое исследование органов грудной и брюшной полости.
91
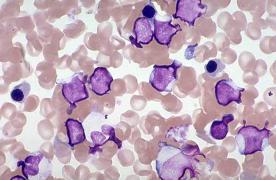
Рис. 5.3. Лимфоцитоз в костном мозге больного хроническим лимфобластным лейкозом
Диагноз. Для постановки диагноза ХЛЛ необходимы наличие
1)в периферической крови более 5х109 морфологически зрелых лимфоцитов,
2)более 30% лимфоцитов в аспирате костного мозга,
3)иммунологическое подтверждение присутствия В-клеточного клона лейкемических лимфоцитов (CD5, CD19, CD20(dim), CD 23).
Дифференциальный диагноз в первую очередь необходимо проводить с заболеваниями, сопровождающимися увеличением л/у, - злокачественными лимфомами и лимфогранулематозом. При этих заболеваниях л/у в отличие от ХЛЛ каменистой плотности, спаяны с окружающими тканями, зачастую кожа над ними гиперемирована. В ан крови при лимфомах реже встречается лейкоцитоз с лимфоцитозом, он менее выражен; для ЛГМ характерна лимфопения, эозинофилия. Решающее значение для диагностики ЛГМ имеет биопсия л/у, где обнаруживаются специфические клетки (Березовского-Штернберга). Для диф. диагноза лимфом и ХЛЛ важное значение имеет иммунофенотипирование с обнаружением специфических антигенов.
Лечение. В терапии больных ХЛЛ долгое время преобладала выжидательная тактика. И до сих пор вопрос о начале лечения заболевания продолжает дискутироваться. У тех больных, у которых лейкозный процесс годами протекает бессимптомно, от проведения специального лечения следует воздержаться, они требуют динамического наблюдения гематолога каждые 2-3 месяца.
Назначение цитостатической терапии должно быть обусловлено наличием следующих симптомов
1.прогрессирующая гепатоспленомегалия и/или лимфоаденопатия,
2.появление аутоиммунной гемолитической анемии или тромбоцитопении,
3.рецидивирующая инфекция.
4.неспецифические симптомы - потливость, усталость, потеря веса,
5.удвоение числа лимфоцитов менее чем за 6 мес,
6.массивная лейкемическая инфильтрация костного мозга (свыше 80% лимфоцитов в миелограмме),
7.лимфоидная инфильтрации костного мозга с развитием анемии или тромбоцитопении,
8.комплексные хромосомные нарушения.
Большинство химиотерапевтических средств, применяемых при лечении ХЛЛ, являются алкилирующими агентами (хлорбутин, лейкеран, циклофосфан) и нуклеозидными аналогами (флударабин). В последние годы предприняты попытки применения
92
