
796
.pdf
Йодное число, выражаемое числом граммов йода, которое может присоединяться к 100 г жира, является мерой ненасыщенности кислот жиров и применяется для оценки качества высыхающих масел и молока.
3. Электрофильные свойства sp2-гибридного углерода C + двойной углерод-углеродной связи:
− гидрирование (гидрогенизация) жидких жиров:
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2O |
|
|
|
|
|
|
|
C(CH2)7CH |
|
|
CH(CH2)7CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2O |
|
|
|
C C17H35 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
H Ni |
|
|
|
|
|
|
|
O |
|||||||||||
CHO |
|
|
C |
|
|
+ 3H |
|
CHO |
|
C |
|||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
(CH ) CH |
|
|
CH(CH ) CH |
.. |
|
|
|
|
|
|
|
|
|
C17H35 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
2 7 |
|
|
|
|
|
|
2 7 |
3 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
CH2O |
|
|
|
|
|
C(CH2)7CH |
|
CH(CH2)7CH3 |
|
|
|
CH2O |
|
|
C C17H35 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||
|
|
|
триолеоилглицерин |
|
|
|
|
|
тристеароилглицерин |
||||||||||||||||||||||
Гидрирование растительных масел лежит в основе производства маргарина.
Терпены
Многие терпены содержат одну или несколько двойных углеродуглеродных связей, поэтому подобно алкенам обладают как нуклеофильными, так и электрофильными свойствами.
1. Нуклеофильные свойства sp2-гибридного углерода C− двойной связи:
а) окисление кислородом воздуха:
|
. |
O |
O . |
O |
. |
|
.. |
|
|||||
. . |
. . |
. . |
O2 |
. . + O3 |
||
|
||||||
|
+ O O |
|
||||
|
α - пинен |
|
|
|
|
|
|
|
б) галогенирование: |
|
|||
|
|
. |
|
Br Br . |
||
|
|
.. . . + |
Br Br |
|
. . |
|
|
|
α - пинен |
211 |
|
|
|
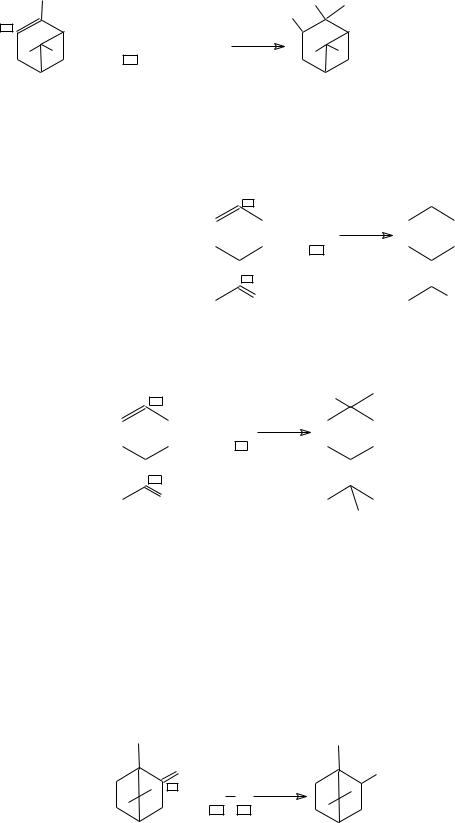
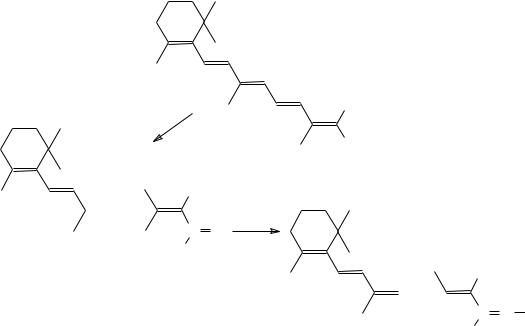
Воски применяются для защиты растений от потери влаги, поражения вредителями и болезнями; используются в производстве мазей, кремов, помад и мыл.
Терпены и терпеноиды (ментол, гераниол и др.) нашли применение в фармацевтической, парфюмерной и косметической промышленности в качестве отдушек. Камфора используется в производстве целлюлоида; в качестве стабилизатора – в производстве бездымного пороха; в медицине – как стимулятор работы сердца.
Каротиноиды применяются для витаминизации пищи и кормов для животных, в качестве пищевого красителя, в медицинской практике − при лечении кожных покровов. Витамин А является фактором роста, предотвращает высыхание роговицы глаз, повышает иммунитет.
Стероиды имеют большое биологическое значение: избыток холестерина, например, вызывает заболевание – атеросклероз; желчные кислоты, вырабатываемые печенью, участвуют в пищеварении, являются эмульгаторами жиров.
Половые гормоны являются регуляторами функции размножения.
214

4.2. Углеводы (сахара)
Углеводы – природные органические соединения, состав которых можно выразить формулой Cn(H2O)m. Формально молекулы углеводов состоят из углерода и элементов воды, что оправдывает их название и подтверждено экспериментально:
С (H O) |
+ m H SO |
конц. |
n C + m H SO |
. H O |
n 2 m |
2 4 |
2 4 |
2 |
Классификация. По отношению к реакции гидролиза все углеводы делят на две группы:
а) моносахариды с общей формулой Cn(H2O)m не подвергаются гидролизу;
б) полисахариды Cn(H2O)m-1 х, где x изменяется от 2 до нескольких десятков тысяч, подвергаются гидролизу с образованием моносахаридов.
В свою очередь, полисахариды делятся на дисахариды (x=2) олигоса-
хариды (x = 3−10) и полисахариды (x > 10).
Моносахариды по числу атомов углерода подразделяются на триозы
C3H6O3, тетрозы C4H8O4, пентозы C5H10O5, гексозы C6H12O6 и т.д. Незави-
симо от числа атомов углерода моносахариды делятся на альдозы, содержащие функциональную альдегидную группу, и кетозы с кетонной функциональной группой:
O C |
1 |
H |
|
CH2OH |
|||||
|
|
||||||||
|
|
|
|
|
|
C |
|
O |
|
H |
|
C2 |
|
OH |
|
||||
|
|
|
|||||||
|
|
|
|||||||
|
|
|
|
|
|
||||
H |
|
C3 |
|
OH |
CH2OH |
||||
|
|
||||||||
H |
|
C4 |
|
OH |
кетотриоза |
||||
|
|
(диацетоновый спирт) |
|||||||
|
|
|
|
|
|
||||
|
5CH2OH |
|
|
|
|
||||
альдопентоза (рибоза) |
|
|
|
|
|||||
Полисахариды, в зависимости от моносахаридного состава, делятся на две группы:
а) гомополисахариды, состоящие из одного типа моносахаридов, например, целлюлоза – полимер глюкозы;
б) гетерополисахариды – сополимеры, в состав которых входят остатки разных полисахаридов, например, глюкоманнаны – полимеры глюкозы и маннозы.
По числу атомов углерода в элементарном звене полисахариды делятся на пентозаны – полимеры пентоз и гексозаны – полимеры гексоз.
215
Нахождение в природе. Углеводы широко распространены в природе, они составляют 80% сухого вещества растений и около 2% сухого вещества животных.
Моносахариды в свободном виде содержатся во фруктах: глюкоза − в винограде и других фруктах, фруктоза – в меде. Моносахариды находятся в природе также в связанном состоянии в виде ди- и полисахаридов, дубильных веществ типа танина, сложных белков – глюко- и нуклеопротеидов.
Дисахариды содержатся во многих растениях – сахарном тростнике, сахарной свекле, кленовом, пальмовом, березовом соках и др.
Древесина содержит до 45% полисахарида целлюлозы, а волокна хлопка, льна и конопли − более 90%. Крахмал содержат многие корнеплоды, злаки и фрукты, Животный крахмал − гликоген содержится в печени и мышцах.
Методы получения. Углеводы образуются в природе в зеленых листьях растений реакцией фотосинтеза:
n CO2 + m H2O |
h |
Сn (H2O) m + n O2 |
|
хлорофилл |
|||
|
|
В промышленности углеводы получают из природного растительного сырья, например, сахарозу получают из сахарной свеклы или сахарного тростника, крахмал – из картофеля или злаков. Также разработаны синтетические методы получения углеводов.
1. Моносахариды:
а) гидролиз полисахаридов:
|
H+ |
(C6H10O5)n + n H2O |
солод nC6H12O6 |
б) поли меризация формальдегида:
|
|
|
O |
Ca(OH)2 |
|
6 H |
|
C |
|
C6H12O6 |
|
|
|
|
|||
|
|
|
H
216
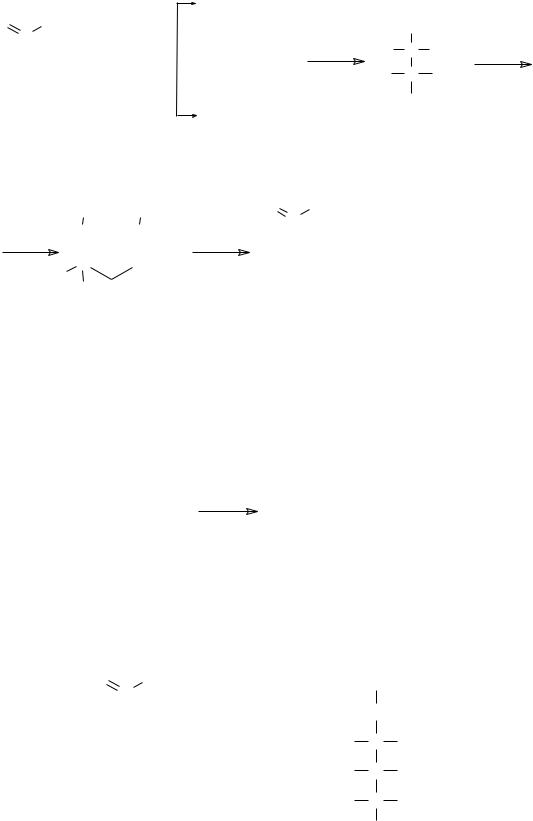

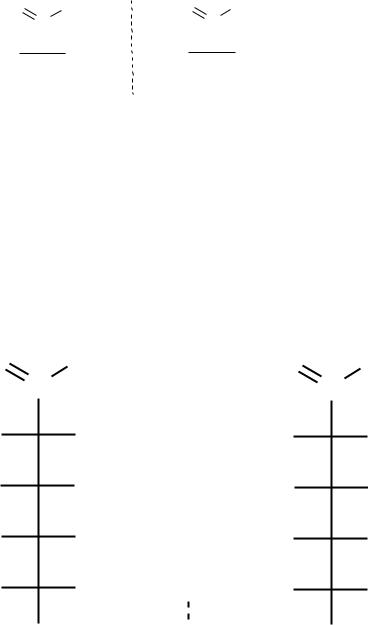
O |
C H |
O |
C H |
||||
H |
|
* |
OH |
HO |
|
* |
H |
|
|
|
|
|
|
|
|
|
CH2OH |
|
CH2OH |
||||
D(+)-глицериновый |
L( )- глицериновый |
||||||
− |
|
|
|
||||
|
альдегид |
|
альдегид |
||||
Для более быстрого и удобного написания конфигураций моноз Э.Фишером предложено изображать их проекционными формулами без обозначения промежуточных (между концевыми функциональными группами) углеродных атомов:
O С H |
|
|
|
|
|
|
O С H |
||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
|
|||||||||||
H |
* |
OH |
|
|
|
|
|
|
HO |
* |
H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
||||||||||
|
|
||||||||||
|
|
|
|||||||||
HO |
* |
H |
|
|
|
|
|
|
H |
* |
OH |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|||||||||
|
|
|
|
||||||||
|
|
|
|
||||||||
H |
* |
OH |
|
|
|
|
|
|
HO |
* |
H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
||||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|||||||
H |
* |
OH |
|
|
|
|
|
|
HO |
* |
H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
CH2OH |
|
CH2OH |
|
||
|
||
|
||
|
||
|
||
|
||
D(+)- глюкоза |
|
L( )-глюкоза |
|
||
|
|
− |
Природные моносахариды относятся D-ряду;
219
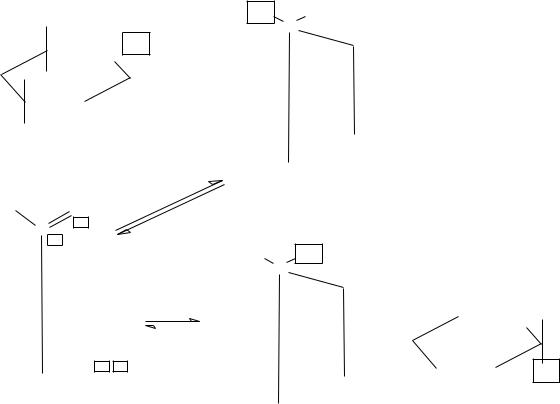
в) кольчато-цепная таутомерия:
H |
|
CH2OH |
|
|
HO C H |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
O |
OH |
|
H |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
OHH |
|
H |
|
|
или |
HO |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
OH |
|
|
|
|
|
|
H |
|
H |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
H |
|
OH |
|
H |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
кольчатая форма, |
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D( ) глюкопираноза, [ ]D = 19 |
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
C |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
- |
+ - |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
H |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
C |
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
OH |
глюкозидный |
|
|
|
|
|
|
|
|||||||||
H |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
C |
|
|
|
|
|
гидроксил |
|
|
CH2OH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
HO |
|
|
|
|
H |
|
H |
|
|
|
|
|
|
|
OH |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
O H |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
HO |
|
|
|
|
|
|
|
H |
|
или |
|
|
OH |
|
H |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
|
|
|
|
|
OH |
|
H |
|
|
|
|
|
|
|
OH |
|
|
H |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
CH2OH |
|
H |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
||||||||||||||||
цепная форма D(+)- глюкозы |
|
|
|
|
|
|
|
CH2OH |
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кольчатая форма, |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20= 113 0C |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α- D(+ )- глюкопираноза, [α] |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
D |
||
Вкристаллической форме моносахариды имеют кольчатое строение
иявляются внутренними кольчатыми полуацеталями. В растворе они представлены двумя кольчатыми и одной цепной таутомерными формами,
находящимися в динамическом равновесии. Кольчатые α−и −формы имеют разные физические свойства. При растворении одной из
кристаллических форм глюкозы быстро наступает равновесие, что характеризуется изменением угла вращения плоскополяризованного луча света до 520. Это явление получило название мутаротация.
Для дисахаридов и полисахаридов характерны 3 типа изомерии:
а) структурная изомерия, обусловленная различными типами моносахаридов, образующих дисахарид:
220

 2
2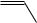


 C N белок
C N белок O
O C
C