
- •3. Острый коронарный синдром: патогенез, диагностика, врачебная тактика в зависимости от формы острого коронарного синдрома
- •Классификация митрального стеноза по степени тяжести.
- •10. Инфекционный эндокардит. Определение. Предрасполагающие факторы. Этиология. Патогенез. Клиническая картина. Критерии диагностики. Принципы лечения.
- •14. Суправентрикулярная экстрасистолия: Определение. Механизмы возникновения, диагностика, лечение.
- •15. Желудочковая экстрасистолия: Определение, механизмы возникновения, диагностика, классификация, лечение.
- •17. Гипертрофическая кардиомиопатия. Определение. Нарушение внутрисердечной гемодинамики. Клиническая картина. Диагностика. Лечение.
- •19. Неотложные состояния в кардиологии: отек легких, сердечная астма. Этиология, патогенез, клиническая картина, лечение
- •23. Пневмония. Определение. Этиология. Классификация. Патогенез пневмонии. Клиническая картина. Лабораторная и инструментальная диагностика пневмонии. Лечение. Принципы антибактериальной терапии.
- •24. Легочная гипертензия. Тромбоэмболия легочной артерии. Патогенез гемодинамических расстройств. Клинические проявления. Диагностика. Лечение.
- •25. Хронический гастрит. Определение. Актуальность темы. Классификация. Основные патогенетические механизмы при хроническом гастрите (тип А, В, С). Клиническая картина. Методы обследования больного. Лечение хронического гастрита.
- •27. Хронический гепатит. Определение. Актуальность проблемы. Классификация. Этиология. Патогенез хронических гепатитов. Основные клинические синдромы. Лабораторная и инструментальная диагностика. Основные лабораторные синдромы. Принципы терапии.
- •31. Хронический гломерулонефрит. Определение. Этиология, патогенез. Классификация. Основные клинические проявления. Методы обследования. Принципы терапии, прогноз.
- •33. Интерстициальный нефрит. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •34. Острое повреждение почек. Определение. Понятие преренальной, ренальной, постренальной острой почечной недостаточности. Клиническая картина. Диагностика. Лечение.
- •36. Железодефицитная анемия. Понятие. Распространенность. Роль железа в организме. Этиология и патогенез. Клиническая картина. Диагностика железодефицитной анемии. Лечение. Прогноз и профилактика.
- •37. В12 (фолиево)–дефицитная анемия. Понятие. Распространенность. Роль витамина В12 и фолиевой кислоты в организме. Этиология и патогенез. Основные клинические синдромы. Диагностика В12-дефицитной анемии. Лечение. Прогноз и профилактика.
- •38. Гемолитические анемии. Определение. Классификация. Понятие внутрисосудистого и внутриклеточного гемолиза. Клиническая картина, диагностика Приобретенные гемолитические анемии. Патогенез. Клиническая картина. Диагностика. Лечение.
- •39. Острый лейкоз. Определение. Этиология. Механизмы нарушения кроветворения. Классификация. Основные клинические синдромы. Методы диагностики. Критерии диагностики острых лейкозов. Принципы терапии. Критерии ремиссии. Прогноз.
- •Этиология.
- •Механизмы нарушения кроветворения.
- •Классификация.
- •Основные клинические синдромы.
- •Критерии диагностики острых лейкозов.
- •Принципы терапии.
- •Критерии ремиссии.
- •Прогноз.
- •42. Геморрагические диатезы. Механизмы первичного и вторичного гемостаза. Классификация. Типы кровоточивости и их клинико-лабораторные критерии.
- •43. Понятие о коагулопатии. Гемофилия. Этиология. Патогенез. Клиническая картина. Прогноз. Лечение.
- •45. Тромбофилии. Классификация (первичные и вторичные тромбофилии). Понятие о первичных тромбофилиях.
- •46. Антифосфолипидный синдром. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •47. Подагра. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •48. Остеоартрит. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •1) остеоартроз, ассоциированный с эндокринными и метаболическими заболеваниями:
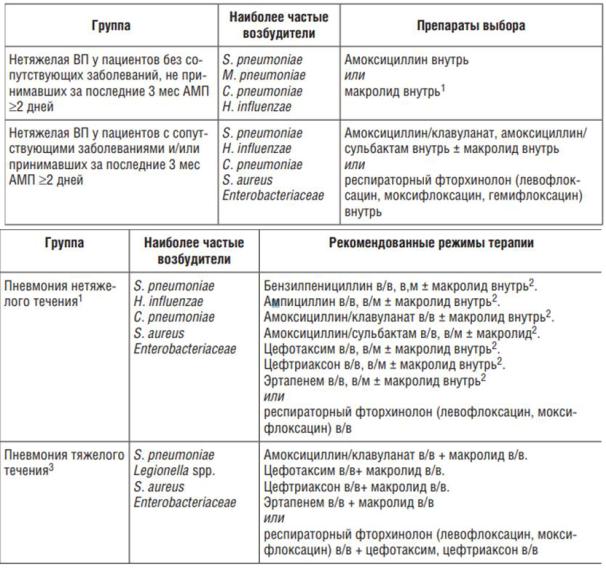
*предпочтительна ступенчатая терапия ** Макролиды являются препаратами выбора при подозрении на «атипичную» этиологию ВП
(C. pneumoniae, M. pneumoniae). Следует отдавать предпочтение наиболее изученным при ВП макролидам с улучшенными фармакокинетическими свойствами (азитромицин, кларитромицин) или благоприятным профилем безопасности и минимальной частотой лекарственных взаимодействий (джозамицин, спирамицин).
24. Легочная гипертензия. Тромбоэмболия легочной артерии. Патогенез гемодинамических расстройств. Клинические проявления. Диагностика. Лечение.
Критерием легочной гипертензии (ЛГ) является повышение давления в легочной артерии:
●систолическое — выше 30 мм рт.ст.;
●диастолическое — выше 9 мм рт.ст.;
●среднее — выше 20 мм рт.ст.
Патогенез легочной гипертензии: ЛГ обусловлена, прежде всего, прекапиллярной легочной вазоконстрикцией, возникающей в ответ на альвеолярную гипоксию. Авторы предположили, что констрикция легочных сосудов в недостаточно вентилируемых участках легких приводит к смещению кровотока из этих участков в зоны с лучшей вентиляцией, тем самым уменьшая шунтирование крови. Этот феномен известен как рефлекс Эйлера–Лильестранда. Генерализованное повышение тонуса мелких артериальных сосудов легких приводит к развитию легочной артериальной гипертензии (ЛГ). В начале болезни легочная вазоконстрикция носит обратимый характер и может регрессировать при коррекции газовых расстройств на фоне лечения. Однако по мере прогрессирования патологического процесса в легких альвеолярно-капиллярный рефлекс утрачивает свое положительное значение из-за
развития генерализованного спазма легочных артериол, что усугубляет ЛГ, и при стойких нарушениях газового состава крови она трансформируется из лабильной в стабильную.
Т.О., важнейшими причинами ЛГ являются альвеолярная гипоксия и гипоксемия, вызывающие, соответственно, локальную вазоконстрикцию и генерализованное сужение артериол. Тромбоэмболия легочной артерии (ТЭЛА) – окклюзия ствола или основных ветвей легочной артерии тромбом или его частичками, сформировавшимися, в основном, в венах нижних конечностей, малого таза, реже в полостях правых отделов сердца и занесенными током крови в легочную артерию.
Факторы риска ТЭЛА
Высокий риск (ОШ>10)
●Перелом шейки бедренной кости/нижней конечности.
●Госпитализация по поводу ХСН III–IV степени/фибрилляции/трепетания предсердий в течение последних 3 мес.
●Протезирование тазобедренного/коленного суставов.
●Тяжелая травма.
●Травма спинного мозга.
●ОИМ в течение последних 3 мес.
●ВТЭ в анамнезе.
Средний риск (ОШ 2–9)
●Артроскопическая операция коленного сустава.
●Аутоиммунное заболевание.
●Переливание крови.
●Центральный венозный катетер.
●Химиотерапия злокачественной опухоли.
●Застойная ХСН/ДН.
●Применение эритропоэтинов.
●Заместительная гормональная терапия.
●Экстракорпоральное оплодотворение.
●Инфекции (пневмония, инфекции мочевых путей, ВИЧ).
●Воспалительные заболевания кишечника.
●Злокачественная опухоль (особенно метастазирующая).
●Применение пероральных контрацептивных препаратов.
●Послеродовый период.
●Тромбоз поверхностных вен.
●Тромбофилия. Низкий риск (ОШ<2)
●Постельный режим более 3 дней.
●Сахарный диабет.
●Артериальная гипертензия.
●Длительное пребывание в положении сидя (самолет/автомобиль).
●Пожилой возраст.
●Лапароскопическая операция.
●Ожирение.
●Беременность.
●Варикозное расширение вен.
Патогенез
Ведущим фактором, определяющим степень гемодинамических расстройств и нарушения вентиляционно-перфузионных соотношений при ТЭЛА, является обструкция легочноартериального русла, степень кот зависит от:
●объема самого тромбоэмбола;
●выраженности генерализованного спазма легочных артериол, происходящего рефлекторно и под воздействием гуморальных вазоконстрикторных факторов, высвобождающихся из тромбоцитов (тромбоксана А2, серотонина, гистамина и др.). В результате возникает несоответствие между размерами тромбоэмбола и выраженностью клинической картины ТЭЛА; скоростью образования вторичного местного тромба, формирующегося в зоне локализации тромбоэмбола и увеличивающего его размеры.
ДН и артериальная гипоксемия возникают в результате прекращения кровотока в хорошо вентилируемых альвеолах, что приводит к увеличению внутрилегочного «мертвого пространства» и ухудшению газообмена. Нарушение вентиляционно-перфузионных соотношений усугубляется выраженным бронхоспазмом, связанным с воздействием на гладкую мускулатуру мелких бронхов биологически активных веществ, выделяющихся из. Кроме того, в результате ишемии альвеол, обусловленной их недостаточной перфузией, нарушается не только их вентиляция, но и выработка сурфактанта, что уже спустя 1–2 сут после ТЭЛА может привести к развитию ателектазов. Вследствие недостаточности кровоснабжения альвеол может развиться инфаркт легкого. Кроме того, снижение кровоснабжения хорошо вентилируемых альвеол еще больше нарушает газообмен в легких и приводит к усугублению артериальной гипоксемии. Наконец, в результате повышения давления проксимальнее области окклюзии открываются артериовенозные анастомозы и происходит шунтирование крови из артериол в вены, что также усугубляет артер гипоксемию.
Вторым следствием окклюзии ветвей легочной артерии является легочная АГ. Она обусловлена:
●механической окклюзией сосудистого русла тромбоэмболом;
●генерализованным спазмом артериол.
В результате на фоне уменьшения емкости артер русла в легких повышается легочное сосудистое сопротивление. Это приводит к значительному ограничению венозного притока крови в левые отделы сердца и развитию синдрома малого сердечного выброса. В тяжелых случаях могут развиться признаки так называемого обструктивного шока, включая потерю сознания (синкопе), значительное снижение АД, уменьшение диуреза, стенокардию и др. Значительные цифры давления в легочной артерии и увеличение постнагрузки на ПЖ могут привести к развитию острого легочного сердца. Повышается систолич и конечнодиастолическое давление в ПЖ, ПП, желудочек и предсердие дилатируются и возникает застой крови в венозном русле большого круга кровообращения.
Выраженность пат проявлений зависит от массивности тромбоэмболии, а также от локализации тромбоэмбола. Наиболее яркие клинические проявления ТЭЛА возникают, когда острое ограничение легочного кровотока достигает 60% от объема всего сосудистого русла легких.
Клиническая картина определяется объемом эмболизации легочного сосудистого русла, локализацией тромбоэмбола, уровнем легочной АГ, степенью гемодинамических расстройств и другими факторами. С практической точки зрения два варианта:
●массивную и субмассивную ТЭЛА;
●немассивную ТЭЛА.
Массивная и субмассивная ТЭЛА обусловлены тотальной и субтотальной окклюзией крупной проксимальной ветви или ствола легочной артерии. Протекает бурно, с яркой клинической симптоматикой и часто заканчивается внезапной смертью. Немассивная ТЭЛА связана с эмболией мелких ветвей легочной артерии.
Основные клинические синдромы при массивной и субмассивной ТЭЛА:
●ДН;
●инфаркт легкого или инфарктная пневмония;
●плеврит (сухой или экссудативный, в том числе геморрагический);
●острое легочное сердце;
●артериальная гипотензия;
●нарушение перфузии внутренних органов.
Жалобы:
1.внезапно появившаяся необъяснимая одышка в покое (ЧД>30 в минуту);
2.боли в грудной клетке (могут локализоваться за грудиной, носят хар-р плевральных болей, усиливающихся при дыхании, кашле и обусловленных развитием инфаркта легкого, инфаркт-пневмонии или сухого плеврита);
3.непродуктивный кашель;
4.кровохарканье;
5.при инфаркт-пневмонии повышение температуры тела;
6.снижение АД, коллапс, разнообразные церебральные расстройства (головокружение, непроизвольные мочеиспускание, дефекация, судороги в конечностях).
Объективное исследование:
1.цианоз в сочетании с бледностью кожных покровов (обусловлено снижением АД и нарушением периферического кровообращения). В некоторых случаях появляется «чугунный» цианоз лица, области шеи и верхней половины туловища;
2.в легких — ослабление дыхания, мелкопузырчатые хрипы или крепитация (инфарктпневмония), шум трения плевры;
3.ССС: тахикардия, акцент II тона на легочной артерии, отражающий гипертензию в малом круге кровообращения. Снижение АД. Набухание шейных вен;
4.при развитии острого легочного сердца выслушивается III тон в пятом межреберье по левому краю грудины. В этом случае правая граница относительной сердечной тупости смещается вправо.
Немассивная ТЭЛА может быть бессимптомна или с менее выраженными симптомами. Немассивная ТЭЛА протекает «под маской» других заболеваний и симптомов:
● повторные «пневмонии» неясной этиологии; ● быстро проходящие в течение 2–3 сут сухие плевриты;
● экссудативные плевриты, в том числе геморрагические; ● повторные «необъяснимые» обмороки, коллапсы, нередко сопровождающиеся чувством нехватки воздуха и тахикардией;
● внезапно возникающее чувство сдавления в груди, затруднения дыхания и последующее повышение температуры тела; ● «беспричинная» лихорадка, не поддающаяся антибактериальной терапии;
● появление и/или прогрессирование симптомов подострого или хронического легочного сердца при отсутствии указаний на хронические заболевания бронхолегочного аппарата.
Диагностика
Лаб и инструментальная диагностика:
1.ЭКГ.
2.Газы артериальной крови.
3.D-димер плазмы.
4.Рентгенография органов грудной клетки.
5.Эхокардиография.
6.Вентиляционно-перфузионная сцинтиграфия легких.
7.Ультразвуковое исследование магистральных вен нижних конечностей.
8.Спиральное КТ-сканирование.
9.Легочная ангиография.
Дополнительно:
1. Катетеризация правых отделов сердца.
ЭКГ. Для исключения ОИМ, для диагностики нарушений сердечного ритма, которые часто обнаруживают у больных с ТЭЛА. В 20–25% случаев при массивной ТЭЛА наблюдаются признаки острой перегрузки правых отделов сердца:
●внезапное углубление зубцов QIII и SI (синдром QIIISI);
●подъем сегмента ST в отведениях III, aVF, V1 и V2 и дискордантное снижение сегмента
ST в отведениях I, aVL, V5 и V6;
●появление отрицательных зубцов Т в отведениях III, aVF, V1 и V2;
●полная и неполная блокада правой ножки пучка Гиса.
D-димер является продуктом деградации фибрина. Его уровень повышается ввиду одновременной активации системы коагуляции и фибринолиза. Нормальный уровень D- димера с высокой степенью вероятности позволяет исключить ТЭЛА и ТГВ (отрицательная прогностическая ценность высокая). В то время как его повышение может быть обусловлено как ТЭЛА, так и такими состояниями, как онкология, воспаление, кровотечение, травма, хирургические вмешательства и некроз (положительная прогностическая ценность низкая).
Рентгенография органов грудной клетки:
●высокое стояние купола диафрагмы на стороне поражения;
●инфильтрация легочной ткани (спустя 12–36 ч от начала заболевания);
●выбухание конуса легочной артерии;
●увеличение правых отделов сердца;
●расширение верхней полой вены и др.
Более специфичен, но редок симптом Вестермарка — обеднение легочного рисунка в области поражения (при массивной ТЭЛА).
Вентиляционно-перфузионная сцинтиграфия легких: наличие выраженного локального снижения перфузии участка легкого при отсутствии здесь сколько-нибудь значительных вентиляционных расстройств и изменений на обычной рентгенограмме. Диагностическая точность 90%.
Мультиспиральная компьютерная ангиография легких в ангиорежиме:
●полная обтурация одной из ветвей легочной артерии и формирование «культи» одной из крупных ее ветвей;
●резкое локальное обеднение сосудистого рисунка, соответствующее бассейну эмболизированной артерии;
●внутриартериальные дефекты наполнения;
●расширение обтурированной ветви легочной артерии проксимальнее места обструкции. В связи с неспецифичностью клинических данных и результатов обычных исследований в диагностике ТЭЛА рекомендовано применение вероятностных шкал. При таком подходе частота правильно установленного диагноза возрастает.
Вероятность ТЭЛА по шкале Уэллса (Wells score) и вероятность ТЭЛА по Женевской (Geneva) шкале
Лечение
1.Тромболитическая терапия: стрептокиназа, урокиназа, альтеплаза.
2.Антикоагулянтная терапия прямыми антикоагулянтами.
3.Антикоагулянтная терапия непрямыми антикоагулянтами.
4.Хирургическое лечение: эмболэктомия, установка кава-фильтра.
Тромболитическая терапия направлена на восстановление легочной перфузии. Ее эффективность тем выше, чем раньше от момента появления симптомов начато введение тромболитика.
Хирургическую эмболэктомию проводят, если имеются противопоказания к выполнению тромболизиса или он оказался неэффективен.
Несколько этапов:
1.В первые 5–7 дней применяют парентеральные антикоагулянты: нефракц гепарин (ВМГ) под контролем АЧТВ или низкомолекулярный гепарин (НМГ), или фондапаринукс. Согласно современным данным на начальном этапе так же мб применены НОАК: ривароксабан или апиксабан, но при условии увеличения их дозы.
2.Для дальнейшего лечения назначают пероральные антикоагулянты: либо антагонист витамина К — варфарин, либо НОАК (ривароксабан, апиксабан, дабигатран). Подбор дозы варфарина проводится под «прикрытием» парентеральных антикоагулянтов, т.е. отмена ВМГ или НМГ или фондапаринукса возможна только при достижении уровня МНО 2,0–3,0. Преимуществом в назначении НОАК является возможность применения фиксированных доз и отсутствие необходимости регулярного лаб контроля.
3.Продолжительность антикоагулянтной терапии зависит от фактора, спровоцировавшего ТЭЛА. Если это временный или обратимый фактора (например, оперативное лечение, травма, иммобилизация, беременность, прием КОК), то после его устранения лечение антикогулянтами ограничивают тремя месяцами. Если же развитие ТЭЛА обусловлено наличием необратимого фр или фактора, кот не может быть устранен за 3 мес (напр, активный злокачественный процесс), то лечение антикоагулянтами продолжают «неопределенно долго». Но «неопределенная длительность» не означает «пожизненное лечение». Такой подход показывает, что этим пациентам периодически (каждые 3–6 мес) должна проводиться оценка факторов риска для определения дальнейшей тактики.
С целью вторичной профилактики ТЭЛА возможна имплантация кава-фильтров в инфраренальную часть нижней полой вены. При этом кровь свободно проходит через ячейки кава-фильтра, а потенциально опасные (крупные) тромбы застревают в нем. Под действием противосвертывающей системы крови застрявшие тромбы растворяются прямо на фильтре. Но если этого не происходит, требуется повторное вмешательство.
