
- •3. Острый коронарный синдром: патогенез, диагностика, врачебная тактика в зависимости от формы острого коронарного синдрома
- •Классификация митрального стеноза по степени тяжести.
- •10. Инфекционный эндокардит. Определение. Предрасполагающие факторы. Этиология. Патогенез. Клиническая картина. Критерии диагностики. Принципы лечения.
- •14. Суправентрикулярная экстрасистолия: Определение. Механизмы возникновения, диагностика, лечение.
- •15. Желудочковая экстрасистолия: Определение, механизмы возникновения, диагностика, классификация, лечение.
- •17. Гипертрофическая кардиомиопатия. Определение. Нарушение внутрисердечной гемодинамики. Клиническая картина. Диагностика. Лечение.
- •19. Неотложные состояния в кардиологии: отек легких, сердечная астма. Этиология, патогенез, клиническая картина, лечение
- •23. Пневмония. Определение. Этиология. Классификация. Патогенез пневмонии. Клиническая картина. Лабораторная и инструментальная диагностика пневмонии. Лечение. Принципы антибактериальной терапии.
- •24. Легочная гипертензия. Тромбоэмболия легочной артерии. Патогенез гемодинамических расстройств. Клинические проявления. Диагностика. Лечение.
- •25. Хронический гастрит. Определение. Актуальность темы. Классификация. Основные патогенетические механизмы при хроническом гастрите (тип А, В, С). Клиническая картина. Методы обследования больного. Лечение хронического гастрита.
- •27. Хронический гепатит. Определение. Актуальность проблемы. Классификация. Этиология. Патогенез хронических гепатитов. Основные клинические синдромы. Лабораторная и инструментальная диагностика. Основные лабораторные синдромы. Принципы терапии.
- •31. Хронический гломерулонефрит. Определение. Этиология, патогенез. Классификация. Основные клинические проявления. Методы обследования. Принципы терапии, прогноз.
- •33. Интерстициальный нефрит. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •34. Острое повреждение почек. Определение. Понятие преренальной, ренальной, постренальной острой почечной недостаточности. Клиническая картина. Диагностика. Лечение.
- •36. Железодефицитная анемия. Понятие. Распространенность. Роль железа в организме. Этиология и патогенез. Клиническая картина. Диагностика железодефицитной анемии. Лечение. Прогноз и профилактика.
- •37. В12 (фолиево)–дефицитная анемия. Понятие. Распространенность. Роль витамина В12 и фолиевой кислоты в организме. Этиология и патогенез. Основные клинические синдромы. Диагностика В12-дефицитной анемии. Лечение. Прогноз и профилактика.
- •38. Гемолитические анемии. Определение. Классификация. Понятие внутрисосудистого и внутриклеточного гемолиза. Клиническая картина, диагностика Приобретенные гемолитические анемии. Патогенез. Клиническая картина. Диагностика. Лечение.
- •39. Острый лейкоз. Определение. Этиология. Механизмы нарушения кроветворения. Классификация. Основные клинические синдромы. Методы диагностики. Критерии диагностики острых лейкозов. Принципы терапии. Критерии ремиссии. Прогноз.
- •Этиология.
- •Механизмы нарушения кроветворения.
- •Классификация.
- •Основные клинические синдромы.
- •Критерии диагностики острых лейкозов.
- •Принципы терапии.
- •Критерии ремиссии.
- •Прогноз.
- •42. Геморрагические диатезы. Механизмы первичного и вторичного гемостаза. Классификация. Типы кровоточивости и их клинико-лабораторные критерии.
- •43. Понятие о коагулопатии. Гемофилия. Этиология. Патогенез. Клиническая картина. Прогноз. Лечение.
- •45. Тромбофилии. Классификация (первичные и вторичные тромбофилии). Понятие о первичных тромбофилиях.
- •46. Антифосфолипидный синдром. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •47. Подагра. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •48. Остеоартрит. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •1) остеоартроз, ассоциированный с эндокринными и метаболическими заболеваниями:
-Расщепление или раздвоение II тона, связанное с неодновременным захлопыванием клапанов легочной артерии и аорты из-за удлинения систолы правого желудочка в условиях повышенного давления в легочной артерии.
-Диастолический шум (шум Грехема-Стилла) - появляется из-за относительной недостаточности клапанов легочной артерии, которая развивается вследствие дилатации фиброзного кольца клапанов легочного ствола у больных митральным стенозом с выраженной гипертензией в малом круге кровообращения. Этот шум является функциональным, диастолическим, высокочастотным, убывающим, тихим, имеет дующий характер, возникает сразу после II тона. У пациентов с митральным стенозом выявляется pulsus differens (симптом Попова) (пульс неодинаковый на правой и левой руках, т.к. при значительной дилатации левого предсердия сдавливается левая подключичная артерия, и наполнение пульса слева уменьшается). Пульс мягкий, слабого наполнения, малый (из-за уменьшения систолического объема левого желудочка при значительной степени сужения митрального отверстия), частый, неравномерный, аритмичный (при наличии мерцательной аритмии).
Инструментальная диагностика
ЭКГ — позволяет выявить признаки гипертрофии ЛП и ПЖ, а также различные нарушения ритма. Характерными признаками гипертрофии ЛП являются:
•раздвоение и увеличение амплитуды зубца Р в отведениях I, II, AVL, V5, V6
(P-mitrale);
•увеличение продолжительности отрицательной (левопредсердной) фазы в отведении V1;
•увеличение общей длительности Р более 10 мсек.
Гипертрофия ПЖ характеризуется наличием высокого зубца R в отведениях V1 иV2, когда RV1 ≥ SV2. В отведениях V5, V6 специфично появление глубокого зубца S. Электрическая ось сердца при гипертрофии ПЖ часто отклонена вправо или расположена вертикально.
Характерными нарушениями ритма являются наджелудочковая экстрасистолия, фибрилляция и трепетание предсердий, которые диагностируются по ЭКГ.
Рентгенография органов грудной клетки. В прямой проекции отмечается выравнивание левого контура сердца и сглаживание талии сердца за счет увеличения ЛП и выбухания дуги ЛА. Такая кон-
фигурация получила название «митральной». Усиление сосудистого рисунка в лёгких, плевральный выпот. Септальные линии, известные как линии Керли, свидетельствуют об отеке междолевых щелей и переполнении лимфатических сосудов.
Методом верификации митрального стеноза является ЭхоКГ.
Рекомендуется эхокардиография у пациентов для диагностики МС, оценки гемодинамической тяжести (средний градиент, площадь МК и давление в легочной артерии) и сопутствующих пороков клапанов, морфологии клапана.
Рекомендуется эхокардиография для динамического наблюдения пациентов с ранее диагностированным МС.
Рекомендуется чреспищеводная эхокардиография при МС для установления наличия тромба в левом предсердии, а также для оценки морфологии и гемодинамики МК у пациентов, когда затруднена визуализация при трансторакальной эхокардиография.
Классификация митрального стеноза по степени тяжести.
В зависимости от площади митрального отверстия выделяют три степени МС:
•легкий МС — площадь отверстия от 2 до 4 см2;
•умеренный МС — площадь отверстия от 1 до 2 см2;
•тяжелый (критический) — площадь отверстия менее 1 см2.
Показания и методы хирургического лечения
Показания к оперативному лечению:
•тромбэмболии сосудов большого круга кровообращения в анамнезе;
•тяжелый МС;
• умеренный МС (площадь МО 1–2 см²) в сочетании с выраженными клиническим проявлениями.
В настоящее время используются следующие методы хирургической коррекции:
•баллонная вальвулопластика — при изолированном или преобладающем МС без выраженных подклапанных изменений или у тяжелых, соматически неоперабельных больных. Противопоказанием к баллонной вальвулопластике является недавний (до 6 мес) эпизод тромбоэмболии;
•комиссуротомия — открытая или закрытая;
•протезирование МК.
Запомните!
При имплантации искусственных клапанов пациенты пожизненно принимают непрямые антикоагулянты (варфарин). Необходимо проводить профилактику инфекционного эндокардита.
Терапевтической лечение
Фармакологическое лечение больных с МС направлено на уменьшение выраженности ЛГ. С этой целью показано применение средств, ограничивающих приток крови в ЛА: диуретиков (фуросемид, торасемид), нитратов (изосорбида 5-ди- нитрат, изосорбида 5-мононитрат).
При наличии синусовой тахикардии показано применение β-адреноблокаторов (метопролол, бисопролол, карведилол). При возникновении тахисистолической формы ФП показано применение сердечных гликозидов, β-адреноблокаторов с целью урежения ЧСС.
Запомните!
Применение сердечных гликозидов у больных с МС при синусовом ритме противопоказано, так как повышение ударного объема ПЖ увеличивает приток и, соответственно, застой крови в малом круге.
С целью профилактики тромбоэмболических осложнений у больных с ФП показано назначение непрямых пероральных антикоагулянтов (варфарина) под контролем МНО (целевые значения 2,0–3,0).
Выраженная правожелудочковая недостаточность требует продолжения терапии петлевыми диуретиками, назначения антагонистов альдостерона (спиронолактон). Целесообразно применение ингибиторов АПФ (эналаприл, периндоприл, лизиноприл) или антагонистов рецепторов к ангиотензину II (лозартан, валсартан, эпросартан), которые снижают активность ренин-ангиотензин-альдостероновой системы (РААС) и положительно влияют на процессы ремоделирования сердца и сосудов. Возникновение тромбоэмболических осложнений требует применения прямых антикоагулянтов (гепарина, НМГ) с последующим переходом на пероральную терапию варфарином.
7. Митральная недостаточность Определение. Этиология. Патогенез гемодинамических изменений. Клиническая картина. Инструментальная диагностика. Классификация митральной регургитации по степени тяжести. Показания к хирургическому лечению. Возможности терапевтической коррекции.
Митральная недостаточность — неполное смыкание створок МК, приводящее к патологическому забросу крови (регургитации) в ЛП из ЛЖ во время его систолы.
Этиология
Различают две формы МН: органическую и функциональную. Органическая недостаточность характеризуется сморщиванием и укорочением створок клапана, отложением в них кальция и поражением подклапанных структур. Наиболее частыми причинами такой МН являются:
•острая ревматическая лихорадка;
•инфекционный эндокардит;
•дегенеративные изменения митрального клапана (фиброз и кальциноз);
•системные заболевания соединительной ткани;
•пролапс МК;
•дисфункция папиллярных мышц, вызванная ИБС, инфарктом миокарда, постинфарктным кардиосклерозом, миокардитом;
•разрыв хорд или папиллярных мышц.
Функциональная МН обусловлена нарушением функции клапана при неизмененных клапанных структурах. Причинами функциональной МН являются заболевания, сопровождающиеся гемодинамической перегрузкой ЛЖ и расширением клапанного кольца:
•артериальная гипертензия;
•«митрализация» при аортальных пороках;
•постинфарктный кардиосклероз.
Патогенез гемодинамических изменений.
Основными гемодинамическими изменениями при МН являются:
•митральная регургитация;
Неполное смыкание створок МК во время систолы ЛЖ приводит к появлению обратного тока крови из ЛЖ в ЛП — регургитации.
•гипертрофия и дилатация ЛП и ЛЖ;
Возвратившаяся в ЛП кровь смешивается с поступившей из легочных вен. ЛП и легочные вены переполняются кровью и давление в них к концу систолы повышается. В диастолу в ЛЖ поступает избыточный объем крови. ЛЖ и ЛП испытывают перегрузку объемом, что ведет к развитию их эксцентрической гипертрофии, то есть сочетанию гипертрофии миокарда и дилатации полости.
•снижение эффективного сердечного выброса;
В тяжелых случаях объем крови, выбрасываемой в аорту, может достигать всего 50% от общей величины ударного объема ЛЖ. Остальное количество крови циркулирует между ЛП и ЛЖ, что ведет к снижению эффективного сердечного выброса.
•легочная гипертензия;
При большой величине митральной регургитации повышается давление в ЛП и венах малого круга кровообращения. Развивается пассивная ЛГ, которая при митральной недостаточности менее выражена, чем при митральном стенозе.
•левожелудочковая сердечная недостаточность.
При длительном течении заболевания и выраженной гипертрофии и дилатации левых камер сердца постепенно снижается сократительная способность ЛЖ и формируется левожелудочковая недостаточность
Клиническая картина
Первые жалобы больных — это слабость, сердцебиение, быстрая утомляемость. Затем появляются жалобы, обусловленные ЛГ: одышка, ортопноэ, кашель, сердечная астма, реже кровохарканье. При длительном течении заболевания появляются жалобы, связанные с вовлечением ПЖ: отеки на ногах, тяжесть в правом подреберье вследствие гепатомегалии, асцит.
Инструментальная диагностика
При электрокардиографическом исследовании выявляются гипертрофия ЛП и ЛЖ.
Признаки гипертрофии ЛЖ:
•увеличение амплитуды зубца R в левых грудных отведениях (V5, V6) и глубины зубца S в правых грудных (V1, V2) или RV5,6 + SV1,2 ≥ 38 мм (признак Соколова–Лайона);
•признаки поворота сердца вокруг продольной оси против часовой стрелки — смещение переходной зоны вправо в V2; углубление зубца Q V5,6; исчезновение или резкое уменьшение глубины зубца S в левых грудных отведениях V5,6;
•смещение электрической оси сердца влево;
•смещение сегмента ST в отведениях V5,6, I, аVL ниже изоэлектрической линии и формирование отрицательного или двухфазного (–/+) зубца Т в отведениях I, аVL, V5,6.
Рентгенография легких: увеличение левых камер, сглаживание талии за счет ЛП и выбухания ствола ЛА, увеличение правых отделов; при контрастировании пищевода в косых проекциях видно его отклонение по дуге большого радиуса, признаки ЛГ, линии Керли (яркие горизонтальные линии в средних и нижних отделах легких вызваны отеком междолевых щелей и переполнением лимфатических сосудов).
Эхокардиография. Достоверными признаками митральной недостаточности является определение при допплерэхокардиографическом исследовании потока крови из ЛЖ в ЛП во время систолыжелудочка (ток регургитации)
Также при ЭхоКГ выявляют увеличение размеров ЛП, гипертрофию и дилатацию ЛЖ, устанавливают причину регургитации (кальциноз, вегетация и др.).
Классификация митральной регургитации по степени тяжести
Различают четыре степени МН.
•легкая МН (I степень) — объем регургитации (ОР) <20% от ударного объема
(УО);
•умеренная МН (II степень) — ОР= 20–40% от УО;
•средней тяжести МН (III степень) — ОР = 40–60% от УО;
•тяжелая МН (IV степень) — ОР >60% от УО.
Оценить тяжесть МН позволяет также цветное допплерографическое исследование. Струя крови во время систолы, возвращающаяся в ЛП, при цветном сканировании окрашена в синий цвет. Определив площадь струи регургитации, можно оценить тяжесть МН:
I степень — менее 4 см2; II степень — 4–8 см2;
III степень — более 8 см2;
IV степень — ток регургитации определяется в устье легочных вен.
Показания к хирургическому лечению.
•тяжелая митральная недостаточность (III–IV степени) с объемом регургитации больше 40–60%, даже при наличии умеренно выраженных клинических проявлений заболевания;
•умеренная и тяжелая митральная недостаточность II–IV степени при наличии признаков систолической дисфункции ЛЖ (одышка в покое, снижение работоспособности, ФВ меньше 60%, индекс КДО больше 100–120 мл/м2).
Виды оперативного вмешательства:
•протезирование МК;
•пластика митрального кольца.
Возможности терапевтической коррекции.
Фармакологическое лечение направлено на компенсацию сердечной недостаточности. С этой целью используются ингибиторы АПФ (эналаприл, периндоприл, лизиноприл), антагонисты рецепторов к ангиотензину II (лозартан, валсартан, эпросартан), диуретики (фуросемид, торасемид), антагонисты альдостерона (спиронолактон), изосорбида 5-мононитраты. При возникновении фибрилляции предсердий терапия направлена на достижение нормосистолии. С этой целью используются β-адреноблокаторы (метопролол, бисопролол, небиволол), сердечныегликозиды (дигоксин).
8. Аортальный стеноз. Определение. Этиология. Патогенез гемодинамических изменений. Классификация по степени тяжести. Клиническая картина, данные объективного осмотра. Инструментальная диагностика. Показания и методы хирургического лечения. Возможности терапевтической коррекции.
Аортальный стеноз - сужение выносящего тракта левого желудочка (ЛЖ) в области аортального клапана, приводящее к затруднению оттока крови из ЛЖ в аорту.
Этиология
1. Склеродегенеративный (кальцинированный) АС в настоящее время является самой распространенной причиной АС у взрослых. Генез изменений аортального клапана при данной патологии до конца не ясен. Из предложенных теорий наибольшего внимания заслуживают две. Одни исследователи считают, что длительное механическое микроповреждение клапана
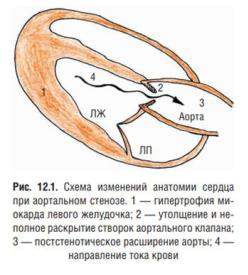
ведет к появлению надрывов эндотелия клапанов и вторичной его кальцификации. Другие авторы придают большое значение существующему хроническому воспалению на аортальном клапане, исходом которого будет склероз клапана и его кальцификация.
2.Врожденный АС характеризуется как сужением самого клапанного аортального кольца, так и сращением между собой створок аортального клапана, который может быть трехстворчатым, двух- и даже одностворчатым.
3.Ревматический АС развивается вследствие воспалительного «склеивания» и сращения комиссур с последующей васкуляризацией створок клапанного кольца, что приводит к втяжению и уплотнению свободных краев створки. В дальнейшем происходит кальцификация створок, и клапанное отверстие, уменьшаясь, приобретает округлую или треугольную форму. Ревматическому поражению клапана свойственно сочетанное нарушение функции (формирование стеноза и недостаточности).
Патогенез гемодинамических нарушений При АС (для преодоления механического препятствия кровотоку) в полости ЛЖ создается
высокое давление, в то время как в аорте его значение остается нормальным. Эту разницу в давлении между ЛЖ и аортой называют «трансаортальным градиентом давления». На протяжении длительного времени ЛЖ адаптируется к повышенной постнагрузке за счет развития концентрической гипертрофии миокарда (увеличение толщины миокарда без дилатации полости). Со временем это приводит к формированию диастолической дисфукции (ДД) за счет увеличения жесткости ЛЖ, нарушения расслабления и повышения КДД (т.е. желудочек не растягивается, поэтому крови туда поступает меньше). Важную роль в наполнении ЛЖ играют усиленные сокращения ЛП, а потеря предсердного компонента (например, при ФП) зачастую приводит к серьезному ухудшению течения заболевания. Из-за того, что не вся кровь переходит в ЛЖ повышается давления в ЛП и легочных венах, что манифестирует признаками застоя в малом круге кровообращения. Важную роль в развитии гемодинамических нарушений при этом пороке играет неспособность ЛЖ увеличивать ударный объем во время физических нагрузок («фиксированный ударный объем»).
Нарушение коронарной перфузии, характерное для АС, обусловлено следующими основными механизмами: уменьшением объема крови, поступающей в коронарные артерии (фиксированный ударный объем), затруднением их наполнения вследствие диастолической дисфункции и повышения потребности гипертрофированного миокарда в кислороде.
Появление систолической дисфункции ЛЖ характерно для конечной стадии АС. При снижении УО увеличивается КСО ЛЖ, что ведет к развитию миогенной дилатации с растяжением кольца митрального клапана и появлением митральной регургитации. Происходит так называемая «митрализации аортального порока». Систолическая дисфункция в сочетании с митральной недостаточностью усугубляет застой в малом круге кровообращения и проявляется тяжелой систолодиастолической левожелудочковой СН.
Классификация по степени тяжести
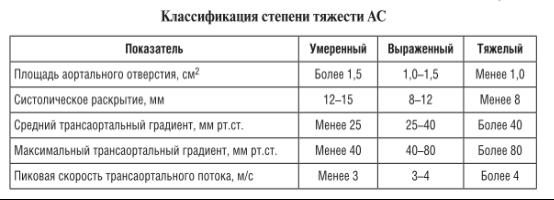
Клиническая картина
1.Быстрая утомляемость, слабость при физической нагрузке, которая обусловлена недостаточной перфузией скелетных мышц, а также явлениями вазоконстрикции.
2.Головокружения, потери сознания (синкопе), как правило, возникают при физической
нагрузке, резком изменении положения тела и обусловлены снижением перфузии головного мозга вследствие фиксированного ударного объема. Появление обмороков также объясняют разбалансировкой барорецепторного механизма при выраженном АС и особенностями вазодепрессорной реакции на критическое увеличение систолического давления в ЛЖ при физической нагрузке. Наиболее распространенным механизмом патогенеза нагрузочных обмороков является активация барорецепторов ЛЖ с сопутствующей артериальной гипотензией и последующей брадикардией. Этот феномен называют рефлексом Бецольда– Яриша. Т.е. смотрите, при физ.работе, нагрузка на сердце увеличивается, давление в ЛЖ растет, активируются барорецепторы, которые активируют вагус, а он снижает ЧСС и АД (т.к. расширяются артериолы БКК), и происходит обморок. Для обмороков, возникающих вне физической нагрузки, наиболее вероятной причиной являются желудочковые аритмии или транзиторные нарушения проводимости.
3.Стенокардия напряжения наблюдается приблизительно у 2/3 пациентов с критическим АС. Клинически сходна со стенокардией напряжения при ишемической болезни сердца: характеризуется давящими, сжимающими болями за грудиной, возникающими при физических нагрузках, купирующимиcя в покое и/или приемом нитратов, иррадиирующими в левую руку. Патогенетически развитие стенокардии обусловлено:
· выраженной гипертрофией миокарда ЛЖ, что увеличивает потребность миокарда в кислороде; · преобладанием мышечной массы над количеством капилляров (так называемая
относительная коронарная недостаточность); · сдавлением субэндокардиальных сосудов гипертрофированным миокардом ЛЖ, что ухудшает перфузию миокарда.
4.Нарушения ритма. При АС нередко возникают нарушения ритма и проводимости,
которые также могут приводить к синкопальным состояниям. Это эпизоды желудочковых нарушений ритма (желудочковые тахикардии, фибрилляции желудочков); пароксизмы фибрилляции предсердий (при этом уменьшается предсердный компонент диастолического заполнения ЛЖ, что приводит к резкому снижению сердечного выброса), а также транзиторных AВ-блокад II и III степени. Считается, что тяжесть аритмии тесно коррелирует с систолической дисфункцией миокарда и не зависит от этиологии клапанного стеноза и величины градиента.
5. Сердечная недостаточность. На начальных этапах заболевания характерно появление одышки при физической нагрузке, что свидетельствует о диастолической дисфункции ЛЖ. В дальнейшем возникают приступы сердечной астмы или альвеолярного отека, что говорит о присоединении к диастолической дисфункции ЛЖ систолической и вовлечении в патологический процесс митрального клапана.
Данные объективного осмотра При общем осмотре выявляется бледность кожных покровов, которая обусловлена
фиксированным ударным объемом и возникающей на этом фоне склонностью периферических сосудов к вазоконстрикции.
Пальпация области сердца характеризуется:
·усиленным, смещенным влево верхушечным толчком, что указывает на гипертрофию ЛЖ
·на основании сердца может определяться систолическое дрожание, усиливающееся при наклоне пациента вперед при полном выдохе
·при развитии левожелудочковой недостаточности верхушечный толчок становится протяженным и смещается вниз и латерально
Артериальный пульс. При тяжелом аортальном стенозе отмечается медленный подъем,
поздний пик и низкая амплитуда пульсовой волны: медленный и малый пульс. Систолическое АД снижено за счет фиксированного ударного объема. Следует отметить, что у пациентов с легким АС с сопутствующей аортальной регургитацией, а также пожилых пациентов с неэластичными артериями систолическое и пульсовое давление может быть нормальным или даже повышенным.
Перкуссия. При развитии дилатации ЛЖ левая граница относительной сердечной тупости смещается кнаружи от среднеключичной линии в пятое межреберье. Также может определяться расширение границы сосудистого пучка во второе межреберье (за счет формирования постстенотического расширения аорты).
Аускультация. При сохранной фракции выброса ЛЖ и неизмененном конечнодиастолическом давлении (КДД) I тон остается нормальным. Выраженное обызвествление и
уменьшение подвижности створок аортального клапана могут вызвать ослабление аортального компонента II тона. Но следует отметить, что также возможно усиление аортального компонента II тона или щелчок — если подвижность створок сохранена.
Вслед за I тоном выслушивается интенсивный веретенообразный мезосистолический шум, который прекращается перед II тоном и лучше всего слышен у левого края грудины. Шум проводится на сонные артерии. По мере прогрессирования АС шум становится все более интенсивным, а пик его — все более поздним. При выраженном обызвествлении аортального клапана высокочастотные компоненты шума могут проводиться в подмышечную область,
имитируя шум митральной регургитации (симптом Галлавердена). Может выслушиваться
IV патологический тон, возникающий за счет увеличения силы сокращения левого предсердия. И тогда выслушивается мелодия трехчленного ритма, состоящая из IV, I и II
тонов (пресистолический галоп).
Инструментальная диагностика ЭКГ. Основным ЭКГ-признаком является гипертрофия ЛЖ. Наиболее типичные признаки гипертрофии ЛЖ:
·отклонение ЭОС влево,
·R V5–V6 больше R V4,
·увеличение времени внутреннего отклонения в V5–V6 более 0,05 с,
·углубление S V1–V2.
·инверсия зубца Т
·депрессия сегмента ST в отведениях с положительными комплексами QRS. Депрессия сегмента ST более чем на 0,2 мм у пациентов с АС (систолическая «перегрузка» ЛЖ) свидетельствует о наличии выраженной гипертрофии ЛЖ.
Распространение кальцинатов с аортального клапана на проводящую систему может вызывать появление различных вариантов атриовентрикулярных и внутрижелудочковых блокад.
Рентгенограмма органов грудной клетки. Рутинное рентгенологическое исследование органов грудной клетки у пациентов с критическим АС может не выявить отклонений, но со временем становится подчеркнута «талия» сердца за счет гипертрофии ЛЖ. Довольно распространенной находкой является постстенотическое расширение восходящей части аорты. При застое крови в малом круге кровообращения выявляется артериальная и венозная легочная гипертензия.
Эхокардиография. Двухмерная трансторакальная ЭхоКГ позволяет обнаружить АС, определить степень его тяжести и этиологию.
Критерии АС по ЭхоКГ:
• уменьшение степени расхождения створок аортального клапана во время систолы (менее 16 мм);
• систолический прогиб створок клапана в сторону аорты;
• уплотнение и неоднородность структуры, кальциноз створок аортального клапана и корня аорты;
•выраженная гипертрофия ЛЖ (увеличение толщины межжелудочковой перегородки и задней стенки ЛЖ более 11 мм, превышение индекса массы миокарда ЛЖ более 125 г/м2 у мужчин и 110 г/м2 у женщин);
•постстенотическое расширение аорты (вследствие увеличения скорости систолического потока крови через суженное аортальное отверстие, высокого давления струи крови на стенку аорты);
•увеличение градиента давления между ЛЖ и аортой, отражает степень сужения аортального клапана.
Ангиография, катетеризация сердца. Проводится перед протезированием аортального
клапана с целью определения гемодинамических параметров: градиента давления между аортой и ЛЖ, давления заклинивания легочной артерии, сердечного выброса, давления в легочной артерии, площади отверстия аортального клапана.
Показания и методы хирургического лечения Показания для протезирования аортального клапана:
•ПАК рекомендуется симптомным пациентам с тяжелым АС
•ПАК рекомендуется пациентам с тяжелым АС, подлежащим аортокоронарному шунтированию (АКШ), операции на восходящей аорте или на других клапанах сердца.
•ПАК рекомендуется асимптомным пациентам с тяжелым АС и патологическим нагрузочным тестом.
•ПАК рекомендуется пациентам с тяжелым АС и систолической дисфункцией ЛЖ (фракция выброса меньше 50%)
•ПАК рекомендуется пациентам с умеренным АС, подлежащим АКШ или операции на аорте либо на других клапанах сердца.
•ПАК рекомендуется бессимптомным пациентам с тяжелым АС и патологическим нагрузочным тестом проявляющимся снижением АД.
•ПАК рекомендуется симптомным пациентам с низкой скоростью кровотока, низким градиентом и сохраненной ФВ ЛЖ только после получения данных о выраженности аортального стеноза.
•ПАК рекомендуется симптомным пациентам с тяжелым АС, низкой скоростью кровотока, низким градиентом, сниженной ФВ ЛЖ и признаками сохраненного сократительного резерва миокарда.
•ПАК рекомендуется взрослым пациентам с бессимптомным тяжелым АС, если операционный риск низкий и имеется один или более из нижеуказанных признаков: значительное повышение мозгового натрий-уретического пептида ( более 100пг.мл); увеличение среднего градиента при проведении нагрузочного теста на 20мм рт.ст и более; выраженная гипертрофия ЛЖ ( межжелудочковая перегородка 15мм и/или задняя стенка ≥ 15 мм) при отсутствии артериальной гипертензии
•ПАК рекомендуется бессимптомным пациентов с критически тяжелым АС (площадь аортального клапана менее 0,6 см2, средний градиент более 60 мм рт. ст. и максимальная скорость кровотока больше 5,5 м/с), когда ожидаемая (рассчитанная на основе прогностических моделей) послеоперационная летальность не более 1,0%.
Катетерная баллонная аортальная вальвулопластика.
Показания к катетерной баллонной аортальной вальвулопластике (КБАВ):
•Катетерная баллонная аортальная вальвулопластика рекомендуется как этапная операция у гемодинамически нестабильных взрослых пациентов с АС и высоким риском для ПАК
•Катетерная баллонная аортальная вальвулопластика рекомендуется как паллиативная операция у взрослых пациентов сАС, у которых ПАК не может быть выполнено из-за выраженной сопутствующей патологии, а проведение эндоваскулярного протезирования аортального клапана невозможно.
У детей при врожденном аортальном стенозе без обызвествления клапана безопасность и эффективность аортальной баллонной вальвулопластики сопоставима с протезированием. В то время как эффективность этого метода у взрослых значительно ниже, поскольку при приобретенном АС створки клапана уплотнены, ригидны и, как правило, имеют обызвествления. Выполнение вальвулопластики на время уменьшает тяжесть стеноза, но следует помнить о возможном повреждении створок (створки переламываются, гнутся по линиям излома), что в свою очередь может привести к их несмыканию и формированию
аортальной недостаточности. В течение полугода примерно в половине случаев развивается рестеноз. Баллонная вальвулопластика не повышает выживаемость взрослых больных с АС и до недавнего времени использовалась лишь как паллиативное вмешательство в ожидании протезирования клапана.
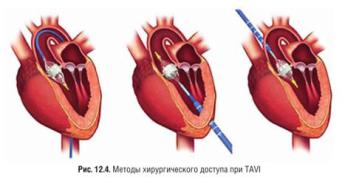
Транскатетерное эндоваскулярное (внутрисосудистое) протезирование аортального клапана (TAVI) — это процедура замены аортального клапана при его критическом стенозе (сужении) доступом через бедренную артерию под местной анестезией.
Показания для транскатетерной имплантации аортального клапана (ТИАК/TAVI):
•Транскатетерную имлантацию аортального клапана рекомендуется проводить мультидисциплинарной команде, включающую кардиолога, кардиохирурга и при необходимости других специалистов.
•Транскатетерную имплантацию аортального клапана рекомендуется выполнять только в кардиохирургических центрах.
•Транскатетерная имплантация аортального клапана рекомендуется пациентам с тяжелым АС и прогнозируемой продолжительностью жизни более 1 года (с учетом сопутствующих заболеваний), которым по оценке мультидисциплинарной команды, противопоказано протезирование аортального клапана и у которых можно ожидать улучшения качества жизни.
•Транскатетерная имплантация аортального клапана рекомендуется пациентам высокого риска с тяжелым симптомным АС, у которых нет абсолютных противопоказаний к ПАК, но у которых ТИАК признана методом выбора с учетом индивидульного профиля риска.
•ТИАК не рекомендуется при несоответствие размеров фиброзного кольца АК типу применяемого протеза, при наличии тромба в ЛЖ, активном инфекционном эндокардите, повышенном риске обструкции коронарных артерий ( короткая дистанция между фиброзным кольцом и устьями коронарных артерий, ассиметричный кальциноз),выраженном атероматозе восходящей аорты с подвижными тромбами, повышенным риском эмболии, патологической извитости или тяжелом стенозе бедренных, подвздошных артерий, брюшной аорты ( для трасфеморального доступа)
Доступ может быть трансфеморальным (катетер вводится через бедренную артерию), трансапикальным (через верхушку сердца) и трансаортальным (через стенку аорты). Система состоит из трехстворчатого биологического клапана (из бычьего перикарда), установленного в стент из нержавеющей стали, баллонного катетера и устройства для введения баллона в доставляющий катетер.
Возможности терапевтического лечения Консервативная терапия пациентов с АС направлена на:
•лечение симптомов заболевания;
•лечение сопутствующей патологии.
Медикаментозная терапия АС носит симтоматической характер. Используются следующие группы препаратов:
1.β-Адреноблокаторы (под контролем ЧСС и АД), при этом не следует добиваться брадикардии, как при лечении стенокардии напряжения.
2.Диуретики назначаются при лечении сердечной недостаточности. Важно помнить о возможном развитии гиповолемии, при которой снижается сердечный выброс и возможно развитие ортостатической гипотензии.
3.иАПФ/БРА, нитраты, являясь смешанными вазодилататорами, уменьшают как пред-, так и постнагрузку.
4. Сердечные гликозиды — учитывая их возможность увеличивать градиент давления на аортальном клапане за счет положительного инотропного действия, применяются с осторожностью. Назначают их только при декомпенсации порока и систолической дисфункции ЛЖ, для снижения ЧСС при постоянной форме фибрилляции предсердий.
Для лечения AВ-блокад по показаниям имплантируются электрокардиостимуляторы.
Для купирования пароксизмов трепетания или фибрилляции предсердий используется кардиоверсия, чаще электрическая. При постоянной форме фибрилляции предсердий осуществляют контроль за ЧСС (с помощью β-адреноблокаторов, антагонистов кальция (верапамила) и/или сердечных гликозидов). Должное внимание следует уделять профилактике инфекционного эндокардита (а/б терапия).
9. Аортальная недостаточность: Определение. Этиология. Патогенез гемодинамических изменений. Клиническая картина, данные объективного осмотра. Инструментальная диагностика. Показания и методы хирургического лечения. Возможности терапевтической коррекции.
Определение.
- Это порок сердца, при котором происходит неполное смыкание створок аортального клапана во время диастолы желудочков, что приводит к возникновению обратного тока крови из аорты
влевый желудочек — аортальной регургитации Этиология
● ОРЛ - створки клапана утолщаются, деформируются и сморщиваютс ● Инфекционный эндокардит - чаще поражает уже измененные створки клапана
врезультате предшествующих заболеваний.
● Относительная АН возникает вследствие расширения аорты и фиброзного кольца аортального клапана при артериальной гипертензии, аневризме аорты любого генеза.
Гемодинамика.
При недостаточности клапана аорты ЛЖ наполняется кровью из левого предсердия, а также за счет аортальной регургитации => постепенное нарастание давления в полости ЛЖ => длительная перегрузка проявляется дилатацией и гипертрофией ЛЖ (эксцентрический тип гипертрофии), что позволяет компенсировать порок.
С течением времени ударный объем остается прежним, или даже может снижаться => увеличение давления в ЛЖ, в ЛП и венах малого круга кровообращения => развитие относительной митральной недостаточности вследствие расширения ЛЖ и растяжения фиброзного кольца => дисфункция и дилатация правого желудочка, регургитация на трехстворчатом клапане => прогрессирование СН с последующей декомпенсацией по большому кругу кровообращения.
+ Ухудшение коронарной перфузии из-за относительной коронарной недостаточностью (вследствие гипертрофии миокарда) и низким диастолическим давлением в аорте (вследствие быстрого возврата крови в ЛЖ), что снижает наполнение коронарного русла в диастолу.
Основные клинические проявления АН:
1)ощущения усиленной пульсации в шее, голове;
2)сердцебиение;
3)головокружения, ощущения преходящей дурноты, обмороки;
4)стенокардия;
5)одышка.
Основные данные физикального обследования:
1)признаки пульсации периферических артерий: «пляска каротид», симптом Мюссе, симптом Квинке, симптом Ландольфи, симптом Мюллера;
2)пульс скорый; высокий, большой и быстрый;
3)повышение систолического и снижение диастолического АД, повышение давления;
