
- •3. Острый коронарный синдром: патогенез, диагностика, врачебная тактика в зависимости от формы острого коронарного синдрома
- •Классификация митрального стеноза по степени тяжести.
- •10. Инфекционный эндокардит. Определение. Предрасполагающие факторы. Этиология. Патогенез. Клиническая картина. Критерии диагностики. Принципы лечения.
- •14. Суправентрикулярная экстрасистолия: Определение. Механизмы возникновения, диагностика, лечение.
- •15. Желудочковая экстрасистолия: Определение, механизмы возникновения, диагностика, классификация, лечение.
- •17. Гипертрофическая кардиомиопатия. Определение. Нарушение внутрисердечной гемодинамики. Клиническая картина. Диагностика. Лечение.
- •19. Неотложные состояния в кардиологии: отек легких, сердечная астма. Этиология, патогенез, клиническая картина, лечение
- •23. Пневмония. Определение. Этиология. Классификация. Патогенез пневмонии. Клиническая картина. Лабораторная и инструментальная диагностика пневмонии. Лечение. Принципы антибактериальной терапии.
- •24. Легочная гипертензия. Тромбоэмболия легочной артерии. Патогенез гемодинамических расстройств. Клинические проявления. Диагностика. Лечение.
- •25. Хронический гастрит. Определение. Актуальность темы. Классификация. Основные патогенетические механизмы при хроническом гастрите (тип А, В, С). Клиническая картина. Методы обследования больного. Лечение хронического гастрита.
- •27. Хронический гепатит. Определение. Актуальность проблемы. Классификация. Этиология. Патогенез хронических гепатитов. Основные клинические синдромы. Лабораторная и инструментальная диагностика. Основные лабораторные синдромы. Принципы терапии.
- •31. Хронический гломерулонефрит. Определение. Этиология, патогенез. Классификация. Основные клинические проявления. Методы обследования. Принципы терапии, прогноз.
- •33. Интерстициальный нефрит. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •34. Острое повреждение почек. Определение. Понятие преренальной, ренальной, постренальной острой почечной недостаточности. Клиническая картина. Диагностика. Лечение.
- •36. Железодефицитная анемия. Понятие. Распространенность. Роль железа в организме. Этиология и патогенез. Клиническая картина. Диагностика железодефицитной анемии. Лечение. Прогноз и профилактика.
- •37. В12 (фолиево)–дефицитная анемия. Понятие. Распространенность. Роль витамина В12 и фолиевой кислоты в организме. Этиология и патогенез. Основные клинические синдромы. Диагностика В12-дефицитной анемии. Лечение. Прогноз и профилактика.
- •38. Гемолитические анемии. Определение. Классификация. Понятие внутрисосудистого и внутриклеточного гемолиза. Клиническая картина, диагностика Приобретенные гемолитические анемии. Патогенез. Клиническая картина. Диагностика. Лечение.
- •39. Острый лейкоз. Определение. Этиология. Механизмы нарушения кроветворения. Классификация. Основные клинические синдромы. Методы диагностики. Критерии диагностики острых лейкозов. Принципы терапии. Критерии ремиссии. Прогноз.
- •Этиология.
- •Механизмы нарушения кроветворения.
- •Классификация.
- •Основные клинические синдромы.
- •Критерии диагностики острых лейкозов.
- •Принципы терапии.
- •Критерии ремиссии.
- •Прогноз.
- •42. Геморрагические диатезы. Механизмы первичного и вторичного гемостаза. Классификация. Типы кровоточивости и их клинико-лабораторные критерии.
- •43. Понятие о коагулопатии. Гемофилия. Этиология. Патогенез. Клиническая картина. Прогноз. Лечение.
- •45. Тромбофилии. Классификация (первичные и вторичные тромбофилии). Понятие о первичных тромбофилиях.
- •46. Антифосфолипидный синдром. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •47. Подагра. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •48. Остеоартрит. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
- •1) остеоартроз, ассоциированный с эндокринными и метаболическими заболеваниями:

–клиническая ремиссия
–клинико-гематологическая ремиссия
По характеру и выраженности геморрагического синдрома (классификация ВОЗ):
•0-й степени — отсутствие геморрагического синдрома;
•1-й степени — петехии и экхимозы (единичные);
•2-й степени — незначительная потеря крови (мелена, гематурия, кровохарканье);
•3-й степени — выраженная потеря крови (кровотечение, требующее переливания крови или кровезаменителей);
•4-й степени — тяжелая кровопотеря (кровоизлияния в головной мозг и сетчатку глаза, кровотечения, заканчивающиеся летальным исходом)
Клиническая картина:
•Появление геморрагической сыпи – пятнисто-петехиального характера
•Клиническая картина проявляется при ТЦ менее 50*109/л, а при ТЦ менее 20*109/л – спонтанные кровотечения из слизистых.
•Изолированная ТЦпения (м.б. анемия, ведь теряем ЭЦ и Hb), нет нейтропении
•Кровотечения при бритье, при чистке зубов и т.д.
Диагностика:
ИТП – диагноз исключения. Мы должны исключить ВИЧ, хр. гепатит С, лейкоз, онкологию, прием ЛС, СКВ, апластическую анемию. Тестирование на гепатит и ВИЧ
•КАК: ТЦ менее 100*109/л.
•Коагулограмма: АЧТВ, время свертывания крови – норма; ↑ время кровоточивости
•Цитологическое исследование ККМ (при ИТП кол-во мегакариоцитов в ККМ норма или ↑)
•Определение специфических АТ (IgG) к гликопротеинам ТЦ
•УЗИ для исключения спленомегалии
Лечение:
•При ТЦ = 50*109/л – наблюдение
•При ТЦ менее 50*109/л с кровоточивостью // с повышенным риском кровотечения – лечение Терапия 1ой линии: ГКС (преднизолон, дексаметазон), иммуноглобулины в/в =
иммуномоделирующее действие Терапия 2о1 линии: спленэктомия, агонисты рецепторов к тромбопоэтину (элтромбопаг, револейд)
Терапия 3ей линии: моноклональные АТ к CD20 (ритуксимаб), цитостатики (винкристин, циклоспорин)
•при ТЦ менее 20*109/л и развитии геморрагич. синдрома – переливание ТЦмассы
•при кровотечениях – местный и общий гемостаз
45. Тромбофилии. Классификация (первичные и вторичные тромбофилии). Понятие о первичных тромбофилиях.
Тромбофилия – состояние, хар-ся повышенной склонностью к тромбообразованию, в основе которого лежат генетически обусловленные или приобретенные нарушения гемостаза и гемореологии Тромбофилии — патологические сдвиги в системе гемостаза, приводящие к развитию
тромбозов, ишемий, инфарктов органов
Классификация
1.Наследственные (первичные)
a.Мутация гена фактора V
b.Мут. Гена протромбина
c. Дефицит Антитромбина III
d.Дефицит протеина С
e.Дефицит протеина S
2.Приобретенные
a. Антифосфолипидный синдром (наличие антифосфолипидных АТ, проявл. Рецедивирующими тромбозами)
Самое главное:
1. Протеины C, S удерживают факторы свертывания в неактивном состоянии (они их

протеолизируют). Если их мало – факторы будут активироваться и приводить к тромбоорразованию
3.Антитромбин III – ингибирует тромбин
Он может снижаться и при заболеваниях печени, ДВС, лечении апагинозой, нефротическом синдроме
4.Диагностика заключается в определении снижения функции протеинов С,S, антитромбина III
Вкоагулограмме снижение АЧТВ и времени свертывания
5.Лечение главным образом антикоагулянты: гепарин, варфарин, сулодексид, АСК Моменты из учебника гематологии:
Резистентность фактора Va к протеину С
Клиника: рецедивирующие тромбоэмболии и флеботромбозы Диагностика: генетическое исследование с пом. ПЦР, отсутсвие увеличения АЧТВ при
добавлении протеина С (потому что к нему не чувствителен и в неактивную форму не переводит – то есть пятый фактор все так и остается активный и приводит к тромбам) Лечение: свежезамороженная плазма + гепарин – в острый период
сулодексид + АСК/клопидогрел – в подострый Дефицит естественных антикоагулянтов (протеинов и АТIII) Антитромбин III
Клиника: венозные и артериальные тромбозы Диагностика: его снижение
Лечение: концентрат АТIII, варфарин/АСК/клопидогрел
С протеинами то же самое, главное помнить, что они удерживают активацию факторов свертывания
46. Антифосфолипидный синдром. Определение. Этиология. Патогенез. Клиническая картина. Диагностика. Лечение.
Антифосфолипидный синдром - это приобретенная аутоиммунная тромбофилия, ассоциированная с наличием антифосфолипидных антител и проявляющаяся рецидивирующими тромбозами (венозными и артериальными) и патологией беременности.
Выделяют первичный и вторичный АФС. Первичный АФС является самостоятельным заболеванием. Вторичный АФС возникает на фоне других аутоиммунных заболеваний (чаще всего системной красной волчанки).
Этиопатогенез АФС
В настоящее время считается, что АФС развивается вследствие появления специфических аутоантител. Антитела направлены против фосфолипид-связывающих белков плазмы крови и мембран клеток, т.е против фосфолипид-белковых комплексов. Однако в литературе они обозначаются как антифосфолипидные антитела (АФА). АФА участвуют в реализации различных механизмов, в результате чего нарушаются нормальные взаимодействия между про- и антикоагулянтами, фибринолизом, тромбоцитами и эндотелием. Нарушается сбалансированная работа системы гемостаза с увеличением прокоагулянтного потенциала. Пусковым фактором для формирования АФА может быть инфекция, воспалительные, в том числе аутоиммунные, заболевания, хирургические вмешательства, длительная иммобилизация, прием эстрогенсодержащих препаратов. АФА являются гетерогенной группой и относятся к Ig классов G, M, реже А.
Мишенями АФА являются:
●β2-гликопротеин I (β2-GPI)
●протромбин
●тромбомодулин
●кининогены
●антитромбин III,
●протеины С и S
●аннексины
Считается, что основные эффекторы - антитела к β2Gp1. Антикоагулянтные свойства β2-GPI определяются его способностью связываться с отрицательно-заряженными фосфолипидами

клеточных мембран (например, фосфатидилсерином), тем самым исключая их участие в коагуляции. При повреждении клетки, ее активации или апоптозе фосфатидилсерин транслоцируется на внешнюю поверхность клеточной мембраны, соединяется с β2-GPI. Образованный комплекс является истинным антигеном и мишенью для АФА.
В результате связывания антител с протромбином, происходит иммобилизации протромбина на поверхности клеточной мембраны, что является прямой предпосылкой к развитию тромбозов.
Аннексин V- анионный фосфолипид-связывающий белок, встречающийся во многих тканях, главным образом на эндотелиальных клетках и в плаценте. Он связывает и нейтрализует представленные на поверхности клетки фосфолипиды, тем самым предотвращает участие клеточной мембраны в активации коагуляции, например, в период развития и инвазии трофобласта. Если аутоантитела вытесняют аннексин A5, поверхности эндотелиоцитов стимулируются и клетки начинают вырабатывать прокоагулянты, провоцируя возникновение тромбозов.
АФА не только серологические маркеры, но и основные патогенетические агенты, вызывающие развитие основных клинических проявлений АФС: тромбоза, акушерской патологии, цитопений и др. Обсуждаются следующие патогенетические механизмы
тромбоза:
1.АФА взаимодействуют с эндотелиальными структурами, приводя к увеличению синтеза вазоконстрикторов и активаторов агрегации Тр (простагландина Е2, тромбоксана) и снижению вазодилататоров (простациклина).
2.повреждение мембран эндотелиальных клеток приводит к появлению фосфолипидов на поверхности мембран, их контакту с β2-GPI и воздействию АФА на этот комплекс, что индуцирует дальнейшее повреждение
3.АФА могут напрямую активировать эндотелиальные клетки, индуцируя экспрессию адгезивных молекул и тканевого фактора, вызывать активацию и агрегацию тромбоцитов
4.АФА способны активировать тромбоциты, которые увеличивают экспрессию гликопротеина IIb/IIIa, синтез тромбоксана А2 и других субстанций с протромботическим эффектом, таким образом инициируется агрегация тромбоцитов и вазоконстрикция. Развивается тромботическая тромбоцитопения.
5.АФА нарушают антикоагулянтные механизм, т.к. их мишенями являются β2Gp-1, протеины С и S.
6.АФА участвуют в активации комплемента. Избыточное образование С5а активирует нейтрофилы, что приводит к экспрессии тканевого фактора, взаимодействующего с фактором VIIa, активации фактора X, генерации тромбина и тромбообразованию. Активация комплемента может быть также значимым механизмом патологии беременности и задержки внутриутробного развития плода, индуцированной АФА. Комплексы антител с β2-GPI могут генерировать образование С5а, который, в свою очередь, индуцирует развитие воспаления и плацентарную недостаточность.
Патогенез акушерских осложнений. Беременность является состоянием, при котором риск
тромботических осложнений увеличивается в разы. При беременности возникают гормональные и механические изменения, приводящие к стазу в кровяном русле, повышение уровней факторов свертывания крови. При беременности повышаются уровень фибриногена, факторов свёртывания, фактора фон Виллебранда, происходит подавление фибринолиза и уменьшение активности антикоагулянтной системы: развитие резистентности к активированному протеин С, снижение уровня протеина S. Патогенез акушерских осложнений при АФС универсален и реализуется через нарушение микроциркуляции, гемостаза и патологию сосудистой стенки. Вследствие этих изменений при АФС во время беременности развивается васкулопатия плаценты, приводящая к плацентарной недостаточности. возникновение дефектов имплантации и нарушений на ранних стадиях развития эмбриона. Важным фактором является снижение уровня интерлейкина-3 (ИЛ-3), т.к. ИЛ-3 является активным фактором роста трофобласта, способствуя имплантации и развитию плаценты. патологическая активация системы комплемента, повышения уровня провоспалительных цитокинов ведет к развитию воспалительных процессов и тканевых повреждений у плода
Клинические проявления АФС. Основными характерными признаками АФС являются тромбозы сосудов и патология беременности. Первичный и вторичный АФС имеют одинаковые клинические проявления. Однако при вторичном АФС клиническая картина дополняется проявлениями основного заболевания. АФС является системным заболеванием, что проявляется поражением разных систем и органов.
Сосудистые тромбозы. Наиболее характерны для АФС венозные тромбозы. Самыми частыми проявлениями венозных тромбозов являются тромбозы глубоких вен нижних конечностей, нередко осложняющиеся тромбоэмболией легочной артерии. Другими проявлениями могут быть тромбозы печеночных вен (синдром Бадда-Киари), почечных, ретинальных и др. Артериальные тромбозы с поражением коронарных, церебральных, мезентериальных и др. артерий также являются характерными для АФС. При АФС возможны рецидивирующие тромбозы и тромбоэмболии и/или множественность локализации поражения.
Акушерские осложнения. Патология беременности – вторая важная особенность АФС. Наиболее распространенным ее проявлением являются рецидивирующие выкидыши, задержка внутриутробного развития плода, преждевременные роды до 34-й недели беременности вследствие плацентарной недостаточности, необъяснимая смерть плода после 10-й недели беременности. Кроме того, осложнить беременность у женщин с АФС может возникновение тромбоза, эклампсии или преэклампсии.
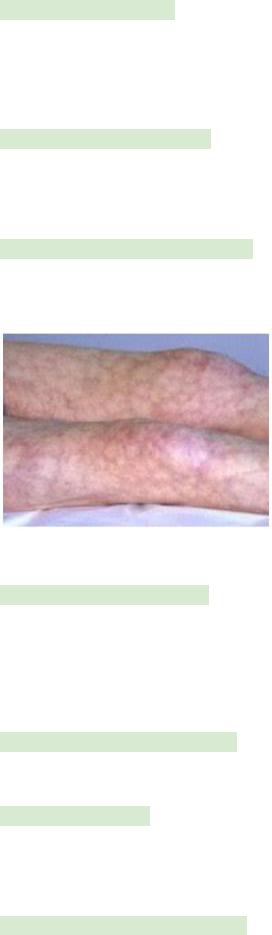
Дерматологические проявления. Livedo reticularis (сетчатое ливедо) встречается у 25% пациентов с АФС и является наиболее характерным кожным проявлением. При осмотре определяется изменения окраски в виде «мраморной кожи», стойкий или преходящий пятнистый красновато-голубой или пурпурный сетчатый цианотический рисунок, которые развивается вследствие вазомоторных нарушений.
К другим кожным проявлениям относятся хр. язвы кожи, ладонная и подошвенная эритема, гангрена пальцев верхних и нижних конечностей, поверхностные некрозы кожи и некоторые другие.
Патология сердца и легких. Кроме вышеописанных патологий сердца и легких, обусловленных тромбозом коронарных артерий (инфаркт миокарда), легочной артерии (ТЭЛа) могут развиваться и другие поражения. Примерно у трети больных встречается патология клапанов по типу эндокардита. Происходит утолщение створок клапанов, возможно формирование неинфекционных вегетаций. Чаще вовлекается митральный клапан, реже аортальный. Поражение клапанов обычно протекает малосимптомно, но возможно развитие их дисфункции (чаще по типу недостаточности). К легочным проявлениям относятся внутриальвеолярные кровоизлияния, острый респираторный дистресс-синдромом, фиброзирующий альвеолит.
Неврологические проявления. В дополнение к нарушениям мозгового кровообращения, обусловленных тромбозом церебральных артерий, у пациентов с АФС наблюдается хроническая головная боль или мигрень, эпилепсия, хорея, нарушения зрения, миелопатия и когнитивная дисфункция.
Патология почек. При АФС основные поражения почек также обусловлены тромбозом почечных артерий или вен. Также возможно формирование нефропатии, обусловленной окклюзией мелких сосудов почек. Нефропатия может быть острой или хронической. Наиболее характерные клинические проявления поражений почек при АФС — артериальная гипертензия (часто тяжелая), протеинурия различной степени выраженности, гематурия, почечная недостаточность.
Гематологические проявления. Основными изменениями со стороны крови является тромбоцитопения и, реже, гемолитическая анемия. Тромбоцитопения встречается у трети

пациентов с АФС, редко бывает выраженной. Геморрагические осложнения, несмотря на тромбоцитопению, наблюдаются редко, и, как правило, они связаны с сопутствующим дефектом специфических факторов свертывания крови, патологией почек или передозировкой антикоагулянтов. В 20% случаев тромбоцитопения может предшествовать развитию достоверного АФС.
Катастрофический АФС. У небольшой части пациентов (около 1%) может развиться тяжелый, опасный для жизни катастрофический АФС. Этот вариант АФС характеризуется быстрым началом и развитием полиорганной недостаточности, обусловленной генерализованным тромбозом сосудов малого калибра. Другое название катастрофического АФС - синдром Ашерсона (Asherson’s syndrome), поскольку был впервые описан R. A. Asherson. В отсутствии лечения смертность более 50%.
Лабораторная диагностика АФС. При проведении лабораторной диагностики наблюдаются реакции, противоположные клиническим проявлениям. In vivo происходит гиперкоагуляция, in vitro – гипокоагуляция. Парадоксальные, по сравнению с клиническими данными, результаты объясняются тем, что аутоантитела к фосфолипид-связывающим протеинам мешают факторам свертывания и процессам активации на фосфолипидных компонентах, которые добавляют в плазму при исследовании коагуляции.
Основными лабораторными показателями, используемыми для диагностики АФС, являются волчаночный антикоагулянт (ВА), антикардиолипиновые антитела и антитела к β2гликопротеину.
Волчаночный антикоагулянт - это группа гетерогенных антител классов IgG или IgM к β2-GP I, протромбину и некоторым другим белкам. При исследовании in vitro эти антитела проявляют свойства антикоагулянтов. Их присутствие увеличивает время свертывания при проведении фосфолипидзависимых тестов - АЧТВ, протромбинового времени. Волчаночный антикоагулянт взаимодействует с фосфолипидами, входящими в состав реагента, нарушает связь фосфолипидов с факторами коагуляции, что in vitro приводит что приводит к нарушению образования протромбиназного комплекса и тромбина, и соответственно, к удлинению времени свертывания крови. Обычно ВА обнаруживают по удлинению у больных АЧТВ, при этом они не имеют выраженных проявлений кровоточивости, в то же время у 30 % из них может развиваться тромбоз, т. е. имеется парадоксальная реакция – удлинение АЧТВ и развитие тромбоза. Тест на определение ВА на фоне терапии НМГ и варфарином не проводится.
Антитела к кардиолипину – это аутоантитела к липидно-белковому комплексу, состоящему из кардиолипина и его ко-фактора β2GPI. Кардиолипин (дифосфатидилглицерол) - мембранный фосфолипид. Наличие в крови антител к кардиолипину является одной из причин получения ложноположительных результатов исследований на сифилис в микрореакции преципитации с кардиолипиновым антигеном (VDRL-тест – Venereal Disease Research Laboratory). Посредством VDRL-теста определяют агглютинацию липидных частиц, которые содержат холестерин и кардиолипин. АФА присоединяются к кардиолипину этих частиц и вызывают их агглютинацию.
Еще одним основным лабораторным тестом, используемым в диагностике АФС, являются антитела к β2-GP I, класса IgG и/или IgM, определенные в высоком титре.
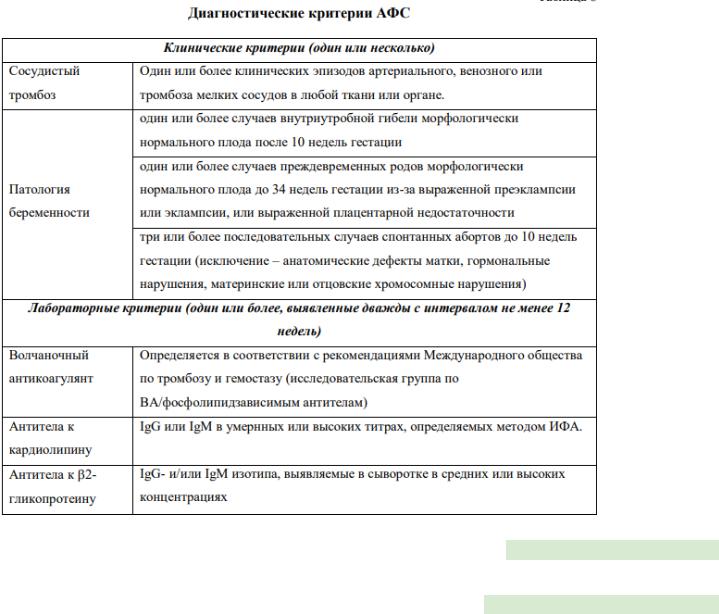
В настоящее время практическая диагностика АФС основана на критериях, которые были утверждены в 2006 году в Сиднее на XI Международном конгрессе по АФА. Выделяют клинические и лабораторные критерии. Обязательным для постановки диагноза является сочетание клинического и лабораторного критерия, при этом АФА должны определяться в высоких титрах. Клинические проявления без наличия АФА и обнаружение АФА без тромботических событий и/или акушерских патологий (т.е. носительство антител) не относятся к АФС. Положительные результаты тестов на АФА должны быть получены не менее двух раз с интервалом не менее 12 недель.
Лечение АФС
заключается в минимизации факторов тромботического риска и назначении антикоагулянтной терапии. Для уменьшения тромботического риска рекомендуется модификация образа жизни (регулярные физические упражнения, отказ от курения, снижение веса, коррекция гипертонии, дислипидемии и диабета), отказ от гормональной контрацепции эстрогенсодержащими препаратами, избегание длительной иммобилизации. Фармакологическое лечение заключается в назначении НМГ или варфарина. Эффективность других пероральных антикоагулянтов в настоящее время не подтверждена. Длительная антикоагулянтная терапия обеспечивается приемом варфарина под контролем МНО. Обычное целевое значение МНО 2
– 3.
Лечение АФС у беременных женщинженщинам с ВТЭО во время беременности рекомендовано обследование на АФС, т.к. это может повлиять на выбор дозы препаратов для тромбопрофилактики, а также длительность проведения антикоагулянтной терапии женщины с предшествующим ВТЭО, связанным с АФС, должны наблюдаться совместно с гематологом. если женщина с АФС и предшествующим ВТЭО принимала пероральные антитромботические средства в течение длительного времени, рекомендовано назначить тромбопрофилактику повышенной дозой НМГ (75% от терапевтической дозы, либо полная терапевтическая доза) антенатально и на протяжении 6 недель после родов или вплоть до возобновления пероральной антикоагулянтной терапии после родов. Не рекомендовано использовать ацетилсалициловую кислоту для тромбопрофилактики во время беременности. Варфарин не рекомендован для лечения и профилактики ВТЭО во время беременности, т.к. он проникает через плаценту и оказывает тератогенное действие, Женщинам, планирующим беременность, рекомендовано заменить варфарин на НМГ. Назначение варфарина рекомендовано рассмотреть в исключительных случаях женщинам с механическими клапанами сердца из-за высокого риска тромбоза даже при терапии НМГ. В этих случаях терапия варфарина с 6 недели до 13 недель меняется на терапию НМГ или гепарином натрия, с последующим возобновлением терапии варфарином, а с 29 недели беременности рассмотреть вопрос о переходе на НМГ в связи с большей их безопасностью во время родоразрешения. В
