
- •2. Основные законы химии: закон сохранения массы и энергии, закон кратных отношений, закон постоянства состава, закон Авогадро и следствия из него, закон простых объемных отношений.
- •4. Основные принципы квантовой теории строения вещества: корпускулярно-волновой дуализм, принцип неопределенности, волновая функция, уравнение Шредингера, атомная орбиталь.
- •Квантовые числа: главное, побочное, магнитное, спиновое
- •Формулировка периодического закона д.И. Менделеева. Структура периодической системы химических элементов. Понятие периода и группы. Значение периодического закона.
- •Свойства атомов элементов: потенциал ионизации, сродство к электрону, электроотрицательность, радиусы Ван-дер-Ваальса. Периодический характер изменений свойств элементов в периоде и группе.
- •Вопрос 9. Метод валентных связей. Сигма- и Пи-связи. Гибридизация атомных орбиталей и геометрия молекул. Неподеленные электронные пары гибридных орбиталей (на примере nh3 и н2о).
- •Вопрос 11. Химическое равновесие. Константа равновесия. Смещение химического равновесия при изменении давления, температуры, концентрации. Принцип Ле-Шателье.
- •Вопрос 12. Растворы. Причины образования растворов. Физические силы (Ван-дер- Ваальса): ориентационные, индукционные, дисперсные. Химические силы: водородная связь, ион-дипольное взаимодействие.
- •Вопрос 13. Способы выражения концентраций растворов. Значение растворов в химии.
- •Вопрос 14. Электролиты. Типы сильных электролитов. Типы слабых электролитов. Константа и степень диссоциации слабых электролитов. Произведение растворимости.
- •Вопрос 15. Вода как слабый электролит. Ионное произведение воды. Водородный показатель среды рН.
- •Вопрос 16. Гидролиз солей. Типы гидролиза, константа и степень гидролиза.
- •Вопрос 17. Оксиды, гидроксиды и соли как важнейшие классы неорганических соединений. Их получение и свойства.
- •Получение гидроксидов
- •Вопрос 18. Степень окисления и правила ее нахождения. Окислители и восстановители. Типы овр.
- •Определение степени окисления проводят, исходя из следующего:
- •Вопрос 19. Комплексные соединения. Определение, строение, номенклатура. Диссоциация комплексных солей. Константа нестойкости. Теория координационной химической связи. Значение комплексных соединений.
- •20. Основные законы и понятия электрохимии: электродный потенциал, уравнение Нернста. Ряд напряжений металлов и его свойства.
- •21. Электролиз расплавов и растворов. Применение электролиза.
- •40. Второй закон термодинамики. Энтропия в классической и статистической термодинамике.
- •41. Энергия Гиббса. Энергия Гельмгольца. Свободная энергия и направление химических реакций.
- •42. Скорость химических реакций. Средняя и мгновенная скорость химической реакции. Константа скорости химической реакции. Влияние концентрации на скорость химической реакции. Закон действующих масс.
- •43. Порядок и молекулярность реакции. Элементарные процессы. Определение порядка реакции. Период полураспада.
- •44. Влияние температуры на скорость реакции. Уравнение Аррениуса. Энергия активации. Определение энергии активации.
- •45. Катализ и его значение в биологических процессах. Классификация каталитических процессов.
- •46. Гомогенный катализ. Теория гомогенного катализа
- •47. Гетерогенный катализ. Роль адсорбции в гетерогенном катализе. Представление об активных центрах.
- •48. Ферментативный катализ, его особенности и значение в биологических процессах.
- •49. Буферные системы, их состав и механизм действия. Расчет рН буферных систем. Буферная ёмкость. Биологическое значение буферных систем. Буферные системы в организма
- •50. Электропроводность растворов электролитов
- •51. Удельная и эквивалентная электропроводность. Зависимость удельной электропроводности от разбавления. Скорости движения ионов. Закон Кольрауша. Подвижность ионов
- •52. Практическое применение электропроводности. Определение степени и константы диссоциации слабых электролитов. Кондуктометрическое титрование.
- •54. Водородный электрод. Электроды I и II рода.
- •55. Измерение эдс. Концентрационные цепи.
- •56. Окислительно-восстановительные электроды и цепи.
- •57. Потенциометрический метод измерения рН. Потенциометрическое титрование.
- •58. Поверхностные явления, Адсорбция. Изотерма адсорбции. Физическая и химическая адсорбция.
- •59. Адсорбция на границе твердое вещество-газ. Теория адсорбции. Уравнения Ленгмюра и Фрейндлиха.
- •60. Адсорбция на границе жидкость-газ. Уравнение Гиббса. Поверхностноактивные и поверхностнонеактивные вещества.
- •Классификация дисперсных систем.
- •Общая характеристика коллоидных систем. Методы получения лиофобных коллоидов
- •Мицеллярная теория строения коллоидной частицы.
- •Устойчивость коллоидных систем. Коагуляция. Действие электролитов. Правило Шульца-Гарди.
- •Молекулярно-кинетические, оптические и электрокинетические свойства коллоидных систем.
- •Общая характеристика растворов вмс.
- •Устойчивость растворов вмс.
- •Изоэлектрическое состояние. Нарушение устойчивости. Расслоение.
- •Коацервация. Лиотропные ряды. Высаливание.
- •Процессы структурообразования в растворах вмс.
- •Набухание и растворения вмс. Степень набухания и скорость набухания. Факторы набухания.
- •Хрупкие и эластичные гели. Застудневание. Свойства студней. Синерезис. Полуколлоиды.
Набухание и растворения вмс. Степень набухания и скорость набухания. Факторы набухания.
ВМС растворяется не в любом, а лишь в «хорошем» растворителе, и практически не растворяется в «плохом». Для пары «ВМС — растворитель» действует правило полярности: для ВМС полярного строения «хорошим» будет полярный растворитель (желатин — вода), неполярные ВМС лучше растворяются в неполярных жидкостях (каучук в бензоле).
Растворение ВМС отличается от растворения низкомолекулярных соединений, его описывают с использованием термина набухание. Растворение ВМС является самопроизвольным термодинамически выгодным процессом.
В процессе набухания ВМС можно выделить четыре стадии в зависимости от растворителя, пространственной структуры полимера, температуры и ряда других факторов процесс может остановиться на любой из них.
Первая стадия отвечает существованию двух фаз: «ВМС» и «растворитель».
На второй стадии молекулы растворителя проникают в полимер, раздвигая цепи и увеличивая его массу и объем. Этой стадии соответствует экзотермический тепловой эффект.
Третьей стадии соответствует переход макромолекул ВМС в фазу растворителя; как правило, он происходит очень медленно. Если набухание прекращается на второй или третьей стадии, говорят об ограниченном набухании ВМС. Ограниченно набухший полимер (структурированная система) называется студнем.
Четвертая стадия отвечает образованию гомогенного раствора ВМС, набухание в этом случае неограниченно.

Количественной мерой набухания является степень набухания
![]()
где V() — масса и объем сухого полимера; т, V — масса и объем набухшего полимера.
Тепловой эффект, сопровождающий процесс набухания, называют теплотой набухания.
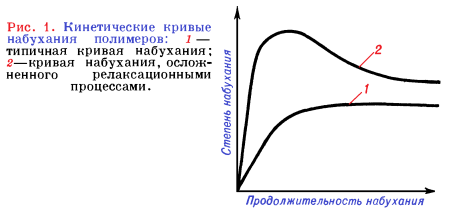
Скорость набухания dx/dτ (τ — продолжительность набухания) обычно имеет максимальное значение в начале процесса. При ограниченном набухании по мере приближения системы к состоянию равновесия dx/dτ—>0, а α—> αmах (αmах — равновесная, или максимальная, степень набухания).
Кинетика набухания может быть описана различными уравнениями.
Для простейшего случая (кривая 1 на рисунке 1) широко используют дифференциальное уравнение 1 или его интегральную форму (уравнение 2):
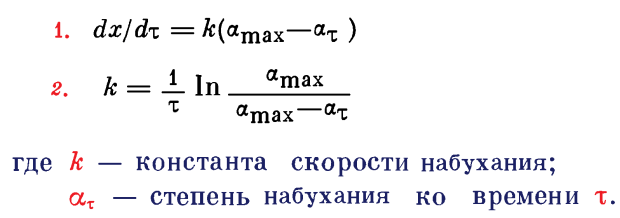
Факторы, влияющие на набухание:
1. Природа ВМС и растворителя (неполярные полимеры хорошо набухают и растворяются в неполярных растворителях, полярные – в полярных).
2. Время жизни ВМС: чем старше полимер, тем хуже он набухает.
3. Температура: интенсифицирует процесс набухания.
4. рН среды.
5. Добавка электролита.
Хрупкие и эластичные гели. Застудневание. Свойства студней. Синерезис. Полуколлоиды.
Хрупкие (ненабухающие и необратимые) гели построены из жестких частиц (типичные представители: гель поликремниевой кислоты, гели гидрофобных коллоидов SnO2, V2O5, TiO2, Fe2O3). Благодаря сильно развитой поверхности сухие хрупкие гели являются хорошими адсорбентами, типичным представителем которых является силикагель, по составу представляющий собой SiO2. Но получают его взаимодействием Na2SiO3 или K2SiO3 с минеральными кислотами, которое в водном растворе сопровождается образованием студня поликремниевой кислоты, из которого после высушивания получают пористые зерна сухого силикагеля (подобным образом получают и пористый алюмогель Al2O3). При внесении в любую жидкость сухие хрупкие гели впитывают ее, не изменяя своего объема (не набухают)
Студни (эластичные гели) являются обратимыми и набухающими. Они образованы гибкими цепными макромолекулами желатины, агар-агара (полисахарид, получаемый из морских красных водорослей), альбумина, пептона, гуммиарабика, каучука и других полимеров, которые не теряют 16 своей эластичности при высушивании и способны к ограниченному или неограниченному набуханию в соответствующих растворителях.
Часто явная коагуляция растворов ВМС происходит в форме застудневания. При этом осадка не образуется, а вся система, утрачивая текучесть, переходит в особое промежуточное состояние, называемое гелем или студнем. Иными словами застудневание – это следствие нарушения агрегативной устойчивости, приводящее к структурообразованию. Это самопроизвольный изотермический процесс перехода раствора ВМС в структурированную систему.
Для эластичных гелей и студней характерно явление синерезиса, т.е. самопроизвольное выделение жидкости. Этот процесс сопровождается уплотнением пространственной структурной сетки вследствие образования дополнительных контактов между частицами или макромолекулами. При этом объем студня или геля уменьшается, однако сохраняется его первоначальная форма. Термодинамически синерезис обусловлен уменьшением энергии Гиббса пересыщенной системы за счет выделения из нее новой макрофазы.
Синерезис является необратимым процессом и свидетельствует о старении («созревании») студня или геля. Ускорению процесса синерезиса способствуют низкие температуры и отсутствие механических вибраций. Наглядным примером может служить отделение сыворотки (свертывание молока, «слеза» в сыре и т.д.). В этом процессе вначале отжимается свободная вода (часть растворителя, выполняющая роль среды, в которой распределены частицы вещества), а затем, частично, и связанная вода (входящая в состав гидратных оболочек макромолекул и участвующая вместе с ними в броуновском движении).
Растворы полуколлоидов – это такие системы, которые при определенных условиях являются истинными растворами, а при смене концентрации дисперсной фазы становятся золями в коллоидном состоянии. К ним относятся растворы танидов, мыл, некоторых органических оснований (этакридина лактат).
