- •2. Основные законы химии: закон сохранения массы и энергии, закон кратных отношений, закон постоянства состава, закон Авогадро и следствия из него, закон простых объемных отношений.
- •4. Основные принципы квантовой теории строения вещества: корпускулярно-волновой дуализм, принцип неопределенности, волновая функция, уравнение Шредингера, атомная орбиталь.
- •Квантовые числа: главное, побочное, магнитное, спиновое
- •Формулировка периодического закона д.И. Менделеева. Структура периодической системы химических элементов. Понятие периода и группы. Значение периодического закона.
- •Свойства атомов элементов: потенциал ионизации, сродство к электрону, электроотрицательность, радиусы Ван-дер-Ваальса. Периодический характер изменений свойств элементов в периоде и группе.
- •Вопрос 9. Метод валентных связей. Сигма- и Пи-связи. Гибридизация атомных орбиталей и геометрия молекул. Неподеленные электронные пары гибридных орбиталей (на примере nh3 и н2о).
- •Вопрос 11. Химическое равновесие. Константа равновесия. Смещение химического равновесия при изменении давления, температуры, концентрации. Принцип Ле-Шателье.
- •Вопрос 12. Растворы. Причины образования растворов. Физические силы (Ван-дер- Ваальса): ориентационные, индукционные, дисперсные. Химические силы: водородная связь, ион-дипольное взаимодействие.
- •Вопрос 13. Способы выражения концентраций растворов. Значение растворов в химии.
- •Вопрос 14. Электролиты. Типы сильных электролитов. Типы слабых электролитов. Константа и степень диссоциации слабых электролитов. Произведение растворимости.
- •Вопрос 15. Вода как слабый электролит. Ионное произведение воды. Водородный показатель среды рН.
- •Вопрос 16. Гидролиз солей. Типы гидролиза, константа и степень гидролиза.
- •Вопрос 17. Оксиды, гидроксиды и соли как важнейшие классы неорганических соединений. Их получение и свойства.
- •Получение гидроксидов
- •Вопрос 18. Степень окисления и правила ее нахождения. Окислители и восстановители. Типы овр.
- •Определение степени окисления проводят, исходя из следующего:
- •Вопрос 19. Комплексные соединения. Определение, строение, номенклатура. Диссоциация комплексных солей. Константа нестойкости. Теория координационной химической связи. Значение комплексных соединений.
- •20. Основные законы и понятия электрохимии: электродный потенциал, уравнение Нернста. Ряд напряжений металлов и его свойства.
- •21. Электролиз расплавов и растворов. Применение электролиза.
- •40. Второй закон термодинамики. Энтропия в классической и статистической термодинамике.
- •41. Энергия Гиббса. Энергия Гельмгольца. Свободная энергия и направление химических реакций.
- •42. Скорость химических реакций. Средняя и мгновенная скорость химической реакции. Константа скорости химической реакции. Влияние концентрации на скорость химической реакции. Закон действующих масс.
- •43. Порядок и молекулярность реакции. Элементарные процессы. Определение порядка реакции. Период полураспада.
- •44. Влияние температуры на скорость реакции. Уравнение Аррениуса. Энергия активации. Определение энергии активации.
- •45. Катализ и его значение в биологических процессах. Классификация каталитических процессов.
- •46. Гомогенный катализ. Теория гомогенного катализа
- •47. Гетерогенный катализ. Роль адсорбции в гетерогенном катализе. Представление об активных центрах.
- •48. Ферментативный катализ, его особенности и значение в биологических процессах.
- •49. Буферные системы, их состав и механизм действия. Расчет рН буферных систем. Буферная ёмкость. Биологическое значение буферных систем. Буферные системы в организма
- •50. Электропроводность растворов электролитов
- •51. Удельная и эквивалентная электропроводность. Зависимость удельной электропроводности от разбавления. Скорости движения ионов. Закон Кольрауша. Подвижность ионов
- •52. Практическое применение электропроводности. Определение степени и константы диссоциации слабых электролитов. Кондуктометрическое титрование.
- •54. Водородный электрод. Электроды I и II рода.
- •55. Измерение эдс. Концентрационные цепи.
- •56. Окислительно-восстановительные электроды и цепи.
- •57. Потенциометрический метод измерения рН. Потенциометрическое титрование.
- •58. Поверхностные явления, Адсорбция. Изотерма адсорбции. Физическая и химическая адсорбция.
- •59. Адсорбция на границе твердое вещество-газ. Теория адсорбции. Уравнения Ленгмюра и Фрейндлиха.
- •60. Адсорбция на границе жидкость-газ. Уравнение Гиббса. Поверхностноактивные и поверхностнонеактивные вещества.
- •Классификация дисперсных систем.
- •Общая характеристика коллоидных систем. Методы получения лиофобных коллоидов
- •Мицеллярная теория строения коллоидной частицы.
- •Устойчивость коллоидных систем. Коагуляция. Действие электролитов. Правило Шульца-Гарди.
- •Молекулярно-кинетические, оптические и электрокинетические свойства коллоидных систем.
- •Общая характеристика растворов вмс.
- •Устойчивость растворов вмс.
- •Изоэлектрическое состояние. Нарушение устойчивости. Расслоение.
- •Коацервация. Лиотропные ряды. Высаливание.
- •Процессы структурообразования в растворах вмс.
- •Набухание и растворения вмс. Степень набухания и скорость набухания. Факторы набухания.
- •Хрупкие и эластичные гели. Застудневание. Свойства студней. Синерезис. Полуколлоиды.
58. Поверхностные явления, Адсорбция. Изотерма адсорбции. Физическая и химическая адсорбция.
Пове́рхностные явле́ния — совокупность явлений, обусловленных особыми свойствами тонких слоёв вещества на границе соприкосновения фаз. К поверхностным явлениям относятся процессы, происходящие на границе раздела фаз, в межфазном поверхностном слое и возникающие в результате взаимодействия сопряжённых фаз.
Поверхностные явления обусловлены тем, что в поверхностных слоях на межфазных границах вследствие различного состава и строения соприкасающихся фаз и соответственно из-за различия в связях поверхностных атомов и молекул со стороны разных фаз существует ненасыщенное поле межатомных, межмолекулярных сил. Вследствие этого атомы и молекулы в поверхностных слоях образуют особую структуру, а вещество принимает особое состояние, отличающееся от его состояния в объеме фаз различными свойствами
Адсорбция (от лат. ad — на, при и sorbeo — поглощаю), поглощение к.-л. вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела.

Изоте́рма адсо́рбции — зависимость количества адсорбированного вещества (величины адсорбции) от парциального давления этого вещества в газовой фазе (или концентрации раствора) при постоянной температуре.
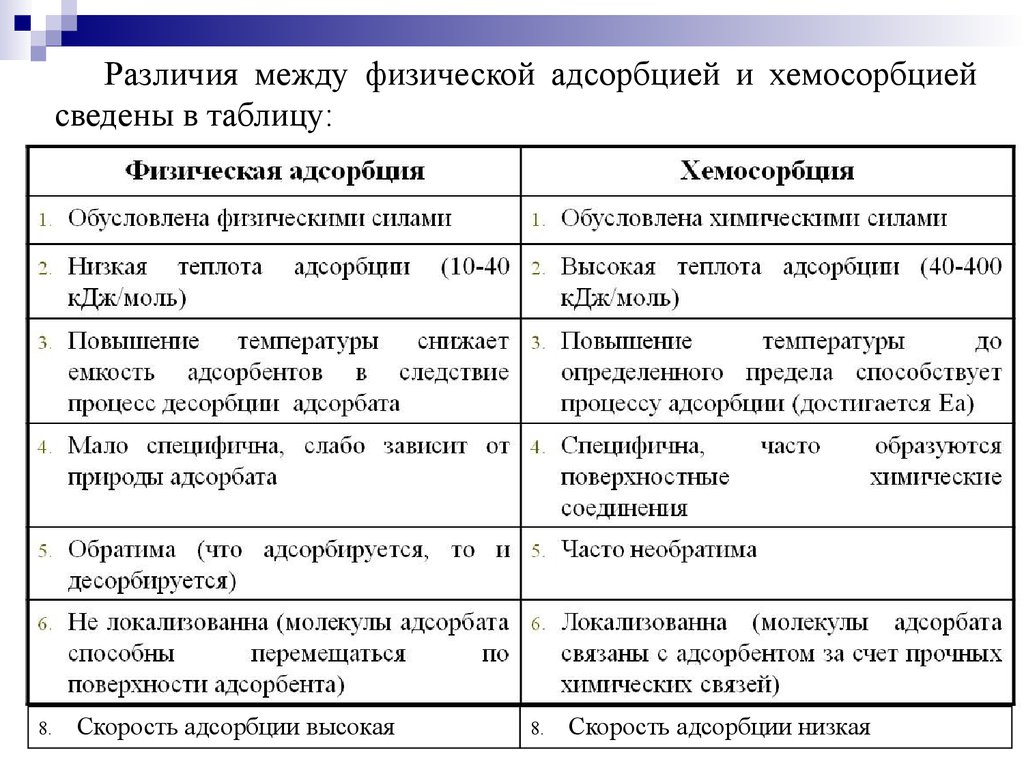
Различают два вида адсорбции – физическая и химическая адсорбция. Физическая адсорбция вызвана Ван – дер – ваальсовыми силами взаимодействия между молекулами адсорбата и адсорбента. Химическая адсорбция, или хемосорбция, обязана химической связи, возникающей между адсорбатом и адсорбентом.
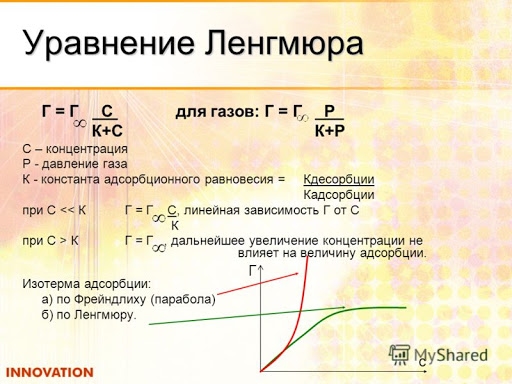
59. Адсорбция на границе твердое вещество-газ. Теория адсорбции. Уравнения Ленгмюра и Фрейндлиха.



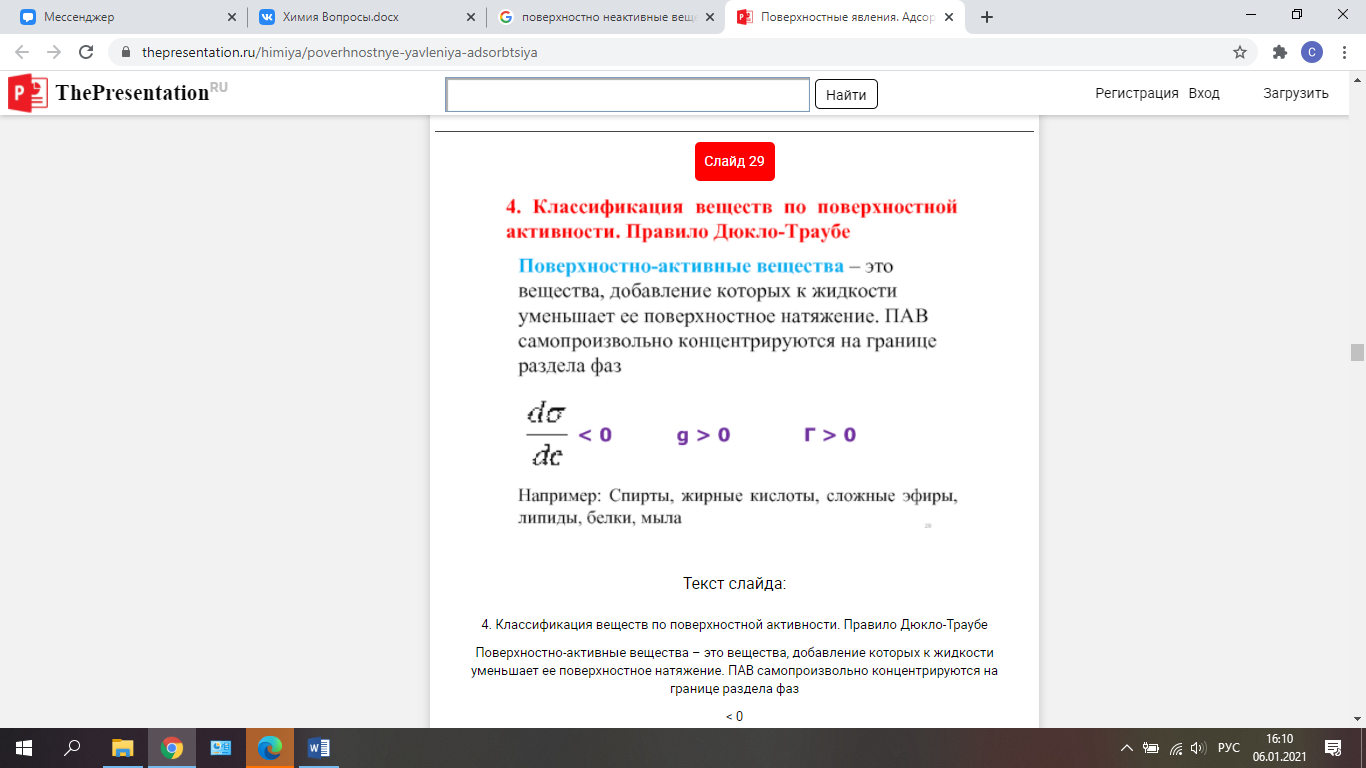
60. Адсорбция на границе жидкость-газ. Уравнение Гиббса. Поверхностноактивные и поверхностнонеактивные вещества.



Классификация дисперсных систем.
Классификация по агрегатному состоянию:
|
Дисперсионная фаза |
||
Дисперсионная среда |
газовая |
жидкая |
твердая |
газовая |
- |
Аэрозоли, туманы, капли |
Аэрогели, аэрозоли, порошки, дымы, пыль |
жидкая |
Пены, газовые эмульсии |
Эмульсии, кремы |
Золи, гели, эмульсии, пасты |
твердая |
Твердые пены, фильтры, сорбенты, мембраны |
Твердые эмульсии |
Твердые золи, сплавы, композиты, покрытия, пленки |
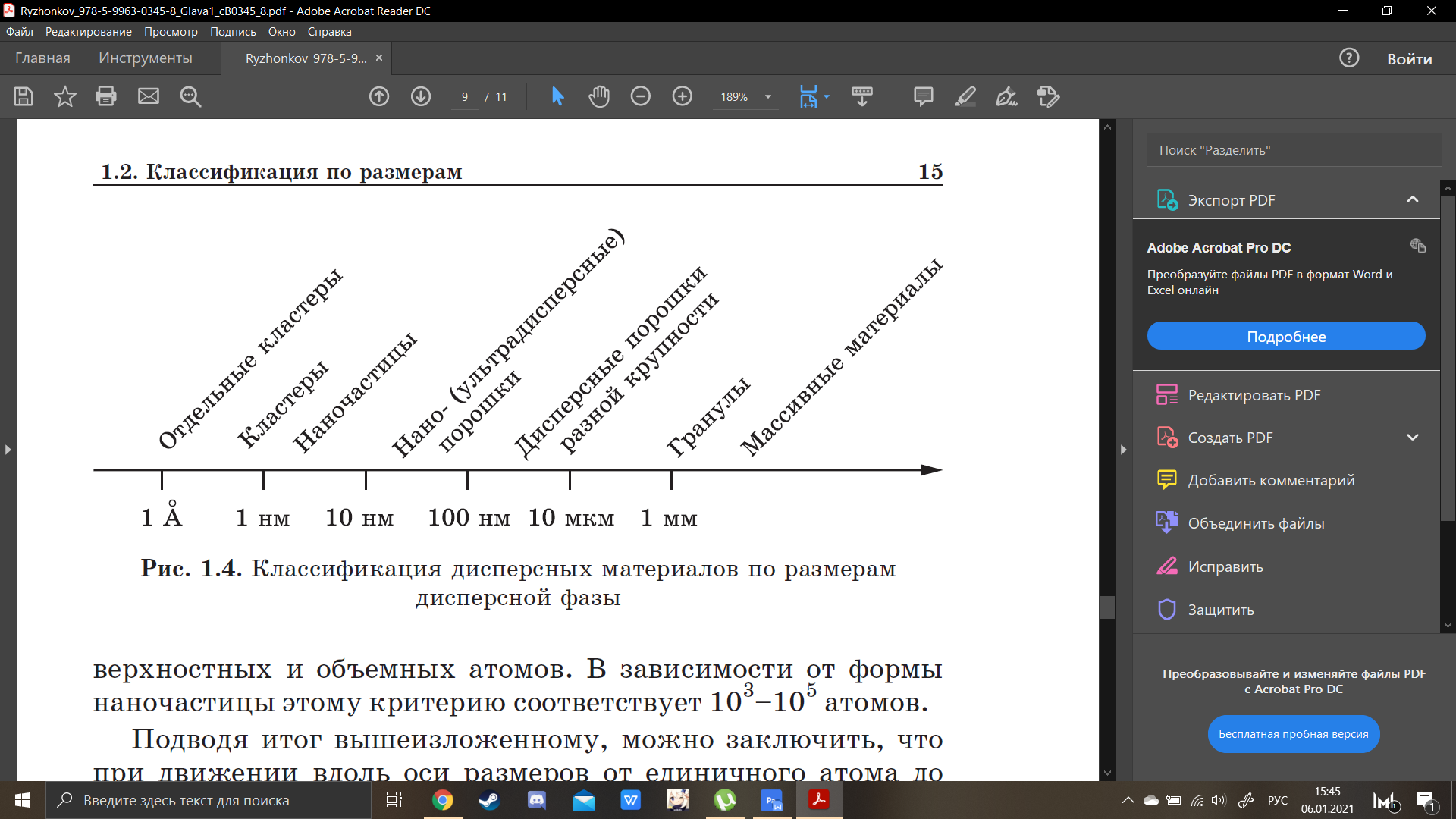
Классификация по размерам
В первом приближении дисперсные системы можно разделить на грубодисперсные и тонко- (высоко-) дисперсные(коллоидно-дисперсные или коллоидные системы). В грубодисперсных системах частицы имеют размеры от 1 мкм и выше, их удельная поверхность не более 1 м2 /г; в коллоидных — от 1 нм до 1 мкм, удельная поверхность может достигать сотен м 2 /г
молекулярно-дисперсные — размер дисперсной фазы менее 1 нм, высокодисперсные — 1–100 нм; среднедисперсные — 100 нм–10 мкм; грубодисперсные — более 10 мкм. В этой классификации нередко среднедисперсные системы называют микрогетерогенными, а высокодисперсные — ультрамикрогетерогенными.
в металлургии, наиболее распространен следующий тип разделения частиц по дисперсности: ультратонкий порошок — размер частиц менее 500 нм; весьма тонкий порошок — 500 нм–10 мкм; тонкий порошок — 10–40 мкм; порошок средней крупности — 40–150 мкм; грубый (крупный) порошок — 150–500 мкм.
для железных порошков дисперсность обычно характеризуется четырьмя классами: крупные — более 450 мкм, средние — 160–450 мкм, мелкие — менее 160 мкм и весьма мелкие — менее 56 мкм.
Для порошков, синтезированных в плазме, используется следующая классификация: наноразмерные (нанокристаллические, ультрадисперсные) — 130–50 нм, высокодисперсные (субмикрокристаллические) — 30–50 100–500 нм, микронные (крупнокристаллические) — 100–500 нм 10 мкм.
В научных кругах используется несколько отличная классификация: 1–100 нм — ультрадисперсные порошки; 100 нм–10 мкм — тонкодисперсные; 10–200 мкм — среднедисперсные; 200–1000 мкм — грубодисперсные.
к нано- (ультрадисперсным) относят системы, в которых размер морфологических элементов (частиц, зерен, кристаллитов) менее 100 нм. Этот класс дисперсных систем также называют нанопорошками, наноразмерными средами, нанокристаллическими материалами.
Классификация по мерности
Классификация дисперсных систем по мерности основывается на геометрии или числе измерений характерных размеров дисперсной фазы.
Характерные размеры и дисперсность трехмерных тел определяются в трех взаимно перпендикулярных направлениях.По современной классификации к нульмерным дисперсным системам относятся нано- (ультрадисперсные) порошки и наночастицы.
Дисперсность двумерных тел характеризуется двумя размерами, которые определяются в двух взаимно перпендикулярных направлениях, ), а третий размер L на дисперсность не влияет. Двумерные системы составляют волокна, нити, капилляры, которые имеют макродлину, а два других размера измеряются в нанометрах.
В случае одномерных тел только один размер а определяет дисперсность.К одномерным материалам относятся пленки, мембраны, покрытия, толщина которых измеряется в нанометрах, а два других измерения имеют макроскопические размеры.
К трехмерным наносистемам относятся объемные наноматериалы.