
Molekulyarnaya_biotekhnologia_Glik_B__Pasternak_Dzh
.pdf
Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
101 |
Рис. 5.24. (Продолжение)
Tag. По завершении нескольких раундов ПЦР, в которых использовались указанные выше праймеры, добавляют вторую пару праймеров, которые связываются по соседству с двумя первыми. Такие тесно расположенные праймеры называются внутренними. Вторая пара праймеров необходима, поскольку без них нельзя амплифицировать полноразмерную молекулу-мишень. Конечным ПЦР-продуктом является кДНК, соответствующая 3'-концу искомой мРНК.
В случае 5'RACE праймером для синтеза первой цепи кДНК служит GSP (рис. 5.23). Новосинтезированную цепь обрабатывают концевой дезоксинуклеотидилтрансферазой в присутст-
102 |
ГЛАВА 5 |
вии dATP. Этот фермент случайным образом присоединяет дезосирибонуклеотиды к 3'- концу цепи. Поскольку в данном случае в реакционной смеси присутствует только dATP, на этом конце появляется цепочка адениновых остатков — ро1у(А)-хвост. С ним спаривается праймер P-oligo(dT). инициирующий синтез второй цепи. Проводят ограниченное число раундов ПЦР с указанными праймерами, а затем добавляют вторые праймеры и амплифицируют кДНК, отвечающую 5'-концу мРНК.
RACE-метод широко применяется по ряду причин. Обычно бывает очень трудно обнаружить кДНК, соответствующую мРНК, которая присутствует в данной ткани в маленькой концентрации. С помощью RACE-метода можно быстро получить кДНК, отвечающие концевым участкам этой мРНК, и при необходимости использовать их в качестве зондов для скрининга кДНК- и геномных библиотек. Кроме того, поскольку неполноразмерные 3'-концевые фрагменты кДНК значительно преобладают над полноразмерными, 5'RACE может восполнить недостающие 5'-концевые сегменты.
Синтез генов с помощью ПЦР
Получение генов с помощью ПЦР — гораздо более быстрый и экономичный метод, чем тот, который основан на отжиге олигонуклеотидов с перекрывающимися концами, заполнении брешей с помощью ДНК-полимеразы и сшивании разрывов ДНК-лигазой. В одной из методик конструирование гена начинается с отжига двух перекрывающихся олигонуклеотидов (А и В), отвечающих центральной части гена (рис. 5.24). После отжига образуется дуплекс с заглубленными 3'-гидроксильными группами, служащими точками инициации синтеза комплементарных цепей при ПЦР. Затем в реакционную смесь добавляют еще два олигонуклеотида, С и D. З'-конец олигонуклеотида С идентичен 5'-концу олигонуклеотида А, а сам этот олигонуклеотид отвечает участку конструируемого гена, непосредственно примыкающему к его центральной части слева. Аналогично, 3'-конец олигонуклеотида D идентичен 5'-концу олигонуклеотида В и отвечает участку гена, примыкающему к его центральной части справа. После денатурации смеси и отжига образуются дуплексы с протяженными выступающими одноцепочечными сегментами, достраивающимися с З'-концов. В ходе последующих раундов ПЦР образуется двухцепочечный продукт, состоящий из указанных выше сегментов, расположенных в порядке CABD. Молекула ДНК с заглубленными 5'-концами не достраивается.
На следующем этапе в реакционную смесь добавляют еще два олигонуклеотида, E и F. 3'-конец олигонуклеотида E идентичен 5'-концу олигонуклеотида С, а сам он отвечает участку реконструируемого гена, примыкающему слева к сегменту С. Аналогичными свойствами обладает олигонуклеотид F, если его соотносить с олигонуклеотидом D. После денатурации и ренатурации смеси образовавшиеся дуплексы с выступающими од ноцеп очечным и участками достраиваются с 3'-гидроксильных концов. В ходе последующих раундов ПЦР образуется двухиепочечный продукт ECABDF.
Следующие пары олигонуклеотидов — один «достраивающий» ген слева, другой справа -последовательно добавляют в смесь до тех пор, пока не будет синтезирован весь ген. Длина этих олигонуклеотидов обычно бывает равна 50 звеньям. Каждый «блок» ПЦР состоит из двадцати 4-минутных раундов. Для синтеза гена длиной 1000 п. н. нужно 10 «блоков», так что ген можно получить в течение одного дня. При этом, как и в случае синтеза генов другими методами, последнюю пару нуклеотидов (т. е. 5'- и 3'-концы) можно снабдить дополнительными последовательностями, фланкирующими кодирующий участок и облегчающими последующее встраивание гена в вектор.
ЗАКЛЮЧЕНИЕ
К числу наиболее важных для молекулярной биотехнологии методов, помимо клонирования генов, относятся методы химического синтеза ДНК, секвенирование ДНК и полимеразная цепная реакция (ПЦР).
Целью химического синтеза является получение одноцепочечных молекул ДНК in vitro. Успеха здесь можно достичь только при высокой эффективности образования фосфодиэфирных связей. В противном случае по окончании
Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
103 |
процесса будет получено очень небольшое число молекул нужного размера. Длина синтезированных in vitro молекул обычно составляет 20-30 нуклеотидов и редко превышает 100 нуклеотидов. Для получения двухцепочечных молекул комплементарные цепи синтезируют по отдельности и затем проводят отжиг. Полученную таким способом ДНК используют в качестве зондов для скрининга геномных библиотек; в качестве линкеров и адаптеров при клонировании генов; для мутагенеза in vitro; для конструирования генов с целью последующего клонирования.
Очень часто для решения биотехнологических и некоторых других задач бывает необходимо знать полную нуклеотидную последовательность клонированного гена. Для секвенирования используют несколько методов; один из них — дидезокси-метод, разработанный Сангером и др. В его основе лежит остановка синтеза цепи после присоединения к ней дидезоксинуклеотида. У такого нуклеотида отсутствует 3'- гидроксильная группа, и дальнейший рост цепи становится невозможным. Для секвенирования в разных пробирках одновременно проводят четыре реакции синтеза ДНК, каждая — в присутствии одного из четырех дидезоксинуклеотидов. Продукты реакций разделяют с помощью гель-электрофореза, проводят радиоавтографию и «считывают» с радиоавтографа нуклеотидную последовательность синтезированного фрагмента ДНК.
Для секвенирования используют также систему на основе фага M13. В ДНК фага встраивают фрагмент ДНК длиной до 500 нуклеотидов, который хотят секвенировать. Эту рекомбинантную ДНК легко получить в одноцепочечной форме и использовать ее в качестве матрицы для секвенирования вставки. Можно использовать также двухцепочечные плазмиды, содержащие клонированную ДНК.
Для определения нуклеотидной последовательности протяженных клонированных сегментов сначала подбирают синтетический олигонуклеотидный праймер, комплементарный участку, соседствующему со вставкой, и с помощью дидезокси-метода секвенируют первые 250—300 нуклеотидов. Затем по результатам секвенирования синтезируют второй праймер и определяют последовательность следующих 250—350 нуклеотидов клонированного участка, и т. д. Этот метод, называемый «праймеропосредованной прогулкой» (или «блуждающей затравкой»), позволяет секвенировать протяженные фрагменты ДНК без их субклонирования, как в случае системы на основе фага М13.
Метод ПЦР произвел настоящую революцию в биотехнологии. Он позволяет в миллионы раз амплифицировать in vitro нужные сегменты ДНК. Процедура состоит в следующем. Подбирают два праймера, гибридизующиеся с участками ДНК, которые фланкируют искомую последовательность. Денатурируют ДНК, отжигают одноцепочечные молекулы с праймерами, добавленными в избытке, и осуществляют синтез ДНК in vitro. Для облегчения синтеза используют термостабильную ДНК-полимеразу, которая не разрушается при температуре денатурации (95 °С). Затем опять проводят денатурацию, отжиг с праймерами и синтез, и т. д. до примерно 30-го раунда. К этому времени в реакционной смеси преобладают фрагменты, на одном конце которых находится одна праймерная последовательность, а на другом — последовательность, комплементарная второму праймеру. ПЦР можно использовать для выявления патогенных микроорганизмов в том или ином биологическом материале; получения больших количеств специфических фрагментов ДНК с целью клонирования; амплификации 5'- и 3’-концов специфических мРНК; синтеза генов; выявления делеций или вставок в генах, ответственных за то или иное наследственное заболевание.
ЛИТЕРАТУРА
Chen E. Y., P. H. Seeburg. 1985. Supercoil sequencing: a fast and simple method for sequencing plasmid DNA. DNA4: 165-170.
Climie S., D. V. Santi. 1990. Chemical synthesis of the thymidylate synthase gene. Proc. Natl. Acad, Set. USA 87: 633-637.
Di Donato A., M. de Nigris, N. Riisso, S. Di Biase, G. DAlessio. 1993. A method for synthesizing genes and cDNAs by the polymerase chain reaction. Anal. Biochem. 212: 291-293.
Erlich H. A., D. Gelfand, J. J. Sninsky. 1991. Recent advances in the polymerase chain reaction. Science 151: 1643-165].
104 |
ГЛАВА 5 |
Fox D. K., B. Westfall, M. Nathan, A. J. Hughes, Jr., A. Rashtchian, D. M. Schuster. 1996. Striding new distances with 5'RACE: long 5'RACE of human APC and TSC-2 cDNA. Focus 18: 33-37.
Itakura K., J. J. Rossi, R. B. Wallace. 1984. Synthesis and use of synthetic oligonycleotides.
Annu. Rev. Biochem. 53: 323-356.
Mullis К. В., F. Ferré, R. A. Gibbs (ed.). 1994. The Polymerase Chain Reaction. Birkhäuser,
Boston, Mass.
Saiki R. KM D. H. Gelfand, S. Stoffel, S. Scharf, R. Higuchi, G. T. Hörn, K. B. Mullis, H. A. Erlich. 1988. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science 239:487-491.
Sanger F., S. Nicklen, A. R. Coulson. 1977. DNA sequencing with chain-terminating inhibitors. Proc. Natl. Acad. Sei. USA 74: 5463-5467.
Schuster D. M., G. W, Buchman, A. Rashtchian. 1992. A simple and efficient method for amplification of cDNA ends using 5'RACE. Focus 14: 46-52.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1.Предположим, что ваш новый ДНК-синтезатор имеет среднюю эффективность присоединения нуклеотидов 98,5%. Каким будет выход продукта, если вы синтезируете гибридизационный зонд длиной 50 нуклеотидов?
2.Какие две стратегии химического синтеза гена длиной 0,5т. п. н. вы можете предложить? Какую из них вы предпочтете?
3.Что такое линкер? Где его используют?
4.Что такое дидезоксинуклеотиды? Как с их помощью определяют нуклеотидную последовательность ДНК?
5.Почему можно определить нуклеотидную последовательность только одноцепочемной ДНК?
6.Как определяют нуклеотидную последовательность клонированной ДНК с помощью векторной системы на основе фага М13?
7.На месте преступления обнаружен один-единственный волос предполагаемого преступника. В нем содержится [0—20 пикограмм (10–12 г) ДНК. Чтобы охарактеризовать
столь малое количество ДНК и определить, идентична ли ее нуклеотидная последовательность таковой у ДНК подозреваемого, нужно 10—100 нанограмм (10~9 г) ДНК. Как получить ее? Какую информацию вам нужно собрать, прежде чем предпринимать какие-то действия?
8.Что такое «длинная матрица», «короткая матрица», как меняется соотношение между ними с увеличением числа ПЦР-раундов?
9.Как синтезируют гены с помощью ПЦР?
10. Как «превратить» концы молекулы мРНК в кДНК?
ГЛАВА 6.
Оптимизация экспрессии генов, клонированных в прокариотических системах
Основная цель экспериментов по клонированию генов, которые предполагается использовать в биотехнологии, — подбор условий для эффективной экспрессии в нужном организме-хозяине. К сожалению, сам факт встраивания того или иного гена в клонирующий вектор еще не означает, что этот ген будет экспрессирован. В то же время, чтобы получение коммерческого продукта было экономически оправданным, уровень его синтеза должен быть достаточно высоким. Для достижения эффективной экспрессии уже сконструировано много специфических векторов; для этого проводились манипуляции с целым рядом генетических элементов, контролирующих процессы транскрипции и трансляции, стабильность белков, секрецию продуктов из хозяйской клетки и т. д. Среди молекулярно-биологических свойств систем экспрессии наиболее важны следующие: 1 ) тип промотора и терминатора транскрипции; 2) прочность связывания мРНК с рибосомой; 3) число копий клонированного гена и его локализация (в плазмиде или Б хромосоме хозяйской клетки); 4) конечная локализация синтезируемого продукта; 5) эффективность трансляции в организме хозяина; 6) стабильность продукта в хозяйской клетке.
Никакой универсальной стратегии оптимизации экспрессии клонированных генов не существует. Большинство таких генов имеют уникальные молекулярные свойства, и оптимальные системы экспрессии для каждого из них приходится подбирать всякий раз заново. Эффективность экспрессии любого чужеродного гена зависит также от его родства с организмом-хозяином. Несмотря на то что многие представители как протак и эукариотических организмов способны к экспрессии чужеродных генов, для получения важных в коммерческом отношении продуктов с помощью технологии рекомбинантных ДНК используют в основном Escherichia colt. Это связано прежде всего с тем, что генетические, моле-кулярно-биологические, биохимические и физиологические свойства этого микроорганизма детально изучены. Кроме того, это наиболее дешевый и быстрый способ получения многих белков. Но для экспрессии некоторых клонированных генов используются и другие организмы-хозяева: В. subtilis, дрожжи, животные, растения и т. д., хотя стратегии, разработанные для Е. coli-систем, в принципе применимы и в этих случаях.
Экспрессия генов при участии сильных регулируемых промоторов
Для эффективной экспрессии любого гена совершенно необходимо наличие сильного регулируемого промотора, расположенного перед данным геном. Такой промотор имеет высокое сродство к PHК-полимеразе, поэтому прилегающие к нему последовательности эффективно (с высокой частотой) транскрибируются. Регулируемость промотора позволяет клетке (и исследователю) осуществлять строгий контроль транскрипции. Для экспрессии клонированных генов широко используется промотор хорошо изученного lac (лактозного)- оперона E, coli. Однако есть и другие промоторы, обладающие полезными для контроля экспрессии свойствами. Для их идентификации перед так называемым геном-репортером, кодирующим легко регистрируемый продукт, но лишенным

106 |
ГЛАВА 6 |
промотора, встраивают случайные фрагменты ДНК (рис. 6.1), Если в результате такой вставки ген-репортер эффективно экспрессируется, то делают вывод, что клонированный фрагмент содержит функциональный промотор. Большинство генов-репортеров кодируют либо продукты, обусловливающие устойчивость к антибиотикам, либо фермент, который идентифицируется с помощью достаточно простого колориметрического теста.
Может показаться, что наиболее подходящим способом оптимизации экспрессии клонированного гена является встраивание его в плазмиду так, чтобы он находился под контролем постоянно функционирующего сильного промотора. Однако непрерывная экспрессия чужеродного гена может оказаться гибельной для клетки-хозяина, поскольку приводит к истощению ее энергетических ресурсов и нарушению метаболизма. Кроме того, плазмиды, несущие постоянно (конститутивно) экспрессирующийся ген, нередко утрачиваются после нескольких клеточных циклов, поскольку не содержащие их клетки растут быстрее и со временем становятся
Рис. 6.1.
Идентификация
сильных
регулируемых промоторов. В плазмиду встраивают ген-репортер без промотора. Хромосомную ДНК. разрезают рестрицируюшей эндонуклеазой
AbcI и встраивают фрагменты в плазмиду. Если генрепортер эффективно экспрессируется, значит, клонированный фрагмент содержит функциональный промотор.
Оптимизация экспрессии генов, клонированных в прокариотических системах |
107 |
в культуре преобладающими. Нестабильность плазмид — это основная проблема, мешающая получению продукта гена, локализованного в плазмиде, в промышленных масштабах. Для ее решения нужно научиться контролировать экспрессию таким образом, чтобы клонированный ген экспрессировался только в определенной фазе клеточного цикла и только в течение определенного времени, а для этого нужно использовать сильные регулируемые промоторы. Плазмиды, сконструированные для этих целей, называются экспрессирующими векторами.
Регулируемые промоторы
Наиболее широко используются следующие сильные регулируемые промоторы: промоторы lac- и trp-оперонов E. соli; специально сконструированный tac-промотор, включающий — 10-область lас-промотора и — 35-область trp-промотора (участки, находящиеся на расстоянии 10 и 35 п. н. до сайта инициации транскрипции); левый, или pL, промотор бактериофага λ; промотор гена 10 бактериофага Т7. С каждым из них связываются соответствующие репрессоры, которые опосредуют включение и выключение транскрипции специфических генов. Кроме того, каждый из этих промоторов узнается холо-ферментом РНК-полимеразой E. coli, в который входит основной сигма-фактор, присутствующий в клетке в значительно больших количествах, чем другие, минорные сигма-факторы. Благодаря этому транскрипция не останавливается по причине недостатка свободных сигмафакторов.
В отсутствие лактозы в среде lас-промотор E. coli находится в репрессированном состоянии, т. е. он выключен белком-репрессором, блокирующим транскрипцию lac- оперона. Индукция, или включение lac-оперона происходит при добавлении в среду лактозы или изопропил-β-D-тиогалактопиранозида (ИПТГ). Оба этих соединения предотвращают связывание репрессора с lac-оператором, и транскрипция возобновляется.
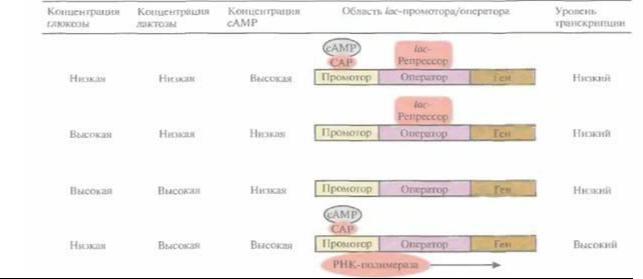
Транскрипция, контролируемая lac-промотором, регулируется также с помощью белка - активатора катаболизма (САР) (рис. 6.2). При связывании САР с промотором повышается сродство последнего к РНК-полимеразе и усиливается транскрипция примыкающих к нему генов. В свою очередь сродство САР к промотору повышается при его связывании с цикличе-
Рис. 6,2. Влияние глюкозы, лактозы и сАМР на транскрипцию, регулируемую lac-промотором E. coli. Стрелка указывает направление транскрипции. (По данным работы Abeles et al., 1992, Biochemistry, p. 383, Jones and Bariett Publishers, Boston, Mass.)
108 |
ГЛАВА 6 |
ским AMP (сАМР), уровень которого повышается при снижении концентрации глюкозы в среде. Таким образом, если репрессор не связан с оператором, то в присутствии индуктора при повышении внутриклеточной концентрации сАМP может произойти усиление транскрипции генов, регулируемых laс-промотором.
На самом деле в плазмидных экспрессируюших векторах используется один из вариантов lac-промотора — lacUV5 с измененной -10-последовательностью, более сильный, чем laс-промотор дикого типа. Транскрипция с промотора tac также подавляется lac- репрессором и возобновляется при добавлении в среду лактозы или ИПТГ.
Промотор trp выключается под действием комплекса триптофан—trp-репрессор, который связывается с trp-оператором и предотвращает транскрипцию trp-оперона. Активация (включение) trp-промотора происходит либо при удалении из среды триптофана, либо при добавлении 3-индолилакриловой кислоты.
Работа промотора рL- регулируется репрессорным белком cl бактериофага λ. На самом деле для регуляции транскрипиии с pL-промотора обычно используется термочувствительная му-тантная форма репрессора cI — белок сI857. Клетки, синтезирующие этот репрессор, сначала выращивают при температуре 28—30 °С; в этих условиях репрессор блокирует транскрипцию с pL-промотора. Когда культура достигает нужной фазы (как правило, середины log-фазы), температуру повышают до 42 °С, при которой сI857-репрессор инактивируется и начинается транскрипция.
Для транскрипции с промотора бактериофага Т7 нужна соответствующая РНКполимераза. Чтобы можно было использовать этот промотор, ген РНК-полимеразы фага Т7 встраивают в хромосому E. coli в составе профага λ, поместив его под контроль lac- промотора. Затем клетки трансформируют плазмидой, содержащей генмишень под контролем Т7-промотора, и добавляют в среду ИПТГ. В этих условиях происходит индукция гена РНК-полимеразы Т7, синтезируется РНК-полимераза и происходят транскрипция и трансляция клонированного гена. Часто между временем индукции гена РНК-полимеразы Т7 и началом транскрипции гена-мишени проходит более часа. Для транскрипции с сильного Т7-промотора создана целая серия плазмид, получивших название рЕТ-векторов.
Эффективность инактивации белка-репрессора и соответственно активации транскрипции зависит от соотношения между числом молекул репрессора и числом копий промотора. Если концентрация репрессора слишком велика, то транскрипция не инициируется, и наоборот, если молекул репрессора очень мало (даже при том, что их больше, чем копий промотора), то транскрипция может идти и в отсутствие индукции. Про такие промоторы говорят, что они «текут». Чтобы осуществлять строгий контроль таких регулируемых систем, разработаны разные стратегии. Например, ген репрессора и соответствующий промотор помещают в две разные плазмиды, присутствующие в клетке в разном числе копий; это позволяет поддерживать нужное соотношение между числом молекул репрессора и числом копий промотора. Обычно ген репрессора находится в малокопийной плаз-миде, число ее копий в клетке не превышает 8, а промотор -- в мультикопийной плазмиде с 30—100 копиями на клетку. Ген репрессора может быть локализован и в хромосомной ДНК, находясь в ней в единственном числе, что позволяет поддерживать низкую концентрацию репрессора. В системах, использующих laс-промо-тор, можно получить lac-репрессор в значительно большем количестве, если заменить lacI-ген его мутантной формой laсIq, что приводит к уменьшению «протекания» промотора, т. е. к снижению уровня транскрипции клонированного гена без индуктора.
Получение больших количеств белковых продуктов
Для получения больших количеств чужеродных белков с помощью рекомбинантных штаммов E. coli была сконструирована плазмида pPLc2833. Она содержит сильный промотор, селективный маркерный ген и короткий участок с несколькими уникальными сайтами для рестрицирующих ферментов (полилинкер), следующий непосредственно за промотором. Эффективность этого экспрессируюшего вектора в осуществлении синтеза чужеродных белков в Е. соli можно еще

Оптимизация экспрессии генов, клонированных в прокариотических системах |
109 |
Таблица 6. I. Зависимость числа копий трех плазмидных экспрессирующих векторов от температуры1)
больше повысить, заменив сайт инициации репликации плазмиды pPLc2833 аналогичным сайтом плазмиды рКМ402. Это приводит к увеличению числа копий модифицированной плазмиды в 5-10 раз при температуре 42 °С (табл. 6.1), Полученная таким образом плазмида рСРЗ содержит pL-промотор и ген ß-лактамазы (ген устойчивости к ампициллину) из pPLc2833, a сайт инициации репликации - из pKN402 (рис. 6.3). Несущие ее клетки сначала выращивают при температуре 28 °С, а затем — при 42 °С. При пониженной температуре ген cI-penpeccopa, интегрированный в ДНК E. соli, экспрессируется, pL-npoмотор не функционирует и образуется обычное число копий плазмиды (табл. 6.1). При повышении температуры cl-penpecop инактивируется, pL- промотор переходит в активное состояние, и число копий плазмиды увеличивается. Все это и делает плазмиду рСР3 эффективным экспрессирующим вектором. Когда ген ДНК-лигазы Т4 был встроен в полилинкер рСР3, то выход его продукта составил примерно 20% от общего количества белка, синтезируемого Е. соli при 42 °С. При этом на долю собственных, наиболее активно синтезируемых белков E, coli, например фактора элонгации EF-Тu, приходится примерно 2%.
Крупномасштабные системы
При культивировании в небольших объемах (от l до 5 л) индукцию экспрессии осуществляют либо изменением температуры, либо добавлени-
Рис. 6.3. Создание плазмиды рСР3. Из плазмиды pKN402 с помощью рестрицирующей эндонуклеазы HaeII вырезают фрагмент с, содержащий температурочувствительный сайт инициации репликации (ori), и сшивают его с НаeII-фрагментами
1 и 3 плазмиды pPLc2833.
Фрагмент 1 содержит pL--промотор и полилинкер (ПЛ), а фрагмент 3 - селективный маркерный ген устойчивости к ампициллину (Ampr).

110 |
ГЛАВА 6 |
ем химического индуктора. Однако в опытных установках (20—100 л) и в промышленных биореакторах (>200 л) температуру нельзя изменить мгновенно, для этого требуется время от 30 до 60 мин; кроме того, на подъем температуры нужна энергия. И время, и энергия стоят дорого. Столь же дорого обходится и применение химического индуктора, например ИПТГ. Все это может сделать процесс неэкономичным. Для преодоления некоторых проблем, связанных с использованием pL-промотора для крупномасштабного производства белковых продуктов, была разработана двухплазмидная система. Ген репрессора cI поместили под контроль trр-про-мотора и включили в малокопийную плазмиду (рис. 6.4), что обеспечило невысокий уровень синтеза репрессора. Вторая плазмида содержала клонированный ген, находящийся под контролем pL-промотора. Как видно из рис. 6.4, А, в отсутствие триптофана включается trр-промотор и синтезируется репрессор cI, выключающий pL-промотор. И наоборот, как видно из рис. 6.4, Б, при наличии триптофана trp-промотор выключается, репрессор не синтезируется, а pL-промотор активно работает.
Культуры с такими двухплазмидными системами можно выращивать на недорогих средах на основе гидролизатов мелассы или казеина, содержащих незначительное количество свободного триптофана, и индуцировать экспрессию клонированного гена добавлением в среду трип-тона. Последний содержит свободный триптофан в количестве, достаточном для эффективной индукции транскрипции. Пробные испытания этой системы показали, что на долю продуктов клонированных генов ß-лактамазы и цитратсин-
Рис. 6.4. Двухплазмидная система, позволяющая контролировать работу pL- промотора фага λ путем регуляции синтеза clpeпрессора с помощью триптофана. Ген репрессора cI вместе с триптофановым промотором (р trp) находятся в одной плазмиде, а pL- промотор и клонированный ген — в другой. Стрелками указано направление транскрипции. А. В отсутствие триптофана в среде ген cI транскрибируется и транслируется, репрессор cI связывается с pL-промотором и блокирует транскрипцию клонированного гена. Б. В присутствии триптофана ген cI репрессируется, его продукт не синтезируется, поэтому клонированный ген транскрибируется и транслируется.
