
Molekulyarnaya_biotekhnologia_Glik_B__Pasternak_Dzh
.pdf
Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
91 |
Рис. 5.13. Остановка синтеза ДНК после присоединения дидезоксинуклеотида к концу растущей цепи. Фоофодиэфирная связь между концевым дидезоксинуклеотидом и следующим нуклеотидом не может образоваться из-за отсутствия 3'-гидроксильной группы.
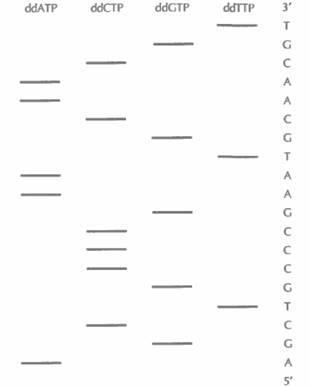
воляет разделить одноцепочечные фрагменты ДНК, даже если они различаются по длине всего на один нуклеотид. На радиоавтографе обнаруживается набор полос, отвечающих меченым фрагментам ДНК, сопоставление которых позволяет прямо «прочитать» нуклеотидную последовательность секвенируемого сегмента ДНК. В примере, приведенном на рис. 5.15, первые шесть нуклеотидов этого сегмента, начиная с 5'-конца, — это AGCTGC. Самая «быстрая» полоса (радиоактивно меченный фрагмент в самом низу геля) соответствует самому короткому фрагменту и находится в дорожке ddATP; следующие полосы располагаются соответственно в дорожках ddGTP, ddCTP, ddTTP и т. д. На большинстве радиоавтографов четко различаются от 250 до 350 полос. Праймерная последовательность находится на фиксированном расстоянии (10—20 нуклеотидов) оттого сайта, по которому встроена клонированная ДНК, что позволяет легко распознать начало клонированного фрагмента.
Секвенирование ДНК с помощью вектора на основе фага M13
Для определения нуклеотидной последовательности клонированных ДНК используются разные подходы. Один из первых основывался на
Рис. 5.14. Удлинение праймера при синтезе цепи в присутствии дидезоксинуклеотидов. В каждой из четырех пробирок образуется уникальный набор олигонуклеотидов разной длины, включающих праймерную последовательность. При этом образуется и какое-то число полноразмерных молекул ДНК. dNTP —
дезоксинуклеозидтрифосфат
92 |
ГЛАВА 5 |
Рис. 5.15. Схематическое изображение радиоавтографа, получающегося при секвенировании ДНК с помощью дидезокси-метода. В каждую из лунок вносили содержимое одной из четырех пробирок, в которых находился один из дидезоксинуклеотидов: ddATP, ddCTP, ddGTP или ddTTP. Нуклеотидная последовательность считывается с радиоавтографа снизу вверх. На рисунке она приведена справа.
применении фага M13 E. coli в качестве вектора. ДНК этого фага представляет собой одноцепочечную кольцевую молекулу. Когда им инфицируют E. coli, сначала образуется двухцепочечная репликативная форма фаговой ДНК, а одноцепочечные кольцевые молекулы, которые затем упаковываются в вирионы, синтезируются на этой двухцепочечной молекуле как на матрице. Клетки, инфицированные М13, не подвергаются лизису; в них непрерывно образуются новые одноцепочечные молекулы ДНК М13, которые, проходя через клеточную мембрану, одеваются белковой оболочкой и выходят в окружающую среду. ДНК М13 содержит несущественную часть, которую можно заменить нужным фрагментом ДНК; при этом инфекционность рекомбинантных вирусных частиц сохранится. МП-система имеет следующие преимущества: выделенная двухцепочечная репликативная форма может функционировать как плазмида, а одноцепочечная фаговая ДНК — использоваться в качестве матрицы для секвенирования ДНК.
Все это позволяет использовать фаг M13 как комбинированную систему для клонирования и секвенирования ДНК. Обычно нужный фрагмент ДНК длиной примерно 500 п. н. встраивают в полилинкер, который является частью клонированного в РФ-ДНК фага М13 модифицированного гена IacZ', Рекомбинантной вирусной ДНК трансформируют компетентные клетки Е. coli и высевают их на чашки со средой, содержащей субстрат X-Gal. При его гидролизе ß-галактозидазой образуется продукт, имеющий синюю окраску. На чашках появляются белые (бесцветные) и синие колонии. Первые отвечают клеткам, инфицированным фагом М13 со вставкой, нарушившей рамку считывания гена IacZ', вторые
— клеткам, инфицированным фагом М13 с функциональным геном IacZ', не несущим вставки. Из белых колоний выделяют фаговые частицы, а из них — одноцепочечную ДНК со вставкой (рис. 5.16), Для секвенирования последней отжигают выделенную ДНК с праймером, который гибридизуется с последовательностью вблизи вставки, затем проводят дидезокси-секвенирование, электрофорез и радиоавтографию и «прочитывают» нуклеотидную последовательность вставки.
Для секвенирования крупных фрагментов ДНК (примерно 2000 п. н.) используют другие стратегии. Одна из них состоит в следующем. Встраивают этот фрагмент в соответствующий плазмидный вектор и строят его подробную рестрикционную карту. Идентифицируют перекрывающиеся фрагменты вставки длиной от 100 до 500 п. н., субклонируют каждый из них в ДНК М13, секвенируют и воссоздают нуклеотидную последовательность всего исходного фрагмента. Чтобы быть уверенным в правильности полученного результата и идентификации какого-либо нуклеотида, необходимо секвенировать обе цепи по нескольку раз. Секвенирование обеих цепей облегчается тем, что каждый из субклонированных фрагментов исходной ДНК может быть встроен в ДНК М13 в противоположных

Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
93 |
Рис. 5.16. Использование бактериофага М13 для клонирования и секвенирования. А. Встраивание фрагмента ДН К в двухцепочечную репликативную форму ДНК М13. Б. Секвенирование комплементарных цепей клонированного фрагмента ДНК с помошью одного и того же лраймера (Р1). Стрелками показана ориентация вставки в векторе.
ориентациях. В результате в одном случае праймер будет инициировать синтез первой цепи, а в другом — второй.
Праймер-опосредованная прогулка («Блуждающая затравка»)
Для секвенирования очень длинных фрагментов ДНК (>5000 п. н.) описанный выше подход уже не может быть использован, поскольку число КПЗ-векторов, содержащих перекрывающиеся субклонированные последовательности, значительно увеличивается. Чтобы решить эту задачу, были разработаны методы секвенирования двухце почечных плазмидных ДНК, не требующие субклонирования. Плазмидную ДНК, содержащую нужную вставку, выделяют и отжигают с синтетическим олигонуклеотидным праймером, который гибридизуется с последовательностью в одной из цепей векторной ДНК, находящейся вблизи вставки. Затем осуществляют дидезоксисеквенирование, позволяющее идентифицировать первые 250—350 нуклеотидов вставки. Исходя из этих данных синтезируют второй олигонуклеотидный праймер, комплементарный сегменту вставки, отстоящему примерно на 300 нуклеотидов от места связывания первого праймера, и секвенируют следующие 250—350 нуклеотидов. Аналогичным образом синтезируют третий праймер и определяют нуклеотидную последовательность следующих 250—350 нуклеотидов (рис. 5.17). Эту процедуру, называемую праймер-опосредованной прогулкой, продолжают до тех пор, пока не секвенируют весь фрагмент. Аналогичным образом секвенируют вторую цепь, начиная с праймера, который гибридизуется с этой цепью вблизи вставки.
К сожалению, в результате ошибочного спаривания праймера заданной длины с более чем одним участком внутри вставки могут быть получены неоднозначные результаты. Чтобы избежать этого, используют праймеры длиной не менее 24 нуклеотидов и стараются строго соблюдать условия отжига. Именно таким образом были секвенированы фрагменты ДНК, клонированные в бактериофаге λ (~20 т. п. н.) или в космидном векторе (~40 т. п. н.).
Некоторые этапы этого процесса недавно были автоматизированы. Это позволило проводить рутинное секвенирование фрагментов длиной несколько десятков тясяч пар нуклеотидов. Во многих случаях праймеры, добавляемые в реакционную смесь в разных пробирках, метят различными флуоресцентными красителями с разной длиной волны флуоресценции. Затем содержимое всех четырех пробирок соединяют и проводят электрофорез на одной дорожке. Дорожку сканируют в луче лазера и регистрируют

94 |
ГЛАВА 5 |
Рис. 5.17. Секвенирование ДНК методом праймер-опосредованной прогулки. 1. Инициация синтеза цепи ДНК с помощью праймера (Р1), комплементарного участку плазмиды, находящемуся вблизи вставки. 2. Секвенирование фрагмента клонированной ДНК длиной 250-350 нуклеотидов. 3. Подбор второго праймера, комплементарного концевому участку уже секвенированной последовательности длиной примерно 20 нуклеотидов. 4. Секвенирование следующего сегмента клонированной ДНК с помощью второго праймера (Р2). 5. Подбор третьего праймера, комплементарного концевому участку этого сегмента размером 20 нуклеотидов. 6. Третий праймер (РЗ) используется для секвенирования следующего сегмента клонированной ДНК. Эту процедуру продолжают до тех пор, пока не будет секвенирована вся вставка.
положение каждой флуоресцирующей полосы. Все данные вводят в компьютер, который сопоставляет их и выводит на дисплей нуклеотидную последовательность,
Полимеразная цепная реакция
Полимеразная цепная реакция (ПЦР) — это эффективный способ получения in vitro большого числа копий специфических нуклеотидных последовательностей. Их амплификация — иногда в миллионы раз — осуществляется в ходе трехэтапного циклического процесса. Для ПЦР необходимы: I) два синтетических олигонуклеотидных праймера (длиной примерно по 20 нуклеотидов), комплементарные участкам ДНК из противоположных цепей, фланкирующим последовательность-мишень; их 3'-гидроксильные концы после отжига с ДНК. должны быть ориентированы навстречу друг другу; 2) ДНКмишень длиной от 100 до - 35 000 п. н.; 3) термостабильная ДНК-полимераза, которая не теряет своей активности при температуре 95° и выше; 4) четыре дезоксирибонуклеотида.
Типичная ПЦР-амплификация состоит в многократном повторении следующих трех реакций.
1.Денатурация. Первый этап ПЦР состоит в тепловой денатурации образца ДНК выдерживанием его при температуре 95 °С в течение по крайней мере ) мин. Помимо ДНК, в реакционной смеси содержатся в избытке два праймера, термостабильная ДНКполимераза Taq, выделенная из бактерий Thermus aquaticus, и четыре дезоксирибонуклеотида.
2.Ренатурация. Температуру смеси медленно понижают до ~55 °С, при этом праймеры спариваются с комплементарными последовательностями ДНК.
3.Синтез. Температуру повышают до ~75 °С - величины, оптимальной для ДНКполимеразы Taq. Начинается синтез комплементарной цепи ДНК, инициируемый 3'- гидроксильной группой праймера (рис. 5.18),
Все реакции проводят в пробирках, погруженных в термостат. Смена температурного режима и его поддержание осуществляются автоматически. Каждый цикл обычно длится
3—5 мин.
Чтобы понять, как именно происходит амплификация определенного сегмента ДНК в ходе ПЦР, нужно четко представлять положение всех праймеров и комплементарных им последователь-

Химический синтез, определение нуклеотидной последовательности и амплификация ДНК
95
Рис. 5.18. Первый раунд ПЦР. ДНК-мишень фланкирована последовательностями 1'—2 в одной цепи и последовательностями 1—2' — в другой. К образцу ДНК добавляют праймеры (Р1 и Р2), ДНК-полимеразу Tag и четыре дезоксирибонуклеозидтри фосфата (dNTP). Смесь нагревают до 95 °С, инкубируют в течение 1 мин и медленно охлаждают до 55 °С. При этой температуре праймеры, добавленные в избытке, спариваются с разделенными цепями. Повышают температуру до 75 °С. В этих условиях происходит синтез обеих цепей ДНК, начинающийся с 3'-гидроксильных концов праймеров. Каждая из синтезированных цепей имеет гораздо большую длину, чем расстояние от 3'-гидроксильной группы «ее» праймера до концевого нуклеотида последовательности, комплементарной второму праймеру. Эти цепи служат матрицами во втором раунде ПЦР.
ностей в амплифицируемых цепях в каждом раунде. В первом раунде каждая из новосинтезированных цепей имеет гораздо большую длину, чем расстояние от 3'-гидроксильной группы «ее» праймера до концевого нуклеотида последовательности, комплементарной второму праймеру. Такие цепи называют «длинными матрицами», именно на них будет идти дальнейший синтез (рис. 5.18).

96 |
ГЛАВА 5 |
Рис. 5.19. Второй раунд ПЦР. Исходным материалом в этом случае является смесь молекул ДНК, образовавшихся в первом раунде (рис. 5.18). При отжиге праймеры гибридизуются с комплементарными им участками как исходных цепей, так и «длинных матриц», синтезированных в первом раунде. В результате ферментативного синтеза in vitro на исходных цепях синтезируются «длинные матрицы», а на «длинных матрицах» — «короткие». Последние начинаются с одного праймера, а заканчиваются последовательностью, комплементарной второму праймеру.
Во втором раунде двухцепочечную ДНК, состоящую из исходной и новосинтезированной («длинная матрица») цепей, опять подвергают денатурации, а затем отжигают с праймерами. Во время синтеза в этом раунде вновь синтезируются «длинные матрицы», а также некоторое количество цепей с праймером на одном конце и с последовательностью, комплементарной второму праймеру, на другом («короткие матрицы») (рис. 5.19). Во время третьего раунда все гетеродуплексы, образовавшиеся ранее, одновременно подвергаются денатурации и отжигу с праймерами, а затем реплицируются (рис. 5.20). В последующих раундах «коротких матриц» становится все больше, и к 30-му раунду их число уже в 106 раз превышает число исходных цепей или «длинных» матриц
(рис. 5.21).
Метод ПЦР получил широкое распространение. Разнообразные случаи его применения мы рассмотрим в последующих главах. Здесь упомянем лишь некоторые из них. Один из важнейших - идентификация патогенных микроорганизмов, возбудителей заболеваний человека, животных и растений. С появлением ПЦР отпала необходимость в выделении и очистке ДНК-мишени; для анализа можно использовать очень небольшое количество неочищенного материала. Для синтеза праймеров, специфичных в отношении исключительно ДНК-мишени, нужно знать нуклеотидную последовательность ДНК предполагаемого патогенного микроорганизма. В этом случае в ходе ПЦР будет амплифицироваться только фрагмент ДНК, длина которого равна суммарной длине двух праймеров и фрагмента ДНК между ними.
ПЦР — высокочувствительный метод, поэтому при наличии в исследуемом образце даже ничтожного количества ДНК, случайно попавшей

Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
97 |
Рис. 5.20. Третий раунд ПЦР. При отжиге праймеры гибридизуются с комплементарными участками исходных цепей, а также «длинных» и «коротких» матриц. При ферментативном синтезе in vitro на исходных цепях синтезируются «длинные» матрицы», а на «длинных» и «коротких» матрицах — только «короткие матрицы».
Рис. 5.21. Тридцатый раунд ПЦР. На этом этапе в реакционной смеси содержатся практически одни «короткие матрицы».
из одной реакционной смеси в другую, могут быть получены ложноположительные результаты. Это заставляет тщательно контролировать все используемые для ПЦР растворы и посуду. Метод ПЦР применяется также для выявления спонтанных мутаций, внесения специфических мутаций in vitro, сборки полноразмерных генов из синтетических олигонуклеотидов, секвенирования ДНК. Во многих случаях возникает необходимость в клонировании ПЦР-продукта. Однако прямое клонирование с помощью лигирования по тупым концам затруднено, по-

98 |
ГЛАВА 5 |
скольку полимераза Tag присоединяет к 3'-концу синтезируемой цепи лишний адениннуклеотид, что снижает эффективность лигирования. Но если вектор для клонирования обработать рестрицирующей нуклеазой с образованием новых тупых концов и затем проинкубировать с полимеразой Taq в присутствии dТТР, то к обоим 3'-концам фрагментов добавится по одному тимидиннуклеотиду. Взаимной комплементарности концевых участков вектора и ПЦР-продукта протяженностью в один-единственный нуклеотид оказывается достаточно для спаривания молекул и их последующего лигирования.
Получение с помощью ПЦР кДНК, отвечающих концам молекул мРНК
С помощью ПЦР можно получать комплементарные ДНК (кДНК), отвечающие 3'- или 5'-концевым участкам специфических информационных РНК (мРНК). Для обозначения этого метода используется сокращение RACE — от англ, rapid amplification of с DNA ends (быстрая
Рис. 5.22. ПЦР-
амплификация кДНК,
комплементарной 3 '-
концевой |
|
части |
|
мРНК. |
Первая |
цепь |
|
кДНК |
образуется |
в |
|
результате |
обратной |
||
транскрипции мРНК при
участии |
oligo(dT) в |
качестве |
праймера |
Вторая |
цепь |
синтезируется на первой цепи как на матрице с
помощью |
полимеразы |
|
Tag |
и |
ген |
специфичного |
|
|
праймера (GSP1). В |
||
последующих |
раундах |
|
ПЦР |
используются |
|
праймеры GSP2 и P.
Химический синтез, определение нуклеотидной последовательности и амплификация ДНК |
99 |
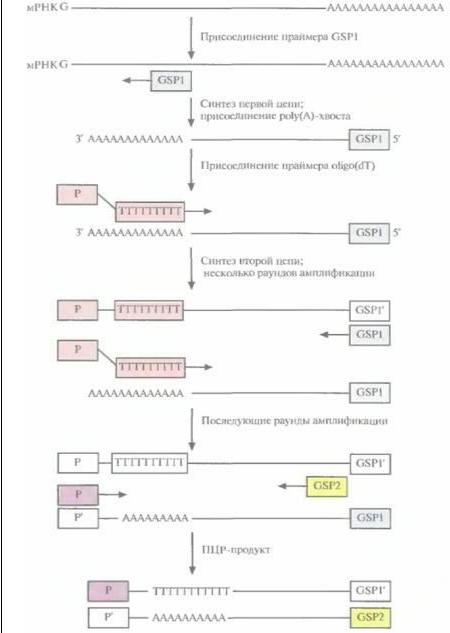
амплификация концов кДНК). Обозначения 3' RACE и 5' RACE относятся к амплификации кДНК, отвечающих соответствующим концам мРНК. В обоих случаях для проведения ПЦР-амплификации нужно знать нуклеотидную последовательность кодирующей области мРНК-мишени, чтобы синтезировать генспецифичный праймер (GSP). В случае 3' RACE праймером для синтеза первой цепи кДН К служит oligo(dT) с присоединенным к нему вторым праймером (Р) (рис. 5.22). Oligo(dT) спаривается с poly(A)- хвостом мРНК, и обратная транскриптаза синтезирует цепь, комплементарную мРНК. Вторая цепь кДНК синтезируется на первой при участии GSP, комплементарного кодирующей области данной мРНК, с помощью полимеразы
Рис. 5.23. ПЦРамплификация кДНК, комплементарной 5'-концевой части мРНК первой цепи, осуществляемая обратной транскриптазой, инициируется праймером GSP. Затем к этой цепи с помощью концевой дезоксинуклеотидилтрансферазы присоединяется ро1у(А)-хвост. Для синтеза второй цепи в качестве праймера используется oligo(dT). Проводят несколько раундов амплификации при участии указанных праймеров, добавляют вторые праймеры (GSP2 и Р) и получают кДНК, отвечающую 5'-концу мРНК.

100 |
ГЛАВА 5 |
Рис. 5.24. Синтез генов с помощью ПЦР. Перекрывающиеся олигонуклеотиды (А и В) отжигают и достраивают образовавшийся дуплекс с заглубленными 3'-гидроксильными концами. Двухцепочечные молекулы денатурируют, добавляют в реакционную смесь вторую пару олигонуклеотидов (С и D), перекрывающихся с продуктами первого раунда ПЦР, и отжигают. Осуществляют второй раунд ПЦР, добавляют следующую пару олигонуклеотидов (Е и F), осуществляют третий раунд ПЦР и т. д. В результате образуется двухцепочечная ДНК. идентичная искомому гену. Одинаковыми буквами со штрихом или без (А' и А, В и В' и т. д.) обозначены комплементарные участки ДНК. Нуклеотидная последовательность каждого олигонуклеотида соответствует таковой определенных сегментов ДНК.
