
Нормальная физиология / КР5 по сердцу
.pdf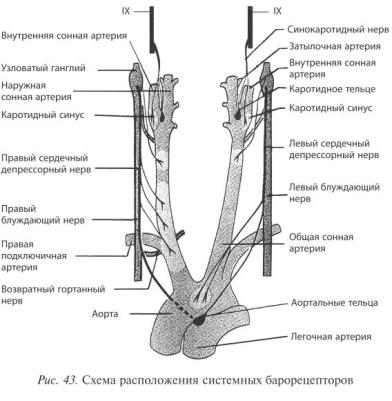
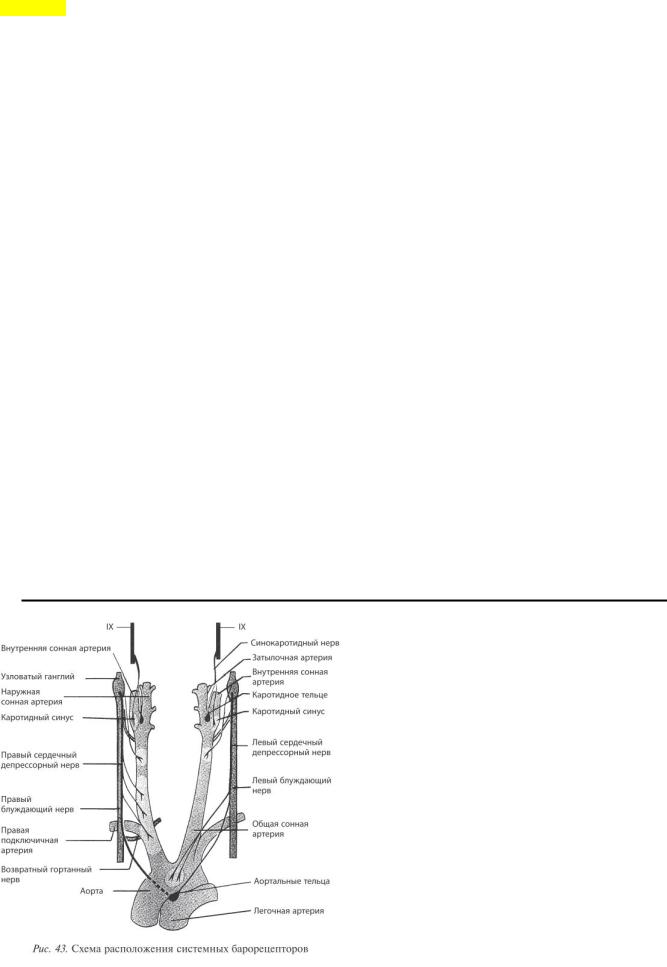
реагирующие на деформацию сосудистой стенки при изменениях кровяного давления. Морфологически они относятся к типу неинкапсулированных механорецепторов. В составе обеих рецепторных зон представлены разнообразные типы нервных окончаний; пока не удалось идентифицировать клеточные элементы, непосредственно отвечающие за первичное восприятие растягивающего стимула. Афферентная импульсация с барорецепторов передается на миелиновые волокна типа А и безмиелиновые типа С. Афферентные волокна от рецепторов дуги аорты идут в составе аортального нерва («депрессорный» нерв, или нерв Людвига— Циона), который является чувствительной ветвью блуждающего нерва.
Чувствительные волокна от рецепторов синокаротидной зоны идут в составе каротидного нерва (нерв Геринга) и далее — языкоглоточного нерва (IX пара черепных нервов).
Пороговое значение абсолютной величины внутрисосудистого (систолического) давления, необходимого для получения устойчивой импульсации по волокнам типа А, составляет около 60–120 мм рт. ст., а в волокнах типа С — 120–150 мм рт. ст. Уровень насыщения, достигаемый при повышении давления, для обеих групп барорецепторов не превышает 200 мм рт. ст., после чего они перестают реагировать на дальнейшее повышение давления. Абсолютный порог чувствительности рецепторов дуги аорты составляет 90–120 мм рт. ст., то есть выше, чем у рецепторов каротидного синуса, где он равен примерно 60–80 мм рт. ст. Область же максимальной импульсной активности составляет со ответственно 150–180
и 120–150 мм рт. ст.
Сосудистые барорецепторы реагируют на изменение не только средней величины артериального давления, но и частоты, а также амплитуды его пульсовых колебаний. Каждая пульсовая волна вызывает импульсное растяжение сосудистой стенки, которое возбуждает рецепторы. При нормальном среднем артериальном давлении импульсная активность в синусовом нерве носит фазный характер, усиливаясь при каждой систоле и уменьшаясь или исчезая после дикротического подъема на пульсовой кривой. При повышении АД частота разрядов каждого волокна увеличивается, а при понижении уменьшается. Импульсная активность в аортальных нервах аналогична таковой в синусных нервах. Вспышки импульсной активности в аортальных нервах возникают несколько раньше, чем в синусных, что определяется скоростью распространения пульсовой волны по магистральным артериям.Афферентные пути от барорецепторов сердечно-сосудистой системы заканчиваются в продолговатом мозге в области ядра одиночного пути (nucleus tractus solitarius).
Таким образом, подавляющее большинство рефлекторных изменений артериального давления осуществляется с обязательным вовлечением ствола головного мозга.
•Спинальные механизмы регуляции давления реализуются в основном в условиях патологии.
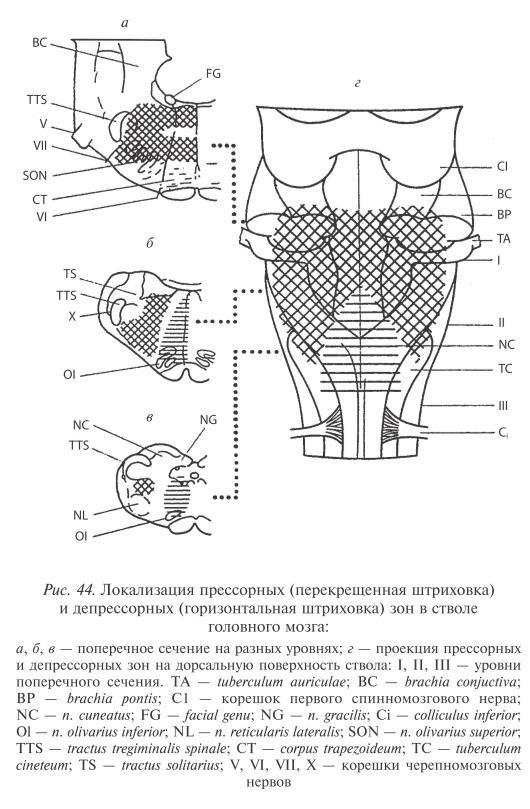
•Совокупность структур ретикулярной формации каудальной части ствола головного мозга, при участии которых происходит замыкание рефлексов сердечно-сосудистой системы, традиционно обозначается как бульбарный (медуллярный) кардиоваскулярный центр (рис. 44 хз вряд ли нужен). Важно подчеркнуть, что данное понятие является сугубо функциональным, поскольку не ассоциируется с каким-либо компактным анатомическим образованием. Уже говорилось, что этот центр содержит нейроны в составе полисенсорных и полимодальных ядер ретикулярной формации (ядро одиночного пути, парамедианное ядро шва, дорзальное ядро вагуса) и одиночные нейроны, диффузно расположенные на вентральной поверхности продолговатого мозга.
•Сердечный компонент нейрогенной регуляции обеспечивается тормозными (депрессорными) влияниями, которые реализуются парасимпатической системой через преганглионарные нейроны и их аксоны в составе блуждающего нерва, а также нисходящими возбуждающими влияниями на спинальные преганглионарные симпатические нейроны, участвующие в иннервации сердца.
oСосудистый компонент формирования артериального давления реализуется через внутриорганный нервный аппарат артериальных сосудов, в составе которого преобладают аксоны и терминали адренергических симпатических нейронов.
oДругой компонент симпатоадреналового механизма регуляции артериального давления обеспечивается рефлекторными влияниями на секрецию адреналина и норадреналина клетками мозгового вещества надпочечников в плазму крови. Эта секреция находится под контролем преганглионарных симпатических волокон, благодаря чему в плазме крови в любой момент времени имеется
физиологически значимая концентрация катехоламинов.
o |
В случае повышения величины кровяного давления в аорте или в каротидном синусе рефлекторно |
|
усиливаются тонические тормозные влияния блуждающих нервов на сердце. |
o |
При этом отмечено и некоторое торможение тонической активности симпатических сердечных |
|
нервов, но по сравнению с усилением парасимпатических тормозных влияний на сердце его роль менее |
|
значима. |
oВ результате уменьшаются частота сердечных сокращений, сократимость миокарда и сердечный выброс, что приводит к снижению артериального давления. Уменьшение давления в аорте и каротидном синусе вызывает, напротив, уменьшение импульсной активности в аортальном и синусовом нервах,

что приводит к рефлекторной активации бульбарных центров регуляции системы кровообращения и усилению тонических симпатических влияний на сердце, а также сосуды. В результате возрастают частота сердечных сокращений, сократимость миокарда, сердечный выброс и артериальное давление. Указанные сдвиги деятельности сердца могут проявляться в ответ на пережатие сонных артерий у животных в эксперименте (синокаротидный прессорный рефлекс) (рис. 45).
oБарорецепторные зоны, участвующие в регуляции сердечной деятельности, имеются и в других отделах сосудистой системы. Например, в легочных и почечных артериях обнаружены рецепторы, функции и электрофизиологические характеристики которых близки к барорецепторам, расположенным в дуге аорты. oПоэтому в случае повышения давления в легочной артерии также рефлекторно замедляется ритм сердца и снижается сердечный выброс, что способствует уменьшению давления в легочной артерии.
oв сосудистой системе есть хеморецепторные зоны, которые находятся в каротидных тельцах, расположенных дистальнее бифуркации сонных артерий, и в аортальном
тельце, расположенном в области дуги аорты. Обе рефлексогенные зоны реагируют на изменение напряжения кислорода в артериальной крови и участвуют таким образом в регуляции дыхания.
oВозбуждение рефлексогенных зон при снижении парциального давления кислорода в артериальной крови вызывает повышение частоты сердечных сокращений, а также констрикцию периферических
сосудов.
oЭтот механизм отличается исключительно высокой чувствительностью. Так, например, у человека увеличение частоты сердечных сокращений отмечено уже при снижении напряжения кислорода в артериальной крови всего на 3 %.
oХеморецепторы каротидных и аортальных телец являются особенно значимыми в рефлекторной регуляции деятельности сердца в условиях острой гипоксической гипоксии (высокогорье, задержка дыхания при нырянии).
oПараллельно с симпатоадреналовой системой в регуляции артериального давления принимает участие еще один механизм — ренин-ангиотензиновая система. Запуск этой системы осуществляется посредством секреции почками протеолитического фермента ренина. Синтез ренина увеличивается посредством местного рефлекса при снижении артериального давления. Под действием ренина от α- глобулина плазмы ангиотензиногена отщепляется биологически инертный декапептид ангиотензин I. В капиллярах легких под действием ангиотензин-превращающего фермента (АПФ) от ангиотензина I отщепляются еще две аминокислоты. В результате образуется октапептид ангиотензин II. Последний обладает двойным физиологическим действием: он является сильным вазоконстриктором и стимулирует секрецию корой надпочечников альдостерона, тем самым уменьшая диурез и увеличивая объем циркулирующей крови. Последующее спонтанное отщепление от молекулы ангиотензина II еще одной аминокислоты приводит к образованию ангиотензина III, обладающего сосудосуживающим действием. В отличие от катехоловых аминов, ангиотензин II и ангиотензин III действуют прежде всего на артериальные сосуды, лишь незначительно влияя на сердечную деятельность и почти не изменяя тонус вен.
oАнгиотензин применяется для лечения артериальной гипотензии, а ингибиторы АПФ и блокаторы ангиотензиновых рецепторов относятся к числу самых распространенных гипотензивных препаратов. Поскольку эти фармакологические агенты оказывают выраженное сосудорасширяющее действие и в отсутствие гипертензии, ренин-ангиотензиновую систему следует считать еще одним механизмом непрерывного контроля артериального давления (рис. 46).
• Кардио-кардиальные. В стенках сердечных камер и в эпикарде расположено большое количество различных по модальности рецепторов. Однако наибольшее значение для рефлекторной регуляции деятельности сердца имеют механорецепторы, расположенные в предсердиях в месте впадения в них полых и легочных вен, а также в левом желудочке. Такие рецепторы в физиологической литературе называются также волюморецепторами. Исследованиями установлено, что А-рецепторы реагируют на изменение напряжения стенок предсердий, а В-рецепторы возбуждаются при их пассивном растяжении при увеличении венозного притока крови к сердцу. Как правило, в ответ на растяжение предсердий рефлекторно усиливаются тормозные влияния блуждающих нервов на сердце, что приводит к снижению частоты сердечных сокращений, сократимости миокарда и сердечного выброса.
Данный рефлекс представляет наглядный пример отрицательной обратной связи в нейрогенной регуляции деятельности сердца. Так, увеличение объема циркулирующей крови, приводя к повышению венозного возврата, вызывает повышение давления в правом предсердии. В результате растяжения предсердий рефлекторно уменьшается частота сердечных сокращений, сократимость миокарда, что приводит к снижению сердечного выброса и венозного притока.
Рефлекс: в ответ на увеличение давления в правом предсердии при исходно низкой частоте сокращений сердца у собак происходило увеличение частоты сердечных сокращений.
Направленность сдвигов частоты сердечных сокращений в ответ на растяжение предсердий зависит от исходной частоты ритма сердца, который косвенно зависит от тонической активности блуждающих нервов.
При низкой исходной частоте сердеч ных сокращений (60–80 уд/мин) в ответ на увеличение давления в правом предсердии развивается рефлекторная тахикардия, тогда как при высокой исходной частоте ритма сердца (120–180 уд/мин) при увеличении давления в правом предсердии имеет место замедление частоты сердечных сокращений, то есть брадикардия.
В клинической кардиологии считается, что при сердечной недостаточности, когда на фоне снижения сократимости миокарда давление в правом предсердии повышается, рефлекс Бейнбриджа, вызывая тахикардию, спо собствует увеличению сердечного выброса. Однако в условиях тахикардии сердце работает неэффективно, так как продолжительность диастолы уменьшается, что ухудшает кровенаполнение сердца и коронарный кровоток. В результате сократимость миокарда еще более снижается и недостаточность насосной функции сердца прогрессирует.
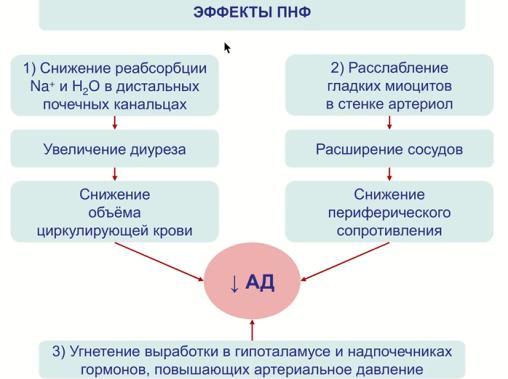
При возбуждении волюморецепторов предсердий происходит увеличение диуреза и уменьшение объема циркулирующей крови. Рефлекс — кардиоренальный рефлекс Генри-Гауэра. Увеличение диуреза в ответ на растяжение предсердий является следствием усиления выработки кардиомиоцитами предсердий натрий уретического пептида.
|
• Кардио-васкулярные. NB: разнонаправленность реакций венозных |
сосудов, возникающих в |
ответ на |
|
|
раздражение рецепторов предсердий. Эти данные свидетельствуют о неспе цифичности направленности |
|||
|
кардиоваскулярных рефлексов. В 1983 г. английский физиолог С. Роте высказал предположение о |
|||
|
наличии сопряженного влияния симпатических нервов на сердце и венозные сосуды, обеспечивающего |
|||
|
при «мобилизации» резервного объема крови из вен увеличение сократимости миокарда. Однако |
|||
|
остаются невыясненными афферентные пути этих рефлексов. |
Вероятно, в этом случае невозможно |
||
|
выделить единственный афферентный путь. |
|
|
|
2) |
СОПРЯЖЕННЫЕ |
РЕФЛЕКСЫ, ОБУСЛОВЛЕННЫЕ АКТИВНОСТЬЮ ЛЮБЫХ |
ДРУГИХ |
|
РЕФЛЕКСОГЕННЫХ ЗОН
реакции сердца в ответ на раздражение рефлексогенных зон, расположенных вне системы кровообращения.
• Рефлекс Гольца проявляется в форме брадикардии или даже полной остановки сердца в ответ на раздражение механорецепторов брюшины. Возможность возникновения этого рефлекса учитывают при проведении оперативных вмешательств в брюшной полости, когда во избежание рефлекторной остановки сердца в область брыжейки вводят новокаин или применяют блокатор М-холинорецепторов — атропин, который устраняет парасимпатические влияния на сердце.
•Рефлекс Тома—Ру – брадикардия вплоть до остановки сердца при сильном давлении или ударе в эпигастральную область может явиться в боксе и других единоборствах причиной преходящей недостаточности мозгового кровообращения с потерей сознания. Кроме того, рефлекторная остановка сердца может наблюдаться при резком охлаждении кожи области живота. Именно такую природу нередко имеют несчастные случаи при нырянии в холодную воду.
•Рефлекс Данини—Ашнера проявляется в форме брадикардии при надавливании на глазные яблоки. Он является примером сопряженного соматовисцерального кардиального рефлекса. Данный рефлекс раньше использовался в неотложной медицине в комплексе мер для купирования приступов пароксизмальной тахикардии.
Ротовая полость также является важной рефлексогенной зоной. При охлаждении ротовой полости в ответ на раздражение чувствительных окончаний тройничного нерва у человека может быть рефлекторное снижение частоты сокращений сердца и расширение коронарных артерий. Например, препарат валидол, содержащий масло мяты, помещают под язык при приступе стенокардии. В результате раздражения рецепторов ротовой полости приступ стенокардии купируется.
К числу сопряженных кардиальных рефлексов относятся также все условные рефлексы, влияющие на деятельность сердца. Примером является так называемая предстартовая лихорадка — состояние, которое наблюдается у спортсменов перед началом соревнований («Предстартовая лихорадка» (ПЛ) – это состояние эмоционального возбуждения, которое часто возникает задолго до выступления. Это избыточное волнение, при котором человек нервничает, суетится.). Оно представляет собой следствие активации симпатоадреналовой системы, которая возникает в ответ на комплекс условных раздражителей, сопутствующих проведению спортивных мероприятий. Характерным примером условнорефлекторных изменений частоты сердечных сокращений у человека является «синдром белого халата», когда при посещении врача возрастает частота сердечных сокращений сердца и повышается артериальное давление. Формирование такого условного рефлекса происходит еще при первом посещении врача ребенком. Если, например, врач выполняет инъекцию препарата, которая сопровождается болью, стрессорной реакцией, приводящей к тахикардии, то возникает условный рефлекс: врач — условный раздражитель, болевой стимул — безусловный. В дальнейшем только посещение врача вызывает у человека услов-норефлекторное повышение частоты сердечных сокращений.
3) НЕСПЕЦИФИЧЕСКИЕ ЭФФЕКТЫ РАЗДРАЖЕНИЯ, КОТОРЫЕ ВОСПРОИЗВОДЯТСЯ В УСЛОВИЯХ ФИЗИОЛОГИЧЕСКОГО ЭКСПЕРИМЕНТА, А ТАКЖЕ ПРИ ПАТОЛОГИИ.
Наиболее изученным среди них является так называемый рефлекс Бецольда—Яриша, который развивается в ответ на внутрикоронарное введение этилового спирта, никотина и некоторых других веществ. В подобных условиях отмечена так называемая триада Бецольда—Яриша: брадикардия, снижение артериального давления (гипотензия) и остановка дыхания (апноэ). Данное обстоятельство целесообразно учитывать в клинике при назначении внутрисосудистых введений фармакологических агентов. При спазме или тромбозе коронарных артерий, приводящих к инфаркту миокарда, кардиомиоцитами выделяются биологически активные вещества, и в результате могут развиваться снижение частоты сердечных сокращений, сердечного выброса и артериального давления, а также остановка дыхания. Следовательно, рефлекс Бецольда—Яриша может приводить к патологическим сдвигам системного кровообращения и дыхания при нарушении коронарного кро во тока. Синдром «внезапной остановки сердца» при инфарк те миокарда может быть обусловлен этим патологическим рефлексом.

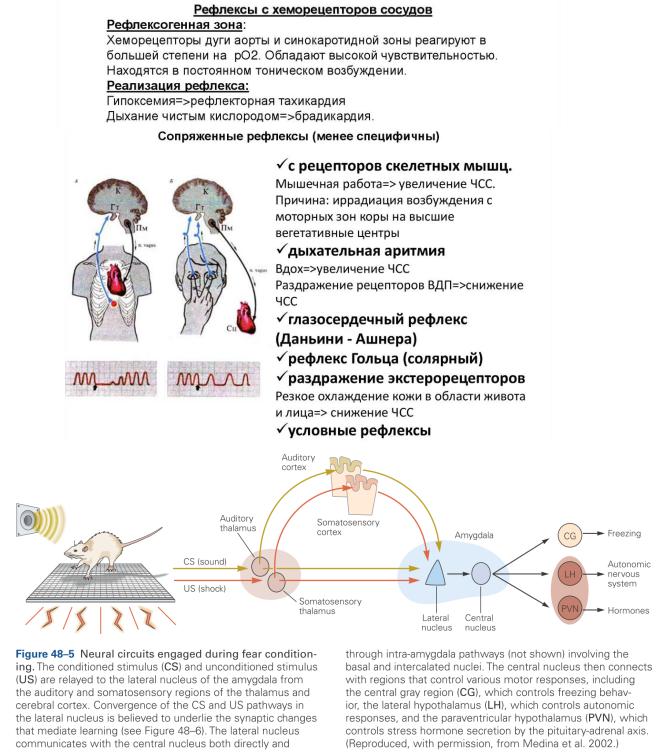
Эмоциональная окраска раздражителя оценивается миндалевидным телом, чтобы определить, существует ли опасность в настоящем. Если миндалевидное тело обнаруживает опасность, оно предупреждает: отражает выражение поведенческих и физиологических ответов через связи с гипоталамусом и стволом мозга. Например, замиранеие опосредуется связями из центрального ядра к вентральной периакведуктальной серой области. Кроме того, миндалевидное тело имеет множество соединений, которые позволяют ему также влиять на другие когнитивные функции. Например, через его широко распространенные проекции на корковые области он может модулировать внимание, восприятие, память и процесс принятия решений. Его связи с модуляторными дофаминергическими, норадренергическими, серотонинергическими и холинергическими ядра, которые также проецируются на корковые области, влияют на когнитивные процессы.
Клеточные и молекулярные механизмы, лежащее в основе «усвоенного» страха, особенно в латеральном ядре, обусловливают функцию ядра как места хранения памяти об условных рефлексах, обеспечивющих страх
Пациенты с повреждением миндалевидного тела не справляются со страхом, когда им предъявляют нейтральный CS (условный стимул) в сочетании с US (безусловный стимул - поражение электрическим током или громкий шум).
Пациенты с повреждением миндалины также не могут распознать выражения страха на лице и не вызывают вегетативные реакции страха на них.

Унормальных людей активность миндалины увеличивается во время спаривания CS-US (рис. 48–7). Эта активность особенно сильна, когда стимулы предъявляются подсознательно.
Унормальных людей испуганные выражения лица также активируют миндалину, даже если они представлены подсознательно. Эти данные подчеркивают важность миндалевидного тела как подсознательного оценщика значения стимула.
Некоторые формы обработки страха уникальны для людей. Например,
просто сказать человеку, что за CS может последовать шок, достаточно, чтобы позволить CS вызвать реакции страха. CS вызывает характерные вегетативные реакции, хотя никогда не был связан с нанесением шока.
Людей также можно обуславливать, позволяя им наблюдать, как кто-то еще обуславливается - наблюдатель учится бояться CS, даже если CS или US никогда не предъявлялись непосредственно наблюдающему субъекту.
Возможности миндалевидного тела человека в эмоциональном обучении и памяти попадают в категорию неявного обучения и памяти (бессознательное вспоминание перцептивных и моторных навыков). Однако в ситуациях опасности гиппокамп и другие компоненты системы медиальной височной доли связаны с явным обучением и памятью (сознательное вспоминание людей, мест и прочее) будет кодировать обучение таким образом, что выученные индикаторы опасности также можно будет вспоминать сознательно.
Исследования пациентов с двусторонним повреждением миндалины или гиппокампа иллюстрируют отдельный вклад миндалины и гиппокампа в имплицитную и явную память соответственно.
Пациенты с повреждением миндалины не проявляют физиологической реакции на CS (что указывает на отсутствие неявного обучения), но хорошо помнят опыт кондиционирования (что указывает на явное обучение), тогда как пациенты с повреждением гиппокампа обычно реагируют на CS, но не имеют сознательной памяти о нем. опыт кондиционирования.
Функция миндалины нарушена при ряде психических расстройств у людей, особенно при расстройствах страха и тревоги (см. Главу 63). Кроме того, миндалевидное тело играет важную роль в обработке сигналов, связанных с наркотиками, вызывающими зависимость (см. Главу 49).
Вопрос 15. Внутрисердечные рефлексы. Основные рефлексогенные зоны и их значение в регуляции деятельности сердца. Роль условных рефлексов в регуляции деятельности сердца.
Интракардиальные рефлексы. В сердце располагаются многочисленные интрамуральные нейроны — как одиночные, так и собранные в ганглии (ядра Догеля, Ремака, Биддера и Людвига). Большинство этих клеток расположено непо-средственно вблизи атриовентрикулярного и синоатриального узлов, образуя вместе с массой эфферентных волокон, лежащих внутри межпредсердной перегородки, внутрисердечные нервные сплетения. Среди этих нейронов имеются эфферентные клетки Догеля первого типа (парасимпатические), кроме того, афферентные клетки Догеля второго типа и вставочные — третьего типа. Таким образом, во внутрисердечном нервном аппарате имеются все элементы, необходимые для замыкания внутриорганных рефлекторных дуг. Однако участие в регуляции сердечной деятельности интракардиальных ганглиозных нервных элементов изучено в меньшей степени, чем экстракардиальных нервов. Очевидно, что интраму ральные ганглии обеспечивают передачу возбуждения с волокон блуждающего нерва на клетки синоатриального и атриовентрикулярного узлов, а также рабочего миокарда предсердий и желудочков, выполняя релейную функцию. В условиях эксперимента на изолированном сердце животных стимуляция интрамуральных нервных элементов может вызывать как положительные, так и отрицательные, то есть различные по знаку, хроно-, батмо-, дромо- и инотропные эффекты сердца. Так, например, растяжение правого предсердия в условиях изолированного сердца приводит к увеличению силы сокращений левого желудочка. Можно поэтому полагать, что интракардиальные рефлексы в какой-то мере обеспечивают согласование сократительной активности различных отделов сердца. Однако в целостной системе кровообращения роль интракардиальных рефлексов, вероятно, не является значимой для регуляции деятельности сердца, тем более что согласование силы сокращений правых и левых отделов сердца осуществляется и без участия интракардиальных рефлексов — механизмом гетерометрической регуляции сердца. Исключением является кардиоренальный рефлекс — увеличение секреции атриопептида (натрийуретического предсердного фактора) при растяжении стенки правого предсердия в результате увеличения объема венозного депо крови.
Таким образом, современная концепция центральной регуляции кровообращения и деятельности сердца исходит из возможности существования серии параллельных контуров регуляции, характеризующихся различными уровнями замыкания рефлекторных дуг. Высокая степень автономности этих контуров регуляции не исключает тесного взаимодействия между ними, которое определяет конечный результат в виде приспособительных реакций сердца и сосудов в условиях действия на систему кровообращения разнообразных внешних и внутренних раздражителей. Одной из ключевых нерешенных проблем нейрогенной регуляции кровообращения и деятельности сердца является вопрос об однозначности и детерминированности нейрогенных рефлекторных реакций сердца и сосудов. Так, например, неоднозначные реакции сердца (брадикардия или тахикардия) отмечены при рефлексе Бейнбриджа. Пережатие сонных артерий у животных в экспериментах может вызывать не только прессорный, но и депрессорный синокаротидный рефлекс. Следовательно, возникает принципиальный вопрос отсутствия строгого детерминизма в рефлекторных реакциях сердца и сосудов. Не вызывает сомнений, что эта проблема требует дальнейших научных исследований.
РЕФЛЕКСОГЕННЫЕ ЗОНЫ:
см. вопрос 14 и:
Основные рефлексогенные зоны:
1. Аортальная рефлексогенная зона — скопление барорецепторов, расположенных в области дуги аорты. Раздражителем барорецепторов является скорость и степень растяжения стенки аорты колебаниями артериального давления.
2. Синокаротидная рефлексогенная зона — плотное скопление механо- и хеморецепторов в области разветвления общей сонной артерии на наружную и внутреннюю. Состоит из каротидного синуса и каротидного клубочка.
Обе рефлексогенные зоны образованы скоплениями хеморецепторов, которые реагируют на изменение напряжения кислорода в артериальной крови и участвуют таким образом в регуляции дыхания. Возбуждение рефлексогенных зон при снижении
парциального давления кислорода в артериальной крови вызывает повышение частоты сердечных сокращений, а также констрикцию периферических сосудов + и механорецепторов, которые чувствительны к растяжению сосуда при повышении артериального давления. При повышении давления возникает возбуждение, которое идет по аортальному нерву центры регуляции деятельности сердечно-сосудистой системы в продолговатом мозге. Ответной реакцией со стороны сердечно-сосудистой системы в такой ситуации будет урежение сердечных сокращений, ослабление сердечного выброса, расширение резистивных сосудов; артериальное давление упадет.

3. В предсердиях в месте впадения в них полых и легочных вен имеются механорецепторы, реагирующие на увеличение венозного возврата, a-рецепторы реагируют на изменение напряжения стенок предсердий, а b-рецепторы возбуждаются при пассивном растяжении камер сердца в ответ на увеличение венозного притока к сердцу. Эти рецепторы называют волюморецепторами, так как они реагируют на объем притекающей крови. Импульсы от них поступают в продолговатый мозг к центрам блуждающих нервов и уменьшают парасимпатическую эфферентную активность. Одновременно импульсы с этих рецепторов поступают в спинной мозг, где повышают тонус симпатических центров. Учащение сердечных сокращений происходит за счет снижения тонуса парасимпатической иннервации и за счет повышения активности симпатической иннервации. Физиологическое значение этого рефлекса заключается в том, что он предотвращает перенаполнение и растяжение полых вен при интенсивном притоке крови путем перекачивания ее в большой круг кровообращения. (кардио-кардиальный рефлекс)
Внутриорганная нервная система имеет афферентные нейроны, дендриты которых образуют рецепторы растяжения (механорецепторы) на волокнах миокарда и коронарных сосудах; имеются также вставочные и эфферентные нейроны. Аксоны последних иннервируют миокард и гладкие мышцы коронарных сосудов. Все эти нейроны связаны между собой синаптическими связями. В эксперименте показано, что увеличение растяжения правого предсердия приводит к усилению сокращений левого желудочка. В естественных условиях увеличение растяжения правого желудочка бывает при возрастании венозного притока (венозного возврата). Следовательно, при увеличении кровенаполнения правой половины сердца происходит усиление сокращения не только правого желудочка, но и левого желудочка, а ведь до левой половины сердца увеличенный объем крови поступит только при следующем сокращении (из малого круга кровообращения). Внутрисердечный рефлекс, усиливающий сокращение левого желудочка необходим для того, чтобы «освободить место» притекающей крови и ускорить выброс ее в артериальную систему.
Такие реакции со стороны сердца имеют место лишь на фоне низкого исходного кровенаполнения сердца и незначительной величины давления крови в устье аорты и коронарных сосудах. При переполнении кровью камер сердца и высоком давлении в устье аорты растяжение венозных приемников в сердце угнетает сокращение миокарда. Это сопровождается уменьшением выброса крови в аорту и затруднением притока крови из вен. Такие реакции имеют важное значение в стабильном обеспечении кровенаполнения артериальной системы.
Внутрисердечные рефлексы, в отличие от гетеро- и гомеометрических видов регуляции, существенно сглаживают и «смягчают» гемодинамические сдвиги, вызванные, в том числе, и миогенной ауторегуляцией. Имеется в виду возможное резкое увеличение энергии сердечного сокращения при гетерометрических и гомеометрических формах ауторегуляции (например, при внезапном повышении венозного притока – в момент струйного переливания крови или кровозаменителей или быстром повышении артериального давления, связанного с какимилибо экстремальными ситуациями: стресс, физическая нагрузка и т.д.).
Чрезмерное увеличение наполнения камер сердца притекающей кровью, а также значительное повышение давления в аорте вызывают уменьшение силы сокращения миокарда за счет внутрисердечных периферичеких рефлексов. Сердце при этом выбрасывет меньше крови в момент систолы. Задержка в желудочках сердца даже небольшого дополнительного объема крови сопровождается повышением давления в них, а это вызывает уменьшение венозного притока. Излишний объем крови, который мог бы оказать отрицательное влияние на артериальное давление, задерживается в венозной системе. Опасность может возникнуть и при уменьшении сердечного выброса в результате критического падения артериального давления. Внутрисердечные рефлексы предупреждают возникновение такой опасности. Эти рефлексы, в отличие от истинных рефлексов осуществляемых с участием ЦНС, имеют меньший латентный период, т.е. реагируют быстро и обеспечивают «оперативную» регуляцию сократительной активности миокарда.
Работа сердца существенно модифицируется также и на уровне локальных интракардиальных (кардиальнокардиальных) рефлексов, замыкающихся в интрамуральных ганглиях сердца.
По сути дела внутрисердечные рефлекторные дуги — часть метасимпатической нервной системы. Эфферентные нейроны являются общими с дугой классического парасимпатического рефлекса (ганглионарные нейроны), представляя единый «конечный путь» для афферентных влияний сердца и эфферентной импульсации по преганглионарным эфферентным волокнам блуждающего нерва. Внутрисердечные рефлексы обеспечивают «сглаживание» тех изменений в деятельности сердца, которые возникают за счет механизмов гомеоили гетерометрической саморегуляции, что необходимо для поддержания оптимального уровня сердечного выброса.
