
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
Гидролиз солей
Гидролиз – реакция взаимодействия вещества с водой.
Нормальная соль – продукт взаимодействия кислоты и основания и не содержит протонов и гидроксид- ионов, следовательно рН растворов солей должно быть таким же как у воды – 7. Но так бывает не для раствора любой соли. Некоторые соли подвергаются гидролизу.
Гидролиз солей – реакция ионного обмена между водой и растворенными в ней солями. Частный случай реакции ионного обмена.
Гидролиз солей – реакция обратимая и протекает обычно по I ступени. Фактически – это реакция обратная к реакции нейтрализации, следовательно, эндотермическая
По отношению к гидролизу все соли можно разделить на 4 группы:
Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются. рН их растворов 7.
Соли, образованные сильной кислотой и слабым основанием. Катион от слабого основания забирает гидроксид-ион от ассоциированной с ним воды, оставшийся протон придает раствору кислую среду, т.е. рН < 7 .
NH4Cl + НОН NH4OH + HCl
NH4 + + Cl + H2O NH4OH + H + + Cl
NH4 + + H2O NH4OH + H +
ZnCl2 + HOH ZnOHCl + HCl

Zn2 + +2 Cl + H2O ZnOH+ + H + +2 Cl
Zn2 + + H2O ZnOH+ + H +
Соли, образованные слабой кислотой и сильным основанием . Анион слабой кислоты стремится присоединить к себе протон из воды,при этом гидроксид-ион остается в растворе (среда щелочная), рН > 7 .
CH3COOK + HOH CH3COOH + KOH
CH3COO + K+ + HOH CH3COOH + K+ + OH
CH3COO + HOH CH3COOH + OH
I ст. Na2CO3 = 2Na + + CO3 2
CO3 2 + Н +– OH НCO3 + OH (pH > 7)
Na2CO3 + H2O 2Na + + НCO3 + OH
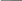 Na2CO3
+ H2O 2NaНCO3 +
NaOH
Na2CO3
+ H2O 2NaНCO3 +
NaOH
II ст. NaНCO3 = 2Na + + НCO3
HCO3 + Н +– OH Н2CO3 + OH
NaНCO3 + H2O Н2CO3 + NaOH
Гидролиз таких солей как Na2CO3 (сода), как правило, ограничивается I ступенью.
Соли слабого основания и слабой кислоты подвергаются полному (необратимому, совместному) гидролизу. В растворах не существуют. В таблицах растворимости это указано прочерком. При попытках получить такие соли путем РИО гидролиз катиона и аниона усиливают друг друга, так как образующиеся протон и гидроксид-ион соединяются в воду, и гидролиз доходит до последней ступени
Cr2(SO4)3 +3 Na2CO3 +3 H2O =↓2 Cr(OH)3 +↑3 CO2 +3 Na2SO4↓
Степень гидролиза (h)- отношение числа гидролизованных молекул к общему числу молекул соли.
Степень гидролиза зависит от
-природы соли,
-температуры,
- концентрации соли
Обычно степень гидролиза менее 5%, но существуют сильно гидролизующиеся соли: Na2CO3 (69%), Na3PO4 (39%).
Поскольку гидролиз – реакция обратимая и эндотермическая, то по принципу Ле Шателье, нагревание и разбавление усиливает гидролиз. Растворы таких солей жранят в концентрированном виде при пониженной температуре, добавляя кислоту (или основание), чтобы сдвинуть равновесие влево.
С гидролизом солей связаны многие процессы жизнедеятельности. Свойство солей гидролизоваться применяют в технике и быту (щелочная среда раствора соды). В природе гидролизминералов способствует переносу элементов в земной коре.
Зная степень гидролиза, можно вычислить рН образующегося раствора, т.к. количество Н+ равно числу гидролизованных молекул соли. Если при гидролизе образуются ОН=, то они связаны с Н+ через ионное произведение воды.
Как и для всякого обратимого процесса для реакции гидролиза можно записать константу равновесия, которая называется константой гидролиза.
