
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
5.Изомерия комплексных соединений
Для комплексных соединений характерно явление изомерии. Оно заключается в существовании соединений одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам. Такие соединения называются изомерами. Изучение изомерии позволило впервые установить пространственное строение таких соединений. Рассмотрим основные типы изомерии комплексных соединений.
Пространственная изомерия. Она обусловлена существованием соединений, имеющих одинаковый порядок связей атомов, но различное их расположение. Пространственная изомерия бывает двух видов: геометрическая и оптическая.
Геометрическая изомерия заключается в том, что комплекс, содержащий неодинаковые лиганды, может существовать в нескольких различных формах в зависимости от пространственного размещения лигандов во внутренней сфере комплекса. К геометрической изомерии в первую очередь относится цис-транс-изомерия в плоско-
квадратных
комплексах
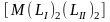 и октаэдрических -
и октаэдрических -
 .
Например, для
возможны два изомера:
.
Например, для
возможны два изомера:

цис-изомер транс-изомер
(оранжево-желтый) (светло-желтый)
При октаэдрическом
расположении шести лигандов для
комплексного соединения
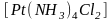 возможны такие два изомера:
возможны такие два изомера:
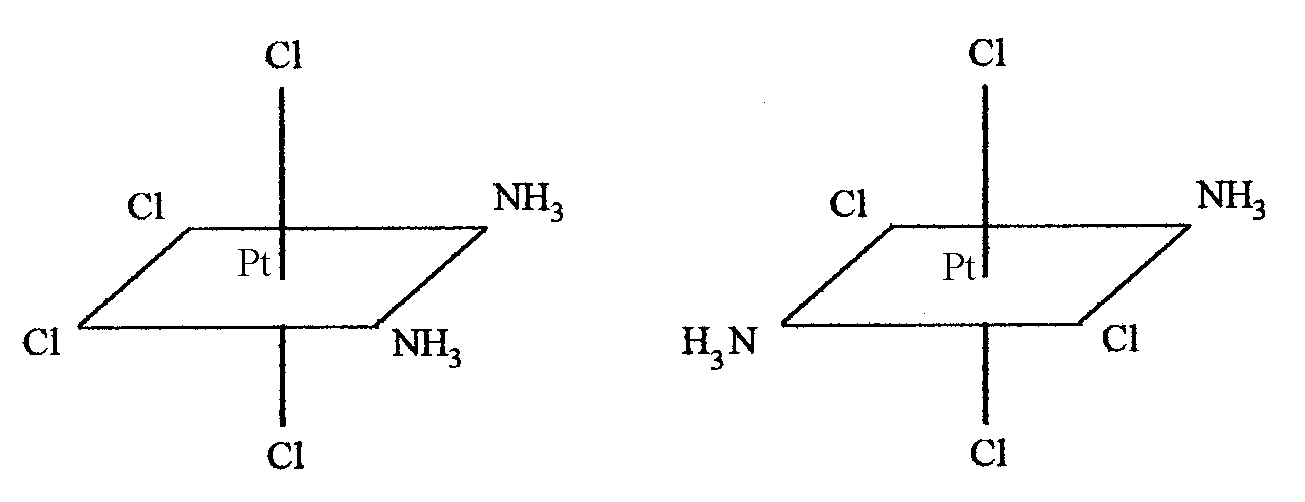 .
.
цис-изомер транс-изомер
(оранжевый) (желтый)
В первом случае молекулы аммиака расположены по одну сторону от комплексообразователя, во втором - по разные стороны.
При увеличении числа неодинаковых лигандов быстро растет число геометрических изомеров.
Геометрические изомеры отличаются реакционной способностью, растворимостью и окраской.
Оптическая изомерия заключается в том, что комплекс может существовать в двух формах (оптических изомерах), одна из которых является зеркальным отражением структуры другой формы, причем структуры этих форм не могут быть совмещены друг с другом в результате простых поворотов.
Например, комплексный
ион
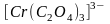 может существовать в виде двух оптических
изомеров:
может существовать в виде двух оптических
изомеров:
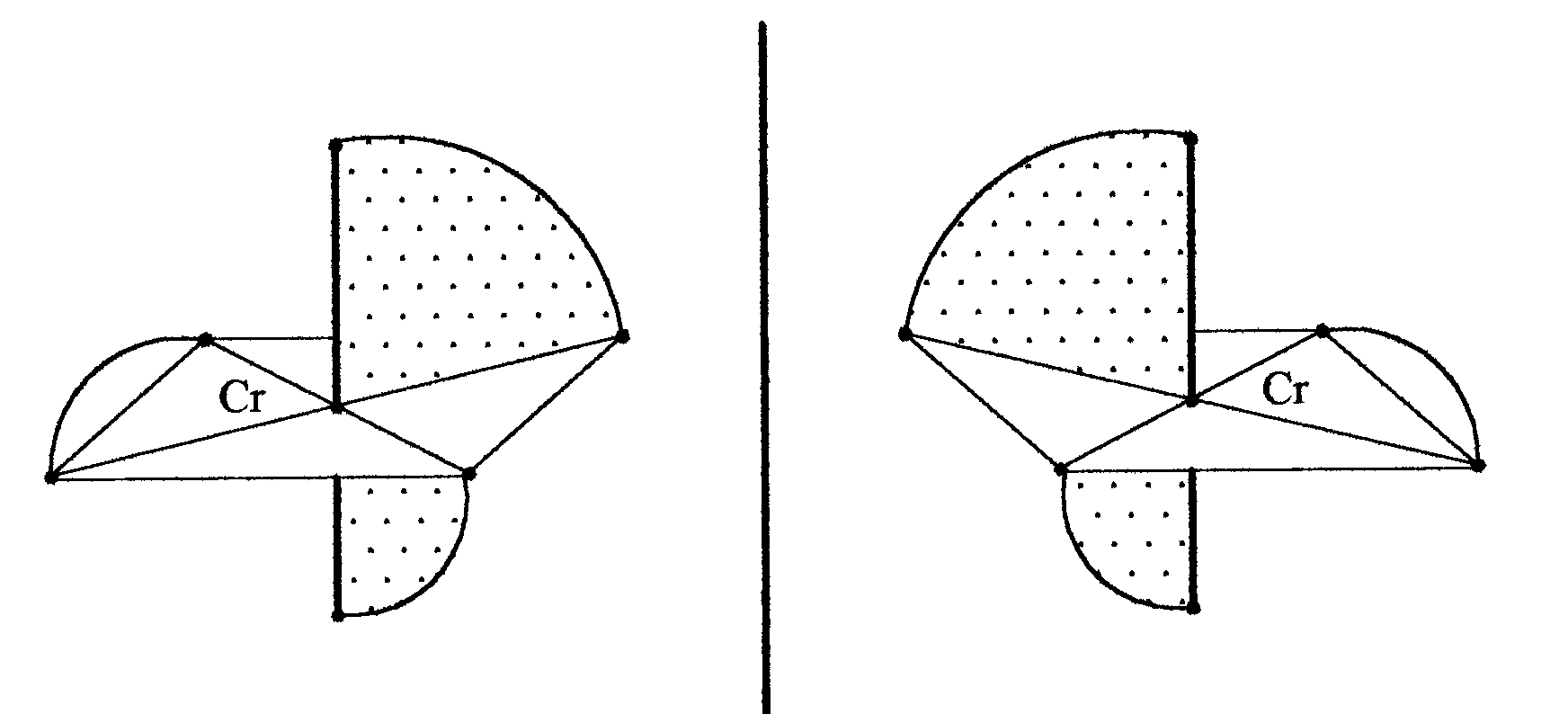
В структуре оптических изомеров отсутствует плоскость симметрии, и поэтому они обладают оптической активностью - вращают плоскость поляризации падающего на них света. Оба изомера вращают плоскость поляризации в равной мере, но в противоположных направлениях. Они имеют одинаковые химические и большую часть физических свойств. Поэтому разделение таких оптически активных изомеров требует особых методов.
Изучение пространственной структуры комплексных соединений позволило И.И.Черняеву в 1926 году открыть важнейшую закономерность, которой подчиняется реакционная способность этих соединений, получившая название «транс-влияние». Суть этой закономерности заключается в том, что неоднородные лиганды в транс-положении оказывают друг на друга влияние, обуславливающее их способность вступать в реакции замещения (обмена). Это явление имеет место в комплексных соединениях с квадратной или октаэдрической структурой.
Лиганды по силе своего трансвлияния можно расположить в следующий ряд:
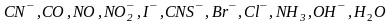 .
.
Слева направо активность лигандов падает.
Так, для комплексного иона
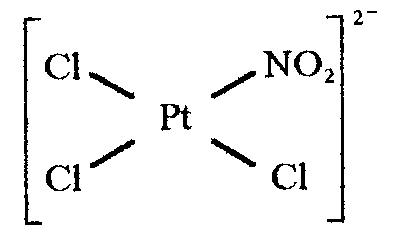
из трех ионов хлора легче других замещается тот, который находится в транс-положении к более транс-активному лиганду . Использование этой закономерности позволяет проводить направленный синтез веществ.
Сольватная
изомерия.
Причиной этого вида изомерии является
различное положение молекул растворителя
во внутренней или внешней сфере комплекса.
Если в роли растворителя выступает
вода, то говорят о гидратной
изомерии.
Типичным примером такого вида изомерии
является
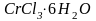 ,
существующий в трех разных формах:
,
существующий в трех разных формах:
;
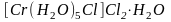 ;
;
(сине-фиолетовый) (светло-зеленый)
 .
.
(темно-зеленый)
Ионизационная изомерия. Она связана с неодинаковым распределением ионов между внешней и внутренней сферой комплексного соединения. Например:
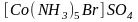 и
и
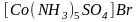 .
.
(красно-фиолетовый) (красный)
Координационная изомерия. Если комплексное соединение содержит одновременно два комплексообразователя, то возможно неодинаковое распределение лигандов между ними. Например:
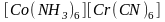 и
и
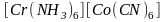 .
.
Изомерия связей. Некоторые монодентатные лиганды имеют в своем составе два атома, способных образовывать связи с комплексообразователем ( , , ). Например, координация лиганда возможна как через атом азота (нитро - комплексы):
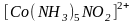 (желто-коричневый),
(желто-коричневый),
так и через атом кислорода (нитрито-комплексы):
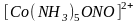 (розовый).
(розовый).
Такие лиганды называют амбидентатными.
Изомерия комплексных соединений не исчерпывается рассмотренными выше видами. Существуют еще и другие, более сложные виды изомерии.
