
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
4.2.Комплексные соединения, содержащие ионные лиганды
Гидроксокомплексы.
В качестве лигандов гидроксокомплексы
имеют ионы
.
Например:
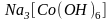 ,
,
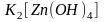 .
Они образуются при растворении амфотерных
гидроксидов металлов в растворах
щелочей. Например:
.
Они образуются при растворении амфотерных
гидроксидов металлов в растворах
щелочей. Например:
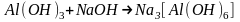 .
.
Ацидокомплексы.
Такие комплексные соединения широко
известны. В них в качестве лигандов
выступают кислотные остатки
кислородсодержащих или бескислородных
кислот. Это комплексы анионного типа.
Например:
;
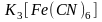 ;
;
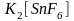 .
.
Кроме перечисленных выше комплексных соединений, содержащих в качестве лигандов частицы только одного вида, существуют комплексы смешанного типа. Например:
 ;
;
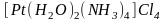 ;
;
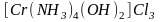 .
Существование подобных соединений
смешанного типа значительно увеличивает
общее количество возможных комплексных
соединений.
.
Существование подобных соединений
смешанного типа значительно увеличивает
общее количество возможных комплексных
соединений.
4.3. Циклические комплексные соединения
К циклическим соединениям относятся такие комплексные соединения, во внутренней сфере которых имеются циклы. Циклы могут образовывать полидентатные лиганды, т.е. частицы, которые занимают два или более координационных места.
Простейшими их
представителями являются оксалат-ион
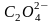 и этилендиамин
и этилендиамин
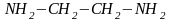 ,
имеющие координационную емкость равную
двум. Например, в комплексном ионе
,
имеющие координационную емкость равную
двум. Например, в комплексном ионе
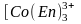 ,
где En
- сокращенное обозначение этилендиамина,
содержится три пятичленных цикла, каждый
из которых, как клешня захватывает
комплексообразователь. Поэтому
циклические комплексы часто называют
клешневидными
или хелатными
(от греч. chele
- клешня). Любой хелатный лиганд обладает
полидентатным характером, но не всякий
полидентатный лиганд проявляет хелатные
свойства. Хелатные
комплексы имеют обычно повышенную
устойчивость по сравнению со структурно
сходными комплексами, не содержащими
внутрикомплексных циклов.
Это важная особенность хелатного
эффекта.
,
где En
- сокращенное обозначение этилендиамина,
содержится три пятичленных цикла, каждый
из которых, как клешня захватывает
комплексообразователь. Поэтому
циклические комплексы часто называют
клешневидными
или хелатными
(от греч. chele
- клешня). Любой хелатный лиганд обладает
полидентатным характером, но не всякий
полидентатный лиганд проявляет хелатные
свойства. Хелатные
комплексы имеют обычно повышенную
устойчивость по сравнению со структурно
сходными комплексами, не содержащими
внутрикомплексных циклов.
Это важная особенность хелатного
эффекта.
Особую группу
составляют
внутрикомплексные
соединения.
В таких соединениях полидентатные
лиганды связаны с комплексообразователем
ковалентной связью, образованной по
разному механизму - обменному и
донорно-акцепторному. Лиганды такого
типа называются комплексными.
Это характерно, например, для аминокислот
и других органических соединений,
содержащих одновременно атом азота и
гидроксогруппу. В этом случае бидентатный
лиганд образует с комплексообразователем
одну ковалентную связь за счет неспаренного
электрона атома кислорода, остающегося
после отщепления атома водорода от
гидроксогруппы и другую ковалентную
связь, образованную за счет неподеленной
пары атома азота. Примером таких
соединений может служить комплекс меди
с аминоуксусной кислотой (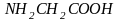 ):
):
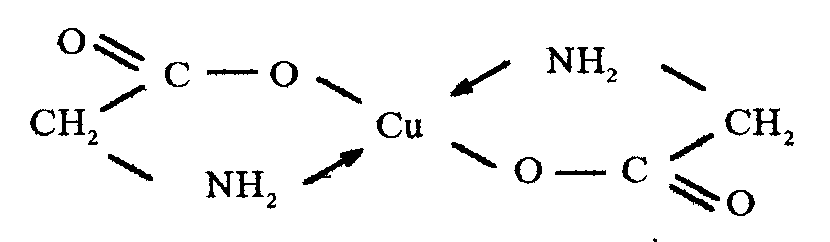 .
.
Внутрикомплексные соединения обычно обладают гидролитической устойчивостью, низкой растворимостью в воде и высокой - в органических растворителях, часто характерной яркой окраской. Эти свойства обеспечили внутрикомплексным соединениям широкое применение в аналитической химии.
4.4. Многоядерные комплексные соединения
Наряду с моноядерными комплексами, включающими только один комплексообразователь, существуют многоядерные, в структуре которых одновременно присутствуют два или более комплексообразователей. В качестве лигандов в них выступают частицы, обладающие несколькими неподеленными парами и образующие мостиковые связи с двумя (редко с тремя) комплексообразователями. В многоядерных комплексах каждые два комплексообразователя могут быть соединены одним, двумя или тремя мостиковыми лигандами одновременно:
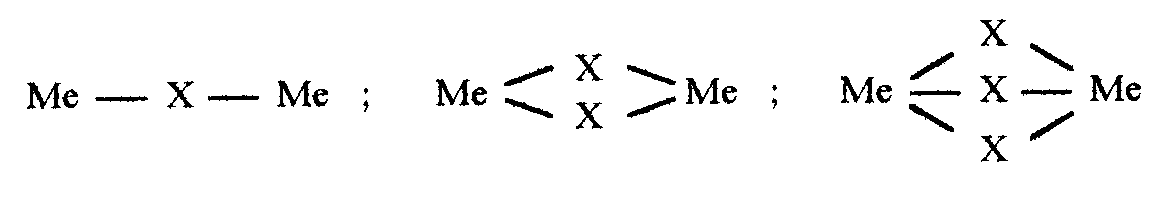
Функции мостиковых
групп могут выполнять как монодентатные
лиганды
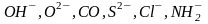 ,
содержащие более одной неподеленной
пары электронов, так и все полидентатные
лиганды.
,
содержащие более одной неподеленной
пары электронов, так и все полидентатные
лиганды.
Например:
 ,
,
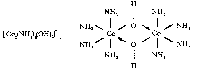 .
.
Мостиковым лигандам дают их обычные названия с добавлением перед ними греческой буквы (мю).
Например,
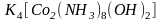 называют ди(-гидроксо)октаам-миндикобальтат(III)
калия.
называют ди(-гидроксо)октаам-миндикобальтат(III)
калия.
