
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
1.Понятие о комплексном соединении
История
развития химии комплексных («complex»
- сложный) соединений насчитывает более
150 лет. Давно было доказано, что молекулы
многих веществ, способных к самостоятельному
существованию, могут взаимодействовать
и образовывать новые более сложные
молекулы. Например, сульфат меди (II)
и аммиак могут существовать раздельно.
Однако при пропускании через водный
раствор сульфата меди (II)
газообразного аммиака они взаимодействуют
и образуется новое комплексное соединение
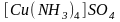 :
:
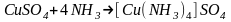 .
.
В
растворе этого соединения не обнаруживается
исходный гидратированный ион
 .
Полученное комплексное соединение
характеризуется собственными физическими
и химическими свойствами, отличными от
свойств исходных веществ.
.
Полученное комплексное соединение
характеризуется собственными физическими
и химическими свойствами, отличными от
свойств исходных веществ.
Исходные
соединения в этом взаимодействии
называют соединениями
первого порядка.
К ним относятся, главным образом, бинарные
и некоторые другие достаточно простые
по своей структуре соединения (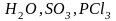 и т.д.). В этих соединениях абсолютные
значения степеней окисления элементов
совпадают с проявляемыми ими валентностями.
и т.д.). В этих соединениях абсолютные
значения степеней окисления элементов
совпадают с проявляемыми ими валентностями.
Соединения, получающиеся в результате взаимодействия соединений первого порядка, называются соединениями высшего порядка. К их числу относятся и комплексные соединения. В комплексных соединениях элементы проявляют дополнительные валентности.
Поскольку комплексные соединения весьма многочисленны и разнообразны, дать общее исчерпывающее определение невозможно. Однако, учитывая выше сказанное, можно считать, что комплексные соединения - это сложные вещества, в которых валентность (число химических связей) центрального атома больше абсолютного значения его степени окисления. Например, - комплексное соединение, так как валентность атома меди в нем равно 4, а степень окисления +2.
2.Структура комплексных соединений
Первой теорией, позволившей объяснить образование комплексных соединений, была координационная теория, предложенная в 1893 году швейцарским ученым Альфредом Вернером. Эта теория дала возможность установить строение комплексных соединений задолго до разработки физических методов определения структуры веществ.
Согласно
теории Вернера, в молекуле комплексного
соединения центральное место занимает
комплексообразователь
(заряженный
или нейтральный атом). Типичными
комплексообразователями являются ионы
и атомы переходных металлов, в частности,
хорошие комплексообразователи - ионы
 ,
атомы элементов VIII
В группы периодической системы.
,
атомы элементов VIII
В группы периодической системы.
Вокруг комплексообразователя расположены ( координированы ) лиганды (от лат. ligar - связывать) - атомы, молекулы или ионы противоположного знака. Молекулы и ионы могут быть простыми или сложными.
Число
химических связей, устанавливаемых
комплексообразователем с лигандами,
называется координационным
числом
(к.ч.) комплексообразователя. Оно может
принимать различные значения. Например,
у меди в комплексе
к.ч.=4, у алюминия в
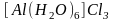 к.ч.=6. Координационные числа имеют
значения от 2 до 12, но чаще всего они
равны 4 или 6. Величина к.ч., как правило
(но не всегда!), в два раза больше степени
окисления комплексообразователя.
Некоторые лиганды содержат несколько
функциональных групп, которые могут
образовывать химические связи с
комплексообразователем. Подобные
лиганды занимают в комплексе координационные
места нескольких обычных лигандов.
Число химических связей, образуемых
лигандом с комплексообразователем,
определяет координационную
емкость (дентатность)
лиганда. Так,
к.ч.=6. Координационные числа имеют
значения от 2 до 12, но чаще всего они
равны 4 или 6. Величина к.ч., как правило
(но не всегда!), в два раза больше степени
окисления комплексообразователя.
Некоторые лиганды содержат несколько
функциональных групп, которые могут
образовывать химические связи с
комплексообразователем. Подобные
лиганды занимают в комплексе координационные
места нескольких обычных лигандов.
Число химических связей, образуемых
лигандом с комплексообразователем,
определяет координационную
емкость (дентатность)
лиганда. Так,
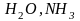 имеют координационную емкость
(дентатность) равную единице, а
NH2CH2CH2NH2
(этилендиамин) - двум. Известны лиганды
с координационной емкостью, равной
трем, четырем и более единицам.
имеют координационную емкость
(дентатность) равную единице, а
NH2CH2CH2NH2
(этилендиамин) - двум. Известны лиганды
с координационной емкостью, равной
трем, четырем и более единицам.
Комплексообразователь и лиганды вместе образуют внутреннюю координационную сферу комплексного соединения - комплексную частицу (ион или молекулу).
Если
внутренняя сфера заряжена, то комплекс
имеет еще и внешнюю
сферу,
поскольку к внутренней сфере будут
притягиваться противоположно заряженные
ионы. Принято в формулах комплексных
соединений внутреннюю сферу отделять
от внешней квадратными скобками. Так,
в комплексном соединении
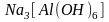 ион
ион
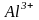 - комплексообразователь, ионы
- комплексообразователь, ионы
 - лиганды, координационное число равно
6,
- лиганды, координационное число равно
6,
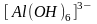 - внутренняя сфера, ионы
- внутренняя сфера, ионы
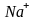 - внешняя
сфера.
- внешняя
сфера.
