
Нормальная физиология / КР4 кровь + эндокринка
.pdf
протекающий воспалительный процесс, не определяя его природы. Материал для исследования: кровь венозная или капиллярная берется в пробирку, содержащую 3,8% раствора цитрата (1 часть цитрата к 4 частям крови).
СОЭ М 1-10 ММ/ЧАС |
УВЕЛИЧЕНИЕ = ВОСПАЛИТЕЛЬНЫЕ ПРОЦЕССЫ, АЛЛЕРГИЯ И ПР. |
СОЭ Ж 2-18 ММ/ЧАС |
ТЕСТ НЕСПЕЦИФИЧЕН – вспомогательный скрининговый тест |
Удельная масса эритроцитов выше, чем удельная масса плазмы, поэтому в пробирке при наличии антикоагулянта (используется цитрат натрия) под действием силы тяжести эритроциты оседают на дно.
Показания к назначению анализа:
Воспалительные заболевания;
Инфекции;
Подозрения на новообразования;
Скрининговое обследование при профилактических осмотрх.
Международный комитет по стандартизации в гематологии (ICSH) рекомендует для определения СОЭ метод Вестергрена (Westergren). Для автоматизации этого метода выпускаются специальные анализаторы, капилляры, штативы, системы взятия крови, позволяющие получать более-менее приемлемые результаты.
В России - микрометод Панченкова. Он прост в исполнении, не дорог, но требует не менее 1 ч для выполнения, не автоматизирован, не снабжен системой документирования результатов, проводится вручную, неудобен при большом
количестве исследований и имеет много источников ошибок.
МЕТОДЫ ОПРЕДЕЛЕНИЯ: 1. Метод Панченкова –
2. Метод Вестергрена
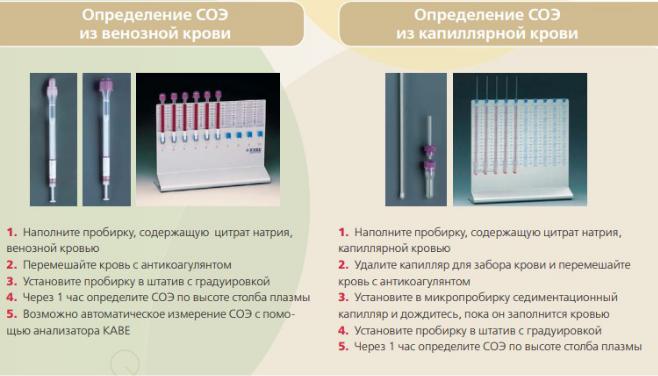
Модифицированный метод Вестергрена: Процедура определения:
1.Произвести забор венозной крови до метки в пробирку (вакуумную или простую), содержащую раствор цитрата натрия.
2.Перемешать кровь с цитратом натрия в пробирке.
3.Установить пробирки в анализатор СОЭ Ves-matic.
4.Нажать кнопку Test для запуска измерения.
5.Через 20 (или 10) мин анализатор автоматически определит СОЭ для 10, 20 или 30 проб.
Клинико-диагностическое значение
СОЭ ускорена
Беременность, послеродовой период, менструации
Воспалительные состояния (острые и хронические инфекции, воспаление легких, ревматизм, инфаркт миокарда, сифилис, туберкулез, травмы, переломы костей, шок, оперативные вмешательства, коллагенозы, болезнь Рейно, отравления химическими соединениями (свинец, мышьяк))
Анемии
Гипер- и гипофункция щитовидной железы
Нефротический синдром
Злокачественные гранулемы
|
Моноклональные гаммапатии (миелома, макроглобулинемия |
Вальденстрема, |
|
иммунопролиферативные заболевания) |
|
|
Гиперфибриногенемия |
|
|
Гиперхолестеринемия |
|
Препараты: морфин, декстран, метилдофа, витамин А
СОЭ замедлена
Эритремии и реактивные эритроцитозы
Хроническая недостаточность кровообращения
Гипофибриногенемия

СРС5. «Жизненный цикл» гормонов. Механизмы действия гормонов на клетки-
мишени.
Система эндокринной регуляции включает в себя следующие звенья, составляющие «жизненный цикл» гормонов.
1)Синтез и секреция специализированными эндокринными клетками.
2)Транспорт кровью: а) в свободном состоянии (гидрофильные гормоны); б) в соединении с белкамипереносчиками (липофильные); в) адсорбированные на форменных элементах крови. Биологическую активность проявляют только гормоны, находящиеся в свободном виде.
3)Действие на рецепторы в клетках-мишенях.
4)Инактивация и экскреция: а) разрушение в местах своего действия, а также в печени, почках и других органах; б) выведение с мочой в неизмененном виде.
Эффект действия гормонов зависит от состояния всех перечисленных звеньев, однако наиболее значимыми являются этапы взаимодействия гормонов с клетками-мишенями и регуляции секреции гормонов.
***Транспортные белки создают резервуар гормонов в крови, поскольку гормоны в связанном виде не подвергаются расщеплению и выведению. При этом активен только несвязанный с белками (свободный) гормон. При разрушении свободных форм таких гормонов будет происходить диссоциация связанной формы. Тем самым концентрация гормона в крови будет поддерживаться на относительно постоянном уровне. В связи с этим стероидные и тиреоидные гормоны имеют длительный период жизни в русле крови (часы). Поскольку белково-пептидные гормоны и биогенные амины не имеют специальных транспортных белков, они оказывают более быстрый эффект, но при этом период их жизни меньше (минуты).
Общие принципы регуляции секреции гормонов
В зависимости от природы регулирующих факторов различают несколько видов регуляции секреции гормонов: а) нервный; б) гуморальный (гормонами и метаболитами.) Основной механизм для большинства гормонов - гуморальный.
1.Гормональная регуляция - основная для секреции гормонов системы «гипоталамус-аденогипофиз- периферические эндокринные железы». В гипоталамусе вырабатываются особые регуляторные гормоны, которые усиливают или тормозят секрецию гормонов аденогипофиза. В свою очередь, гормоны аденогипофиза стимулируют секрецию гормонов щитовидной железы, коры надпочечников и половых желез. В этой системе действуют и обратные связи: например, гормоны аденогипофиза регулируют секрецию гормонов гипоталамуса.
2.Метаболическая регуляция является основной для секреции гормонов поджелудочной железы и паращитовидных желез. Осуществляется по принципу отрицательной обратной связи и направлена на поддержание относительного постоянства концентрации в крови какого-либо метаболита. Например, повышение концентрации глюкозы в крови стимулирует секрецию инсулина, а он снижает концентрацию глюкозы.
3.Нервная регуляция является ведущей для секреции гормонов гипоталамуса и нейрогипофиза, эпифиза, а также мозгового вещества надпочечников.
В большинстве случаев в регуляции секреции какого-либо гормона участвуют несколько механизмов. Например, на уровень секреции инсулина влияет не только глюкоза (основной регулирующий фактор), но и некоторые гормоны (адреналин, глюкагон и др.), а также симпатические и парасимпатические нервные воздействия.
Принцип отрицательной обратной связи. Играет важную роль в регуляции деятельности практически всех эндокринных желез. Отрицательные обратные связи обеспечивают относительное постоянство уровня гормонов в крови.
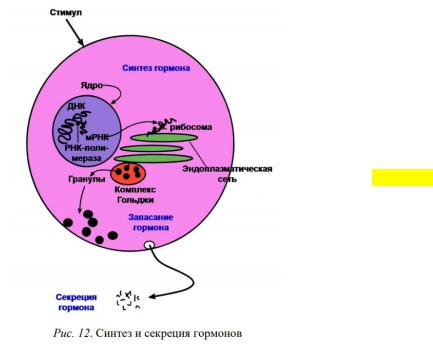
По завершении синтеза молекула пре-прогормона проникает через мембрану шероховатой эндоплазматической сети, теряя по ходу этого процесса свой сигнальный пептид. Затем прогормон поступает в комплекс Гольджи, где включается в окруженные мембраной пузырьки (везикулы, или гранулы), которые отсоединяются от аппарата Гольджи и перемещаются по цитоплазме к клеточной мембране. Специфические протеолитические ферменты внутри гранул расщепляют прогормон на составные части.
Процессы секреции гормонов тесно сопряжены с процессами их биосинтеза. Степень их сопряженности зависит от химической природы гормона и особенностей механизмов его секреции. По особенностям механизмов секреторные процессы можно разделить на три типа:
1)освобождение гормонов из клеточных секреторных гранул (секреция белково-пептидных гормонов и катехоламинов);
2)высвобождение гормонов из белково-связанной формы (секреция тиреоидных гормонов);
3)относительно свободная диффузия гормонов через клеточные мембраны (стероидные гормоны).
Возвращаясь к функциональным характеристикам секреторных гранул, необходимо остановиться еще на одном их свойстве, играющем решающую роль в собственно секреторном процессе. Гранулы обладают способностью направленно перемещаться (транспонироваться) к периферии клетки и транспортировать депонированные в них гормоны к плазматическим (клеточным) мембранам. Это движение гранул во внутрисекреторных клетках осуществляется при участии особых «контрактильных» органелл клетки (элементов цитоскелета) – тонковолокнистых микрофиламентов (диаметр 5 нм), построенных из сократительного белка актина, и полых микротрубок (диаметр 25 нм), состоящих из комплекса сократительных белков тубулина и динеина. Обработка клеток ядами – цитохалазином В, специфически разрушающим микрофиламенты, либо колхицином, или винбластином, вызывающими диссоциацию микротрубок, – приводит к торможению секреторных процессов. Внутриклеточный транспорт гранул, осуществляемый при участии микрофиламентов и микротрубок, как и все активные двигательные процессы, энергозависим и требует расхода АТФ. Кроме того, для его осуществления также необходимо присутствие Са2+ . Транспортированные к плазматическим мембранам гормональные гранулы могут вступать с ними в контакт. Мембраны гранул и плазматические мембраны при участии Са2+ контактируют между собой, и содержащийся в гранулах секрет выбрасывается во внеклеточное пространство через образующиеся в клеточной мембране «поры». Этот процесс называется экзоцитозом. После завершения экзоцитоза опустошенные гранулы способны в некоторых случаях реконструироваться и возвращаться в цитоплазму.
Таким образом, секреторные гранулы являются специализированным аппаратом гормонпродуцирующей клетки, который обусловливает:
1)окончательное образование гормона;
2)его хранение в недиффундируемой форме;
3)внутриклеточный транспорт и экзоцитоз гормонов.
По существующим данным специфический регуляторный стимул секреции, поступающий в гормонпродуцирующую ткань, прежде всего вызывает усиленное образование циклического АМФ (цАМФ), а также увеличение внутриклеточной концентрации ионов Са2+ в результате их усиленного вхождения через плазматическую мембрану извне и (или) освобождения из связанной внутри клетки формы. Ионы Са2+ и цАМФ стимулируют энергозависимый переход гормональных гранул к клеточной мембране при участии элементов цитоскелета – микрофиламентов и микротрубок, что обеспечивают контакт липидной мембраны гранул с плазматическими мембранами. После достижения контакта гранулы расплавляются, в результате чего происходит выброс водорастворимых гормонов через липопротеидные мембраны клетки в тканевую жидкость. Одна часть опустошенных гранул может реконструироваться и возобновлять свои функции, другая – необратимо распадается, а их место занимают гранулы, новообразованные из комплекса Гольджи.
Некоторая часть гранул лизируется в цитоплазме, и тогда гормон диффундирует через цитоплазматическую мембрану в тканевую жидкость.
Циркуляторный транспорт гормонов
Гормоны циркулируют в крови в нескольких физико-химических формах: в свободном виде (в виде водного раствора); в форме комплексов со специфическими белками плазмы; в форме неспецифических комплексов с плазменными белками; в форме неспецифических комплексов с форменными элементами. Все эти формы находятся в равновесии друг с другом, причем во всех известных случаях это равновесие в состоянии покоя значительно сдвинуто в сторону комплекса со специфическими белками. Концентрация этой формы в условиях физиологического покоя составляет 80 %, а иногда и более от суммарной концентрации данного гормона в крови. Некоторые гормоны (в частности стероиды и иодтиронины), попадая в кровь, связываются с белками плазмы. Такое связывание преследует, вероятно, две цели: во-первых, гормон в какой-то степени «защищается» от присутствующих в крови инактивирующих систем и, во-вторых, он «запасается» в крови, так что при необходимости оказывается легкодоступным для своих тканей-мишеней. Некоторые белки плазмы обладают особенно высоким сродством к определенным гормонам, причем степень сродства служит мерой интенсивности связывания данного гормона. Эти белки обычно являются глобулинами. К ним относятся тиронинсвязывающий глобулин (ТСГ), который взаимодействует с тироксином и трийодтиронином; транскортин, связывающий такие стероидные гормоны, как кортизол; секс-гормонсвязывающий глобулин (СГСГ), который связывает всевозможные половые гормоны. Другие белки плазмы (в частности альбумин) обладают низким сродством к гормонам, но высокой емкостью связывания, что обусловлено их повышенной концентрацией в крови. Различие связывающих свойств белков плазмы по отношению к данному гормону видно на примере транспорта тироксина в крови. Основное количество присутствующего в ней тироксина связано с обладающим высоким сродством, но низкой емкостью ТСГ, а меньшая часть транспортируется преальбуминовой фракцией, обладающей средним сродством и средней емкостью. С альбумином тироксин в нормальных условиях практически не связан, поскольку этот белок, несмотря на свою высокую емкость, проявляет крайне низкое сродство к гормону. Свободный (несвязанный) гормон, белок плазмы и комплекс гормон– белок находятся в динамическом равновесии, которое может быть выражено следующим уравнением: [Г] × [Б] ↔ [ГБ], где [Г], [Б] и [ГБ] означают соответственно концентрации свободного гормона, белка-переносчика и комплекса гормон– белок
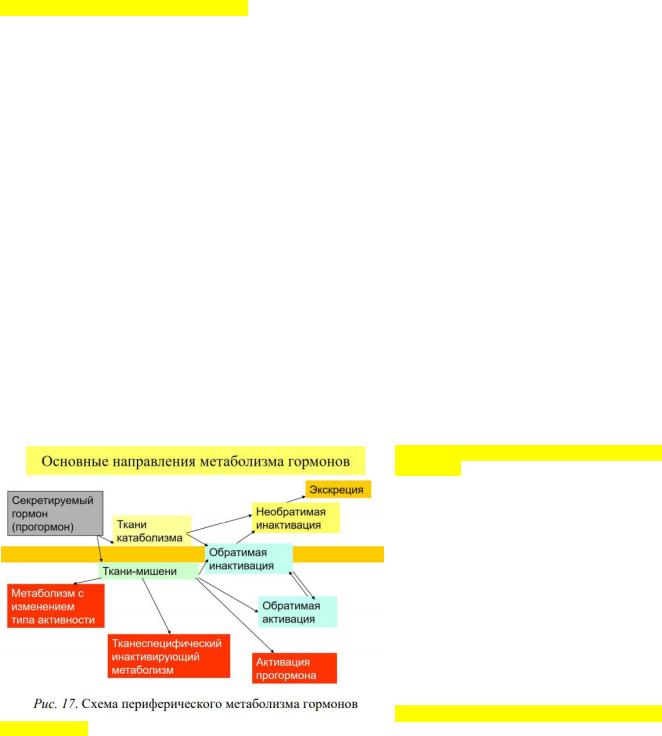
Периферический метаболизм гормонов
Важный компонент эндокринного контура
– метаболизм гормонов. Важнейшую роль в периферических превращениях гормонов играют процессы катаболизма – совокупности процессов ферментативной деградации исходной химической структуры секретируемых гормональных соединений. Химическая деградация гормонов, осуществляемая с помощью специальных ферментных систем, протекает обычно в различных тканях, но прежде всего в спланхнической системе и почках.
Пути экскреции гормонов и их
метаболитов
Большая часть секретируемых гормонов перед выведением из организма подвергается метаболическим превращениям. Лишь небольшая доля гормонов (0,5–10 %) экскретируется в неизмененном виде. В составе выводимых жидкостей плохо растворимые в воде метаболиты стероидных гормонов экскретируются преимущественно в форме глюкуронидов, сульфатов и некоторых других эфиров, обладающих высокой водорастворимостью. Метаболиты аминокислотных гормонов, как правило, хорошо растворимые в воде, экскретируются главным образом в свободной форме, и лишь незначительная их часть выделяется в составе парных соединений с кислотами. Метаболиты белковопептидных гормонов выводятся преимущественно в форме свободных аминокислот, их солей и небольших пептидов. Как и все выводимые из организма продукты, гормональные метаболиты экскретируются в первую очередь с мочой и желчью. Желчные компоненты затем в составе каловых масс окончательно выводятся из организма через кишечник. Соотношение мочевой и желчной экскреции гормональных метаболитов может быть неодинаковым. У человека значительно преобладает почечномочевой путь, обеспечивающий выведение 65–95 % метаболитов. Однако некоторая часть экскретируемых с мочой гормональных продуктов попадает в нее вторично. Эта часть соединений сначала выводится с желчью в кишечник, а затем обратно всасывается из 87 кишечника в кровь и только тогда попадает в почки. С другой стороны, у некоторых грызунов (крысы, мыши) до 65 % метаболитов

гормонов, в частности стероидных, выводятся из организма с калом. При этом исходно с желчью экскретируется до 90 % соединений. Однако и в этом случае часть метаболитов подвергается реабсорбции в кишечнике и выводится из организма с мочой. Некоторая часть гормональных метаболитов выводится из организма с потом и слюной. В большинстве случаев эти пути экскреции имеют второстепенное значение. И лишь у жвачных животных, секретирующих большое количество слюны, экскреция гормональных соединений со слюной может играть заметную роль в выведении. Большинство гормонов и их метаболитов выводится из организма почти полностью через 48–72 ч, причем 80–90 % попавшего в кровь гормона выводится уже в первые сутки. Исключение составляют тиреоидные гормоны, аккумулируемые в организме в течение ряда суток главным образом в форме тироксина.
Механизмы действия гормонов на клетки-мишени.
КЛЕТКИ-МИШЕНИ Специфически взаимодействуют с сигнальными молекулами с помощью специальных белков-рецепторов. Белки-рецепторы могут располагаться на наружной мембране клетки, в цитоплазме, или на ядерной мембране и на других органеллах клетки.
Функции рецептора: (1) «узнавание» гормона; (2) преобразование и передача сигнала Строение рецептора: метаботропный рецептор, содержит 3 домена:
(1)сигнал-связывающий – выступает над мембраной. Содержит участок связывния гормона (по принципу лиганд-акцептор).
(2)трансмембранный – пересекет мембрану, у метаботропных – «серпантинный» (пересекает мембрану 7 раз, эффекторный д. сопряжен с G-белком – начальный эффектор-активирующий субстрат)
(3)эффекторный – находится в цитоплазме, активируется при связывании (1) с лигандом. Происходит изменение конформации рецептора -> запуск реакции.
ионотропные содержат субъединицу, связывающую сигнальную молекулу и ионный канал, трансмембранный домен – монотопный, не сопряжен с G-белком.
Гормоны белково-пептидной природы и биогенные амины вследствие своей гидрофильности не проникают через клеточные мембраны и воздействуют на мембранные рецепторы.
Стероидные и тиреоидные гормоны, обладающие липофильностью, наоборот, проникают в клетку и взаимодействуют с цитоплазматическими и ядерными рецепторами.
Таким образом, выделяют гормоны с мембранным и внутриклеточным механизмом действия.
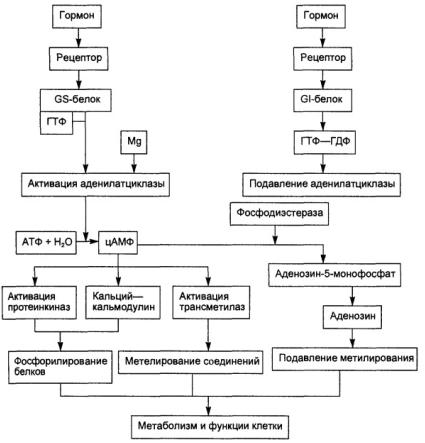
Мембранный
oАденилатциклазная система (Gs – активирующие – АКТГ-РГ, СТГ-РГ, глюкаког, АДГ, ЛГ, ФСГ,
ТТГ, хорион. ГТ, АКТГ, паратгормон, простагландины, бета-адренэргические катехоламины; Gi – ингибирующие – соматостатин, ангиотензин II, дофамин, альфа-2-адренэргические
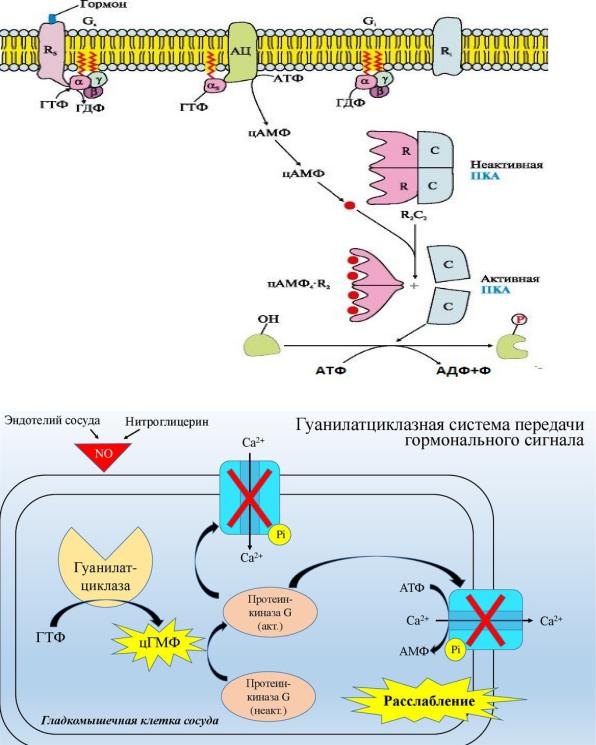
катехоламины)
oГуанилатциклазная система – предсердный натрий-уретически фактор, гистамин, NO
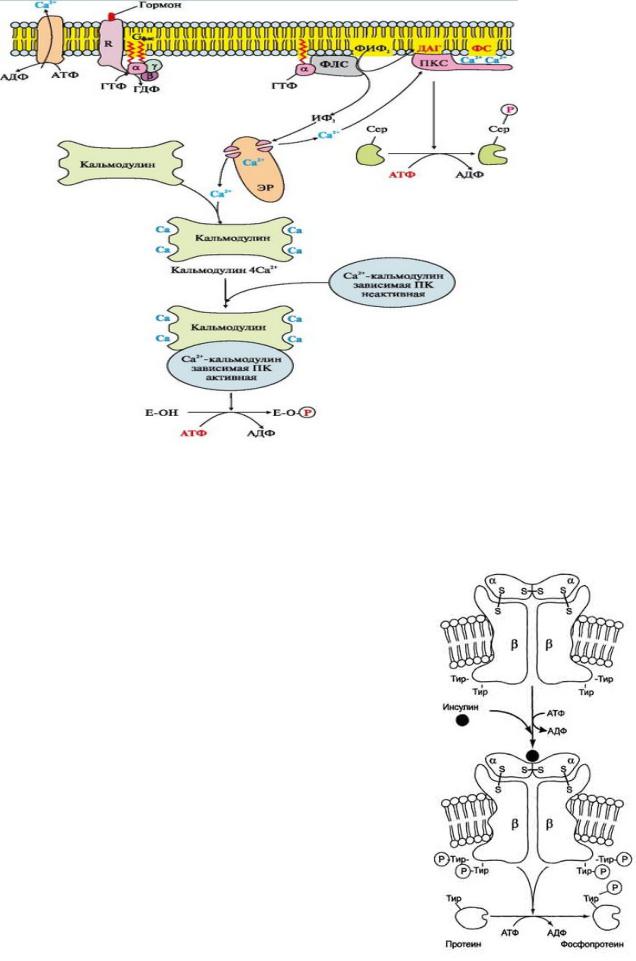
o Инозитолфосфатный механизм (Gq белки) – гонадолиберин, тиролиберин, дофамин, тромбоксаны А2, лейкотриены, паратгормон, брадикинин, вазопрессин
o Тирозин-киназный механизм – инсулин, ФР тромбоцитов, макрофагальный колониестимулирующий фактор
Присоединение инсулина в центр связывания, образованный а- субъединицами, вызывает кооперативные конформационные изменения рецептора. β-Субъединицы проявляют тирозинкиназную активность и катализируют трансаутофосфорилирование (первая β-субъединица фосфорилирует вторую β-субъединицу, и наоборот) по нескольким остаткам тирозина. Фосфорилирование приводит к изменению заряда, конформации и субстратной специфичности фермента (Тир-ПК). Тирозиновая-ПК фосфорилирует определенные клеточные белки, которые получили название субстратов рецептора инсулина (IRS 1). В свою очередь эти белки участвуют в активации каскада реакций фосфорилирования:
•фосфопротеинфосфатазы (ФПФ), которая дефосфорилирует специфические фосфопротеины;
•фосфодиэстеразы, которая превращает цАМФ в АМФ и цГМФ в ГМФ;
•ГЛЮТ 4 - переносчиков глюкозы в инсулинзависимых тканях, поэтому повышается поступление глюкозы в клетки мышц и жировой ткани;
•тирозиновой протеинфосфатазы, которая дефосфорилирует β- субъединицы рецептора инсулина;
• регуляторных белков ядра, факторов транскрипции, повышающих или снижающих экспрессию генов определенных ферментов.
Внутриклеточный
Для мембанных механизмов характерно: (1) один из этапов передачи сигнала – фосфорилирование белков; (2) прекращене активации происходит за счет механизмов, инициируемых самими участниками процессов.
Этапы передачи сигнала в клетку.
1)связывание сигнальной молекулы с рецептором;
2)активация рецептора;
3)синтез в клетке молекул, усиливающих сигнал в ответ на активацию рецептора;
4)активация ферментативных реакций в клетке;
5)ослабление сигнализации.
На каждом этапе возможны нарушения передачи сигнала, что является причиной развития ряда заболеваний. Причины нарушений:
Недостаточность гормона (гипосекреция)
Гиперсекреция гормона
Нарушения, связанные с рецепторным аппаратом клеток-мишеней
oНедостаточность синтеза белков-рецепторов
oГенетические дефекты белка-рецептора, приводящие к снижению сродства к гормонам
oБлокирование белков-рецепторов лигандами (например, антителами при аутоиммунных заболеваниях)
Факторы эффективности действия гормонов:
Концентрация гормона
Количество (и качество) рецепторов на мембране или в цитоплазме клетки-мишени
pH среды
Концентрация ионов
Присутствие лигандов, взаимодействующих с рецепторами

