
Нормальная физиология / КР4 кровь + эндокринка
.pdf
Вопрос 14. Гормоны поджелудочнои железы, их роль в регуляции углеводного, белкового и жирового обмена. Регуляция эндокриннои функции поджелудочнои железы.
Инсулин Инсулин — пептидный гормон, выделяющийсяиз В-клеток островков Лангерганса.
Структура. Инсулин представляет собой пептид, состоящий из двух цепей: А-цепь из 21 аминокислоты и В-цепь из 30 аминокислот связаны друг с другом через два дисульфидных мостика.
Место синтеза. Инсулин образуется в В-клетках островков Лангерганса. Среди клеток островков Лангерганса 80% составляют В-клетки, 15% приходится на А-клетки, синтезирующие глюкагон, и только небольшая часть клеток продуцирует соматостатин (D- клетки) или панкреатический полипептид. Инсулин, секретируемый поджелудочной железой, сначала попадает в воротную вену печени, где его концентрация многократно превышает таковую в периферической крови.
Регуляция секреции инсулина
Секреция инсулина прежде всего стимулируется повышением концентрации глюкозы и аминокислот в плазме крови, а также некоторыми гастроинтестинальными гормонами.
Регуляция синтеза субстратом. Синтез инсулина усиливается при повышении концентрации в плазме крови глюкозы, аминослот (прежде всего лейцина, а также аргинина и аланина),
ацетоуксусной кислоты и в меньшей степени жирных кислот.
Роль ионных каналов. Концентрация глюкозы в плазме служит, несомненно, наиболее важным регулятором секреции инсулина. Глюкоза отчасти действует через ионные каналы в клеточной мембране. Она поступает в клетку и распадается в ходе гликолиза. При этом образуется АТФ, который ингибирует АТФ-чувствительные калиевые каналы (К-АТФ-каналы) в клеточной мембране. Эти каналы необходимы для поддержания мембранного потенциала. Их ингибирование приводит к деполяризации, которая инициирует открывание кальциевых каналов. Последующее повышение внутриклеточной концентрации кальция приводит к стимуляции секреции инсулина.
■■■ Глюкокиназа, фосфорилирующая глюкозу и таким образом запускающая гликолиз, в В- клетках имеет очень низкую аффинность, ее полунасыщепие субстратом наблюдается только при концентрации глюкозы 10 ммоль/л. Поэтому образование АТФ и секреция инсулина достигают максимального значения только при очень высокой концентрации глюкозы (гораздо больше 10 ммоль/л).
Гиперкалиемия способствует выработке инсулина, а гипокалиемия тормозит его секрецию изза влияния концентрации К+ на уровень мембранного потенциала.
Ингибирование Катф независимо от глюкозы приводит к деполяризации клеточной мембраны и к выработке инсулина. Так действует сульфонилмочевина, которая за счет ингибирования канала Катф усиливает секрецию инсулина. Поэтому она используется как оральное антидиабетическое средство.
■■■ Фазы секреции инсулина. Продукция инсулина происходит пульсаторно. Если при потреблении глюкозы резко повышается ее концентрация в крови и затем сохраняются высокие абсолютные значения, то происходит двухфазная секреция инсулина: сначала быстрое транзисторное повышение секреции в течение 10 мин, затем вторичное возрастание
выделения гормона. Часть инсулииосодержащих везикул может экзоцитироваться сразу при повышении внутриклеточной концентрации кальция, в то время как другая часть должна быть подготовлена к освобождению. При стабильно высокой концентрации глюкозы секреция инсулина снова снижается примерно через 2-3 ч.
Стимуляция гастроинтестинальными и панкреатическими гормонами. Синтез инсулина стимулируется глюкозозависимым инсулинотропным полипептидом (GLP), глюкагоном, секретином, желудочным ингибиторным пептидом (G1P), гастрином, кортикотропином (АКТЕ) и соматотропином (действуют через инозитолтрифосфат), а также холецистокинином (действует через инозитолтрифосфат и диацил глицерол). Действие гормонов усиливает влияние глюкозы на секрецию инсулина, т. е. они сенсибилизируют В-клетки к глюкозе. При низкой концентрации глюкозы в плазме гормоны не действуют.
Усиленное действие гастроинтестинальных гормонов на секрецию инсулина наблюдается во время приема пищи: еще до всасывания питательных веществ в кишечнике и до повышения концентрации в плазме глюкозы и аминокислот, секреция инсулина повышается. Поэтому при пероральном приеме глюкозы она значительно сильнее, чем при внутривенном введении.
Торможение секреции инсулина. Секреция инсулина затормаживается соматостатином, амидином и панкреастатином. Соматостатин образуется и секретируется в близлежащих D- клетках островков Лангерганса. Его секреция стимулируется глюкозой, аминокислотами, жирными кислотами, ацетилхолином, адреналином (через р-рецепторы), глюкагоном, вазоактивным интестинальным пептидом (ВИП), секретином и холецистокинином.
Регуляция вегетативной нервной системой. Ацетилхолин стимулирует секрецию инсулина путем активации деполяризующих натриевых каналов. Симпатическая система тормозит секрецию инсулина за счет норадреналина (через α2-рецепторы) и комедиатора галанина, также участвующего в процессе. Они, но крайней мере, частично действуют через активацию калиевых каналов, которые гиперполяризуют клетку. Селективная активация постсин. β2рецепторов стимулирует выделение глюкагона, паракринно усиливающего секрецию инсулина, из соседних А-клеток.
Действие инсулина
Основное действие инсулина заключается в накоплении энергии в случае, если наблюдается избыток энергетических субстратов (например, глюкозы).
Метаболические эффекты. Действие инсулина нацелено на накопление энергетических субстратов: инсулин стимулирует потребление клетками (прежде всего мышечными и жировыми) глюкозы, аминокислот и жирных кислот. Потребление глюкозы клетками, в частности, стимулируется усиленным встраиванием в клеточную мембрану глюкозного транспортера, GLUT4. Инсулин способствует разрушению триглицеридов в хиломикронах и ЛПОНП крови. Образующиеся при этом свободные жирные кислоты и глицерин под воздействием инсулина поступают в жировую ткань и там снова накапливаются. Инсулин стимулирует образование гликогена и синтез белков, но в тоже время тормозит липолиз, гликогенолиз, протеолиз и глюконеогенез. С другой стороны, инсулин стимулирует гликолиз.
Действие на внутриклеточный транспорт. Действие инсулина отчасти связано с активацией
Na+/H+-oбменника и Na+,K+,2Cl- -котранспортера в клеточной мембране. Активность обоих переносчиков приводит к набуханию клеток, что, по крайней мере в печени, ингибирует распад макромолекул (гликогена и белков). Активация Na+/H+-обменника далее приводит к клеточному алкалозу. Поскольку оптимальный pH главных ферментов гликолиза находится в щелочной области, инсулин стимулирует гликолиз за счет вызываемого им алкалоза. Натрий, проникающий в клетку через Na+/H+-обменник и Na+,K+2Cl- -котранспортер, выкачивается из клетки с помощью Na+/K+-АТФазы в обмен на К+.

Следствием активации Na+,К+,2Cl- -котранспортера и Nа+/К+-АТФазы является поступление в клетку К+. Связывание фосфата с глюкозой, поступающей в клетку, также приводит к потреблению фосфата. Наконец, инсулин стимулирует попадание в клетку Mg2+. Наряду с этим повышается всасывание Na+ в почках через стимуляцию эпителиального натриевого канала.
Действие на силу сердечных сокращений и клеточное деление. Инсулин повышает мощность сердца. Он стимулирует деление клеток и участвует в ростовых процессах.
Инсулин и старение. Активация фосфатидил-инозитол-(РI) 3-киназного пути с помощью инсулина, по-видимому, играет важную роль при старении. Торможение этого действия увеличивает продолжительность жизни у многих видов животных, возможно, и у человека.
Гпюкагон
Основной задачей глюкагона является обеспечение энергетических субстратов при гипогликемии или повышенных затратах энергии.
Секреция. Глюкагон — это пептид, образующийся в А-клетках островков Лангерганса поджелудочной железы и в клетках тонкого кишечника из белка-предшественника (препроглюкагона). От энтерального проглюкагона также отщепляется глюкагоноподобный пептид GLP1. Секреция глюкагона стимулируется развитием гипогликемии, повышением концентрации аминокислот и снижением концентрации свободных жирных кислот. Кроме того, выделению глюкагона способствуют ацетилхолин, адреналин (β-рецепторы) и гастроинтестинальные гормоны. Секрецию ингибируют у-аминомасляная кислота и соматостатин.
Действие. Действие глюкагона сначала направлено на мобилизацию субстратов энергии. Глюкагон стимулирует гликогенолиз, липолиз, образование кетоновых тел из жирных кислот, распад белков и глюконеогенез из аминокислот. Инсулин и глюкагон, таким образом, действуют антагонистически. При введении аминокислот секреция обоих гормонов препятствует изменению концентрации глюкозы в плазме и свободных жирных кислот в крови. Другие эффекты глюкагона включают увеличение сердечного выброса (в очень высокой концентрации), а также рост скорости клубочковой фильтрации в почках.
Недостаток глюкагона. Возникает при повреждении поджелудочной железы. Однако в этом случае более серьезные последствия вызывает одновременно развивающийся дефицит инсулина.
Изолированный дефицит глюкагона не приводит к серьезным нарушениям, так как он может компенсироваться секрецией гормонов-агонистов (в том числе адреналином) и снижением выделения инсулина.
Избыток глюкагона. Избыток из-за опухоли А-клеток встречается редко. Он требует повышенной секреции инсулина и может привести к его относительному недостатку.


(постголод, нарушение пищеварения) недостаточная секреция инсулина приводит к дефициту содержания К и фосфатов, как при сахарном диабете.
Реалиментация стимулирует выработку инсулина у пациентов, в ряде случаев вызывая опасную для жизни гиперкалиемию и гиперфосфатемию. Реалиментации нередко подвержены пациенты, страдающие от алкоголизма. Алкоголь не стимулирует секрецию инсулина и при питании исключительно алкоголем возникает недостаток инсулина, как при голодании.
ДОПОЛНИТЕЛЬНО:
PP-клетки – панкреатический полипептид – торможение секреции желудочного и панкреатического соков
эпсилон-клетки (Е-клетки) – секреция грелина, гормона голода

1 СРС. Гемоглобин, его функции и соединения (физиологические и патологические)
Гемоглобин – это гемопротеин с молекулярной массой около 60 тыс. Да, окрашивающий эритроцит в красный цвет (является пигментом) после связывания молекулы кислорода с ионом железа +2. НОРМА: Ж 120-140 г/л, М 130-160 г/л
**основной дыхательный пигмент эритроцитов, способный нестойко связываться с кислородом и углекислым газом, что обеспечивает эритроцитам выполнение их основной функции — газообмена.
Молекула гемоглобина состоит из белковой части – глобина (из полипептидных цепей) и небелковой части – 4 субъединиц гема – порфирин с ионом железа.
*синтез гема протекает в митохондриях эритробластов; синтез глобина – на полирибосомах, контролируется генами 11 и 16 хромосом.
Функции гемоглобина:
1.Транспортная – транспорт углекислого газа (23%) из тканей в легкие и кислорода из легких в органы;
2.Дыхательная;
3.Буферная – поддержание кислотно-основного равновесия, pH крови;
4.Влияет на форму и размер эритроцитов и их способность к деформации;
5.Регуляция кровотока и давления крови (оксид азота NO, вырабатываемый эндотелиоцитами, связывается с гемоглобином; при определенных условиях гемоглобин высвобождает NO, что вызывает вазодилатацию путем расслабления гладкой мускулатуры сосудов. Расширение сосудов усиливает снабжение кислородом клеток рядом с местом выделения NO).
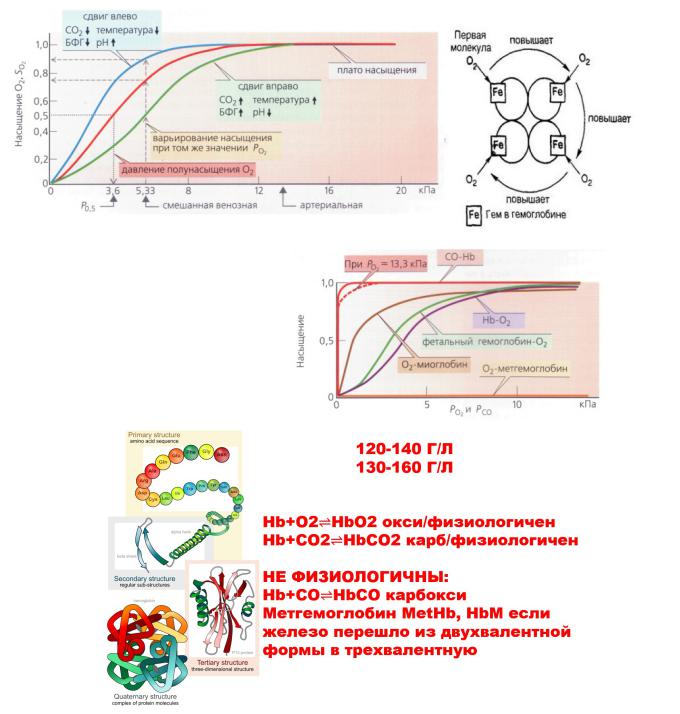
КООПЕРАТИВНОСТЬ
КИСЛОРОД СВЯЗЫВАЕТСЯ С ГЕМОГЛОБИНОМ, ОКСИГЕНАЦИЯ ПРИВОДИТ К СДВИГУ ОДНОГО ABДИМЕРА НА 15 ГРАДУСОВ ПО ОТНОШЕНИЮ К ДРУГОМУ AB-ДИМЕРУ. ЭТО ВАЖНО, ПОСКОЛЬКУ ЭТА СТРУКТУРНАЯ ПЕРЕСТРОЙКА ОПРЕДЕЛЯЕТ ПОВЕДЕНИЕ ГЕМОГЛОБИНА ПО СВЯЗЫВАНИЮ КИСЛОРОДА.
ПОСЛЕ ПРИСОЕДИНЕНИЯ ПЕРВОЙ МОЛЕКУЛЫ КИСЛОРОДА СВЯЫЗЫВАНИЕ ПОСЛЕДУЮЩИХ ОБЛЕГЧАЕТСЯ/ФАСИЛИЦИРУЕТСЯ
Виды гемоглобина:
А-тип (adult – взрослый, HbA) состоит из 2 альфа и 2 бета цепей. 1 г гемоглобина А связывает 1,34 мл кислорода + фенотип HbA2 2 альфа, 2 дельта (2%).
Эмбриональные гемоглобины типа Gower I (4 эпсилон цепи, HbE) и Gower II (2 альфа и 2 эпсилон цепи) – в первые 3 месяца жизни плода.
Гемоглобин F (faetus – плод, HbF) фетальный – 2 альфа и 2 гамма цепи. Сродство к кислороду на 20-30 % больше, чем у взрослого гемоглобина. БОЛЕЕ АФИНЕН К
КИСЛОРОДУ. НЕУСТОЙЧИВ ПРИ ПЕРЕПАДАХ рН, ИЗМЕНЕНИЯХ ТЕМПЕРАТУРЫ
МУТАНТНЫЕ ФОРМЫ ГЕМОГЛОБИНА:
Гемоглоби́н S (HbS) — это особая мутантная форма гемоглобина, образующаяся у больных с серповидноклеточной анемией и склонная к кристаллизации вместо образования нормальной четвертичной структуры и растворения в цитоплазме эритроцита. В гемоглобине S имеется единичная аминокислотная замена по сравнению с нормальным гемоглобином Α: L-глутаминовая кислота в 6-й позиции β-цепи глобина замещена на L-валин. Поскольку валин имеет неполярный радикал, располагающийся на поверхности молекулы, в результате этой замены растворимость гемоглобина резко падает.
Hb C – в 6-м положении бета-цепи глутаминовая кислота замещена на лизин. Форма снижает пластичность ЭЦ, у гомозигот по мутации – гемолитическая анемия, у гетерозигот 28-44 % мутантные, но анемия не развивается. Кристаллизуется.
Соединения гемоглобина Физиологические:
1. Оксигемоглобин – соединение с кислородом.
Сродство гемоглобина к кислороду и диссоциация оксигемоглобина зависят от напряжения = парциального давления (P) кислорода, углекислого газа в крови, pH крови, ее температуры и концентрации 2,3-дифосфоглицерата в эритроцитах. Сродство повышают увеличение P кислорода, снижение P углекислого газа в крови, нарушение образования 2,3-ДФГ в эритроцитах. Повышение концентрации 2,3-ДФГ, снижение P кислорода и повышение P углекислого газа, закисление среды, повышение температуры крови снижают сродство гемоглобина к кислороду, тем самым облегчая его отдачу в ткани.
*2,3-ДФГ связывается с бета цепями гемоглобина, облегчая отсоединение кислорода от гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах.
2.Карбогемоглобин – соединение с углекислым газом.
3.Восстановленный = дезоксигемоглобин – оксигемоглобин, отдавший кислород.
ОКСИ-КОНФОРМАЦИЯ: НАПРЯЖЕННАЯ ДЕЗОКСИ: РАССЛАБЛЕННАЯ – БЕЗ КИСЛОРОДА
Патологические:
1.Карбоксигемоглобин – соединение с угарным газом. Очень прочное! Лишает гемоглобин возможности присоединять кислород.
2.Метгемоглобин – вариант гемоглобина, который образуется при переходе двухвалентного железа в трехвалентное. В результате гем утрачивает способность связываться с кислородом и транспортировать кислород в ткани, что приводит к развитию гипоксии.
*содержание гемоглобина в отдельном эритроците составляет 27,5-33,2 пикограмма. Снижение этой величины - гипохромное (пониженное) содержание гемоглобина, увеличение – о гиперхромное (повышенное) содержание гемоглобина. Гиперхромия – при В12-дефицитной анемии, гипохромия – при железодефицитной анемии.
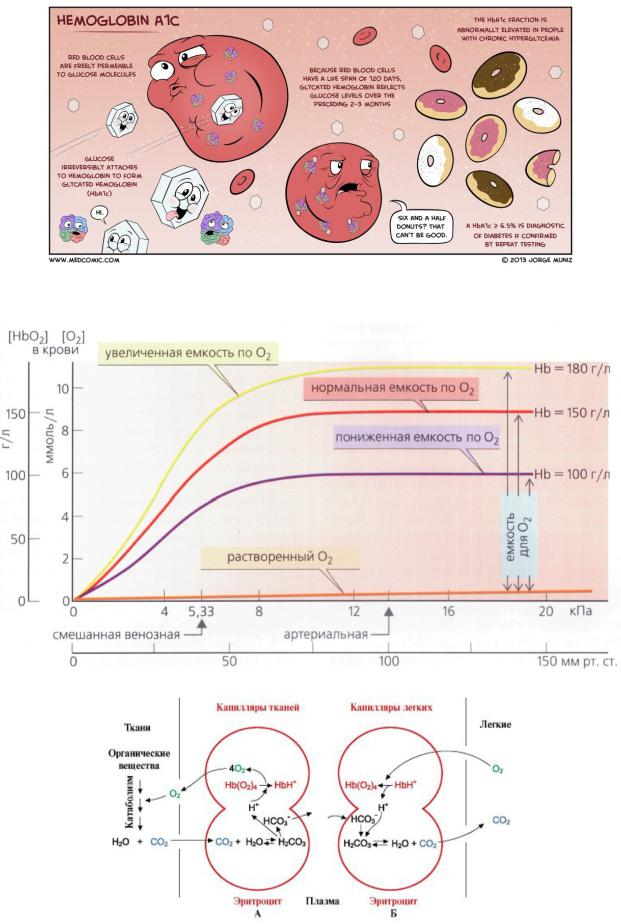
ГЛИКИРОВАННЫЙ ГЕМОГЛОБИН (4%)
КИСЛОРОДНАЯ ЁМКОСТЬ КРОВИ
ГЕМОГЛОБИН:БУФЕР
