
- •1.01. Кинематика поступательного и вращательного движения формулы
- •Примеры решения задач
- •1.02. Динамика поступательного движения формулы
- •Примеры решения задач
- •1.03. Закон сохранения импульса тела. Столкновения частиц формулы
- •Примеры решения задач
- •1.04. Закон сохранения энергии формулы
- •Примеры решения задач
- •1.05. Динамика вращательного движения формулы
- •Примеры решения задач
- •1.06. Гармонические колебания формулы
- •Дополнительно. Волны в упругой среде. Акустика
- •Примеры решения задач
- •1.07. Уравнение состояния идеального газа. Молекулярно-кинетическая теория формулы
- •Примеры решения задач
- •1.08. Первое начало термодинамики формулы
- •Примеры решения задач
- •Список используемой литературы
- •Введение
- •Рекомендации по решению задач
- •Требования к оформлению
- •Критерии и шкала оценивания устной защиты решения задач
1.07. Уравнение состояния идеального газа. Молекулярно-кинетическая теория формулы
Количество вещества:
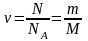 ,
,
здесь N – количество частиц (молекул или атомов), NA = 6,022∙1023 моль–1 – постоянная Авогадро, m – масса вещества, M – молярная масса (масса одного моля вещества);
Масса одной молекулы или одного атома:
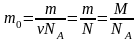 ;
;
Средняя кинетическая энергия теплового движения молекул:
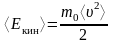 ,
,
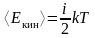 ,
,
здесь
 – среднее значение квадрата скорости
молекул (средняя квадратичная скорость),
k
= 1,38∙10–23
Дж∙К–1
– постоянная Больцмана, T
– термодинамическая (абсолютная)
температура, i
– число степеней свободы;
– среднее значение квадрата скорости
молекул (средняя квадратичная скорость),
k
= 1,38∙10–23
Дж∙К–1
– постоянная Больцмана, T
– термодинамическая (абсолютная)
температура, i
– число степеней свободы;
Среднее значение квадрата скорости молекул (средняя квадратичная скорость):
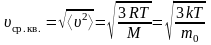 ,
,
здесь R = NA∙k = 8,31 Дж∙моль–1∙К–1 – универсальная газовая постоянная (молярная газовая постоянная);
Средняя арифметическая скорость молекул:
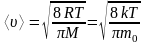 ;
;
Наиболее вероятная скорость молекул:
 ;
;
Уравнение состояния идеального газа:
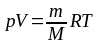 ;
;
Давление газа:
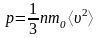 ,
,
 ,
,
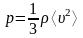 ,
,
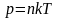 ,
,
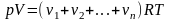 ,
,
здесь n = N/V – концентрация молекул, V – объём, занимаемый газом, ρ – плотность газа.
Закон Дальтона:
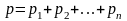 :
:
здесь p – давление смеси газов, pi – парциальное давление i-го компонента смеси;
Изопроцессы:
Изотермический процесс: T = const, p1V1 = p2V2;
Изобарический процесс: p = const, V1T2 = V2T1;
Изохорический процесс: V = const, p1T2 = p2T1.
Барометрическая формула (распределение давления в однородном поле силы тяжести и распределение частиц в однородном силовом поле, соответственно):
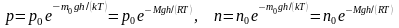 ,
,
здесь p – давление на высоте h, n – концентрация молекул на высоте h, p0, n0 давление и концентрация частиц на уровне моря (h = 0), m0 – масса одной молекулы, M – молярная масса, g – ускорение свободного падения, k – постоянная Больцмана, T – термодинамическая (абсолютная) температура, R – универсальная газовая постоянная;
Распределение Максвелла (распределение молекул по скоростям):
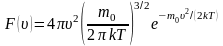 ,
,
здесь ʋ – скорость молекулы;
Число молекул, скорости которых заключены в пределах от ʋ до ʋ + dʋ:
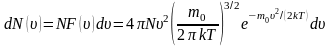 ,
,
здесь N – общее число молекул;
Среднее число соударений, испытываемых одной молекулой газа в единицу времени:
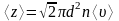 ,
,
здесь d – эффективный диаметр молекулы, n – концентрация молекул, ‹ʋ› – средняя арифметическая скорость молекул;
Среднее длина свободного пробега:
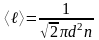 ;
;
Импульс, переносимый молекулами из одного слоя в другой через элемент поверхности:
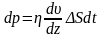 ,
,
здесь η – динамическая вязкость газа, dʋ/dz – градиент (поперечный) скорости течения его слоев, ΔS – площадь элемента поверхности, dt – время переноса;
Динамическая вязкость:
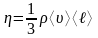 ,
,
здесь ρ – плотность газа;
Вязкое трение:
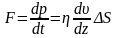 ,
,
здесь F – сила внутреннего трения между движущимися слоями газа;
Закон Фурье:
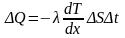
здесь ΔQ – теплота, прошедшая посредством теплопроводности через сечение площадью ΔS за время Δt, λ – теплопроводность, dT/dx – градиент температуры;
Теплопроводность (коэффициент теплопроводности) газа:
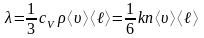 ,
,
здесь cV – удельная теплоемкость газа при постоянном объеме;
Закон Фика:
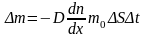 ,
,
здесь Δm – масса газа, перенесенная в результате диффузии через сечение площадью ΔS за время Δt, D – коэффициент диффузии, dn/dx – градиент концентрации молекул;
Диффузия (коэффициент диффузии):
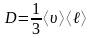 .
.
