
- •Введение
- •Оформление работы:
- •1. Дата.
- •2. Тема: номер и название работы.
- •Организация учебного процесса по биохимии
- •Правила техники безопасности при работе в биохимической лаборатории
- •Тема 1. Реакция среды
- •Работа 1. Определение реакции среды молока и яйца с помощью универсальной индикаторной бумаги
- •Работа 2. Определение реакции среды бесцветных растворов с помощью прибора Михаэлиса
- •Работа 3. Определение рН гомогената мышечной ткани, раствора яичного белка с помощью прибора Михаэлиса Приготовление гомогената из тканей животных
- •Ход опыта
- •Лучи света
- •Матовое стекло
- •Работа 4. Определение рН растворов и биологического материала электрометрическим (потенциометрическим) методом
- •Вопросы для самоподготовки по теме 1
- •Тема 2. Буферные системы
- •Работа 5. Приготовление ацетатного буферного раствора и изучение зависимости величины рН от соотношения компонентов
- •Работа 6. Изучение действия на буферный раствор небольшого количества кислоты
- •Работа 7. Изучение действия на буферный раствор большого количества кислоты
- •Работа 8. Изучение действия небольшого количества щелочи на буферный раствор
- •Работа 9. Изучение действия на буферный раствор большого количества щелочи
- •Работа 10. Влияние разбавления водой буферного раствора на величину его рН
- •Вопросы для самоподготовки по теме 2
- •Тема 3. Коллоидные растворы
- •Работа 11. Получение гидрофобного коллоидного раствора гидроксида железа Fe(oh)3.
- •Работа 13. Диализ коллоидных растворов
- •Работа 14. Изучение механизма коагуляции золя железа
- •Работа 15 . Изучение защитного действия гидрофильных коллоидов (эмульсоидов)
- •Вопросы для самоподготовки по теме 3
- •Tеma 4. Адсорбция и абсорбция
- •Работа 16. Адсорбция органических красок животным углем
- •Работа 17. Определение количества уксусной кислоты, адсорбированной животным углем
- •Вопросы для самоподготовки по теме 4
- •Тема 5. Химия и обмен белков
- •Работа 18. Определение количества белка в гомогенате мышечной ткани, яйце рефрактометрическим методом
- •Работа 19. Определение белка по методу Лоури
- •Работа 20. Разделение смеси аминокислот методом распределительной хроматографии на бумаге
- •Работа 21. Определение количества аминокислот в биоматериале по азоту аминогрупп методом формольного титрования по Серенсену
- •Работа 22. Изучение действия пепсина на переваривание белка
- •Вопросы для самоподготовки по теме 5
- •Тема 6. Ферменты (энзимы)
- •Работа 23. Приготовление раствора фермента -амилазы (кф 3.2.1. 1) слюны
- •Работа 24. Обнаружение в слюне амилазы и определение специфичности ее действия
- •Работа 25. Изучение влияния рН среды на активность амилазы слюны
- •Работа 26. Изучение влияния температуры на активность энзимов
- •Работа 27. Изучение действия активаторов и ингибиторов на активность ферментов
- •Вопросы для самоподготовки по теме 6
- •Тема 7. Углеводы и их обмен
- •Работа 28. Изучение механизма переваривания углеводов и определение активности -амилазы (кф 3.2.1.1.) слюны
- •Работа 29. Обнаружение гликогена в тканях животных
- •Вопросы для самоподготовки по теме 7
- •Тема 8. Липиды и их обмен
- •Работа 30. Изучение растворимости жира
- •Работа 31. Определение кислотного числа жира
- •Работа 32. Определение йодного числа.
- •Работа 33. Исследование эмульгирования жира
- •Работа 34. Изучение механизма переваривания липидов и определение активности панкреатической липазы (кф 3. 1. 1. 3)
- •Работа 35. Реакция обнаружения холестерола в растительном и животном маслах.
- •Вопросы для самоподготовки по теме 8
- •Тема 9. Витамины
- •Работа 36. Обнаружение витамина а в жире
- •Работа 37. Обнаружение витамина д в жире
- •Работа 38. Обнаружение витамина с в биоматериале
- •Вопросы для самоподготовки по теме 9
- •Тема 10. Минеральные вещества и вода
- •Работа 39. Определение количества кальция в молоке и гомогенате мышечной ткани по де Ваарду
- •Работа 40. Определение содержания кальция в молоке и гомогенате мышечной ткани комплексонометрическим методом
- •Работа 41. Определение количества неорганического фосфора в молоке и гомогенате мышечной ткани
- •Вопросы для самоподготовки по теме 10
- •Тема 11. Молоко
- •Работа 42. Определение общей кислотности молока по Тернеру
- •Работа 43 Выделение казеиногена из молока и исследование его свойств.
- •Работа 44. Определение редуктазы молока
- •Работа 45. Определение количества лактозы в молоке с помощью рефрактометра
- •Вопросы для самоподготовки по теме 11
- •Рекомендуемая литература.
Ход опыта
Взять гомогенат мышечной ткани и выполнить с ним все необходимое согласно 1-му этапу работы 2. При выполнении 2-го этапа для устранения искажающего влияния окраски или мутности в гнезда компаратора ставят пробирки согласно схеме (рис. 1.). Остальное, в том числе нахождение величины рН, делается как и в работе 2.
Лучи света
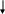
Матовое стекло







г лаза
наблюдателя
лаза
наблюдателя
Рис. 1.
Задание: определить рН гомогената мышечной ткани с универсальным и основным индикаторами и сделать вывод о его реакции.
Работа 4. Определение рН растворов и биологического материала электрометрическим (потенциометрическим) методом
Метод основан на измерении э.д.с. растворов и переводе ее значения с помощью рН-метра (потенциометр) в величину рН. Этим методом можно определить рН любых растворов (сильноокрашенных, сильномутных, вязких — раствора яичного белка, молока, коллоидов), а также гомогенатов растительных и животных тканей при температуре от 0°С до + 100°С.
Используют различные рН-метры (ЛПУ-01, рН-121, рН-340 и др.). Точность метода до 0,01 и выше (зависит от цены деления).
Ход опыта
Включить рН-метр ЛПУ-01 в сеть и прогреть 30 мин. В стаканчик налить исследуемый раствор (в чашку положить гомогенат) и, погрузив электроды, поставить на столик датчика. Тумблер «виды работ» поставить в положение «рН», а переключатель «пределы измерений» - в положение «-214». По показанию термометра установить тумблер «температура» соответственно температуре исследуемого раствора. Записать показания стрелки прибора по нижней шкале рН (-214), которая считается шкалой грубой настройки. Затем тумблер «пределы измерений» поставить в положение, соответствующее значению рН, найденному по нижней шкале. После установки неподвижно стрелки прибора записать величину рН по верхней шкале (точная настройка), прибавив ее показания, например, 1,15 -к первой цифре найденного «предела измерений», например «6», если был выбран «предел измерений» 610. Следовательно, 6 + 1,15 = 7,15 — это и есть рН исследуемого раствора.
Задание: 1. Определить рН молока, мышц, яйца и сделать вывод о реакции среды объекта.
2. Сравнить найденные в опыте значения рН для молока, гомогената мышц и раствора яичного белка и желтка яйца с их нормативными значениями.
Вопросы для самоподготовки по теме 1
1. Понятие о сН и рН, единицы измерения.
2. Ионное произведение воды, константа диссоциации. Вывод формул. Взаимосвязь сН и сОН, рН и рОН.
3. Характеристика реакции среды но величине сН и рН: кислая, нейтральная, щелочная.
4. Колориметрический метод определения рН. Его сущность, разновидности, точность; применение в товароведении. Прибор Михаэлиса.
5. Электрометрический метод определения рН - сущность, точность, применяемый прибор, использование в практике.
6. Величина рН молока, мяса, яйца.
7. Биологическая роль и регуляция реакции среды в организме животных.
Тема 2. Буферные системы
В организме животных и человека с кормами и продуктами питания поступают, а так же образуются в процессе обмена веществ значительное количество кислых и щелочных продуктов, однако, значение рН биологических жидкостей и тканей организма характеризуется значительной устойчивостью и постоянством.
Так, например, рН крови различных млекопитающих и птиц - 7,2 - 7,5; рН крови лягушки - 7,8 ;
рН мяса:
1) у отдохнувших животных – 6,6 – 7,0;
2) после убоя – 5,4 – 5,5;
3) у утомленных животных – 5,1 – 5,6;
4) в мышцах кур – 5,8 – 5,9;
рН свежего молока – 6,68;
рН яичного белка – 7,8;
рН яичного желтка – 5,9.
В регуляции реакции среды участвует весь организм животного в целом. Большая роль в этом процессе принадлежит так называемым буферным системам. Буферные системы представляют собой в большинстве случаев смесь слабой кислоты и ее соли, образованной сильным основанием, или смесь слабого основания и его соли, образованной сильной кислотой.
Буферные системы способны противодействовать изменению рН раствора при добавлении кислоты или щелочи, а также при разбавлении раствора.
Механизм действия буферной системы рассмотрим на примере ацетатной буферной смеси, состоящей из уксусной кислоты СН3СООН и уксуснокислого натрия СH3COONa.
Если к такой системе добавить немного сильной кислоты НСl, то анионы СН3СОО- будут связывать водородные ионы в слабодиссоциирующие молекулы уксусной кислоты:
СНзСООNа + НСl = СНзСООН + NaCl,
что можно представить в ионном виде:
СН3СОО- + Н+ = СНзСООH.
Поэтому концентрация водородных ионов (pH) в буферном растворе остается почти неизменной.
При добавлении небольшого количества щелочи (например, NaOH) к той же буферной системе происходит реакция нейтрализации между уксусной кислотой и NaOH:
СНзСООН + NaOH = CH3COONa + Н2О;
или в ионном виде:
H+ + OH- = H2O
Казалось бы, что в результате удаления из раствора ионов Н+ кислотность его должна уменьшиться, но этого практически не происходит, так как уменьшение концентрации водородных ионов в растворе вызывает сдвиг равновесия реакции диссоциации слабой уксусной кислоты в сторону распада ее на ионы:
С НзСООН СН3СОО- + Н+
В результате этого количество водородных ионов вновь пополняется, и значение рН раствора заметно не изменяется.
Таким образом, при добавлении кислоты к буферному раствору концентрация водородных ионов (рН) будет сохраняться в нем почти неизменной до тех пор, пока не окажется связанной вся соль; при добавлении щелочи рН не изменится до тех пор, пока не будет израсходована вся кислота буферной смеси. После этого буферное действие прекращается и при дальнейшем прибавлении кислоты или щелочи наступает резкое изменение рН раствора. Чем выше концентрация кислоты и соли в буферном растворе, тем дольше он противостоит изменению рН, тем больше его буферная емкость.
(Буферная емкость измеряется количеством грамм-эквивалентов кислоты или щелочи, которое необходимо добавить к 1 л буферного раствора, чтобы изменить его рН на единицу).
При разбавлении раствора водой соотношение компонентов не изменяется и рН буферного раствора остается постоянным.
