
Нормальная физиология / КР6 Сосудистая система, регуляция кровообращения
.pdf
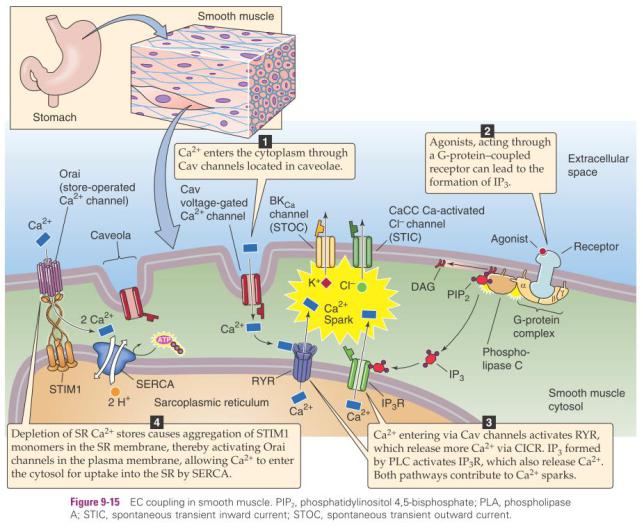
РЕГУЛЯЦИЯ МЫШЕЧНОГО СОКРАЩЕНИЯ В ГЛАДКИХ МЫШЦАХ. ВЗАИМОДЕЙСТВИЕ АКТИНА И МИОЗИНА.
Пусковой стимул – входящий ток кальция. НО! в гладких мышцах нет тропонина,
вместо которого – большое кол-во кальмодулина.
(не перевод картинки)
1.Ca(2+) с кальмодулином образует кальмодулин-кальцией комплекс;
2.кальмодулин-кальциевый комплекс активирует миозинкиназу;
3.миозинкиназа фосфорилирует легкие цепи миозина;
4.конформация «головки» миозина изменяется и приобретает АТФазную ктивность (увеличение активности миозиовой АТФазы позволяет связывать актин);
5.миозин связывается с актином (может образоваться множество мостиков – тонус) -> скольжение -> цикл сокращения.
6.Фосфатаза дефосфорилирует головки миозина – происходит разрыв мостика.
NB: молекула АТФ разрывает акто-миозиновый мостик
Молекулы актина заякорены на плотных тельцах – dense bodies (они выполняют роль Z- диска саркомеров)
сила сокращения мышцы прямо пропорциональна внутриклеточной концентрации кальция
ФАРМАКО-МЕХАНИЧЕСКОЕ СОПРЯЖЕНИЕ –
активация сократительных белков без изменения величины МП, посредством воздействия сигнальных молекул на мембранные рецепторы. Увеличение входа внеклеточного кальция.
|
АГОНИСТ |
|
|
|
ЭФФЕКТ |
|
|
|
РЕЦЕПТОР |
|
|
|
ВТОРИЧНЫЙ |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
ПОСРЕДНИК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
АНГИОТЕНЗИН |
|
|
|
СОКРАЩЕНИЕ |
|
|
|
АТ II РЕЦЕПТОР |
|
|
|
IP3 (Gq) |
|
|
II |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
ВАЗОПРЕССИН |
|
|
|
СОКРАЩЕНИЕ |
|
|
|
РЕЦЕПТОР |
|
|
|
IP3 (Gq) |
|
|
|
|
|
|
|
|
|
|
ВАЗОПРЕССИНА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
ЭНДОТЕЛИН |
|
|
|
СОКРАЩЕНИЕ |
|
|
|
РЕЦЕПТОР |
|
|
|
IP3 (Gq) |
|
|
|
|
|
|
|
|
|
|
ЭНДОТЕЛИНА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
АДЕНОЗИН |
|
|
|
РЕЛАКСАЦИЯ |
|
|
|
РЕЦЕПТОР |
|
|
|
cAMP (Gi) |
|
|
|
|
|
|
|
|
|
|
АДЕНОЗИНА (А1) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
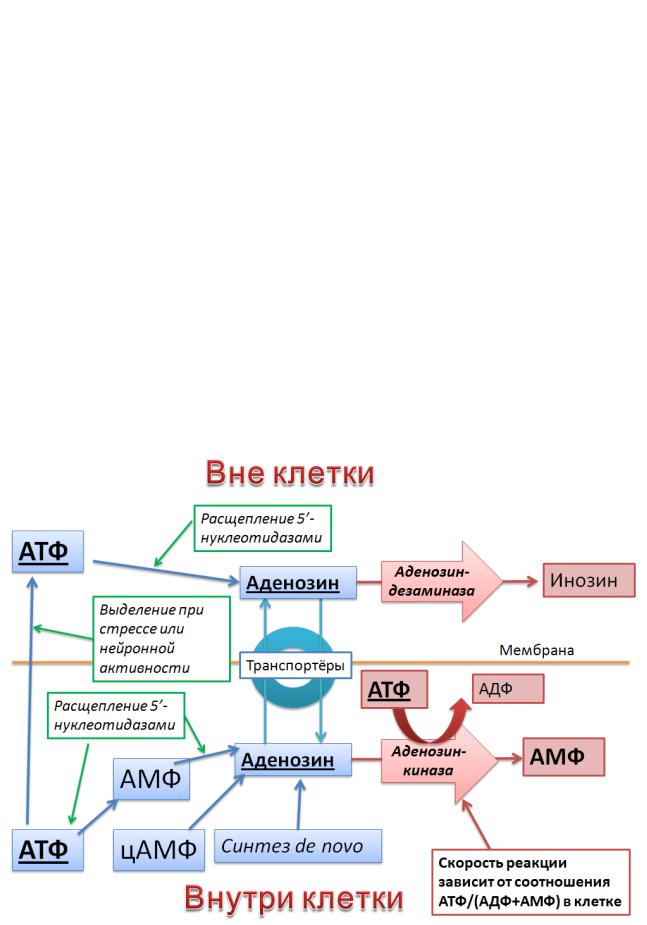
Функция аденозина как «сигнала усталости» напрямую следует из биохимии его образования и инактивации. Внутри клетки аденозин может образовываться несколькими путями: при расщеплении АТФ или АМФ ферментами 5′-нуклеотидазами, при разрушении цАМФ и, наконец, обычным синтезом «с нуля» (de novo). Основной способ его инактивации внутри клетки — присоединение фосфорильной группы ферментом аденозинкиназой. В этой реакции расходуется одна молекула АТФ, а «на выходе» получается по одной молекуле АДФ и АМФ
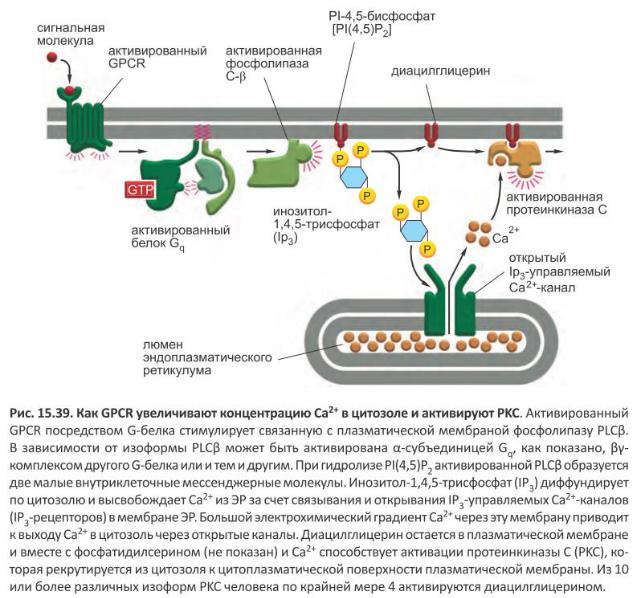
Аденозиновые рецепторы (GPCR, типы А1, А2А, А2В, А3). По структуре это горячо любимые нашим небольшим научным коллективом рецепторы, сопряженные с G-белком, или серпантинные рецепторы, или 7-трансмембранные рецепторы. Все эти три названия отражают их структурные особенности: это белки, пронизывающие мембрану клетки семью «стежками».
Внутри клетки они также образуют петлю, к которой прикреплен молекулярный «адаптер» — G-белок. Молекула, которая служит химическим сигналом , входит с внешней стороны в связывающий участок — щель между «стежками» рецептора, — что изменяет конформацию рецептора (в том числе и с внутренней стороны) и переключает G-белок в другое положение. А уж он запускает внутри клетки каскад биохимических изменений, в конечном итоге приводящих к тому или иному ответу.
Эндотелин — мощное сосудосуживающее вещество, которое выделяется из поврежденного сосудистого эндотелия. Эндотелиальные клетки выделяют также сосудосуживающие вещества. Самым важным из них является эндотелин — пептид, состоящий из 27 аминокислот. Чтобы вызвать мощную вазоконстрикцию, достаточно очень небольшого количества эндотелина (нескольких нанограммов). Это вещество присутствует в эндотелиальных клетках практически всех кровеносных сосудов, но количество эндотелина резко увеличивается при повреждении эндотелия сосудов в случае травмы тканей или после внутрисосудистого введения повреждающих химических веществ. После тяжелого повреждения сосудов местный выброс эндотелина и последующая вазоконстрикция способны остановить кровотечение из артерий диаметром до 5 мм.
Как полагают, повреждение эндотелия при гипертензии может привести к значительному выделению эндотелина и сужению сосудов. Для лечения легочной гипертензии (но не для снижения кровяного давления у пациентов с артериальной гипертонией!) назначают препараты, блокирующие рецепторы к эндотелину.

Вопрос 3. Базальный тонус сосудов. Феномен Бейлисса-Остроумова и релаксация напряжения
МЕХАНИЗМЫ РЕГУЛЯЦИИ МЕСТНОГО КРОВОТОКА
Регуляция местного кровотока может быть краткосрочной (кратковременной) и долгосрочной (долговременной).
Краткосрочная регуляция обусловлена быстрым, в течение нескольких секунд или минут, расширением (вазодилатацией) или сужением (вазоконстрикцией) артериол, метартериол и прекапиллярных сфинктеров, что обеспечивает необходимые изменения кровотока в тканях.
Долгосрочная регуляция осуществляется медленно, в течение нескольких дней, недель и даже месяцев. В целом долговременные изменения обеспечивают лучшую регуляцию кровотока в зависимости от потребностей ткани и связаны в основном с увеличением или уменьшением количества кровеносных сосудов, снабжающих ткани кровью.
БАЗАЛЬНЫЙ ТОНУС СОСУДОВ
Концентрация Са 2+ и базальный тонус сосудов. Базальный тонус сосудов определяется миогенным тонусом и активностью гладкомышечных клеток, зависимой от тканевых метаболитов. Из-за зависимости активности киназы легких цепей миозина от Са2+ - кальмодулина внутриклеточная концентрация ионов Са2+ играет важную роль в определении тонуса кровеносных сосудов. Мембранный потенциал гладкомышечных клеток находится в пределах от –40 до –60 мВ и близок к пороговому потенциалу потенциалзависимых кальциевых каналов, поэтому он оказывает значительное влияние на вход Са 2+ и его внутриклеточную концентрацию Таким образом, изменения мембранного потенциала, например вызванные открыванием K+ -каналов, напрямую выражаются в Са 2+ - опосредованном изменении тонуса гладкой мускулатуры сосудов. Наряду с мембранным потенциалом на внутриклеточную концентрацию Са 2+ влияет его вход по катионным каналам, активируемым рецепторами, и высвобождение кальция из саркоплазматического ретикулума, которое стимулируется агонистами. Кроме того, некоторые факторы, модулирующие базальный тонус сосудов, влияют на чувствительность к Са 2+, что является результатом изменения активности фосфатазы легких цепей миозина.

МИОГЕННЫЙ ТОНУС – ФЕНОМЕН БЕЙЛИСА-ОСТРОУМОВА
Механизм миогенной реакции. Увеличение трансмурального давления приводит к сокращению гладкой мускулатуры (эффект Бейлиса-Остроумова; миогенная реакция) в терминальных артериях и артериолах большинства сосудистых областей. Посредством этого сокращения, стимулированного растяжением, которое является основным механизмом ауторегуляции кровоснабжения в органах, кровоснабжение поддерживается при изменениях артериального давления прежде всего в почках и головном мозге.
Миогенная реакция обеспечивает поддержание постоянного давления фильтрации в капиллярах при ортостазе, который сопровождается повышением артериального давления в сосудах ног примерно на 80–90 мм рт. ст. и препятствует возникновению отеков.
Миогенная реакция. Молекулярные механизмы, участвующие в миогенной реакции, пока не до конца ясны. После механической стимуляции клетки путем растяжения происходит быстрая деполяризация с последующим открыванием потенциалзависимых кальциевых каналов. При последующем сокращении наряду с повышением тонуса, напрямую вызванным кальцием, важную роль играют различные механизмы Са2+ -сенсибилизации. К ним относятся сфиногозин-1-фосфат, активные формы кислорода и метаболиты арахидоновой кислоты, например 20-оксиэйкозатетраеновая кислота (20-НЕТЕ). Механочувствительный элемент, вызывает исходную деполяризацию, пока не идентифицирован. Наряду с различными неселективными катионными каналами семейства TRP, которые напрямую или косвенно активируются механизмами, связанными с G-белками, и внутриклеточными процессами трансдукции сигнала, описано участие и других структур, например каналов семейства К2Р (TRЕК-1 и ТRААК), каналов ЕNаC и каналов ClСа.


Вопрос 4. Нейрогенный тонус сосудов. Нервная регуляция тонуса сосудов.
Сосудодвигательные нервы:
СИСТЕМЫ КРАТКОСРОЧНОГО РЕГУЛИРОВАНИЯ.
СРАБАТЫВАЮТ ЗА СЕКУНДЫ, ТАК КАК ВКЛЮЧАЮТ ТОЛЬКО НЕРВНЫЕ ВЛИЯНИЯ НА СЕРДЦЕ И СОСУДЫ
Из методички кафедры:
Нервные влияния для микроциркуляторного русла не являются ведущими. Следует отметить, что большинство сосудов имеют только симпатическую адренергическую иннервацию. Выделяющийся из симпатических нервных норадреналин взаимодействует с α1- и β2-адренорецепторами сосудов. В покое по симпатическим нервам проходит примерно 4-5 имп./с. Эти нервные импульсы обеспечивают нейрогенный компонент сосудистого тонуса. Увеличение импульсации по симпатическим нервам (максимально до 10-12 имп./с) вызывает сужение сосудов. Расширение сосудов происходит при уменьшении симпатической импульсации до 1- 2 имп./с. Вместе с тем, в сосудах мышц нижних конечностей, а также потовых желез кожи обнаружены симпатические холинергические нервы, из которых выделяется ацетилхолин. Возбуждение указанных нервов вызывает расширение сосудов.
Парасимпатическая иннервация сосудов большого круга кровообращения практически отсутствует. Только в двух регионах - ротовая полость (chorda tympani - барабанная струна - веточка лицевого нерва), иннервирующая слюнные железы и зубы, и органах малого таза (n.pelvicus - тазовый нерв) обнаружены парасимпатические нервы, вызывающие вазодилатацию. Из этих нервных окончаний выделяется ацетилхолин, взаимодействующий с М-холинорецепторами эндотелия и гладких мышц и комедиатор – вазоактивный интестинальный пептид (ВИП). Под влиянием ацетилхолина эндотелий сосудов выделяет оксид азота (NO), который обладает мощным сосудорасширяющим эффектом. Но NO разрушается быстро, через 6-12 с, а ВИП – медленнее, поэтому на фоне стимуляции парасимпатических нервов в указанных регионах имеет место длительная вазодилатация. Кроме того, под влиянием ацетилхолина отмечена эндотелий независимая вазодилатация.
Нейрогенный тонус сосудов
Сохраняющееся активное напряжение, изометрически развиваемое гладкой мускулатурой сосудов, называют тонусом сосудов. Это напряжение находится в равновесии с силой растяжения, создаваемой артериальным давлением. Наряду с этой функцией гладкая мускулатура сосудов обладает функцией исполнительного элемента для регуляции кровоснабжения.
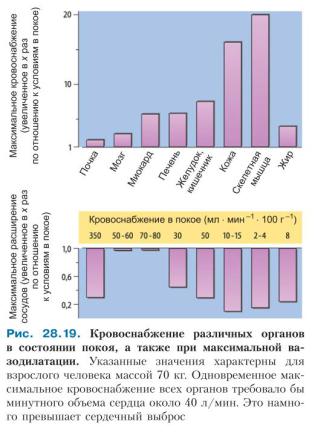
Обычно кровеносные сосуды находятся в определенном тонусе, т. е. всегда имеет место определенный уровень вазоконстрикции, который называют тонусом в покое. Тонус
впокое обусловлен двумя факторами.
Основную роль играет базальный тонус, который вызван локальными
влияниями в самой стенке сосуда или в непосредственной близости от нее.
Базовый тонус усиливается почти во всех областях кровоснабжения органов (за исключением плаценты и пупочных сосудов) посредством вазоконстрикторных стимулов симпатически-адренергических нервных волокон, окружающих кровеносные сосуды. Таким образом, нейрогенный тонус разных органов выражен
в различной степени.
Органы с высокими и относительно слабо изменяющимися требованиями к кровоснабжению (например, головной мозг и почки) характеризуются слабым симпатически-адренергическим тонусом сосудов, сосудистые области с сильно изменяющимися требованиями к кровоснабжению (скелетная мускулатура, желудочнокишечный тракт, печень и кожа), напротив, имеют значительный симпатический тонус в состоянии покоя. Базовый тонус в некоторых областях кровоснабжения органов тоже выражен в разной степени. В сосудах кожи и внутренних органов он выше, чем в скелетной мускулатуре и особенно высок в головном мозге.
Степень кровоснабжения. Соответствующее кровоснабжение в состоянии покоя в каждом органе в основном обусловлено сопротивлением потоку в органе, которое определяется особым строением сосудов, а также сосудистым тонусом в покое. Тонус в покое является значимым для максимально возможного усиления кровоснабжения: чем
выше тонус сосуда, |
т. е. его «предсокращение», тем выше потенциал вазодилатации. |
||||
В |
отдельных |
участках |
сосудистого |
||
русла максимально |
возможное |
увеличение |
|||
кровоснабжения выражено |
в |
различной |
|||
степени |
(рис. |
28.19). |
В |
областях |
|
кровоснабжения с |
сильно |
изменяющимися |
|||
функциональными |
требованиями |
имеют |
|||
относительно |
сильные |
|
изменения |
||
кровоснабжения. Напротив, кровоснабжение жизненно важных органов, таких головной мозг и почки, со стабильно высокими и слабо изменяющимися требованиями поддерживается специальными механизмами регуляции.
