
Нормальная физиология / КР6 Сосудистая система, регуляция кровообращения
.pdf
Взаимоотношение встречных потоков по полым венам
Гемодинамические особенности кровотока в полых венах обусловлены не только величиной их участия в венозном возврате (по верхней полой вене протекает 1/3, а по нижней — 2/3 величины суммарного венозного притока), но также, и расположением сосудистых регионов этих вен относительно гидростатической точки равновесия. При вертикальном положении человека гидростатическое давление в системе нижней полой вены резко возрастает, что обусловлено действием на сосуды и кровь силы тяжести, а также высокой растяжимостью венозных сосудов. Высокое гидростатическое давление в венозных сосудах, особенно нижних конечностей, затрудняет венозный приток крови к сердцу по нижней полой вене. Однако гидростатическое давление в венозных сосудах системы верхней полой вены (в частности в венозных синусах мозговой оболочки, венах шеи, подключичных венах) в условиях вертикального положения тела человека становится отрицательным по отношению к атмосферному. Поэтому, за исключением твердых венозных синусов мозговой оболочки, вены шеи и верхних конечностей находятся в относительно спавшемся состоянии, что способствует венозному оттоку из них.
В отсутствие же гравитационных влияний на организм человека, например, в условиях невесомости, отток крови по верхней полой вене будет затруднен. Очевидно, что в условиях действия силы тяжести на организм человека при ортостатической или антиортостатической пробах то есть постуральных реакциях системы кровообращения, соотношения гидростатического давления в верхней и нижней полых венах и, следовательно, условия кровотока в них будут изменяться. Например, в горизонтальном положении у человека отток крови из головного мозга осуществляется через ярёмные вены, а в вертикальном - через вертебральные, поскольку ярёмные вены спадаются. В клинической практике кровоток по полым венам можно определить методом магниторезонансной томографии (МРТ).
Величина венозного возврата зависит также от объёма циркулирующей крови. Уменьшение объёма циркулирующей крови приводит к снижению венозного возврата, сердечного выброса и артериального давления. Поэтому процессы фильтрации и реабсорбции в капиллярах также влияют на объем циркулирующей крови и величину венозного возврата крови к
сердцу.
Центральное венозное давление. Венный пульс
Центральное венозное давление (ЦВД) – это давление, измеренное в месте впадения полых вен в правое предсердие. Оно примерно равно давлению в правом предсердии и изменяется в пределах 0 ± 3 мм. рт. ст.
В клинической практике центральное венозное давление у человека измеряется обычно инвазивно, одновременно с измерением сердечного выброса правого желудочка и давления в лёгочной артерии при помощи катетера Свана-Ганца (рис.34).
Однако в настоящее время предпочтение отдается неинвазивным
https://t.me/kalecurly |
https://vk.com/kalecurly |
методам оценки центрального венозного давления. В этом случае центральное венозное давление определяют косвенно, методами эхокардиографии, по степени изменения кровотока в нижней полой вене при глубоком дыхании. Считается, что давление в правом предсердии можно принять за 5 мм рт. ст., если нижняя полая вена после глубокого вдоха коллабирует (спадается) более, чем на 50%; в остальных случаях давление в правом предсердии следует принять равным 15 мм.рт.ст.
Рис.34. Мультипараметрическое измерение показателей системной, легочной и внутрисердечной гемодинамики у человека
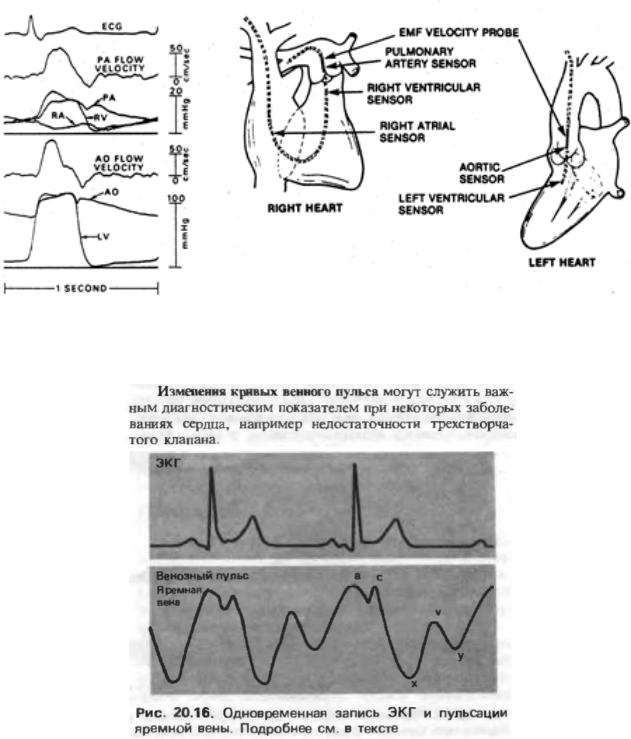
В центральных венах, расположенных в непосредственной близости от сердца, возникают колебания давления и скорости кровотока, обусловленные работой сердечной мышцы. Во время систолы предсердий, отток крови из вен в предсердия прекращается, и поэтому давление в полых венах повышается. Когда предсердия расслабляются, и кровь снова поступает в предсердия, давление в полых венах уменьшается. Эти колебания и составляют сущность венного пульса (рис.35). У человека обычно венный пульс можно определить в наружной яремной вене.
https://t.me/kalecurly |
https://vk.com/kalecurly |
Таким образом, если причиной артериального пульса является распространение пульсовой волны по стенке артериальных сосудов, то причиной венного пульса является прекращение и возобновление оттока крови из центральных вен к сердцу.
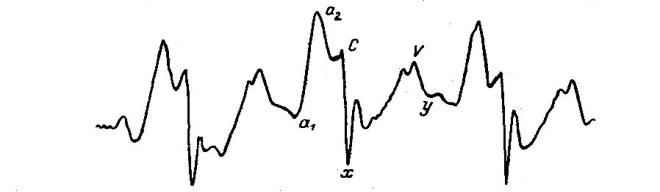
В отличие от однообразного характера изменений давления в желудочках при работе сердца, фазная кривая изменения давления в предсердиях весьма сложна и имеет несколько максимумов и минимумов. Во время систолы предсердий давление в них резко повышается (участок a1 – a2 на рис.35).
Рис 35. Венозный пульс. Пример оригинальной записи
Устья полых вен перекрываются сокращающимся миокардом, и поступление крови из полых вен в предсердия прекращается. В начале диастолы предсердий давление в них понижается. Однако это снижение давления приостанавливается с началом систолы желудочков и некоторого прогибания внутрь полости предсердий створок атриовентрикулярных клапанов (точка С). В результате этого давление в предсердиях вновь повышается, несмотря на то, что кровь в них еще не поступает. В период изгнания крови из желудочков атриовентрикулярная перегородка смещается в сторону верхушки сердца. В результате этого в расслабленных предсердиях происходит резкое снижение давления до минимальных значений («систолический коллапс» (участок С-х). После этого давление в предсердиях начинает медленно повышаться и достигает максимума (точка V). Это связано с поступлением крови из полых вен в предсердия, тогда как в желудочках начинается расслабление кардиомиоцитов в диастолический период. Когда давление в желудочках становится меньше давления в предсердиях, атриовентрикулярные клапаны открываются, и кровь с ускорением поступает из предсердий в желудочки. В результате, давление в предсердиях вновь снижается («диастолический коллапс», (участок V-y на рис.35). С этого момента снова начинается систола предсердий. Таким образом, характер фазных изменений давления в предсердиях оказывается взаимосвязанным с мгновенными изменениями венозного кровотока.
Важно отметить, что в норме венный пульс «отрицательный», поскольку четко выражена волна систолического коллапса С-х. В случае перегрузки правого желудочка и нарастании слабости правого предсердия опорожнение вен затрудняется и поэтому исчезает волна х. В указанных условиях на записи кривой венного пульса отражается преимущественно деятельность правого желудочка: вена набухает во время его систолы, что выражается положительной волной V, и спадается во время диастолы (маловыраженная отрицательная волна y). Такую форму венного пульса называют «положительной», или желудочковой. Положительный желудочковый пульс регистрируется при тромбоэмболии легочной артерии, недостаточности трехстворчатого клапана, выраженном венозном застое в большом круге кровообращения, т.е. сердечной недостаточности и ряде других патологий сердца.
При повышении центрального венозного давления на 1 мм рт.ст. венозный возврат уменьшается на 14%. ЦВД возрастает при кашле, при натуживании. Во время вдоха
https://t.me/kalecurly |
https://vk.com/kalecurly |
центральное венозное давление может снижаться до -5- -10 мм.рт.ст., а венозный возврат крови к сердцу – возрастает. Есть оптимальный режим центрального венозного давления. Однако при значительном снижении давления в грудной полости может быть коллапс центральных вен, что ограничивает венозный возврат крови к сердцу.
Поскольку ЦВД в какой-то мере отражает давление наполнения правого желудочка, то его уменьшение менее 5-10 мм. вод.ст., например, при уменьшении объёма циркулирующей крови, может привести к ухудшению кровенаполнения правого сердца и снижению в результате – сердечного выброса. Повышение же ЦВД выше 100-120 мм вод.ст., например, при резком увеличении объёма циркулирующей крови, может привести к угнетению сократимости миокарда и развитию сердечной недостаточности. Величина ЦВД не полностью коррелирует с объёмом циркулирующей крови, что обусловлено тоническими реакциями венозных сосудов, которые обладают способностью пассивно расширяться при увеличении объема крови и активно сужаться при его уменьшении. Этот механизм направлен на поддержание нормального венозного давления и обеспечение адекватного возврата крови к сердцу. Поэтому уменьшение или увеличение объёма циркулирующей крови от его нормального уровня на 5-10% практически полностью компенсируется изменением емкости венозного русла без изменений ЦВД.
https://t.me/kalecurly |
https://vk.com/kalecurly |
СРС 1. Особенности кровоснабжения и гемодинамики в миокарде.
Кровоснабжение сердца осуществляется двумя коронарными (венечными) артериями – левой и правой, которые отходят от начальной части аорты. Однако большая часть крови (до 85%) протекает через левую коронарную артерию, которая снабжает левое предсердие, всю переднюю стенку и большую часть задней стенки левого желудочка, часть передней стенки правого желудочка и передние две трети межжелудочковой перегородки. Правая коронарная артерия снабжает правое
предсердие, часть передней стенки и всю заднюю стенку правого желудочка, межпредсердную перегородку и заднюю треть межжелудочковой перегородки. От коронарных артерий в толщу миокарда отходят многочисленные мелкие артерии.
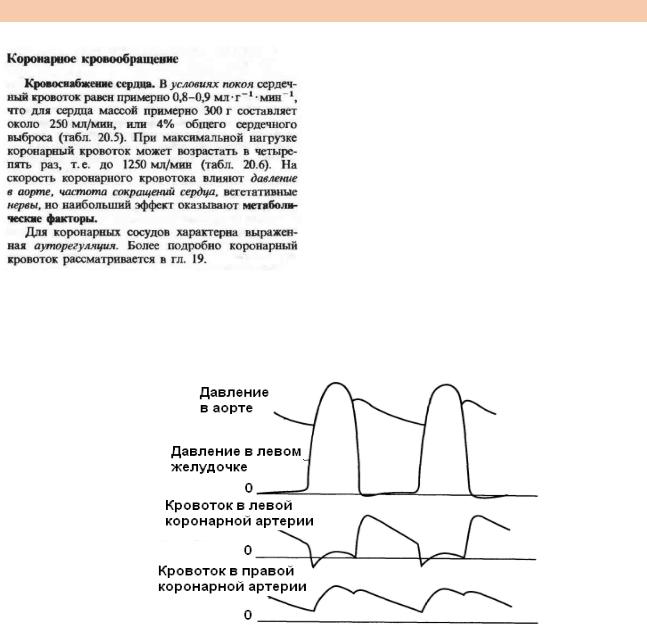
Особенностью коронарного кровотока является его зависимость от фаз сердечного цикла: в диастолу кровоток максимален, а в систолу – минимален. (рис. 1).
Рис.1 Изменения коронарного кровотока в зависимости от систолы и диастолы сердца.
Эта зависимость особенно выражена в субэндокардиальных слоях миокарда желудочков вследствие большей величины их систолического напряжения. Таким образом, перфузия миокарда кровью осуществляется в основном в период диастолы и поэтому кровоснабжение миокарда улучшается при увеличении продолжительности диастолы.
https://t.me/kalecurly |
https://vk.com/kalecurly |
Величина коронарного кровотока у человека в покое составляет около 250 мл/мин. При интенсивной физической нагрузке коронарный кровоток может возрастать в 5–6 раз. Многократное увеличение коронарного кровотока обеспечивается в основном расширением коронарных сосудов, которое при их высоком исходном базальном тонусе осуществляется факторами метаболической регуляции, а также нервными, гуморальными и миогенными механизмами. Важно подчеркнуть, что даже в покое миокард экстрагирует большую часть кислорода артериальной крови - до 70 - 80%. Поэтому повышение потребности миокарда в кислороде может удовлетворяться исключительно за счёт увеличения коронарного кровотока.
Внастоящее время общепринятой является аденозиновая гипотеза американского физиолога Р. Берне (1963 г.), согласно которой в ответ на увеличение сократимости миокарда в нем усиливается синтез аденозина, что вызывает дилатацию коронарных артерий. Установлено также, что на фоне возрастания сократимости миокарда увеличивается синтез оксида азота эндотелиальными клетками коронарных артерий. С другой стороны, синтез оксида азота уменьшается в условиях атеросклероза коронарных артерий при эндотелиальной дисфункции, что сопровождается снижением коронарного кровотока. Таким образом, основными факторами, вызывающими расширение коронарных артерий в ответ на увеличение потребностей миокарда в кислороде, являются аденозин и эндотелиальный оксид азота.
Роль нейрогенных механизмов в увеличении коронарного кровотока в норме не столь значима, как метаболических факторов. Однако внезапное усиление тонуса симпатических нервов сердца, например, при стрессе, может сопровождаться выраженным спазмом коронарных артерий и приводить к резкому ухудшению кровоснабжения миокарда, развитию ишемии и даже инфаркта миокарда.
Вусловиях эксперимента стимуляция симпатических эфферентных волокон, идущих к сердцу, может вызывать как сужение, так и расширение коронарных сосудов. Адренергическая констрикция обеспечивается активацией α1,2-адренорецепторов. Наряду с норадреналином из симпатических нервов высвобождается также нейропептид Y (NPY), который также обладает выраженным констрикторным действием на коронарные сосуды. Расширение коронарных артерий при стимуляции симпатических нервов сердца происходит в ответ на активацию норадреналином β1,2-адренорецепторов гладкомышечных клеток. Возможна и реализация этого эффекта вторично, метаболическим путем, поскольку симпатические нервы усиливают работу сердца и высвобождение аденозина кардиомиоцитами. Следует также отметить, что активация β3-адренорецепторов эндотелиальных клеток способствует усилению ими синтеза оксида азота и вазодилатации. Таким образом, в нейрогенной симпатической регуляции тонуса коронарных сосудов имеет место взаимодействие констрикторных и дилататорных влияний, опосредованных соответственно α1,2-адренорецепторами и рецепторами к NPY и β1,2,3- адренорецепторами.
Стимуляция блуждающего нерва в эксперименте приводит к увеличению коронарного кровотока. Гладкомышечные и эндотелиальные клетки коронарных сосудов содержат М-хо- линорецепторы различных подтипов (M1-5). Ацетилхолин, высвобождающийся из вагусных терминалей, диффундирует в артериальные сосуды, взаимодействует с М-холинорецепторами коронарных артерий и вызывает эндотелий-зависимую дилатацию последних. Наряду с ацетилхолином из окончаний блуждающего нерва выделяются и другие вазодилататоры, в частности вазоактивный интестинальный пептид (VIP), также оказывающий коронарорасширяющий эффект. Поскольку парасимпатические влияния на сердце вызывают увеличение продолжительности диастолы, это также может способствовать возрастанию коронарного кровотока.
Всердце синтезируются простагландины (I2, Е2 и др.), которые могут уменьшать симпатические влияния на сердце и коронарные артерии. Синтез простагландинов увеличивается при ишемии миокарда и имеет в этом случае защитный характер. Серотонин обладает констрикторным действием, а простациклин, брадикинин, гистамин вызывают дилатацию артериальных сосудов.
https://t.me/kalecurly |
https://vk.com/kalecurly |
Непосредственная роль гормонов, за исключением катехоламинов, в регуляции кровоснабжения сердца по сравнению с метаболическими и нейрогенными механизмами сравнительно невелика. Расширение коронарных артерий под влиянием тироксина происходит, вероятно, вторично, вследствие пермиссивного эффекта при участии β2-адренорецепторов. Инсулин расширяет коронарные артерии также вторично, возможно, в ответ на ускорение поглощения глюкозы миокардом и возрастания его метаболизма. Ангиотензин и вазопрессин вызывают сужение коронарных артерий. В условиях стресса и увеличения при этом синтеза кортизола надпочечниками потенцируются прямые эффекты катехоламинов, что может привести к коронароспазму. Избыток кортизола, непосредственно влияя на липидный и углеводный обмен, способствует развитию атеросклероза коронарных артерий.
Женские половые гормоны обладают кардиопротекторным действием, поскольку они оказывают антистрессорный эффект и тормозят развитие атеросклероза. Мужские половые гормоны усиливают действие стрессорных факторов на коронарные артерии. Поэтому атеросклероз коронарных артерий развивается у мужчин в среднем раньше, чем у женщин.
Миогенные механизмы регуляции коронарного кровотока обусловлены зависимостью сократительной активности гладких мышц артериальных сосудов от внутрисосудистого давления крови (феномен Остроумова—Бейлиса). Однако степень выраженности и физиологическое значение этого механизма для работающего сердца в интактном организме пока мало изучены.
https://t.me/kalecurly |
https://vk.com/kalecurly |

СРС 2. Особенности кровоснабжения головного мозга
Интенсивность кровотока в сосудах мозга человека высока и составляет в состоянии покоя около 15% сердечного выброса, т.е. 55-60 мл/мин/100 г ткани. Кровоснабжение серого вещества значительно выше, чем белого (80-110 и 15-25 мл/мин/100г соответственно). При относительно небольшой массе (2% от массы тела) мозг потребляет до 20 % всего кислорода и 17 % глюкозы, которые поступают в организм человека. Интенсивность потребления кислорода мозгом составляет в среднем 3-4 мл/мин/100 г. В отличие от других органов мозг практически не располагает запасами кислорода. Этим определяется наличие многофакторной системы регуляции мозгового кровообращения и механизмов компенсации при поражении одного или нескольких бассейнов кровоснабжения.
Кровь к головному мозгу поступает по четырем артериям: двум сонным и двум позвоночным. Отток крови осуществляется по двум яремным венам и двум венозным позвоночным коллекторам. Важным фактором, исключительно специфичным для головного мозга и оказывающим влияние на кровообращение, является ликвор (спинномозговая жидкость). Вены головного мозга не имеют жесткого каркаса и при повышении давления спинномозговой жидкости спадаются, а при превышении давления ликвора над венозным давлением происходит коллапс вен и нарушение венозного оттока. В ответ на выраженное повышение артериального
давления мозговые артерии расширяются, что приводит к повышению давления ликвора, сжатию вен мозга и оттоку ликвора в спинальную полость. При этом сопротивление артерий снижается, а вен — возрастает, так что общее сопротивление сосудистой системы мозга в целом практически не меняется.
Регуляция мозгового кровотока крайне сложна. При относительном постоянстве общего мозгового кровотока локальный кровоток в различных отделах мозга не постоянен и зависит от интенсивности их функционирования. Так, при напряженной умственной работе локальный кровоток в коре головного мозга человека может возрастать в 2-3 раза по сравнению с состоянием покоя. Локальная функциональная (рабочая) гиперемия – эффект значительного увеличения регионарного кровотока активированных зон мозга при незначительном увеличении полушарного кровотока. В зависимости от активации тех или иных зон головного мозга локальный кровоток в них может повышаться до 180 мл/мин/100 г ткани.
В регуляции мозгового кровотока принимает участие несколько взаимосвязанных и взаимодействующих регуляторных контуров, каждый из которых может функционировать самостоятельно. Выделяют три регуляторных контура: миогенный, гуморальный и нейроген-
ный. |
|
https://t.me/kalecurly |
https://vk.com/kalecurly |
Миогенная ауторегуляция мозгового кровотока стабилизирует его величину у здорового человека при изменении величины среднего артериального давления от 60 до 180 мм. рт. ст. Наиболее широкие пределы ауторегуляции отмечены в мозжечке и аденогипофизе и несколько уже в коре. Относительно участия эндотелия в ауторегуляции кровотока высказано предположение, что она происходит благодаря механорецепторным свойствам эндотелиальных клеток, их способности реагировать на напряжение сдвига и трансмуральное давление путем изменения синтеза оксида азота.
Вместе с тем, основным в регуляции мозгового кровообращения является метаболический контур. Величина просвета артерий зависит от напряжения углекислого газа (pСО2) в крови капилляров и тканях мозга, концентрации ионов Н+ в околососудистом пространстве и напряжения кислорода (pО2). Повышение напряжения СО2 вызывает выраженную дилатацию сосудов мозга. Так, при повышении рСО2 вдвое мозговой кровоток возрастает также в два раза. Действие СО2 опосредовано соответствующим увеличением концентрации ионов Н+, образующихся при диссоциации угольной кислоты. Уменьшение напряжения кислорода (рО2) в артериальной крови (гипоксия) вызывает расширение мозговых сосудов, а увеличение (гипероксия) – сужение. Однако влияние рО2 на просвет сосудов меньше, чем влияние рСО2. Важно подчеркнуть, что при выраженном снижении парциального давления кислорода в атмосферном воздухе, например, в условиях высокогорья, может развиваться высокогорный отек мозга вследствие увеличения проницаемости капилляров, что приводит к выходу жидких компонентов плазмы в межклеточное пространство.
Метаболическая реакция клеток мозга играет существенную роль при локальных перераспределениях крови между областями мозга, имеющими разный уровень функциональной активности. Локальное повышение функциональной активности нервных клеток приводит к повышению в межклеточной среде концентрации ионов калия, что ведет к местному расширению сосудов и возрастанию кровотока. Поскольку уровень концентрации ионов калия в межклеточной среде головного мозга может меняться в течение долей секунды от момента усиления функциональной активности нейронов, указанный механизм считается быстрым контуром регуляции. Более медленный контур регуляции мозгового кровотока связан с повышением напряжения СО2 в мозговом веществе вследствие активного потребления кислорода работающими клетками. Это вызывает локальное снижение рН в межклеточной среде и приводит к расширению сосудов активно функционирующей области мозга.
Биологически активные вещества и гормоны могут оказывать как констрикторные, так и вазодилататорные влияния на мозговые сосуды. К внутрисосудистым вазоконстрикторам относятся: вазопрессин, ангиотензин, простагландины группы Р, катехоламины. Сосудорасширяющий эффект оказывают: аденозин, ацетилхолин, гистамин (средние и крупные артерии), брадикинин (мелкие артерии). По современным представлениям оксид азота (NO), образующийся в эндотелии сосудов, также рассматривается как метаболический регулятор, который способствует расширению микрососудов и улучшению мозговой микроциркуляции.
Нейрогенная регуляция сосудов головного мозга менее эффективна, чем метаболическая, однако, ее значимость может существенно возрастать при возникновении нарушений мозгового кровообращения.
https://t.me/kalecurly |
https://vk.com/kalecurly |

Рис. 2. Нейрогенная регуляция сосудов головного мозга ( По [6]).
Основной зоной приложения нейрогенных влияний являются мелкие артериальные мозговые сосуды диаметром до 25-30 мкм. Доказано существование адренергических, холинергических, серотонинергических и пептидергических нервных волокон, а также нервных окончаний, выделяющих оксид азота. Реакции мозговых сосудов в ответ на нейрогенные влияния во многом зависят от выраженности механизмов ауторегуляции, исходного тонуса сосудов, напряжения СО2, О2, состава и концентрации ионов, присутствия биологически активных веществ в спинномозговой жидкости и тканях мозга. Именно поэтому конечный эффект нейрогенных влияний на мозговой кровоток не однозначен.
Основной источник нервных влияний на сосуды мозга - постганглионарные симпатические волокна, начинающиеся в верхних шейных ганглиях, которые оказывают преимущественно констрикторные влияния. Существование парасимпатических дилататорных влияний на мозговые сосуды признается не всеми исследователями. Вместе с тем, тригеминоваскулярная система является важнейшим звеном патогенеза приступов мигрени и кластерной головной боли. Так, например, вазодилатация и ощущение боли во время приступа мигрени обусловлены выделением из сенсорных окончаний тройничного нерва сосудорасширяющих нейропептидов, важнейшим из которых является пептид, связанный с геном кальцитонина (CGRP – Calcitonin gene related peptide). В паренхиме мозга сосуды иннервируется внутренними периваскулярными нервами, берущими начало из базального ядра, голубого пятна и ядра шва и интернейронами, многие из которых являются ГАМК-ергическими, способствующими вазодилатации. В настоящее время в клинической практике применяется ряд препаратов – циклических производных ГАМК - пирацетам и его аналоги фепирон и карфедон (фенотропил), которые улучшают мозговое кровообращение, восстанавливают нарушенные функции центральной нервной системы после ишемического инсульта.
https://t.me/kalecurly |
https://vk.com/kalecurly |
