
- •И.С. Колпащикова, е.Р. Кофанов, е.М. Алов углеводороды. Галогенпроизводные углеводородов
- •1. Алканы
- •1.1. Гомологический ряд, изомеры
- •Гомологический ряд алканов. Число структурных изомеров
- •1.2. Строение метана
- •1.3. Строение этана
- •1.4. Вращение вокруг простой углерод-углеродной связи. Конформации
- •1.5. Физические свойства
- •1.6. Химические свойства
- •1.6.1. Хлорирование и бромирование метана. Механизм реакции
- •1.6.2. Строение метильного радикала
- •1.6.3. Расчет изменения энергии в ходе реакции
- •1.6.4. Энергетическая диаграмма реакции. Связь энергии
- •Хлорирования метана
- •Бромирования метана
- •1.6.5. Причина различной реакционной способности галогенов
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •1.6.6. Галогенирование высших алканов. Механизм
- •1.6.7. Медленная стадия. Энергетическая диаграмма
- •1.6.8. Причина различной устойчивости радикалов
- •1.6.9. Зависимость скорости образования радикалов
- •1.6.10. Расчет реакционной способности различных связей
- •1.6.11. Селективность в реакциях хлорирования
- •Малореакционного Br• с пропаном
- •1.6.12. Нитрование
- •1.6.13. Сульфоокисление и сульфохлорирование
- •1.6.14. Окисление
- •1.6.15. Термическое разложение алканов, крекинг
- •1.6.16. Ионные реакции алканов
- •1.7. Методы синтеза алканов
- •1.7.1. Гидрирование алкенов и алкинов
- •1.7.2. Реакция Вюрца
- •2.2. Плоскополяризованный свет. Оптическая активность
- •2.3. Строение молекул и оптическая активность
- •2.4. Обозначение конфигураций
- •2.5. Соединения с несколькими хиральными центрами.
- •2.6. Методы разделения энантиомеров
- •3. Циклоалканы
- •3.1 Номенклатура. Изомерия
- •3.2. Физические свойства
- •3.3. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •3.4. Химические свойства
- •3.5. Способы получения
- •4.2. Строение этена
- •4.3. Физические свойства
- •Физические свойства алкенов
- •4.4. Химические свойства
- •4.4.1. Гидрирование. Теплота гидрирования
- •4.4.2. Теплота гидрирования и устойчивость алкенов
- •4.4.3. Присоединение галогенов
- •4.4.3.1. Механизм реакции
- •4.4.3.2. Реакционная способность галогенов в реакции АdЕ
- •4.4.4. Присоединение галогеноводородов
- •4.4.4.1. Механизм реакции
- •4.4.4.2. Направление электрофильного присоединения
- •К пропену
- •4.4.4.3. Реакционная способность и селективность
- •4.4.4.4. Перегруппировка
- •Механизм реакции
- •4.4.5. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •4.4.6. Присоединение серной кислоты
- •4.4.7. Гидратация алкенов. Присоединение спиртов
- •4.4.8. Гидроборирование алкенов
- •4.4.9. Алкилирование алкенов
- •4.4.10. Полимеризация алкенов
- •4.4.11. Окисление
- •4.4.12. Реакция аллильного замещения. Галогенирование
- •Характеристики химических связей в молекуле алкинов
- •Характеристики связей с-н в алканах, алкенах и алкинах
- •5.2. Физические свойства
- •5.3. Химические свойства
- •5.3.1. Реакции присоединеня
- •5.3.1.1. Каталитическое гидрирование и восстановление
- •5.3.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •5.3.1.3. Нуклеофильное присоединение
- •5.3.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •5.3.3. Взаимодействие алкинов с карбонильными соединениями
- •5.3.4. Окисление алкинов
- •5.3.5. Радикальное присоединение бромоводорода
- •5.4. Способы получения
- •6. Диены
- •6.1. Устойчивость сопряженных диенов
- •Теплоты гидрирования алкенов и диенов
- •Гибридизация атомов углерода и длины простых углерод-углеродных связей
- •6.2. Химические свойства
- •6.2.1. Электрофильное присоединение
- •6.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •6.2.4. Полимеризация
- •6.3. Способы получения
- •7. Арены
- •7.1. Сравнение свойств бензола со свойствами алкенов
- •Сравнение химических свойств циклогексена и бензола
- •7.2. Теплота гидрирования. Энергия резонанса
- •7.3. Строение бензола
- •7.4. Ароматичность
- •7.5. Физические свойства
- •Физические свойства аренов
- •7.6. Химические свойства
- •7.6.1. Электрофильное замещение
- •7.6.1.1. Нитрование
- •Превращения -комплекса
- •1.6.1.2. Галогенирование
- •7.6.1.3. Сульфирование
- •7.6.1.3. Алкилирование по Фриделю-Крафтсу
- •7.6.1.4. Ацилирование
- •7.6.1.5. Хлорметилирование
- •7.6.1.6. Формилирование
- •7.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •7.6.3. Реакции окисления
- •7.7. Методы синтеза
- •8. Электрофильное замещение в производных
- •8.1. Влияние заместителей на реакционную способность
- •8.2. Механизм ориентации - влияние заместителей на выбор
- •Классификация заместителей. Электронные эффекты
- •9. Многоядерные ароматические соединения
- •9.1. Нафталин
- •9.1.1. Строение нафталина
- •9.1.2. Химические свойства
- •9.1.2.1. Реакции электрофильного замещения
- •9.1.2.2. Ориентация в реакциях электрофильного замещения
- •9.1.2.3. Восстановление и окисление нафталина
- •9.2. Антрацен и фенантрен
- •10. Гетероциклические соединения
- •10.1. Пятичленные гетероциклы
- •10.1.1. Строение
- •10.1.2. Химические свойства
- •10.1.3. Способы получения
- •10.2. Пиридин
- •10.2.1. Строение пиридина
- •10.2.2. Химические свойства
- •10.3. Хинолин
- •11. Галогеналканы
- •11.1. Нуклеофильное замещение
- •Реакции нуклеофильного замещения
- •11.1.1. Бимолекулярное нуклеофильное замещение
- •Бимолекулярного нуклеофильного замещения, sn2 - процесс согласованный одностадийный:
- •11.1.2. Мономолекулярное нуклеофильное замещение
- •Мономолекулярного нуклеофильного замещения. Sn1-двухстадийный процесс
- •Мономолекулярного нуклеофильного замещения
- •11.1.3. Сравнение реакций sn 1 и sn 2
- •Влияние условий реакции на относительное значение двух механизмов
- •11.1.4. Амбидентные ионы
- •11.2. Реакции отщепления (элиминирование)
- •11.2.1. Бимолекулярное отщепление е2
- •Состав продуктов е2-реакции 2-замещенных пентанов (под действием c2h5oөk)
- •Состав продуктов реакции трет-пентилбромида с алкоголятами калия roөk (70-75о с)
- •5.2.2. Мономолекулярное отщепление е1
- •11.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •12.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола. Отщепление – присоединение
- •12.3. Бимолекулярное нуклеофильное замещение путем
- •12.4. Ориентация при нуклеофильном замещении
- •13. Магнийорганические соединения
- •13.1. Получение и строение магнийорганических соединений
- •13.2. Синтез спиртов и кислот
- •Оглавление
- •Углеводороды. Галогенпроизводные углеводородов
- •150023, Ярославль, Московский пр., 88
- •150000, Ярославль, ул. Советская, 14а
- •И.С. Колпащикова, е.Р.Кофанов, е.М.Алов
- •Углеводороды.
- •Галогенпроизводные углеводородов
Гибридизация атомов углерода и длины простых углерод-углеродных связей
|
Соединение |
Связь С–С |
Гибридизация |
Длина связи, нм |
|
CH3 C2H2–C3H2–CH3 |
C2–C3 |
sp3– sp3 |
15,410-2 |
|
CH2=C2H–C3H–CH3 |
C2–C3 |
sp2– sp3 |
15,210-2 |
|
CH2=C2H–C3H=CH2 |
C2–C3 |
sp2– sp2 |
14,810-2 |
Поскольку sp2-орбитали расположены ближе к ядру, чем sp3-орбитали, длина углерод-углеродной связи должна изменяться в следующем порядке: Сsp2–Сsp2 < Сsp3–Сsp2 < Сsp3–Сsp3, что и наблюдается в действительности. Чем короче связь, тем больше ее энергия, т.е. уменьшение длины связи увеличивает устойчивость молекулы.
Вероятно, стабильность сопряженного диена в некоторой степени связана со взаимодействием -электронных облаков соседних -связей, дополнительное электронное взаимодействие уменьшает энергию диена. Возникающая делокализация -электронов делает молекулу более стабильной. На рис. 6.2 показано перекрывание р-орбиталей атомов С2 и С3.

Рис. 6.2. Взаимодействие -электронннх облаков в сопряженном диене
Связь С2-С3 не является ни простой, ни двойной. Каков порядок этой связи? Если порядок углерод-углеродной связи для этана - 1, этилена - 2, ацетилена - 3, то порядок для любой связи между атомами углерода может быть определен путем измерения длины этой связи и сравнения ее с длиной связи углерод-углерод в этане, этилене и ацетилене. Этим методом было установлено, что порядок связи C2-C3 в I,3-бутадиене составляет 1,2 (Рис. 6.3).

Рис. 6.3. Зависимость порядка связи углерод-углерод от ее длины:
1 - простая связь С-С в этане; 2 - двойная связь С=С в этилене; 3 - тройная связь С≡ С в ацетилене; 4 - связь С2–С3 (кратность 1,2) в 1,3-бутадиене
6.2. Химические свойства
6.2.1. Электрофильное присоединение
Галогены, галогенводороды и некоторые другие электрофильные реагенты образуют с сопряженными диенами смесь двух продуктов (1,2- и 1,4-присоединение). В результате реакции 1,3-бутадиена с бромом (20 оС, CCl4) и с бромоводородом (в отсутствие пероксидов, т.е. механизм AdE) реагент присоединяется не только к соседним атомам углерода при двойной связи (1,2-присоединение), но и к концевым атомам сопряженной системы (1,4-присоединение).
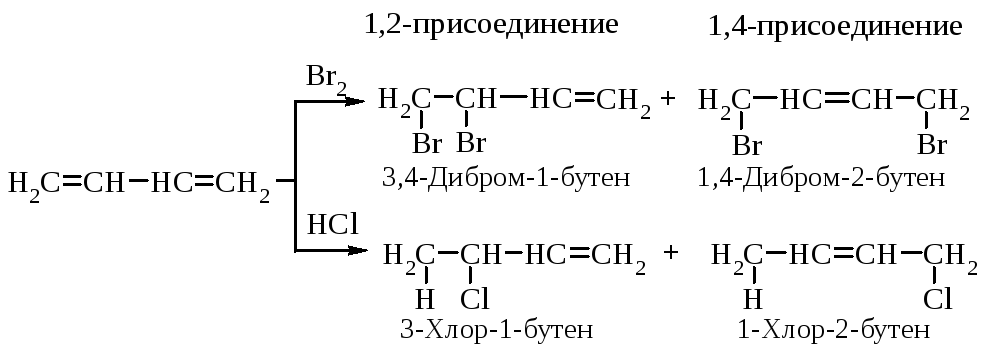
Как объяснить образование таких продуктов? Присоединение хлороводорода и брома к диенам так же, как и присоединение к алкенам, протекает по механизму AdE. Рассмотрим его на примере взаимодействия хлороводорода с 2,4-гексадиеном.

Образование этих продуктов показывает, что первая стадия - присоединение протона - протекает с образованием карбокатиона I, а не II.
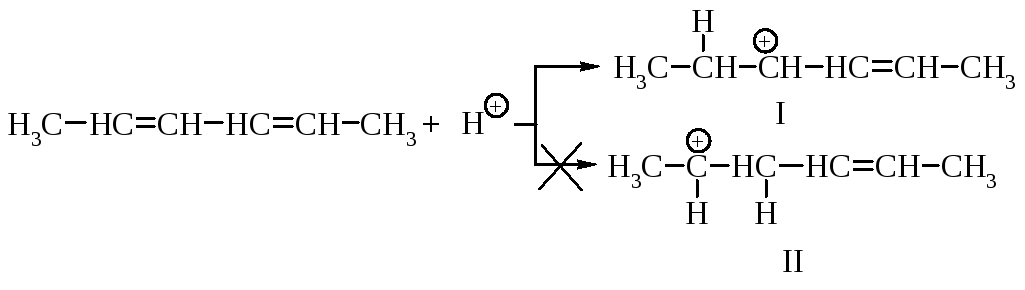
Оба карбокатиона являются вторичными. Почему же предпочтительнее образование иона I? Дело в том, что в ионе I атом углерода, несущий положительный заряд, находится в -положении по отношению к двойной связи, такой карбокатион называется аллильным.
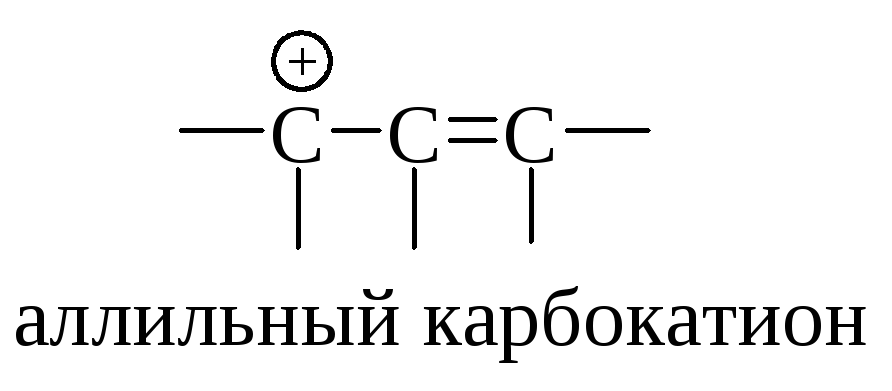
Аллильный карбокатион почти так же устойчив, как третичный карбокатион. Теперь ряд устойчивости карбокатионов можно дополнить аллил-катионом:
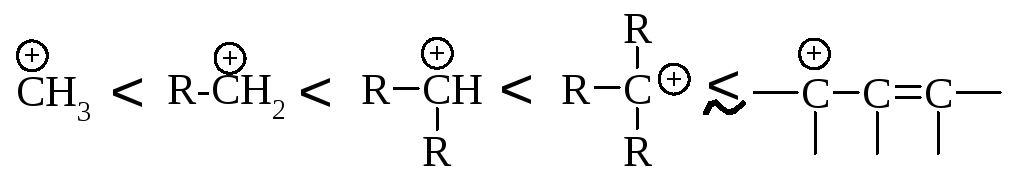
В чем причина устойчивости аллил-катиона? До сих пор мы считали, что молекуле или иону может быть приписана только одна структура. Но аллильный карбокатион I может быть изображен также и структурой III:
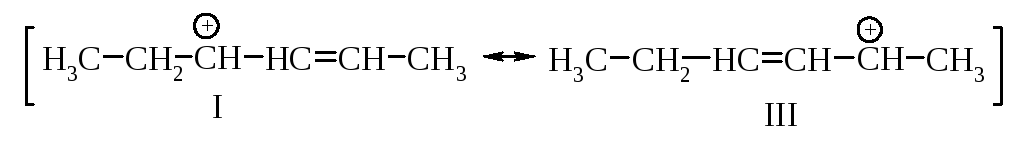
Эти структуры отличаются только положением двойной связи и положительного заряда. Какой же способ изображения правильно показывает распределение электронов? Ни один. В реально существующем аллил-катионе распределение электронов является промежуточным: половина положительного заряда находится на одном атоме углерода и половина - на другом, а связи между этими атомами углерода не являются ни двойными, ни простыми, а промежуточными между ними.
![]()
Изображение реального строения аллил-катиона с помощью только одной структуры с принятыми химиками обозначениями ( - отсутствие электрона, черточка - пара электронов ковалентной связи и т.д.) невозможно. Оно не позволяет представить распределение двух -электронов по р-орбиталям трех атомов углерода.
Для решения подобных проблем химики предложили концепцию резонанса. Основное положение этой теории состоит в следующем: если частица может быть представлена двумя или более структурами, в которых атомные ядра соединены одинаково, а различно только распределение -электронов, то реальное распределение -электронов не может быть удовлетворительно представлено ни одной из них. Реальная молекула представляет собой нечто промежуточное между ними – резонансный гибрид этих структур. Такие гипотетические структуры называют граничными (каноническими). Граничные структуры соединяют знаком ↔.
Граничные структуры должны иметь одинаковое число неспаренных электронов. Структура
![]()
не может быть граничной структурой для аллильного катиона I.
Энергия реальной молекулы (резонансного гибрида) меньше, чем энергия любой из граничных структур. Вклад отдельных канонических структур в истинную структуру частицы неодинаков, наиболее устойчивая структура дает наибольший вклад. Наибольшая стабилизация достигается в тех случаях, когда структуры, вносящие вклад в резонансный гибрид, энергетически эквивалентны. Выигрыш энергии за счет суммирования вкладов всех граничных структур называют энергией резонанса.
Таким образом, в реальном аллил-катионе положительный заряд не локализован на определенном атоме, а распределен между двумя атомами углерода.
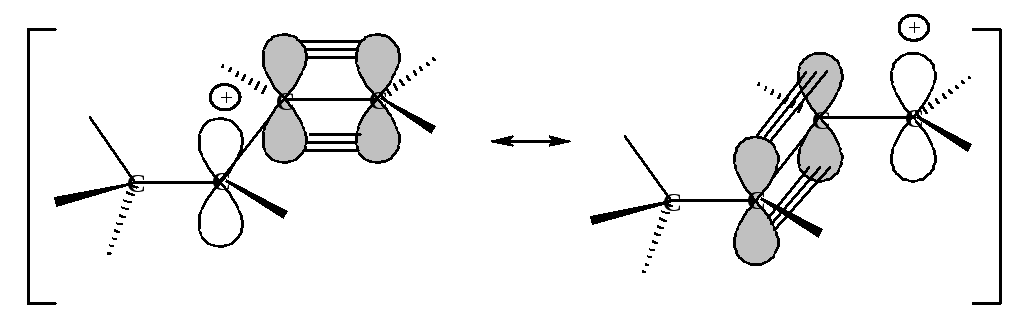
Все атомы, участвующие в резонансе, лежат в одной плоскости, при этом достигается максимальное перекрывание р-орбитали.
Вернемся к механизму реакции хлороводорода с 2,4-гексадиеном. Во второй стадии анион хлора может присоединяться к любому из атомов с положительным зарядом. В результате образуются два продукта.
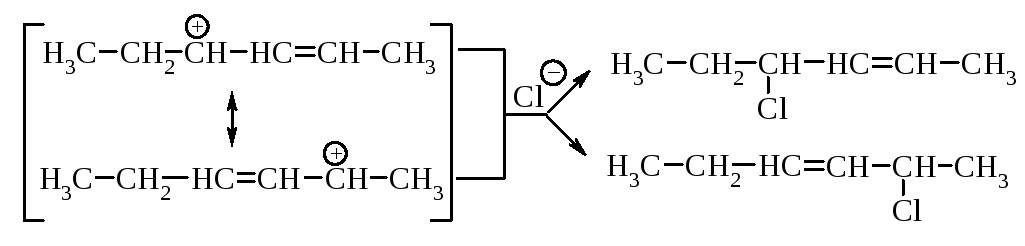
6.2.2. 1,2- и 1,4-Присоединение. Кинетический контроль, термодинамический контроль
При взаимодействии бромоводорода с 1,3-бутадиеном соотношение количеств получающихся продуктов 1,2- и 1,4-присоединения зависит от температуры и времени реакции.
При низкой температуре (минус 80 оС) образуется смесь, с массовой долей продукта 1,4-присоединения 20 % и продукта 1,2-присоединения - 80 %. При температуре 40 оС - продукта 1,4-присоединения 80 % и продукта 1,2-присоединения - 20 %.
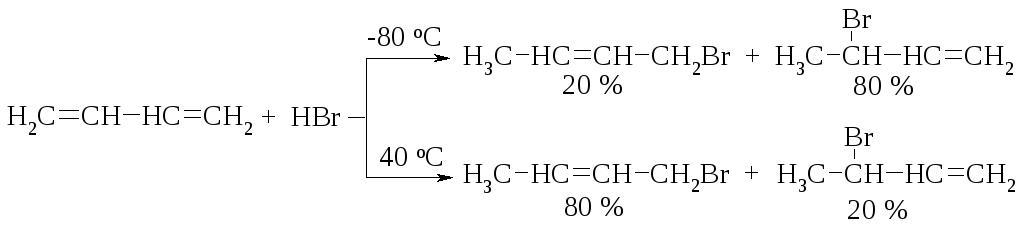
Каждый изомер совершенно устойчив при низкой температуре:
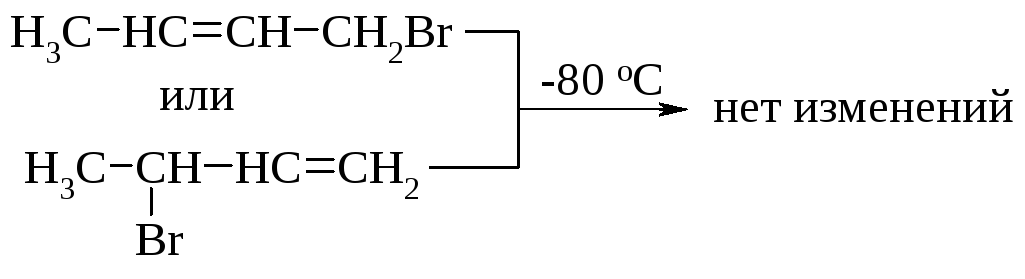
Однако любой из продуктов 1,2- или 1,4-присоединения при нагревании до 40 оС превращается в смесь изомеров, получаемую в реакции I,3-бутадиена с бромоводородом при температуре 40 оС:

При минус 80 оС оба продукта устойчивы, не превращаются друг в друга. Следовательно, соотношение, в котором их выделяют, и есть то соотношение, в котором они образуются: 20 % продукта 1,4-присоединения и 80 % продукта 1,2-присоединения. Значит, при низкой температуре 1,2-присоединение происходит быстрее, чем 1,4-присоединение, т.е. количества продуктов определяются энергиями активации реакций их образования.
Если при нагревании любой из продуктов превращается в одну и ту же смесь, то смесь эта является равновесной, и в ней преобладает более устойчивый продукт 1,4-присоединения. Это означает, что при высокой температуре соотношение продуктов определяется равновесием.
Рассмотрим механизм реакции. На первой стадии образуется аллильный карбокатион. При минус 80 оС бромид-ион, вероятно, не может быстро отойти от только что возникшего карбокатионного центра. Он быстро присоединяется к соседнему атому углерода и образует 3-бром-1-бутен.
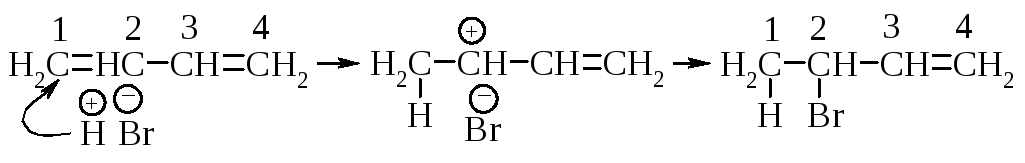
Энергия активации присоединения аниона брома к атому C2 должна быть меньше, чем энергия активации присоединения аниона брома к концевому атому углерода (С4). Этот продукт при минус 80 оС образуется быстрее. Его называют кинетически контролируемым продуктом реакции (см. п. 1.6.9).
На рис. 6.4 показан более низкий энергетический барьер между карбокатионом и продуктом 1,2-присоединения. При 40 оС скорость 1,2-присоединения увеличивается, но вместе с ней растет и скорость обратной реакции, т.к. и ее энергетический барьер невысок.
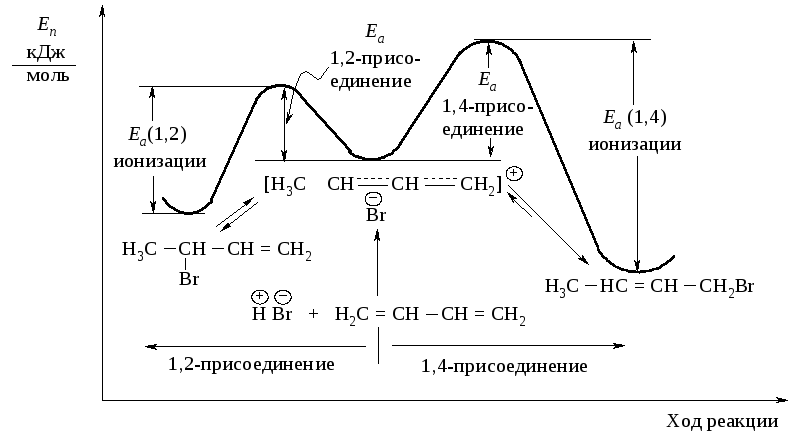
Рис. 6.4. Кинетический и термодинамический контроль в реакции присоединения НВr к 1,3-бутадиену
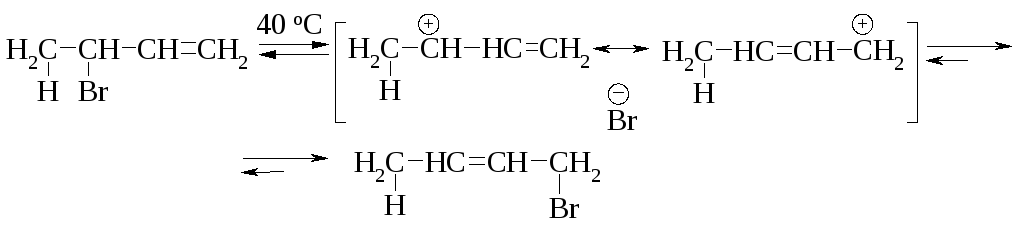
При повышенной температуре становится возможным присоединение BrӨ к концевому атому углерода и образование продукта 1,4-присоединения. Таким образом, увеличивается скорость образования продукта 1,2-присоединения, его ионизации [низкий энергетический барьер Еа(1,2)] и скорость его превращения в продукт 1,4-присоединения. Последний может также ионизироваться, но отщепление иона BrӨ от этого изомера будет происходить гораздо труднее из-за его устойчивости [высокий энергетический барьер Еа(1,4)]. При высокой температуре продукт 1,4-присоединения будет накапливаться. Ввиду большей устойчивости продукта 1,4-присоединения его называют термодинамически контролируемым продуктом реакции.
-
Термодинамически контролируемый продукт – это более устойчивый продукт, который накапливается не в результате более быстрого образования, а в результате равновесия.
Термодинамический контроль выступает на первый план при увеличении времени реакции и температуры (контроль равновесием).
Обратите внимание, что в реакции AdЕ сопряженных диенов более устойчивый продукт образуется с меньшей скоростью. Это характерно для ряда других реакций, например, электрофильного сульфирования и алкилирования ароматических углеводородов (аренов). Изучение присоединения к сопряженным диенам дает объяснение, почему при разных температурах из одних и тех же исходных веществ образуются разные продукты.
