
- •Принципиальная схема свертывания крови
- •Показатели свертывающей системы крови
- •План обследования системы крови
- •Клиническое обследование
- •Семиотика изменений эритроцитов
- •Пойкилоцитоз
- •Острая постгеморрагическая анемия
- •Хроническая постгеморрагическая анемия
- •Железодефицитная анемия
- •Наследственный микросфероцитоз (болезнь Минковского-Шоффара).
- •Гипо- и апластичечкие анемии
- •Семиотика изменений лейкоцитов. Лейкоцитоз. Лейкопения
- •Нейтрофилез. Сдвиг лейкоцитарной формулы
- •Моноцитоз. Моноцитопения. Базофилия. Базопения. Эозинофилия. Эозинопения. Агранулоцитоз.
- •Лейкемоидные реакции
- •Тромбоцитопеническая пурпура
- •Наследственные коагулопатии. Гемофилии
- •Злокачественные болезни крови. Лейкоз
- •Локачественные болезни крови. Лимфогранулематоз
- •Уход за детьми с патологией системы кроветворения.
Кровь - внутренняя среда организма - жидкость, содержащая клеточные элементы, заключенная в кровеносной системе и пребывающая в постоянной циркуляции благодаря деятельности сердца и экстракардиальных факторов. Основные функции крови: - транспортная - доставка на периферию к тканям и клеткам тела кислорода из легких, необходимого для окислительных процессов, а также питательных веществ из кишечника (белков, углеводов, жиров, витаминов, солей, воды); - удаление СО2 и продуктов обмена через экскреторные системы (легкие, кишечник, печень, почки, кожу); - участие в процессах нейрогуморальной регуляции; - защитная (клеточный и гуморальный иммунитет); - участие в физико-химической регуляции гомеостаза (температурного, осмотического, кислотно-щелочного, онкотического, коллоидно-осмотического, химического). Кроветворение (гемопоэз) - процесс образования и развития форменных элементов крови в кроветворных органах. Эритроциты, зернистые лейкоциты и тромбоциты образуются в костном мозге (эритропоэз, гранулопоэз, тромбоцитопоэз), лимфоциты - в костном мозге, селезенке и тимусе (лимфоцитопоэз), моноциты - в костном мозге (моноцитопоэз). Все клетки крови имеют одну родоначальную форму - стволовую кроветворную клетку. Различают три основных отдела клеток-предшественников: отдел стволовых кроветворных клеток, отдел клеток-предшественников миело- и лимфопоэза, отдел унипотентных клеток-предшественников (Рис ).
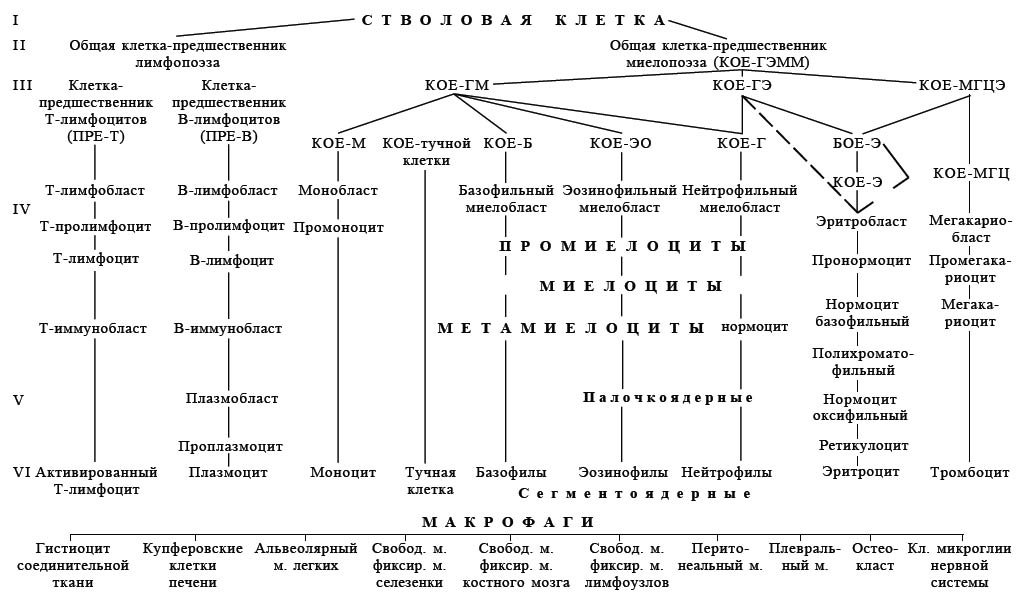
Схема кроветворения (И. Л. Чертков, А. И. Воробьев)
Схема предусматривает выделение 6 классов клеточных форм: I - класс полипотентных клеток-предшественников, способных дифференцироваться по всем росткам кроветворения; II - класс частично детерминированных полипотентных клеток-предшественников: это ограниченно полипотентные клетки-предшественники миелопоэза и лимфопоэза с ограниченной способностью к самоподдержанию; III - класс унипотентных клеток-предшественников, не способных к длительному самоподдержанию, но способных к пролиферации и дифференцировке. Это клетки-предшественники отдельных рядов дифференцировки в кроветворно-лимфатической системе, на уровне которых осуществляется основная количественная регуляция кроветворения. В костном мозге различаются две категории клеток-предшественников лимфоцитов: предшественники В- и Т-лимфоцитов. Клетки трех первых классов схемы кроветворения морфологически неидентифицируемые, существуют в двух формах - бластной и лимфоцитоподобной. На уровне IV класса появляются принципиальные различия между кроветворной и лимфатической системами. Это морфологически распознаваемые пролиферирующие клетки, дающие начало отдельным рядам миелопоэза (гранулоцитопоэз, моноцитопоэз, эритропоэз, метакариоцитопоэз и лимфопоэз). В V класс входят созревающие клетки, в VI - зрелые клетки с ограниченным жизненным циклом. Для гранулоцитопоэза первая морфологически распознаваемая клетка - миелобласт, последняя пролиферирующая клетка ряда - миелоцит. Метамиелоцит и палочкоядерный гранулоцит - класс созревающих клеток (V класс), зрелая клетка - сегментоядерный гранулоцит (VI класс).
Кроветворения во внутриутробном периоде. Эмбриональное кроветворение начинается очень рано. Его характерными особенностями можно считать следующие: - последовательное изменение тканей и органов, являющихся основными плацдармами формирования элементов крови, - желточный мешок, печень, селезенка, тимус, лимфатические узлы и, наконец, костный мозг; - изменение типа кроветворения и продуцируемых клеток - от мегалобластического к нормобластическому.
В последние десятилетия окончательно утвердилась клоновая теория кроветворения. По современным представлениям, дифференцировка клеток крови осуществляется через ряд последовательных ступеней. Каждая следующая ступень означает возникновение клеток с меньшей степенью универсальности последующего направления развития и меньшей способностью к самоподдержанию. Доказано существование единой полипотентной стволовой клетки, способной дифференцироваться в направлении и миелопоэза, и лимфопоэза. Показано, что в процессе позднего фетогенеза происходит накопление стволовых клеток в костном мозге, их общее количество увеличивается в 100 раз и более. Примерно такое же количество стволовых клеток будет и в постнатальном периоде, однако их свойства уже станут иными. Стволовые клетки плода имеют более высокий пролиферативный потенциал и большие репопуляционные свойства. Эти факты и ряд других выдвигаются в качестве аргумента о существовании закона клональной «сукцессии», или последовательной смены клонов стволовых кроветворных клеток в течение жизни человека.
Имеется несколько этапов становления функции кроветворения в течение внутриутробного периода. Самым первым моментом становления системы принято считать 19-й день и по локализации - сугубо внеэмбрионально, в структурах желточного мешка. К 6-й неделе диаметр желточного мешка достигает 5 мм. Развивающийся мезодермальный слой включает свободнолежащие мезенхимальные клетки, клетки крови и клетк-и сосудов. Здесь же в плазме находятся самые примитивные клетки крови, которые, начиная с этого срока, приобретают способность мигрировать в другие «территории». Основной клеткой крови, происходящей на стадии желточного мешка, является только эритроцит, но допускается возникновение на этой стадии и примитивных мегакариоцитов и клеток, напоминающих гранулированные лейкоциты. После 10 нед беременности очаги кроветворения в желточном мешке уже не обнаруживаются, они постепенно переносятся в печень и селезенку. Этот перенос начинается с 6-й недели, но расцвета достигает к 10-12 нед. Очаги кроветворения обнаруживаются в печени вне сосудов и в энтодерме как кластеры, состоящие главным образом из недифференцированных бластов. На 2-м месяце гестации в крови наряду с мегалобластами и мегалоцитами могут быть обнаружены мегакариоциты, макрофаги и гранулоциты. Еще через месяц достигает своего максимума интенсивность кроветворения в селезенке и уже к 5 мес оно близко к исчезновению из этого органа. С 3-го месяца внутриутробного развития кроветворение начинает также происходить в селезенке и прекращается к 5-му месяцу внутриутробного развития. Лимфопоэз возникает на 2-м месяце. На 50-60-е сутки лимфоциты появляются в крови, вилочковой железе, селезенке, лимфатических узлах, миндалинах, групповых лимфатических фолликулах (пейеровы бляшки). Кровяные клетки моноцитарного ряда появляются на 18-20-й день гестации.
Костный мозг закладывается в конце 3-го месяца эмбрионального развития за счет мезенхимных периваскулярных элементов, проникающих вместе с кровеносными сосудами из периоста в костномозговую полость. С 4-го месяца начинается костномозговое кроветворение, которое к концу внутриутробного развития и на протяжении всего постнатального периода становится основным. Костный мозг в пренатальном периоде - красный. Его объем с возрастом плода увеличивается в 2,5 раза (например, на 9-й неделе объем костного мозга составляет 16 мл, а к рождению - 43 мл). У новорожденного масса костного мозга составляет примерно 1,4% от массы тела (около 40 г). С возрастом масса костного мозга увеличивается и у взрослого человека составляет в среднем 3000 г. Красный костный мозг в пренатальном периоде развития присутствует во всех костях и окружен эндостом, выстилающим костные полости. Лишь к концу гестации начинают появляться в костном мозге конечностей жировые клетки. В процессе роста изменяется соотношение красного и желтого костного мозга. С возрастом увеличивается и масса различных кровяных клеток в костном мозге.
Основным отличием состава форменных элементов крови плода является постоянное нарастание числа эритроцитов, содержания гемоглобина, количества лейкоцитов. Если в первой половине внутриутробного развития (до 6 мес) в крови обнаруживается много незрелых элементов (эритробластов, миелобластов, про- и миелоцитов), то в последующие месяцы в периферической крови плода содержатся преимущественно зрелые элементы. Изменяется и состав гемоглобина.
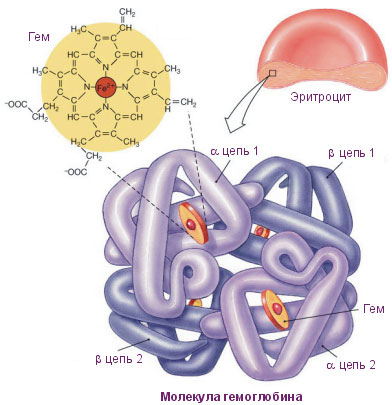
Гемоглобин (от греч. haima - кровь и лат. globus - шар) состоит из четырёх субъединиц. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Гем представляет собой комплекс протопорфирина с атомом железа.
В начале внутриутробного развития ребенка (9-12 недель) в мегалобластах находится примитивный гемоглобин (HbP), который заменяется фетальным (HbF). Он становится основной формой в пренатальном периоде. С 3-й недели гестации начинается синтез гемоглобина взрослого (HbA), интенсивность образования которого увеличивается с возрастом плода. Однако к рождению фетальный гемоглобин составляет приблизительно 60%, а HbA - 40% всего гемоглобина эритроцитов периферической крови. Важным физиологическим свойством примитивного и фетального гемоглобинов является их более высокое сродство к кислороду, что имеет важное значение во внутриутробном периоде, когда плод развивается в условиях относительной гипоксии.
Основные этапы кроветворения:
С 3 недели по 6 неделю кроветворение происходит в желточном мешке (появляются первые клетки крови - мегалобласты с примитивным гемоглобином).
С 6 недели по 5 месяц - печеночное кроветворение (образуются эритроидные клетки, нейтрофилы, мегакариоциты).
С 12 недели по 5 месяц - печеночно-селезеночное кроветворение (в селезенке образуются лимфоциты и моноциты).
С 4 месяца начинается костномозговое кроветворение, которое становится основным до конца внутриутробного периода и в течение всей жизни.
У детей после рождения кроветворение происходит в красном косном мозге всех костей. В возрасте 4-х лет красный костный мозг постепенно превращается в желтый. В возрасте 12-15 лет гемопоэз сохраняется только в костном мозге плоских костей, ребер, телах позвонков, проксимальных отделах плечевых костей, предплечья, бедренной кости.
Эритроциты (от греч. erythros - красный + kytos - клетка) составляют более 99% клеток крови. Они составляют 45% объема крови. Эритроциты - красные кровяные тельца, имеющие форму двояковогнутых дисков диаметром от 6 до 9 мкм, а толщиной 1 мкм с увеличением к краям до 2,2 мкм. Эритроциты такой формы называются нормоцитами. Особая форма эритроцитов приводит к увеличению диффузионной поверхности, что способствует лучшему выполнению основной функции эритроцитов - дыхательной. Специфическая форма обеспечивает также прохождение эритроцитов через узкие капилляры.
Эритроциты выполняют в организме следующие функции: 1) основной функцией является дыхательная - перенос кислорода от альвеол легких к тканям и углекислого газа от тканей к легким; 2) регуляция рН крови благодаря одной из мощнейших буферных систем крови - гемоглобиновой; 3) питательная - перенос на своей поверхности аминокислот от органов пищеварения к клеткам организма; 4) защитная - адсорбция на своей поверхности токсических веществ; 5) участие в процессе свертывания крови за счет содержания факторов свертывающей и противосвертывающей систем крови; 6) эритроциты являются носителями разнообразных ферментов (холинэстераза, угольная ангидраза, фосфатаза) и витаминов (В1, В2, В6, аскорбиновая кислота); 7) эритроциты несут в себе групповые признаки крови.
Сразу после рождения красная кровь новорожденных характеризуется повышенным содержанием гемоглобина и большим количеством эритроцитов. В среднем сразу после рождения содержание гемоглобина равно 210 г/л (колебания 150-240 г/л - см. Приложение). С конца 1-х начала 2-х суток жизни происходит снижение содержания гемоглобина - в связи с гемолизом эритроцитов. К 2-4 месяцам уровень гемоглобина может снижаться до 100 г/л. Это состояние называется физиологическая анемия. Она возникает не у всех детей и связана с истощением запаса железа в организме ребенка с одной стороны, и с недостаточным поступлением железа с пищей - с другой. Потом уровень гемоглобина начинает опять повышаться и после 6 месяцев составляет 110-140г/л.
Цветовой показатель характеризует содержание гемоглобина в эритроцитах. Если цветовой показатель составляет 0,85-1,1 - такое состояние называется нормохромия, более чем 1,1 - гиперхромия, менее 0,8 - гипохромия. У новорожденных детей отмечается гиперхромия (1,1- 1,2), так как эритроциты большие и содержат большое количество гемоглобина. А в период физиологической анемии содержание гемоглобина в эритроцитах уменьшается и наблюдается склонность к гипохромии. Снижение цветового показателя крови наблюдается в состояниях, когда либо уменьшается синтез гемоглобина, что приводит к уменьшению содержания гемоглобина в эритроците, либо когда изменяется размер эритроцита в сторону уменьшения (микроцитоз). Увеличение цветового показателя крови наблюдается при макроцитозе, т.е. когда эритроцит больше своих размеров и вмещает большее количество гемоглобина, что встречается при фолиеводефицитной и В12-дефицитной анемии, приеме цитостатиков, гипотиреозе.
Так как во внутриутробном периоде ребенок развивается в условиях относительной гипоксии, уровень эритроцитов в это время высокий и сразу после рождения составляет около 6 Т/л (колебания 5 - 7 Т/л).
Т - тера - приставка в системе СИ (SI, фр. LeSystèmeInternationald'Unités - Система Интернациональная - международная система единиц), обозначающая 1012 (1 000 000 000 000 - один триллион). В первые дни после рождения часть эритроцитов разрушается путем гемолиза с образование большого количества непрямого (не связанного) билирубина. В печени к данной форме билирубина присоединяется две молекулы глюкуроновой кислоты и образуется билирубин-диглюкурунид, который по-другому называется связанный (с глюкуроновой кислотой) или прямой (прямо реагирует с диазореактивом). Эту реакцию катализирует глюкуронилтрансфераза. Однако у новорожденных детей количество и активность этого катализатора снижены. Поэтому превращения несвязанного билирубина в связанный происходит медленно и у новорожденных детей наблюдается повышенное содержание в крови несвязанного билирубина, который является водонерастворимым и плохо выводится через почки. Это обуславливает появление желтушного окрашивания кожи и склер на 2-3 день жизни ребенка, что называется физиологическая желтуха новорожденных.
После рождения уровень эритроцитов снижается, достигая 3,1 Т/л в период физиологической анемии. Затем уровень эритроцитов повышается и после 6 месяце составляет более 4,0 Т/л (4,0 - 5,5).
Красная кровь новорожденных отличается от крови детей более старших возрастов не только в количественном, но и в качественном отношении. Для крови новорожденного прежде всего характерен отчетливый анизоцитоз (эритроциты разные по размерам), отмечаемый в течение 5-7 дней, и макроцитоз, т.е. несколько больший в первые дни жизни диаметр эритроцитов, чем в более позднем возрасте. Средний диаметр эритроцита у взрослых 7,2 мкм, у новорожденных - до 8 мкм. В связи с этим отмечается и физиологическая гиперхромия - цветовой показатель составляет 1,1 - 1,2. У новорожденных также отмечается пойкилоцитоз (эритроциты имеют разную форму) и полихроматофилия (различная степень окрашивания эритроцитов). Эти особенности эритроцитов могут сохраняться до 2 месяцев.
Количественное соотношение эритроцитов различных диаметров выражается графически в виде эритроцитометрической кривой Ляпунова - Прайс-Джонса (Александр Михайлович Ляпунов 1857-1918, - профессор математики, академик Петербургской Академии Наук; С. Price Jones, 1863--1943, английский врач).
Кривая
Ляпунова - Прайс-Джонса представляет
собой график распределения эритроцитов
по их диаметру: по оси абсцисс отмечают
диаметр эритроцитов (в мкм), по оси
ординат - проценты эритроцитов
соответствующей величины. Полученные
точки соединяют линиями, которые в
совокупности образуют эритроцитометрическую
кривую.
У здоровых людей в норме
эритроцитометрическая кривая имеет
правильную форму с довольно узким
основанием, границы которого находятся
в пределах 5 - 9 мкм, высота кривой достигает
70% и приходится на 7,5 мкм.
При макро- и мегалоцитарных анемиях кривая имеет неправильную пологую форму с широким основанием, иногда с двумя вершинами, и сдвинута вправо, в сторону больших диаметров. При микросфероцитозе кривая также растянута, но сдвинута влево, в сторону меньших диаметров.
У здоровых новорожденных кривая Ляпунова - Прайс-Джонса в первые сутки имеет асимметричный характер (сдвинута вправо) и только к концу первой недели жизни приобретает обычный симметричный вид.
Кровь новорожденных содержит много молодых, еще не совсем зрелых, форм эритроцитов, указывающих на активно протекающие процессы эритропоэза. В течение первых часов жизни количество ретикулоцитов - предшественников эритроцитов - колеблется от 8 до 40‰ - физиологический ретикулоцитоз. Количество ретикулоцитов в грудном и более старшем возрасте составляет 5 - 10‰. ‰ - проми́лле (от лат. pro mille, букв. «за тысячу») - одна тысячная доля. В данном случае - количество ретикулоцитов на 1000 эритроцитов.
Кроме этих молодых форм эритроцитов, в крови новорожденных как вполне нормальное явление встречаются ядросодержащие формы эритроцитов, чаще нормоциты и эритробласты. В заметном количестве их удается обнаружить только в течение нескольких первых дней жизни, а затем они встречаются в крови как единичные клетки.
Наличие большого числа эритроцитов, повышенное количество гемоглобина, присутствие большого количества молодых незрелых форм эритроцитов в периферической крови в первые дни жизни свидетельствуют об интенсивном эритропоэзе как реакции на недостаточность снабжения плода кислородом в период внутриутробного развития и в родах.
Длительность жизни эритроцитов у новорожденных в первые дни жизни составляет 12 дней, что в 5-10 раз меньше средненормальной длительности жизни эритроцитов у детей старше года и взрослых (80-120 дней).
Скорость оседания эритроцитов (СОЭ) зависит от многих химических и физических свойств крови. У новорожденного СОЭ составляет 2-3 мм/ч, у детей грудного возраста 6-7 мм/ч, у детей после года - 5-10 мм/ч. Более медленное оседание эритроцитов у новорожденных объясняется низким содержанием в крови фибриногена и холестерина, а также сгущением крови, особенно ярко выраженным в первые часы после рождения.
Осмотическая резистентность эритроцитов - устойчивость эритроцитов к гипотоническим растворам. Резистентность - свойство эритроцитов противостоять разрушительным воздействиям: осмотическим, механическим, тепловым и другим. В лабораторной практике наибольшее значение приобрело определение осмотической резистентности эритроцитов.
Эритроциты в гипертонических солевых (NaCl) растворах сморщиваются, а в гипотонических - набухают. При значительном набухании наступает гемолиз эритроцита. Для проведения пробы готовят в пробирках растворы хлорида натрия различной концентрации (от 0,7% до 0,22 % NaCl), за тем вносят в них один и тот же объем крови (0,02 миллилитра) и оставляют на 1 час при комнатной температуре. Через 1 час пробирки центрифугируют и определяют концентрацию раствора, соответствующую первым признакам и полному гемолизу.
Сначала гемолизируются самые неустойчивые эритроциты (минимальная резистентность), что проявляется слегка розовым окрашиванием раствора над осажденными эритроцитами. При уменьшении концентрации раствора гемолизируется все больше и больше эритроцитов. Концентрация гипотонического раствора, при которой происходит гемолиз всех эритроцитов, соответствует максимальной осмотической резистентности. Большего разведения эритроциты не выдерживают и разрушаются. При этом раствор приобретает интенсивный красный цвет, а осадка эритроцитов нет. В норме минимальная осмотическая резистентность эритроцитов у взрослых людей колеблется между 0,46--0,48 %, максимальная -- между 0,32--0,34 % физиологического раствора. Осмотическая резистентность эритроцитов у новорожденных детей снижена и гемолиз происходит при меньшем разведении и большей концентрации: минимальная составляет 0,48 - 0,52%, максимальная - 0,28 - 0,36%.
Определение осмотической резистентности эритроцитов имеет большое клиническое значение при гемолитических анемиях. Снижение осмотической резистентности эритроцитов характерно для наследственной сфероцитарной гемолитической анемии, аутоиммунной гемолитической анемии и некоторых форм наследственных немикросфероцитарных анемий. Гемолиз могут вызывать и другие факторы: химические, термические и биологические. При талассемии и гемоглобинопатиях резистентность эритроцитов повышена. Резистентность эритроцитов увеличивается (понижение нижней и верхней границ) после больших кровопотерь, спленэктомии, при гемоглобинозе С, застойных желтухах, в некоторых случаях при полицитемии и железодефицитных анемиях. Случаи расширения границ осмотической резистентности (одновременное понижение минимальной и повышение максимальной) наблюдается в начале острого гемолитического криза и в остром периоде В12-дефицитной анемии.
Все лейкоциты (от греч. λευκος - леукос - белый + κύτος - цитус - клетка) выполняют защитную функцию и делятся на гранулоциты и агранулоциты. Все виды лейкоцитов способны к активному движению и могут переходить через стенку капилляров и проникать в ткани, где они выполняют свои защитные функции.
К гранулоцитам относятся нейтрофилы, эозинофилы и базофилы.
Нейтрофилы (от лат. neuter - ни тот, ни другой + греч. philio - люблю) фагоцитируют бактерии и являются микрофагами, так как они являются сравнительно небольшими клетками. При инфекциях нейтрофилы накапливаются в большом количестве в месте проникновения бактерий в организм. Они первыми приходят в очаг повреждения. Гной - это не что иное, как погибшие нейтрофилы. Нейтрофилы могут вырабатывать особые антимикробные вещества, а также продуцируют интерферон, обладающий противовирусным действием. По нейтрофилам можно определить пол человека, так как у при женском генотипе имеются круглые выросты - «барабанные палочки».
Эозинофилы (eosine - эозин - гистологический краситель, окрашивает белки в розовый цвет + греч. philios - любящий). Основной функцией эозинофилов является обезвреживание и разрушение токсинов белкового происхождения, чужеродных белков, а также комплекса антиген-антитело (они способны его фагоцитировать). Эозинофилы продуцируют фермент гистаминазу, который разрушает гистамин, освобождающийся из поврежденных базофилов и тучных клеток при различных аллергических состояниях, аутоиммунных заболеваниях. Эозинофилы продуцируют плазминоген, который является предшественником плазмина - главного фактора фибринолитической системы крови. При заражении гельминтами эозинофилы проникают в просвет кишечника, разрушаются там, в результате высвобождаются вещества, токсичные для гельминтов.
Базофилы (греч. basis - основа, основание + phileō - люблю - гранулоциты, окрашиваемые основными (щелочными) красителями) продуцируют и содержат биологически активные вещества (гепарин, гистамин и др.), чем и обусловлена их функция в организме. Гепарин препятствует свертыванию крови в очаге воспаления. Гистамин расширяет капилляры, что способствует рассасыванию и заживлению. В базофилах содержатся также гиалуроновая кислота, влияющая на проницаемость сосудистой стенки; фактор активации тромбоцитов (ФАТ); тромбоксаны, способствующие агрегации тромбоцитов; лейкотриены и простагландины. При аллергических реакциях (крапивница, бронхиальная астма) под влиянием комплекса антиген-антитело происходит дегрануляция базофилов и выход в кровь биологически активных веществ, в том числе гистамина, что определяет клиническую картину заболеваний.
К агранулоцитам относятся лимфоциты и моноциты.
Лимфоциты (от лимфа и греч. kýtos - клетка) являются центральным звеном иммунной системы организма. Они осуществляют формирование специфического иммунитета, синтез защитных антител, лизис чужеродных клеток, реакцию отторжения трансплантата, обеспечивают иммунную память. Различают Т- и В-лимфоциты, которые определяют клеточный и гуморальный иммунитет.
Моноциты (от греч. monos - один + kytos - клетка - одноядерный агранулоцит) обладают выраженной фагоцитарной функцией. Это самые крупные клетки периферической крови и их называют макрофагами. Моноциты находятся в крови 2-3 дня, затем они выходят в окружающие ткани, где, достигнув зрелости, превращаются в тканевые макрофаги (гистиоциты). Моноциты способны фагоцитировать микробы в кислой среде, когда нейтрофилы не активны. Фагоцитируя микробы, погибшие лейкоциты, поврежденные клетки тканей, моноциты очищают место воспаления и подготавливают его для регенерации. Моноциты синтезируют отдельные компоненты системы комплемента. Активированные моноциты и тканевые макрофаги продуцируют цитотоксины, интерлейкин (ИЛ-1), фактор некроза опухолей (ФНО), интерферон, тем самым осуществляя противоопухолевый, противовирусный, противомикробный и противопаразитарный иммунитет; участвуют в регуляции гемопоэза. Макрофаги принимают участие в формировании специфического иммунного ответа организма. Они распознают антиген и переводят его в так называемую иммуногенную форму (презентация антигена). Моноциты продуцируют как факторы, усиливающие свертывание крови (тромбоксаны, тромбопластины), так и факторы, стимулирующие фибринолиз (активаторы плазминогена).
Плазмоциты - клетки лимфоидной ткани, продуцирующие иммуноглобулины и развивающиеся из клеток - предшественниц В-лимфоцитов через более молодые стадии (плазмобласт - проплазмоцит). В норме в периферической крови плазмоциты присутствуют очень редко.
Количество лейкоцитов сразу после рождения относительно велико и составляет 11-18 Г/л, достигая иногда 30 Г/л. Затем количество лейкоцитов снижается. До 1 года уровень лейкоцитов часто бывает более 10 Г/л, после 1 года составляет у здоровых детей 5 - 10 Г/л. Г - гига - приставка в системе СИ, обозначающая 109 (1 000 000 000 - один миллиард).
Лейкоцитарная формула - это соотношение различных форм лейкоцитов. Наиболее часто рассматривается соотношение нейтрофилов и лейкоцитов, так как содержание эозинофилов, базофилов, моноцитов практически не претерпевает существенных изменений в процессе роста ребенка. Сразу после рождения преобладают нейтрофилы (60-65%) по сравнению с лимфоцитами (20-30%). Абсолютный (количество клеток в единице объема) и относительный (процентное содержание) нейтрофилез в первые дни после рождения объясняется поступлением в организм ребенка через плаценту материнских гормонов, сгущением крови в первые часы внеутробной жизни, рассасыванием внутритканевых кровоизлияний, адаптацией организма к внешним условиям. Начиная со 2-го дня жизни количество нейтрофилов снижается, а количество лимфоцитов увеличивается и количество этих клеток становится приблизительно одинаковое (40-45 %) на пятый день жизни. Это состояние называется первый физиологический перекрест. Далее количество лимфоцитов увеличивается до 60 - 65% и стабилизируется, а количество нейтрофилов уменьшается до 20 - 30%. После 3-4 лет наблюдается обратная тенденция: снижение количества лимфоцитов и увеличение количества нейтрофилов. И в возрасте пяти лет их количество снова приблизительно одинаковое - второй физиологический перекрест. После этого лейкоцитарная формула постепенно приближается к формуле взрослого.
Таким образом, у здоровых детей количество нейтрофилов больше до 5 дней и после 5 лет, а количество лимфоцитов больше в период от 5 дней до 5 лет.
Оценивается также соотношение различных форм нейтрофилов, циркулирующих в периферической крови. У здоровых детей можно обнаружить сегментоядерные нейтрофилы - самые зрелые, их предшественники - палочкоядерные нейтрофилы, их предшественники - метамиелоциты (юные клетки), а также у новорожденных детей - миелоциты.
Сдвиг лейкоцитарной формулы. Для того, чтобы определить наличие сдвига лейкоцитарной формулы влево или вправо, следует оценить процентное содержание и соотношение нейтрофилов.
В реальном анализе крови лейкоцитарная формула выглядит следующим образом (слева направо указаны разные формы лейкоцитов - их первые буквы): Б Э Ю П С Л М Пл Б - базофилы, Э - эозинофилы, Ю - юные нейтрофилы (метамиелоциты), П - палочкоядерные нейтрофилы, С - сегментоядерные нейтрофилы, Л - лимфоциты, М - моноциты, Пл - плазматические клетки.
К нейтрофилам относятся: юные, палочкоядерные и сегментоядерные.
Если отмечается процентное увеличение количества молодых форм нейтрофилов - палочкоядерных и юных, говорят о сдвиге лейкоцитарной формулы влево.
Если отмечается процентное увеличение количества зрелых форм нейтрофилов - сегментоядерных, говорят о сдвиге лейкоцитарной формулы вправо.
У новорожденных детей отмечается сдвиг лейкоцитарной формулы влево за счет большого содержания палочкоядерных, и в меньшей степени - метамиелоцитов (юных).
Кровяные пластинки, или тромбоциты - бляшки Биццоцеро (G. Bizzozero, 1846-1901, итал. врач) - образования круглой, овальной или веретенообразной формы, имеющие средний диаметр 2-3 мкм.
Кровяные пластинки образуются из мегакариоцитов путем отшнуровывания частиц протоплазмы. Из одного мегакариоцита образуется 3000-4000 тромбоцитов. Тромбоциты человека не являются клетками в полном смысле, так как не содержат ядра, однако обладают многими свойствами клетки: подвижностью, антигенной и ферментативной активностью, интенсивным обменом веществ.
Основная функция тромбоцитов - участие в образовании тромба. В тромбоцитах содержатся тромбоцитарные факторы свертывания крови, которые обозначаются арабскими цифрами. Важной также является ангиотрофическая функция тромбоцитов - поддержание нормальной резистентности и функции микрососудов. С помощью электронной микроскопии и микроавторадиографии установлено, что тромбоциты периодически смыкаются с эндотелиальными клетками и «изливают» в них свое содержимое. Тромбоциты являются физиологическими «кормильцами» эндотелия капилляров, который не в состоянии извлекать ряд необходимых веществ прямо из плазмы. На ангиотрофическую функцию расходуется ежедневно около 15% всех циркулирующих в крови тромбоцитов.
Если эндотелиальные клетки лишаются тромбоцитарной «подкормки», то они быстро подвергаются дистрофии и начинают пропускать через свою цитоплазму эритроциты. Вышедшие из капилляров эритроциты образуют мелкие кровоизлияния, что наблюдается при тромбоцитопениях и тромбоцитопатиях.
Тромбоциты способны к передвижению за счет образования псевдоподий и фагоцитозу инородных тел, вирусов, иммунных комплексов, тем самым, выполняя защитную функцию. Тромбоциты содержат большое количество серотонина и гистамина, которые влияют на величину просвета и проницаемость капилляров, определяя тем самым состояние гистогематических барьеров. Количество тромбоцитов у детей не зависит от возраста и пола и составляет 180 - 400 Г/л. Продолжительность жизни тромбоцитов равна 8-11 дням. Около 35--40 % циркулирующих тромбоцитов ежедневно разрушаются вследствие старения и непрерывно протекающего в организме процесса свертывания.
Гематокрит (Ht) - соотношение всех форменных элементов крови и плазмы крови. Выражается в процентах или в литрах на литр (л/л). У новорожденных гематокрит составляет около 50-75%, т.е кровь содержит 50-75% форменных элементов, а остальные 25-50% - плазма. В дальнейшем количество форменных элементов по отношению к плазме крови снижается и гематокрит после 1 года составляет около 34-40%. Повышенный гематокрит может быть связан либо с гиперпродукцией клеток крови (прежде всего - эритроцитов), либо с уменьшением объема плазмы. Наиболее частые причины повышения гематокрита:
усиленное образование эритропоэтина (при новообразованиях почек);
гидронефроз и поликистоз почек;
гипоксией различного происхождения (например, адаптация к условиям высокогорья).
Наиболее частые причины снижения гематокрита:
сниженное образование эритроцитов в костном мозге;
потеря крови (острые кровотечения);
ускоренное разрушение эритроцитов в крови;
анемии;
увеличение объема крови (например, при внутривенном введении жидкостей);
гиперпротеинемии;
разжижении крови (гипергидратации).
Повышенный гематокрит встречается чаще, чем низкий гематокрит.
Гемограмма здоровых детей различного возраста (средние величины)
Возраст детей |
Эритроциты, Т/Л |
Hb, г/л |
Лейкоциты, Г/Л |
Лейкоцитарная формула, % |
||||
нейтро-филы |
лимфо-циты |
моно-циты |
эозино-филы |
базо-филы |
||||
2-4 нед |
5,31 |
170,0 |
10,25 |
26,0 |
58,0 |
12,0 |
3,0 |
0,5 |
1-2 мес |
4,49 |
142,8 |
12,1 |
25,25 |
61,25 |
10,3 |
2,5 |
0,5 |
2-3 » |
4,41 |
132,6 |
12,4 |
23,5 |
62,5 |
10,5 |
2,5 |
0,5 |
3-4 » |
4,26 |
129,2 |
11,89 |
27,5 |
59,0 |
10,0 |
2,5 |
0,5 |
4-5 » |
4,45 |
129,2 |
11,7 |
27,5 |
57,75 |
11,0 |
2,5 |
0,5 |
5-6 » |
4,55 |
132,6 |
10,9 |
27,0 |
58,5 |
10,5 |
3,0 |
0,5 |
6-7 » |
4,22 |
129,2 |
10,9 |
25,0 |
60,75 |
10,5 |
3,0 |
0,25 |
7-8 » |
4,56 |
130,9 |
11,58 |
26,0 |
60,0 |
11,0 |
2,0 |
0,5 |
8-9 » |
4,58 |
127,5 |
11,8 |
25,0 |
62,0 |
10,0 |
2,0 |
0,5 |
9-10 » |
4,79 |
134,3 |
12,3 |
26,5 |
61,5 |
9,0 |
2,0 |
0,5 |
10-11 » |
4,69 |
125,8 |
13,2 |
31,5 |
57,0 |
9,0 |
1,5 |
0,25 |
11 мес-1 год |
4,67 |
129,2 |
10,5 |
32,0 |
54,5 |
11,5 |
1,5 |
0,5 |
1-2 года |
4,82 |
127,5 |
10,8 |
34,5 |
50,0 |
11,5 |
2,5 |
0,5 |
2-3 » |
4,76 |
132,6 |
11,0 |
36,5 |
51,5 |
10,0 |
1,5 |
0,5 |
3-4 » |
4,83 |
129,2 |
9,9 |
38,0 |
49,0 |
10,5 |
2,0 |
0,5 |
4-5 лет |
4,89 |
136,0 |
10,2 |
45,5 |
44,5 |
9,0 |
1,0 |
0,5 |
5-6 » |
5,08 |
139,4 |
8,9 |
43,5 |
46,0 |
10,0 |
0,5 |
0,25 |
6-7 » |
4,89 |
136,0 |
10,6 |
46,5 |
42,0 |
9,5 |
1,5 |
0,5 |
7-8 » |
5,1 |
132,6 |
9,98 |
44,5 |
45,0 |
9,0 |
1,0 |
0,5 |
8-9 » |
4,84 |
137,7 |
9,88 |
49,5 |
39,5 |
8,5 |
2,0 |
0,5 |
9-10 » |
4,9 |
136,0 |
8,6 |
51,5 |
38,5 |
8,0 |
2,0 |
0,25 |
10-11 » |
4,91 |
144,5 |
8,2 |
50,0 |
36,0 |
9,5 |
2,5 |
0,5 |
11-12 » |
4,83 |
141,1 |
7,9 |
52,5 |
36,0 |
9,0 |
2,0 |
0,5 |
12-13 » |
5,12 |
132,4 |
8,1 |
53,5 |
35,0 |
8,5 |
2,5 |
0,5 |
13-14 » |
5,02 |
144,5 |
8,3 |
56,5 |
32,0 |
8,5 |
2,5 |
0,5 |
14-15 » |
4,98 |
146,2 |
7,65 |
60,5 |
28,0 |
9,0 |
2,0 |
0,5 |
Система свертывания крови - одна из физиологических систем, поддерживающих кровь в жидком состоянии, благодаря динамическому равновесию свертывающих и противосвертывающих факторов. Формируется во внутриутробном периоде развития, причем некоторые факторы этих систем к рождению ребенка не достигают той степени зрелости, которые свойственны взрослому человеку.
Принципиальная схема свертывания крови
Процесс гемостаза обеспечивается тремя основными звеньями: сосудистым, плазменным и тромбоцитарным. 1. К сосудистому звену гемостаза относится аргирофильность каркаса сосудов, сократительная функция прекапилляров, коллаген сосудистой стенки, участвующий в образовании тромба. Сосудистоезвено гемостазаморфологически в основном заканчивает свое развитие к рождению ребенка. Однако, вследствие недостаточности аргирофильного каркаса сосудов наблюдается повышенная ломкость и проницаемость капилляров, а также снижение сократительной функции прекапилляров. Последние две особенности, вероятно, являются механизмами, поддерживающими высокий уровень обмена веществ, свойственный детям первых дней жизни. Уже к концу периода новорожденности механическая резистентность сосудов достигает показателей, свойственных детям старшего возраста и взрослым. 2. К плазменному звену гемостаза относятся плазменные факторы, обозначаемые римскими цифрами (их XIII). Плазменное звено гемостаза к рождению ребенка отличается следующими особенностями. Содержание в крови проакцеллерина (V фактор), антигемофильного глобулина А (VIII фактор), фибринстабилизирующего фактора (XIII) к рождению ребенка уже не отличается от уровня, свойственного взрослым. В то же время активность витамин К-зависимых факторов в первые часы и дни жизни относительно низкая. Это касается протромбина (II фактор), проконвертина (VII фактор), антигемофильного глобулина В (IX фактор), фактора Стюарта-Прауэра (X фактор) и факторов контакта (XI и XII факторы). Особенно низкая активность этих факторов наблюдается на 3-й день жизни. Затем их активность начинает возрастать, что объясняется как достаточным поступлением в организм витамина К, так и созреванием белковосинтетической функции гепатоцитов. 3. Тромбоцитарное звено гемостаза. Тромбоциты способны к агрегации под влиянием коллагена и других веществ, а также содержат тромбоцитарные факторы свертывания крови.
Тромбоцитарные факторы свертывания принято делить на эндогенные (образующиеся в самих тромбоцитах) и экзогенные (факторы плазмы, адсорбированные на поверхности тромбоцитов).
Эндогенные факторы тромбоцитов принято обозначать арабскими цифрами. Наиболее изучены 12 эндогенных тромбоцитарных факторов.
Хотя количество тромбоцитов к рождению практически не отличается от такового у взрослых, однако их функциональная активность (способность к агрегации под влиянием аденозиндифосфата и коллагена) снижена, что объясняется особенностями метаболизма кровяных пластинок в этот период.
Таким образом, почти все факторы свертывания у новорожденных детей имеют сниженную или низкую активность по сравнению со взрослыми. Снижение активности - явление физиологическое, предохраняет новорожденных от тромбозов, которые могут возникнуть в результате повреждения тканей во время родов и попадания в кровь тканевого тромбопластина. К концу первого года жизни показатели свертывающей и противосвертывающей систем крови приближаются к значениям, свойственным взрослым. Хотя у детей старше одного года отмечаются индивидуальные колебания, показатели свертывающей системы крови отличаются определенным постоянством. Большие колебания отмечаются у детей в пре- и пубертатном периодах, что, по-видимому, объясняется значительной гормональной перестройкой, наблюдаемой в этот период жизни. Остальные показатели у детей практически не отличаются от показателей взрослых (время свертывания крови, длительность кровотечения, время рекальцификации плазмы, толерантность плазмы к гепарину). Лишь протромбиновые индекс и время и тромбиновое время у новорожденных снижены и замедлены.
Процесс гемостаза разделяют на два этапа: 1) первичный гемостаз, сосудисто-тромбоцитарный, или начальный, в котором принимают участие стенки сосудов, тромбоциты и отчасти эритроциты; 2) вторичный гемостаз, коагуляционный, или собственно свертывание крови, когда в процесс включаются плазменные факторы коагуляции.
Сосудисто-тромбоцитарный, или начальный, гемостаз играет большую роль в первичной остановке кровотечения путем образования тромбоцитарной пробки.
Противосвертывающая система представлена гепарином, антитромбопластином, антитромбоном и другими факторами. У новорожденных детей отмечается высокий уровень гепарина, сохраняющийся в течение первых 10 дней жизни. Активность тканевого и плазменного антитромбопластинов, антитромбина III, антиактиваторов XI и Х факторов, антитромбиновая активность снижены. Фибринолитическая активность крови сразу после рождения увеличена, она снижается до уровня взрослых в течение нескольких дней. Уровень плазминогена у новорожденных значительно снижен, и нормы взрослых он достигает только к 3-6 мес. Таким образом, почти все факторы свертывания у новорожденных детей имеют сниженную или низкую активность по сравнению со взрослыми. Снижение активности - явление физиологическое, предохраняет новорожденных от тромбозов, которые могут возникнуть в результате повреждения тканей во время родов и попадания в кровь тканевого тромбопластина. К концу первого года жизни показатели свертывающей и противосвертывающей систем крови приближаются к значениям, свойственным взрослым.
