
- •Введение
- •Рекомендации по решению задач
- •Требования к оформлению
- •Критерии и шкала оценивания устной защиты решения задач
- •1. Кинематика поступательного и вращательного движения Формулы
- •Примеры решения задач
- •2. Динамика поступательного движения Формулы
- •Примеры решения задач
- •3. Закон сохранения импульса тела. Столкновения частиц Формулы
- •Примеры решения задач
- •4. Закон сохранения энергии Формулы
- •Примеры решения задач
- •5. Динамика вращательного движения Формулы
- •Примеры решения задач
- •6. Гармонические колебания. Волны в упругой среде. Акустика. Специальная теория относительности Формулы Гармонические колебания
- •Волны в упругой среде. Акустика
- •Специальная теория относительности
- •Примеры решения задач
- •Молекулярно-кинетическая теория
- •Элементы статистической физики
- •Примеры решения задач
- •8. Физические основы термодинамики. Реальные газы. Жидкости Формулы Физические основы термодинамики.
- •Реальные газы. Жидкости
- •Примеры решения задач
- •Список используемой литературы
8. Физические основы термодинамики. Реальные газы. Жидкости Формулы Физические основы термодинамики.
Связь между молярной (C) и удельной (c) теплоемкостями газа:
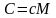 ,
,
здесь M – молярная масса;
Молярные теплоемкости при постоянном объеме и постоянном давлении, соответственно:
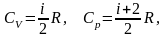
здесь i – число степеней свободы, R – универсальная газовая постоянная;
Удельные теплоемкости при постоянном объеме и постоянном давлении, соответственно:
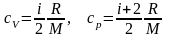 ;
;
Уравнение Майера:
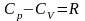 ;
;
Показатель адиабаты:
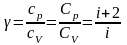 ;
;
Внутренняя энергия идеального газа, изменение энергии идеального газа, соответственно:
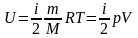 ,
,
 ,
,
здесь, m – масса газа, T – термодинамическая температура, p – давление газа, V – объём газа;
Работа газа при изобарном процессе (p = const):
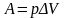 ;
;
Работа газа при изотермическом процессе (T = const):
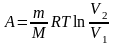 ;
;
Работа газа при адиабатном процессе:
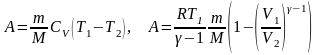 ;
;
здесь V1, V2 – начальный и конечный объемы газа, соответственно, T1, T2 – начальная и конечная температуры газа, соответственно;
Уравнение Пуассона (уравнение газового состояния при адиабатном процессе):
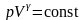 ;
;
Связь между начальным и конечным значениями параметров состояний газа при адиабатном процесс:
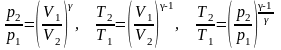 ;
;
Формула Больцмана:
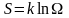 ,
,
здесь S – энтропия, Ω – статистический вес;
Энтропия и изменение энтропии, соответственно:
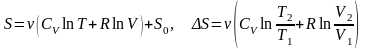 ,
,
здесь S0 – начальное значение энтропии, ν – количество вещества;
Первое начало термодинамики:
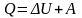 ,
,
здесь ΔU – изменение внутренней энергии идеального газа, Q – количество теплоты, A – работа газа;
1) Первое начало термодинамики для изотермического процесса:
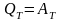 ,
ΔU=
0;
,
ΔU=
0;
2) Первое начало термодинамики для изобарического процесса:
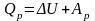 ,
,
где
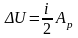 ;
;
 ;
;
3) Первое начало термодинамики для изохорического процесса:
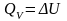 ,
A
= 0;
,
A
= 0;
4) Первое начало термодинамики для адиабатического процесса:
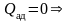
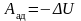 ;
;
Количество теплоты:
1) Теплота сгорания топлива:
 ;
;
2) Теплота нагревания:
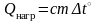 ;
;
3) Теплота плавления:
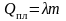 ;
;
4) Теплота парообразования:
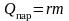 ,
,
здесь q – удельная теплота сгорания топлива, c – удельная теплоёмкость вещества, λ – удельная теплота плавления, r – удельная теплота парообразования;
Работа тепловой машины:
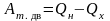 ,
,
здесь Aт.дв. – работа тепловой машины, Qн – количество теплоты, полученной тепловой машиной от нагревателя, Qх – количество теплоты, переданного от тепловой машины холодильнику;
Коэффициент полезного действия реальной тепловой машины:
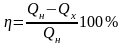 ;
;
Коэффициент полезного действия идеальной тепловой машины:
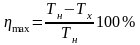 ,
,
здесь Tн – температура нагревателя, Tх – температура холодильника.
Реальные газы. Жидкости
Уравнение Ван-дер-Ваальса для произвольного количества вещества ν газа:
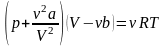 ,
,
здесь a и b – постоянные Ван-дер-Ваальса (рассчитанные на один моль газа), V – объем, занимаемый газом, p – давление газа на стенки сосуда;
Внутреннее давление, обусловленное силами взаимодействия молекул:
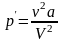 ;
;
Связь критических параметров – объема, давления и температуры газа – с постоянными a и b Ван-дер-Ваальса:
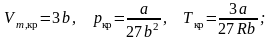
Внутренняя энергия реального газа
 ,
,
здесь CV – молярная теплоемкость газа при постоянном объеме;
Поверхностное натяжение
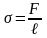 ,
,
здесь F – сила поверхностного натяжения, действующая на контур ℓ, ограничивающий поверхность жидкости, или
 ,
,
здесь ΔE – изменение свободной энергии поверхностной пленки жидкости, связанное с изменением площади ΔS поверхности этой пленки;
Формула Лапласа в общем случае записывается в виде
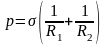 ,
,
здесь p – давление, создаваемое изогнутой поверхностью жидкости; σ – коэффициент поверхностного натяжения; R1 и R2 – радиусы кривизны двух взаимно перпендикулярных сечений поверхности жидкости, а в случае сферической поверхности:
 ;
;
Высота подъема жидкости в капиллярной трубке
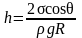 ,
,
здесь θ – краевой угол; R – радиус канала трубки; ρ – плотность жидкости; g – ускорение свободного падения;
Высота подъема жидкости между двумя близкими и параллельными плоскостями
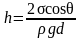 ,
,
здесь d – расстояние между плоскостями.
Расход жидкости в трубке тока (рис. 8.1)
а )
объемный расход QV
= υS;
)
объемный расход QV
= υS;
6) массовый расход Qm = ρυS,
здесь S – площадь поперечного сечения трубки тока; υ – скорость жидкости; ρ – ее плотность;
Уравнение неразрывности струи
υ1S1 = υ2S2,
здесь S1 и S2 – площади поперечного сечения трубки тока в двух местах; υ1 и υ2 – соответствующие скорости течений.
Уравнение Бернулли для идеальной несжимаемой жидкости, в общем случае
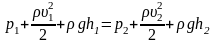 ,
,
здесь
p1
и p2
– статические давления жидкости в двух
сечениях трубки тока; υ1
и υ2
– скорости жидкости в этих сечениях;
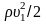 и
и
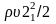 – динамические давления жидкости в
этих же сечениях; h1
и h2
– высоты их над некоторым уровнем (рис.
8.1); ρgh1
и ρgh2
– гидростатические давления;
– динамические давления жидкости в
этих же сечениях; h1
и h2
– высоты их над некоторым уровнем (рис.
8.1); ρgh1
и ρgh2
– гидростатические давления;
Уравнение Бернулли в случае, когда оба сечения находятся на одной высоте (h1 = h2):
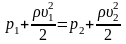 ;
;
Скорость течения жидкости из малого отверстия в открытом широком сосуде
,
здесь h – глубина, на которой находится отверстие относительно уровня жидкости в сосуде;
Формула Пуазейля. Объем жидкости (газа), протекающей за время t через длинную трубку,
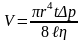 ,
,
здесь – радиус трубки; ℓ – ее длина; Δp – разность давлений на концах трубки; η – динамическая вязкость (коэффициент внутреннего трения) жидкости;
Число Рейнольдса для потока жидкости в длинных трубках.
 ,
,
здесь
 – средняя по сечению скорость течения
жидкости; d
– диаметр трубки, и для движения шарика
в жидкости
– средняя по сечению скорость течения
жидкости; d
– диаметр трубки, и для движения шарика
в жидкости
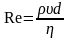 ,
,
здесь υ – скорость шарика; d – его диаметр;
Число Рейнольдса Re есть функция скорости υ тела, линейной величины ℓ, определяющей размеры тела, плотности ρ и’ динамической вязкости η жидкости, т.е.
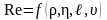 ;
;
При малых значениях чисел Рейнольдса, меньших некоторого критического значения Reкр движение жидкости является ламинарным. При значениях Re >> Reкр, движение жидкости переходит в турбулентное.
Критическое число Рейнольдса для движения шарика в жидкости Reкр = 0,5; для потока жидкости в длинных трубках Reкр = 2300.
Формула Стокса. Сила сопротивления F, действующая со стороны потока жидкости на медленно движущийся в ней шарик,
F = 6πηrυ,
здесь r – радиус шарика; υ – его скорость.
Формула справедлива для скоростей, при которых число Рейнольдса много меньше единицы (Re < 1).
