
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ 89
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •1.2.1 Радикало-функциональная номенклатура
- •1.2.2 Систематическая (заместительная) номенклатура
- •1.3 Вопросы и упражнения для самопроверки:
- •2. ИЗОМЕРИЯ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ
- •2.1 Структурная изомерия
- •2.2 Стереоизомерия
- •2.2.1.1 Геометрическая изомерия или цис-транс-изомерия один из видов стереоизомерии, возникающий при разном расположении одинаковых заместителей по одну или по разные стороны плоскости π связи или неароматического цикла (Рис.2.1).
- •2.2.1.2 Хиральность.
- •2.2.1.3 Оптическая изомерия. Энантиомеры и диастереомеры
- •2.2.1.4 Относительная и абсолютная конфигурации
- •2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
- •2.3 Вопросы и упражнения для самопроверки
- •3.1. Образование ковалентных связей
- •3.2.3 Ароматичность
- •3.3 Взаимное влияние атомов в молекуле
- •3.3.1 Индуктивный эффект
- •3.3.2 Мезомерный эффект
- •3.4. Вопросы и упражнения для самопроверки
- •4. КИСЛОТНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •4.1 Теория Бренстеда-Лоури, протолитическая
- •4.2. Вопросы и упражнения для самопроверки
- •5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- •5.1 Механизмы органических реакций
- •5.2.1 Гидратация алкенов. Роль кислотного катализатора
- •5.2.2 Реакции присоединения к асимметричным алкенам (правило Марковникова)
- •5.2.3 Реакция присоединения к α, β-ненасыщенным карбонильным соединениям
- •5.3.1 Галогенирование бензола
- •5.3.2 Ориентирующее действие заместителей в бензольном ядре. Ориентанты первого и второго рода
- •5.4 Нуклеофильное замещение у насыщенного атома углерода
- •5.5 Механизм и стереохимия реакций элиминирования (Е)
- •5.6 Окисление и восстановление органических соединений
- •5.6.1 Окисление гидроксильных и оксо-групп
- •5.6.2 Окисление непредельных и ароматических соединений
- •5.6.3 Реакции восстановления
- •5.6.4 Обратимые окислительно-восстановительныесистемы
- •5.7. Вопросы и упражнения для самопроверки
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- •6.1 Способы получения альдегидов и кетонов
- •6.2 Химические свойства альдегидов и кетонов (карбонильных соединений)
- •6.2.1 Реакция альдегидов с нуклеофилами
- •6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
- •6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
- •6.2.2 Реакции конденсации
- •6.2.2.1 Кето-енольная таутомерия альдегидов и кетонов. Альдольное присоединение
- •6.2.2.2 Кротоновая конденсация или альдольно - кротоновая конденсация
- •6.3 Окисление и восстановление альдегидов и кетонов
- •6.4 Вопросы и упражнения для самопроверки
- •7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- •7.1. Основные пути получения карбоновых кислот:
- •7.2. Малоновый синтез карбоновых кислот
- •7.3. Классификация карбоновых кислот
- •7.4 Химические свойства карбоновых кислот
- •7.4.2. Восстановление карбоновых кислот
- •7.4.3. Декарбоксилирование карбоновых кислот
- •7.5. Дикарбоновые кислоты
- •7.6. Угольная кислота и ее производные
- •7.7. Вопросы и упражнения для самопроверки
- •8. ПОЛИ- И ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ
- •8.1. Аминоспирты
- •8.2 Классификация одноосновных гидроксикислот
- •8.2.1 Получение гидроксикислот
- •8.2.2 Специфические реакции гидроксикислот
- •8.3. Многоосновные гидроксикислоты
- •8.4. Оксокислоты
- •8.5 Вопросы и упражнения для самопроверки
- •9. АМИНОКИСЛОТЫ
- •9.1. Изомерия аминокислот
- •9.2. Классификации аминокислот
- •9.2.1. Классификации аминокислот по биологической ценности
- •9.2.2. Классификации аминокислот на основе химического строения аминокислот
- •9.2.2.3. Современная классификация α-аминокислот
- •9.4. Кислотно-основные свойства аминокислот
- •9.5. Способы получения аминокислот
- •9.6. Химические свойства
- •9.7. Специфические реакции α, β, γ, δ-аминокислот
- •9.8. Качественные реакции на аминокислоты, пептиды, белки.
- •9.9. Методы количественного определения аминокислот
- •9.10. Редко встречающиеся аминокислоты
- •9.11.2 Вторичная структура полипептидной цепи
- •9.11.3 Третичная структура белков
- •9.12. Вопросы и упражнения для самопроверки
- •Классификация углеводов
- •10.1. Моносахариды, классификация
- •10.2. Циклическое строение моносахаридов
- •10.3. Химические свойства моносахаридов
- •10.3.1. Реакции полуацетального гидроксила
- •10.3.3. Окисление и восстановление моносахаридов
- •10.3.4. Изомеризация в щелочной среде
- •10.4. Качественные реакции моносахаридов. Отличительные реакции пентоз и гексоз
- •10.5. Производные моносахаридов
- •10.6. Олигосахариды
- •10.6.1. Химические свойства олигосахаридов
- •10.7. Полисахариды
- •10.7.1. Гомополисахариды
- •10.7.2. Гетерополисахариды
- •10.8. Гликопротеины
- •10.9. Вопросы и упражнения для самопроверки
- •11. БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •11.1. Пятичленные ароматические гетероциклы
- •11.2. Шестичленный ароматический гетероцикл
- •11. 3. Нуклеиновые кислоты (НК)
- •11.3.1 Нуклеозиды
- •11.3.2. Нуклеотиды
- •11.3.3. Нуклеозидциклофосфаты
- •11.3.4. Рибо- и дезокси-рибонуклеиновые кислоты
- •11.4. Вопросы и упражнения для самопроверки
- •12. ЛИПИДЫ
- •12.1. Высшие жирные кислоты
- •12.2. Классификация омыляемых липидов
- •12.2.1. Простые липиды
- •12.2.1.1.Химические свойства простых липидов
- •12.2.2 Сложные липиды
- •12.2.2.2. Гликолипиды
- •12.3. Неомыляемые липиды
- •12.3.1 Терпены (изопреноиды)
- •12.3.3. Стероиды
- •12.4. Вопросы и упражнения для самопроверки
- •13. Методы, используемые для изучения соединений в органической химии
- •Литература
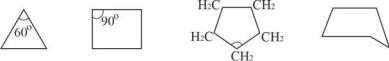
2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
В 1885 году Адольф фон Байер предложил теорию, объясняющую некоторые аспекты химии циклических соединений. В циклоалканах с плоской структурой к торсионному и напряжению Ван-дер-Ваальса прибавляется угловое или байеровское напряжение. Последнее обусловлено отклонением валентных углов в цикле от нормального тетраэдрического угла (109,5O).
Согласно Байеру, когда углерод связан с четырьмя другими атомами, угол между любой парой связей равен тетраэдрическому углу 109,5o. Но цикл циклопропана представляет собой треугольник с тремя углами по 60o, а циклобутан – это квадрат с четырьмя углами по 90o. Таким образом, в циклопропане и циклобутане каждая пара связей сжата соответственно до 60o или 90o, чтобы соответствовать геометрии цикла. Эти отклонения валентных углов от «нормального» тетраэдрического значения делают молекулы напряженными и, следовательно, нестабильнымипо сравнению с молекулами, вкоторых валентныеуглы являются тетраэдрическими. Поскольку отклонение валентных углов в циклопропане (109,5O – 60O = 49,5O) больше, чем в циклобутане (109,5O – 90O = 19,5O), циклопропан более нестабилен и более подвержен реакциям раскрытия цикла, чем циклобутан. Атомы водорода в данных плоских молекулах находятся в заслоненном положении. В результате значительного торсионного и углового напряжений четырехчленный плоский цикл также неустойчив.
плоский цикл |
конформация конверта |
Углы правильного пятиугольника (108O) очень близки к тетраэдрическому углу (109,5O), поэтому циклопентан практически не подвержен угловой деформации. Однако в плоской форме сильно
38

проявляется торсионное напряжение (напряжение заслонения). При переходе плоского циклопентана в неплоскую конформацию конверта торсионное напряжение несколько снижается.
Углы правильного шестиугольника (120O) несколько больше угла тетраэдра и в плоской форме сильно проявляется напряжение заслонения, поэтому у циклогексана возникают менее напряженные неплоские конформации. Среди них более устойчивыми являются конформации кресла. В данных конформациях циклогексана отсутствует угловое напряжение (Рис.2.11).
потенциальная энергия
полукреслo |
|
|
полукреслo |
|
ванна |
|
|
45 кДж/моль |
30 кДж/моль |
45 кДж/моль |
|
|
|
||
23 кДж/моль |
23 кДж/моль |
||
твист-форма |
твист-форма |
||
креслo |
|
|
креслo |
Рис. 2.11 Конформации кресла,ванны,Z- конформации
В кресловидной конформации циклогексана расположение атомов водорода у всех атомов углерода такое же, как в заторможенной конформацииэтана,аатомовуглерода – как вскошеннойконформации бутана (Рис.2.12).
Рис. 2.12 Заторможенная конформация циклогексана (кресла)
39
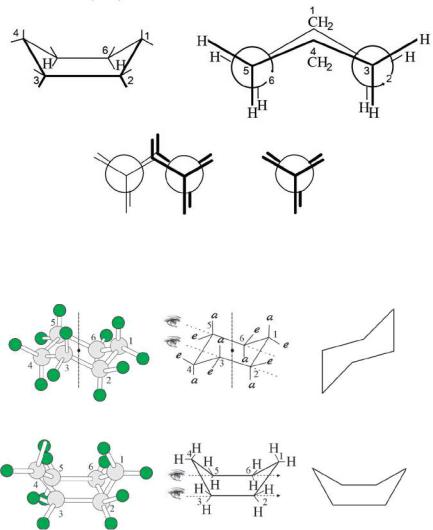
В конформации ванны ввиду заслоненного положения атомов водорода при углеродах С-2, С-3, С-5, С-6 напряжение цикла увели-
чивается (2.13; 2.14).
Рис. 2.13 Заслоненная конформация циклогексана (ванна)
Следовательно, конформация кресла является энергетически более выгодной.
кресло
ванна
Рис. 2.14 Экваториальные и аксиальная связи в циклогексане
40
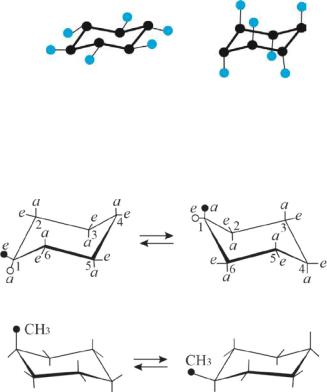
Вернемся к модели конформации кресла циклогексана (рис.2.14). Хотя кольцо циклогексана не плоское, мы можем считать, что атомы углерода лежат примерно в одной плоскости, а атомы водорода занимают два вида положения: шесть атомов водорода лежат в плоскости (экваториальные), а шесть атомов водорода располагаются выше или ниже плоскости (аксиальные), параллельно оси симметрии молекулы (Рис.2.15).
Рис. 2.15 Аксиальные и экваториальные положения атомов водорода
Связи С–Н, параллельные оси симметрии, называются аксиальными. Связи С–Н, расположенные к оси под углом 109,5O, называются экваториальными.
(a)
(б)
Рис. 2.16 Инверсия цикла в циклогексане (а) и метилциклогексане (б)
Молекула циклогексана может принимать две, во всехотношениях эквивалентные, креслообразные конформации. При переходе из одной в другую аксиальныеатомы водородастановятся экваториальными и
41
