
Теория-1
.pdfпрепаратами:
Субстраты свободнорадикального окисления — препараты ненасыщенных жирных кислот.
Природные антиоксиданты - препараты аминокислот, белков, нуклеиновых кислот и их производных, которые реагируют с продуктами свободнорадикального окисления.
Биоантиоксиданты — препараты витаминов, гормонов, флавоноидов.
Модуляторы свободнорадикального окисления — препараты, содержащие микроэлементы.
Механизм действия наиболее распространѐнных антиоксидантов состоит в обрыве реакционных цепей: молекулы антиоксиданта взаимодействуют с активными радикалами с образованием малоактивных радикалов. Окисление замедляется также в присутствии веществ, разрушающих гидроперекиси. В этом случае падает скорость образования свободных радикалов. Даже в небольшом количестве антиоксиданты уменьшают скорость окисления, поэтому в течение некоторого периода времени продукты окисления не обнаруживаются. В практике торможения окислительных процессов большое значение имеет явление синергизма — взаимного усиления эффективности антиоксидантов в смеси, либо в присутствии других веществ.
67. Как связано состояние антиоксидантной системы с углеводным обменом? Какие биохимические тесты можно использовать для оценки антиоксидантной системы клетки?
Состояние углеводного обмена при сахарном диабете характеризуется компенсацией и декомпенсацией. Компенсация – это состояние, при котором под влиянием лечения диабета достигнуты нормогликемия и аглюкозурия.
Декомпенсация – течение диабета, при котором количество глюкозы в сыворотке крови превышает 13,9 ммоль/л (более 250 мг на 100 мл), а в моче – более 50 г в сутки при наличии различной степени ацетонурии (кетоза).
Наряду с повышением образования количества свободных радикалов при сахарном диабете снижается активность антиоксидантной системы, представленной глютатионом, супероксиддисмутазой, витаминами Е и С.
Диагностика
определением содержания отдельных антиоксидантов в плазме [10, 13, 48, 50, 346] и клетках крови [10, 51, 105, 122] используют показатель, обозначаемый как антиоксидантная активность (АОА) плазмы крови. АОА плазмы (сыворотки) крови - это интегральный показатель, отражающий ее способность противодействовать развитию свободнорадикальных реакций [84, 162]. Основными компонентами тест-систем для определения АОА плазмы крови являются: система генерации радикалов и субстрат или молекула-мишень, которая подвергается свободнорадикальному окислению [267, 290]. Добавление в модельную систему плазмы крови, содержащей различные водо- и жирорастворимые антиоксиданты, приводит к уменьшению образования радикалов и торможению окисления субстрата.
Особенности метаболизма нервной ткани. Липидные компоненты и белки нервной ткани. Нейромедиаторы, строение, биосинтез.
Липиды нервной ткани
Особенностью нервной ткани является использование липидов в качестве пластического (структурного) материала, в то время как в других тканях эту функцию выполняют белки. Липиды представлены цереброзидами, ганглиозидами, сфингомиелинами, плазмалогенами, фосфатидилсеринами, фосфатидилхолинами, фосфатидилинозитами,
фосфатидилэтаноламинами и холестерином. Миелиновые мембраны имеют 3 слоя белка и 2 слоя липидов
Белки и пептиды нервной ткани
Специфическими белками являются белок S-100, белок 14-3-2, нейрофизин, нейротубулин, нейростенин.
Пептиды: карнозин, анзерин, гомокарнозин, гомоанзерин, энкефалины, эндорфины, пептид сна
Особенности обмена аминокислот в нервной ткани
В нервной ткани концентрация свободных аминокислот в 8 раз больше, чем в плазме крови. Центральное место в обмене принадлежит глутаминовой кислоте, глутамину, аспарагиновой кислоте, ацетиласпарагиновой кислоте, у-аминомасляной кислоте. Глутаминовая кислота нейтрализирует аммиак в нервной ткани, превращаясь в глутамин, который удаляется через ГЭБ в кровь. у-Аминомасляная кислота образуется путем декарбоксилирования глутаминовой кислоты. Ацетиласпарагиновая кислота — это запасная форма хранения аминокислот в нервной ткани.
Образование аммиака в нервной ткани
Образование аммиака происходит в пуриновом цикле: путем гидролитического дезаминирования АМФ образуется ИМФ и аммиак. ИМФ, далее конденсируясь с аспарагиновой кислотой, образует аденилосукцинат, который, расщепляясь, образует вновь АМФ (и фумарат).
Энергетический обмен в нервной ткани
Глюкоза — основной источник энергии, так как через ГЭБ в нервные клетки поступает только глюкоза, которая, расщепляясь в аэробном гликолизе, образует ПВК, превращающуюся с помощью пируватдегидрогеназного комплекса в ацетил-КоА, который вступает в ЦТК, давая восстановленные эквиваленты для окислительного фосфорилирования, приводящего к образованию АТФ. В отличие от других тканей организма человека ВЖК не проникают через ГЭБ и не могут быть использованы в качестве энергетического материала.
Медиаторы нервной системы Связь миллиардов нейронов в нервной системе осуществляется посредством медиаторов: ацетилхолина, норадреналина, дофамина, серотонина, гистамина, глицина, у-аминомасляной кислоты.

ацетилхолин, сложный эфир холина и уксусной кислоты. К нейромедиаторам относятся некоторые аминокислоты, а также биогенные амины, образующиеся при декарбоксилировании аминокислот. Известные нейромедиаторы пуринового ряда —
производные аденина. Самую большую группу образуют пептиды и белки.
69. Белки мышечной ткани, особенности строения. Механизмы мышечного сокращения скелетных и гладких мышц. Роль минеральных факторов в мышечном сокращении.
Белки делятся на три основных группы:
1.Саркоплазматические белки (35%);
2.Миофибриллярные белки (45%);
3.Белки сарколемы (стромы).
Энергообеспечение мышечной ткани. Синтез креатина и
креатинфосфата.
Источники энергии следующие.
Специальные реакции субстратного фосфорилирования.
Гликолиз, гликогенолиз.
Окислительное фосфорилирование.
Специальные реакции субстратного фосфорилирования.
Участие специальных реакций субстратного фосфорилирования в обеспечении энергией мышечной клетки различна - это зависит от интенсивности, продолжительности, мощности и длительности мышечной работы.
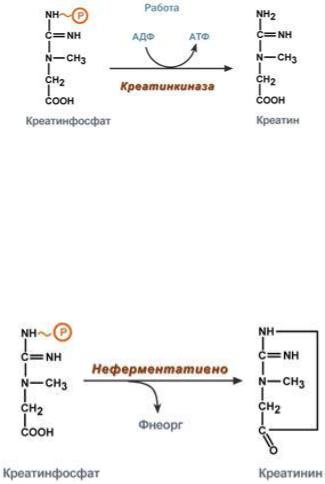
Креатинфосфокиназная реакция.
Креатин ~ фосфат + АДФ ←→А ТФ + креатин.
Это самый быстрый способ ресинтеза АТФ. Запасов креатинфосфата хватает для обеспечения мышечной работы в течение 20 с.
Максимально эффективен. Не требует присутствия кислорода, не дает побочных нежелательных продуктов, включается мгновенно. Его недостаток - малый резерв субстрата (хватает только на 20 с работы). Обратная реакция может протекать в митохондриях с использованием АТФ, образовавшейся в процессе окислительного фосфорилирования.
Мембрана митохондрий хорошо проницаема как для креатина, так и для креатин-фосфата, а креатинфосфокиназа есть и в саркоплазме, и в межмембранном пространстве митохондрий.
Миокиназная реакция. Протекает только в мышечной ткани! 2 АДФ.миокислота →АТФ + АМФ Реакция катализируется миокиназой (аденилаткиназой).
Главное значение этой реакции заключается в образовании АМФ - мощного аллостерического активатора ключевых ферментов гликолиза, гликогенолиза, ГБФ-пути. Необходимо отметить, что увеличение концентрации АМФ в саркоплазме оказывает активирующее влияние на ферменты гликолиза
Гликолиз, гликогенолиз.
Не требуют присутствия кислорода (анаэробные процессы). Обладают большим резервом субстратов. Используется гликоген мышц (2 % от веса мышцы) и глюкоза крови, полученная из гликогена печени.
Недостатки следующие.
1.Небольшая эффективность: 3 АТФ на один глюкозный остаток гликогена. 2.Накопление недоокисленных продуктов (лактат).
3.Гликолиз начинается не сразу - только через 10-15 с после начала мышечной работы. 4.Окислительное фосфорилирование.
Преимущества.
1.Это наиболее энергетически выгодный процесс - синтезируется 38 молекул АТФ при окислении одной молекулы глюкозы.
2.Имеет самый большой резерв субстратов: может использоваться глюкоза, гликоген, глицерин, кетоновые тела.
3.Продукты распада (CO2 и H2O) практически безвредны.
Недостаток: требует повышенных количеств кислорода.
Важную роль в обеспечении мышечной клетки кислородом играет миоглобин, у которого сродство к кислороду больше, чем у гемоглобина: при парциальном давлении кислорода, равном 30 мм.рт.ст., миоглобин насыщается кислородом на 100 %, а гемоглобин - всего на 30 %. Поэтому миоглобин эффективно отнимает у гемоглобин доставляемый им кислород.
Синтез креатина и креатинфосфата.
Креатин – вещество скелетных мышц, миокарда, нервной ткани. В виде креатинфосфата креатин является "депо" макроэргических связей, используется для быстрого ресинтеза АТФ во время работы клетки.
Особенно показательна роль креатина в мышечной ткани. Креатинфосфат обеспечивает срочный ресинтез АТФ в первые секунды работы (5-10 сек), когда никакие другие источники энергии (анаэробный гликолиз, аэробное окисление глюкозы, β-окисление жирных кислот) еще не активированы, и кровоснабжение мышцы не увеличено.
При мышечной работе ионы Са2+, высвободившиеся из саркоплазматического ретикулума, являются активаторами креатинкиназы
Около 3% креатинфосфата постоянно в реакции неферментативного дефосфорилирования превращается в креатинин
Синтез креатина идет последовательно в почках и печени в двух трансферазных реакциях. По окончании синтеза креатин с током крови доставляется в мышцы или мозг.
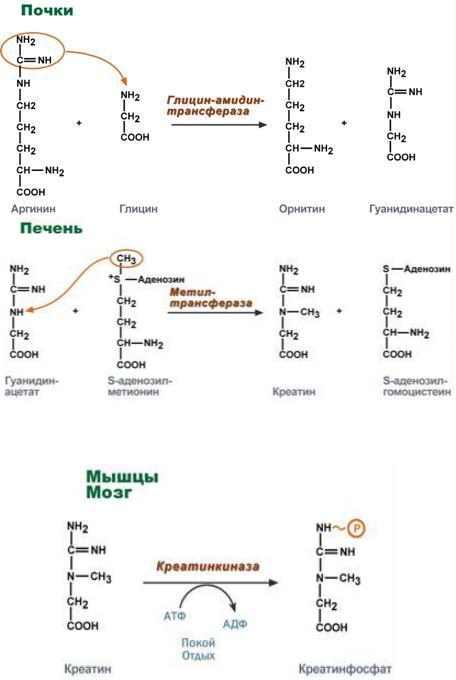
Здесь при наличии энергии АТФ (во время покоя или отдыха) он фосфорилируется с образованием креатинфосфата.
71.Компоненты межклеточного матрикса. Строение, роль белков коллагена и эластина, протеогликанов и гликозамингликанов.
межклеточный матрикс - супрамолекулярный комплекс, образованный сложной сетью связанных между собой макромолекул. В организме человека межклеточный матрикс формирует такие высокоспециализированные структуры, как хрящ, сухожилия, базальные мембраны, а также (при вторичном отложении фосфата кальция) кости и зубы.
Межклеточный матрикс костной и зубной ткани
Неорганическая часть В состав костей входит 99% всего кальция организма, 87% фосфора, ~ 60% магния и -25%
натрия. Кальций в костях находится в форме минерала гидроксиапатита, В костной ткани содержится много микроэлементов, таких как медь, стронций, барий, цинк, фтор и др., которые играют важную роль в обмене веществ в организме. Минеральная часть костей включает также карбонаты, гидроксиды и цитраты.
Минеральный состав зуба различен в разных его частях. Твѐрдые части зуба (эмаль, дентин и цемент) содержат от 70% (цемент и дентин) до 96 - 97% (эмаль) неорганических веществ. Основную часть этих веществ составляют фосфат кальция, входящий в состав кристаллов гидроксиапатита (75%), а также карбонат и фторид кальция.
Органическая часть Органические вещества костного матрикса представлены белками, липидами и
небольшим количеством протеогликанов.
Основной белок костной ткани - коллаген I типа (90 - 95%). Кроме него, в матриксе костей присутствуют такие белки, как коллаген V типа, остеонектин, остеокальцин, так называемые морфогенетические белки кости (BMP) и ферменты - щелочная фосфатаза (в остеобластах) и кислая фосфатаза (в остеокластах). Оба эти фермента служат маркѐрами соответствующих клеток костной ткани.
Главный компонент органических веществ зубной ткани - коллаген I типа. Углеводы и липиды присутствуют в небольших количествах. Содержание органических веществ в твѐрдых частях зуба варьирует от 2% (эмаль) до 30% (дентин и цемент).
Mежклеточный матрикс суставного хряща
Основные компоненты межклеточного хрящевого матрикса - коллаген II типа, агрекан, гиалуроновая кислота и вода. Кроме них, в мат-риксе находятся малые протеогликаны, коллагены VI, IX, XI типов, связывающий белок, другие неколлагеновые белки, разнообразные ростовые факторы. "Эндоскелет" хрящевого матрикса образован фибриллярной сетью, которая состоит из коллагенов II, IX и XI типов и придаѐт хрящу прочность.
Коллаген XI типа находится внутри фибрилл, образованных коллагеном II типа, он играет определѐнную роль в сборке этих фибрилл. Коллаген IX типа антипараллельно присоединяется к фибриллам коллагена II типа. Микрофибриллы, которые образуются тетрамерами коллагена VI типа, присоединяются к фибриллам коллагена II типа и к гиалуроновой кислоте.
Mежклеточный матрикс кожной ткани
Основной организующий компонент матрикса кожной ткани - коллаген VII типа.
Пучки фибрилл, образованные димерами этого коллагена, своими С-концами могут присоединяться к lamina densaбазальной мембраны (как бы "заякориваться" в ней) и образовывать петли в субэпидермисе. Такие "заякоренные" фибриллы могут соединять lamina densa базальной мембраны с "якорными дисками". "Заякоренные" фибриллы также захватывают фибриллы коллагена I и III типов
Таким способом "заякоренные" фибриллы коллагена VII типа обеспечивают присоединение эпидермиса к дерме.
Коллаген.
Коллаген составляет 25–33% от общего количества белка организма взрослого человека, или 6% от массы тела. Видимые в оптическом микроскопе коллагеновые волокна состоят из различимых в электронном микроскопе фибрилл – вытянутых в длину белковых молекул, названных тропоколлагеном. Тропоколлаген – основная структурная единица коллагена
Коллагеновое волокно представляет собой гетерогенное образование и содержит, кроме белка коллагена, другие химические компоненты. Молекула тропоколлагена – это белок коллаген. Одной из отличительных черт данного белка является то, что 1/3 всех его аминокислотных

остатков составляет глицин, 1/3 – пролин и 4-гидроксипролин, около 1% – гидроксилизин;
В разных тканях преобладают разные типы коллагена, а это, в свою очередь, определяется той ролью, которую коллаген играет в конкретном органе или ткани.
Коллаген - ярко выраженный полиморфный белок. В настоящее время известно 19 типов коллагена, которые отличаются друг от друга по первичной структуре пептидных цепей, функциям и локализации в организме.
ЭЛАСТИН
Эластин - основной белок эластических волокон, которые в больших количествах содержатся в межклеточном веществе таких тканей, как кожа, стенки кровеносных сосудов, связки, лѐгкие.
Резиноподобные свойства названных тканей обеспечиваются особенностями состава и строения эластина - гликопротеина
Общими для эластина и коллагена являются большое содержание глицина и пролина, наличие оксипролина, хотя последнего в эластине примерно в 10 раз меньше, чем в коллагене. Как и в коллагене, в эластине мало метионина и отсутствуют триптофан и цистеин. В отличие от коллагена в эластине значительно больше валина и ала-нина и меньше глутаминовой кислоты и аргинина.
При ферментативном гидролизеэластина в гидролизате обнаруживаются десмозин и изодесмо-зин. Очевидно, именно благодаря своей структуре десмозин и изодесмозин могут одновременно входить в состав четырех пептидных цепей. По-видимому, этим можно объяснить, что эластин в отличие от других фибриллярных белков способен растягиваться в двух направлениях.
Оказалось, что это лизиннорлейцин, который обеспечивает наряду с десмозином и изодесмозином поперечные связи в молекуле эластина:
Гликозаминогликаны - линейные отрицательно заряженные гетерополисахариды. гликозаминогликаны могут связывать большие количества воды, в результате чего межклеточное вещество приобретает желеобразный характер.
Гликозаминогликаны представляют собой длинные неразветвлѐнные цепи гетерополисахаридов. Они построены из повторяющихся дисахаридных единиц. Одним мономером этого дисахарида является гексуроновая кислота, вторым мономером - производное аминосахара/
Н-р, гиалуроновая к-та:
Протеогликаны - высокомолекулярные соединения, состоящие из белка (5-10%) и гликозаминогликанов (90-95%). Они образуют основное вещество межклеточного матрикса соединительной ткани
Основной протеогликан хрящевого матрикса называется агрекан. Это очень большая молекула, в которой к одной полипептидной цепи присоединены до 100 цепей хондроитинсульфатов и около 30 цепей кератансульфатов. В хрящевой ткани молекулы агрекана собираются в агрегаты с гаалуроновой кислотой и небольшим связывающим белком. Оба компонента присоединяются к агрекану нековалент-ными связями в области домена G1.
72.Минеральные компоненты пищи. Классификация. Биохимическая функция. Биоусвояемые формы. Биохимическая функция цинка, селена и хрома, меди, железа.
Минеральные вещества В количественном отношении наиболее важным неорганическим компонентом пищи является вода. У взрослого человека суточная потребность в воде составляет примерно 2,4 л. Эта цифра включает воду, поступающую в организм с твердой и жидкой пищей, в виде напитков, а также воду, образующуюся в дыхательной цепи
Жизненно необходимые элементы подразделяются на макроэлементы (суточная потребность >100 мг) и микроэлементы (суточная потребность <100 мг). К макроэлементам относятся натрий (Na), калий (К), кальций (Ca), магний (Мg), хлор (Cl), фосфор (Р), сера (S) и иод (I). К жизненно важным микроэлементам, необходимым лишь в следовых количествах, относятся железо (Fe), цинк (Zn), марганец (Μn), медь (Cu), кобальт (Со), хром (Сr), селен (Se) и молибден (Мо). Фтор (F) не принадлежит к этой группе, однако он необходим для поддержания в здоровом состоянии костной и зубной ткани.
Цинк.
Биологическая роль цинка определяется его необходимостью для нормального роста, развития и полового созревания, а также обеспечения нормального кроветворения, вкуса и обоняния. Цинк необходим для синтеза белков, контролирует сократительную функцию мышц и участвует в синтезе инсулина. требуется для нескольких ферментов, таких как карбоксипептидаза, алкогольнаядегидрогеназа печени, углеродная ангидраза.
Железо.
Этот элемент тесно связан с важнейшими функциями организма, является незаменимой составной частью гемоглобина и миоглобина. Железо входит в состав окислительновосстановительных ферментов, участвует в насыщении мышечной ткани кислородом и играет важную роль в кроветворении. Требуется для многих белков и ферментов, особенно гемоглобина. Источники в рационе включают красное мясо, зелѐные
листовые овощи, рыбу (тунец, лосось),сухофрукты, бобы, |
виноград, |
цельные |
и |
обогащѐнные зѐрна. |
|
|
|
Селен.
Биохимические функции селена определяют селенсодержащие белки (СБ). Недостаток микроэлемента может приводить к нарушению клеточной целостности, изменению метаболизма тиреоидных гормонов, активности биотрансформирующих ферментов, усилению токсического действия тяжѐлых металлов, повышению концентрации глютатиона в плазме.
Характерной особенностью СБ млекопитающих является то, что они, по-видимому, связаны с окислительно-восстановительными процессами, проходящими внутри клетки и вне ее. кофактор, существенный для активности
антиоксидантных ферментов, таких как глутатионпероксидаза.
Медь.
Медь встречается в большом количестве ферментов, например, в цитохром-с-оксидазе, в содержащем медь и цинк ферменте супероксид дисмутазе, и в переносящем молекулярный кислород белке гемоцианине. Предполагается, что медь и цинк конкурируют друг с другом в процессе усваивания в пищеварительном тракте, поэтому избыток одного из этих элементов в пище может вызвать недостаток другого элемента. При недостатке меди в хондро- и остеобластах снижается активность ферментных систем и замедляется белковый обмен, в результате замедляется и нарушается рост костных тканей
Хром.
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина),углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
73.Макро- и микроэлементы. Роль кальция в метаболизме и костной системе (обосновать роль витаминов и других минералов).
Все минеральные вещества в зависимости от их концентрации, подразделяются на макро- и микроэлементы. Содержание макроэлементов превышает 50 мг/кг массы тела (натрий и калий, кальций, магний, фосфат, хлорид, сульфат). Содержание микроэлементов составляет менее 50 мг/кг массы тела (медь, цинк, селен, кобальт и др.).
Микроэлементы выполняют важную физиол. роль и необходимы для нормальной жизнедеятельности. Дефицит или избыток их приводит к т. наз. биогеохим. эндемиям - заболеваниям растений, животных и человека. Территории распространения этих заболеваний наз. биогеохим. провинциями. Так, распространение эндемич. зоба во мн. горных и внутри-континент. районах связано с дефицитом I в пище и воде, кариес зубов-с дефицитом F в воде, флюороз - тяжелое заболевание скелета-с избытком F
Для борьбы с дефицитом микроэлементов используют фторирование питьевой воды, иодирование поваренной соли, препараты Со (витамин В12) в медицине.
Эти элементы слагают плоть живых организмов. К макроэлементам относят те элементы, рекомендуемая суточная доза потребления которых составляет более 200 мг. Макроэлементы, как правило, поступают в организм человека вместе с пищей.
Биогенные элементы
Кислород — 70%Углерод — 17%Водород — 10%Азот — 3%
Эти макроэлементы называют биогенными (органогенными) элементами или макронутриентами. Из макронутриентов преимущественно построены такие органические вещества, как белки, жиры, углеводы и нуклеиновые кислоты.
Кальций.
Кальций - наиболее распространенный элемент в организме
Кроме структурной функции кальций влияет на проницаемость клеточных мембран, действуя как вторичный мессенжер, инициируя ответы клеток на различные стимулы. Перемещение кальция из внутриклеточного пространства во внеклеточную среду обеспечивает такие события, как дифференцировку клетки, сокращение, секрецию и перистальтику. Множество ферментов, включая те, что участвуют в системе свертывании крови, зависят от кальция. Кальций влияет на функцию эндокринных желез (особенно околощитовидных), оказывает противовоспалительное и десенсибилизирующее действие, находится в биологическом антагонизме с ионами натрия и калия. Кальций необходим для нормальной возбудимости нервной системы, сократимости мышц, является активатором многих ферментов и гормонов, представляет собой важный компонент, необходимый для свертывания крови.
Кальций обладает высокой биологической активностью, выполняет в организме
