
книги / Технология переработки нефти и газа. Первичная переработка нефти и газа
.pdfи механических примесей (8) от газового конденсата и его после- дующую стабилизацию (9) и переработку.
Сероводород, как правило, перерабатывается на месте (10) с по- лучением элементарной серы.
Углеводороды тяжелее пропана перерабатываются на фракцио- нирующей установке (12) с получением ШФЛУ и стабильного газо- вого бензина.
4.3. Подготовка углеводородных газов к переработке
Углеводородные газы помимо чисто углеводородных компонен- тов могут содержать в своем составе H2S, N2, CO2, капельки конденса- та, воды, частички горных пород, т.е. они являются дисперсной систе- мой с жидкой и твердой дисперсными фазами. В связи с этим, прежде чем газ направлять на переработку, его готовят – очищают от мехпри- месей, капелек конденсата и воды, удаляют кислые компоненты.
4.3.1. Очистка газов от жидкой и твердой дисперсных фаз
Очистку газа от дисперсной фазы (механических частиц, капе- лек конденсата и воды) проводят с помощью различных сепарацион- ных устройств. В зависимости от дисперсного состава и требований на очистку газа применяют различные по эффективности и конструк- ции сепарационные устройства, которые по принципу действия де- лятся на гравитационные, инерционного типа (насадочные), центро- бежные и фильтрующие. В большинстве случаев сепарационные уст- ройства объединяют в себе несколько из этих принципов.
Гравитационные сепараторы. Они бывают различных конст-
рукций (горизонтальные, вертикальные, шаровые). Однако общим для них является наличие отстойной (осадительной) камеры, где идет отделение дисперсных частиц под действием силы тяжести. В низу сепаратора имеется встроенный или вынесенный сборник улавливае- мой пыли или жидкости. Такой тип сеператоров обычно используется первым по ходу очистки газа, который на этом участке содержит наи- большее количество капель жидкости, а конкретная конструкция се-
131
ператоров выбирается с учетом таких факторов, как производитель- ность по газу, давление, наличие в газе механических примесей, тре- буемая степень очистки и др.
Инерционные сепараторы насадочного типа. Представляют со-
бой аппараты, заполненные насадкой с развитой поверхностью кон- такта фаз (от 10 до 500 м2/м3). Улавливание капель происходит за счет их ударения о поверхность насадки и резких многократных поворотов потока газа в каналах насадки.
В качестве насадок применяют кольца Рашига, многослойные жалюзи из пластин или уголков, а также сетчатые пакеты из рукав- ной, вязаной чулочной вязкой сетки из проволоки (d = 0,25 мм). Сте- пень удаления капель жидкости такими сепараторами может дости- гать 99 %.
Данные сепараторы работают следующим образом: газ, двигаясь вертикально снизу вверх, огибает насадку, и за счет инерционных сил
исил трения из него выделяются капли жидкой фазы, стекающие в низ аппарата (в сборник). Так как жидкость стекает в низ аппарата навстречу потоку газа, то при определенной скорости газа может про- изойти остановка течения пленки жидкости (зависание жидкости и за- хлебывание насадки). Скорость газа, при которой наступает это явле- ние, называется критической (Wкр).
Обычно рабочую скорость газа принимают равной 0,5–0,85 от Wкр. Для сетчатых сепараторов Wкр в 1,5–2 раза выше, чем для жа- люзийных. Обычно их используют для окончательной очистки газа
иустанавливают на концевых участках ступени очистки газа. Центробежные сепараторы. В них для отделения дисперсных
частиц используют центробежную силу, возникающую в предвари- тельно закрученном потоке газа. При этом чем выше скорость закрут- ки и меньше радиус закрученного потока, тем выше эффективность сепаратора.
Существует 2 типа центробежных сепараторов – циклонные и прямоточные. В первом случае поток газа входит в сепаратор тан- генциально и завихряется вокруг центральной трубы. Очищенный газ
132
отводится сверху, а жидкость под действием центробежной силы от- брасывается к корпусу и стекает в сборник. Эффективность таких се- параторов 90–95 %.
Фильтрующие сепараторы предназначены для окончательной тонкой очистки газа от дисперсных включений (d = 0,5–10 мкм). В качестве фильтрующего материала используют стекловолокно.
Для очистки углеводородных газов от механических примесей используют также электрофильтры, действие которых основано на ионизации молекул газа. Образующиеся ионы двигаются в элек- трическом поле к противоположно заряженным электродам. При этом отрицательно заряженные ионы передают заряд пылинкам и увлека- ют их к осадительным электродам, где они разряжаются и оседают. Степень очистки 90–98 %.
Помимо сухой очистки для удаления мехпримесей из УГ ис- пользуют и так называемую мокрую очистку, основанную на контак- те запыленного газа с жидкостью, которая и удерживает частицы пы-
ли. Ее проводят в скрубберах, мокрых циклонах, промывательных ап-
паратах, барботерах. В таких аппаратах степень очистки составляет 80–90 %, а для пенных барботеров она достигает 98–99 % (для частиц диаметром более 5 микрон).
4.3.2. Очистка углеводородных газов от вредных примесей
К вредным примесям углеводородных газов относятся коррози- онно-активные серосодержащие соединения, негорючие инертные га- зы. Это в первую очередь Н2S, СOS (серооксид углерода), СS2 (серо- углерод), меркаптаны (СnH2n–1–SH), сульфиды (R–S–R/), дисульфиды
(R–S–S–R/), СО2, азот, гелий.
Природный газ очищают даже при малых количествах Н2S, т.к. допустимое содержание последнего перед закачкой в газопрово- ды не должно превышать 20 мг/м3. Кроме того, очистку газа проводят с целью утилизации сернистых соединений.
Характеристики вредных примесей, входящих в состав углево- дородных газов, представлены ниже.
133
4.3.2.1. Характеристики вредных примесей
Сероводород – наиболее активное из серосодержащих соедине- ний. В нормальных условиях – бесцветный газ с неприятным запахом тухлых яиц, плотностью 1,93 кг/м3. Очень ядовит: острое отравление человека наступает уже при концентрации 0,2–0,3 мг/м3, а концентра- ция выше 1 мг/м3 – смертельна. Предельно допустимая концентрация (ПДК) сероводорода в воздухе – не более 0,008 мг/м3.
Сероводород хорошо растворим в воде (около 3,0 об./об. воды при нормальном давлении). Диапазон взрывоопасных концентраций его смеси с воздухом достаточно широк и составляет от 4 до 45 об. %.
При контакте с металлами (особенно если в газе содержится влага) вызывает сильную коррозию.
Серооксид углерода – в нормальных условиях бесцветный лег- ковоспламеняющийся газ, не имеющий запаха, конденсирующийся при температуре минус 50,2 °С.
Теплота испарения серооксида углерода – 15,2 кДж/кг. Пределы взрывоопасных концентраций смеси его с воздухом – 12–29 об. %.
Хорошо растворим в сероуглероде, толуоле, этаноле и воде. При нагревании разлагается с образованием СО2, CS2, СО и серы. ПДК се- рооксида углерода – не более 1 мг/м3 в производственных помещени- ях и не более 0,15 мг/м3 в населенных пунктах.
Сероуглерод – в нормальных условиях бесцветная жидкость плот- ностью 129,7 кг/м3, кипящая при 46,3 °С. Хорошо растворим в этаноле и хлороформе и ограниченно растворим в воде (при 0 °С – 0,242 об. %, при 20 °С – 0,210 об. %, а при 50 °С – 0,012 об. %). При повышенных температурах реагирует с водородом, образуя сероводород.
Сероуглерод ядовит, вызывает острые отравления при концен- трациях в воздухе 0,001 мг/м3. Используется в промышленности как экстрагирующее вещество.
Меркаптаны (тиолы) – сероорганические соединения с резким неприятным запахом, не растворимые в воде, но хорошо растворяю- щиеся в органических растворителях.
134
При контакте с металлами вступают с ними в реакции, образуя меркаптиды металлов (меркаптановая коррозия). Они являются ядами для большинства катализаторов.
Из-за резкого запаха меркаптаны (этилмеркаптан) используют в качестве одорантов природного газа при испытании на плотность газовых сетей и систем. При нагревании до 300 °С меркаптаны разла- гаются с образованием сульфидов и сероводорода.
Сульфиды (тиоэфиры) – хорошо растворимые в углеводородах вещества. Они нейтральны, не реагируют со щелочью. При нагрева- нии до 400 °С разлагаются с образованием сероводорода и двух ал- кенов.
Дисульфиды – также легко растворимые в углеводородах веще- ства. По сравнению с сульфидами более реакционноспособны. При нагревании разлагаются на меркаптаны, алкены и сероводород.
Диоксид углерода – бесцветный негорючий газ, обладающий кислыми свойствами. При нормальном давлении и температуре ми- нус 78,5°С переходит в твердое состояние («сухой лед»), минуя жид- кое состояние. В воде диоксид углерода растворим ограничен- но (0,335 об. % при 0 °С и 0,169 об. % при 20 °С). Является термиче- ски очень стойким веществом и диссоциирует лишь при температурах выше 2000 °С.
Азот и гелий – инертные газы, ухудшающие горючие свойства природного газа. Хотя последний содержится в газе в относительно небольших количествах, его специально извлекают как ценный про- дукт для нужд народного хозяйства.
4.3.2.2.Методы очистки углеводородных газов
ихарактеристики поглотителей
Очистку газов предпринимают не только для доведения содер- жания в них вредных примесей до установленных норм, но и для их извлечения с целью промышленной утилизации. Более 30 % мирового производства серы получают из природных газов, богатых сероводо- родом, содержание которого в некоторых из них достигает 50– 70 об. %. Это, в частности, месторождения Харметтен, Пантер-Ривер и Барберри в Канаде, Миссисипи в США, Жаолангиуанг в КНР и др.
135
Внастоящее время существует много методов очистки УГ от вредных примесей, которые условно можно разделить на 2 груп-
пы – абсорбционные и адсорбционные. Первые допускают любое на-
чальное содержание примесей в газе. Адсорбционные используют, когда содержание примесей не превышает 3–5 об. %, однако они по- зволяют очистить газ более глубоко.
Абсорбционные методы по характеру используемого абсорбента делятся на методы хемосорбции, физической абсорбции, комбиниро- ванные и окислительные.
Воснове физической абсорбции лежит физическое растворение извлекаемых компонентов в абсорбенте. В качестве последнего ис- пользуют N-метилпирролидон, гликоли (ди- и триэтиленгликоли), трибутилфосфат, сульфолан, метанол и др.
Хемосорбция основана на химическом взаимодействии Н2S и CО2 с активным компонентом абсорбентов, в качестве которых ис- пользуют моно-, ди- и триэтаноламины, диизопропаноламин, метил- диэтаноламин (МДЭА), щелочи.
В комбинированных процессах используют смешанные абсор- бенты (хемосорбенты и физические абсорбенты). Например, в про- цессе «Сульфинол» поглотителями являются сульфолан и диизопро- паноламин.
Окислительные процессы основаны на необратимом превраще- нии поглощаемого сорбентом сероводорода в элементарную серу. Сорбент в этом случае содержит катализатор окисления и представ- ляет собой водно-щелочной раствор катализатора (горячий раствор мышьяковых солей, триалон Б и др.).
Адсорбционные процессы основаны на селективном физическом поглощении Н2S и CО2 в порах твердых поглотителей, в качестве ко- торых используют активные угли или синтетические цеолиты.
Выбор того или иного метода очистки зависит от многих факто- ров, таких как начальные и конечные концентрации Н2S и CО2, об- ласть применения очищаемого газа (в быту, в химии, в двигателях), возможность использования определенного поглотителя и другие
136
факторы, однако основным критерием является концентрация Н2S, CО2 и сероорганических соединений в исходном газе.
При высоких концентрациях кислых компонентов применяют методы физической абсорбции, основной недостаток которых – низ- кая избирательность в отношении углеводородов. Хемосорбционные и комбинированные процессы рекомендуются при средних концен- трациях Н2S и CО2, а окислительные – при низких.
При любом методе очистки большое значение имеют свойства поглотителя. Основные требования, предъявляемые к нему:
–поглотитель должен иметь низкое давление насыщенного па- ра, чтобы потери с очищаемым газом были минимальны;
–он должен обладать высокой способностью поглощать кислые компоненты в широком интервале их парциальных давлений;
–должен иметь невысокую вязкость для обеспечения хорошего контакта с газом;
–иметь малую растворяющую способность по отношению к уг- леводородам;
–обладать низкой коррозионной активностью;
–иметь высокую стойкость к окислению и др.
Характеристики некоторых физических и химических абсорбен- тов приведены в табл. 4.4 и 4.5.
Хемосорбционные процессы очистки
Из них наиболее широкое применение получили процессы очи- стки аминами (моно- и диэтаноламины), которые при взаимодействии с Н2S и CО2 дают химические соединения, распадающиеся при повы- шении температуры и снижении давления. При этом протекают сле- дующие реакции:
2RNH2 + H2S ↔ |
(RNH3)2S, |
(4.1) |
2RNH2 + CO2 + H2O ↔ |
(RNH3)2CO3 . |
(4.2) |
Рассмотрим технологическую схему очистки УГ от кислых со- единений МЭА (рис. 4.2).
137
Таблица 4.4
Характеристики некоторых физических абсорбентов
Абсорбент |
Формула |
Молекуляр- |
Относительная |
Температура |
|
ная масса |
плотность, ρ 420 |
кипения, °С |
|||
Этиленгликоль |
С6Н6О2 |
62 |
1,116 |
197 |
|
Диэтиленгликоль |
С4Н10О3 |
106 |
1,118 |
245 |
|
(ДЭГ) |
|||||
|
|
|
|
||
Триэтиленгликоль |
С6Н14О4 |
150 |
1,126 |
287 |
|
(ТЭГ) |
|||||
|
|
|
|
||
Сульфолан (тетрагид- |
С4Н12О2 |
124 |
1,260 |
286 |
|
ротиофендиоксид) |
|||||
|
|
|
|
||
N-метилпирролидон |
С5Н11N |
85 |
1,030 |
206 |
|
(N-МП) |
|||||
|
|
|
|
||
Трибутилфосфат |
(С4Н9О)3РО |
266 |
0,970 |
289 |
|
(ТБФ) |
|||||
|
|
|
|
Таблица 4.5
Некоторые эксплуатационные свойства аминов (хемосорбентов)
|
Теплота ис- |
Теплота реакции |
Поглоти- |
Предпочтитель- |
||
Наименование |
парения при |
при взаимодейст- |
тельная ем- |
ное содержание |
||
0,1 МПа, |
|
вии с |
кость, м3/м3 |
в растворе, |
||
|
кДж/кг |
Н2S |
|
CО2 |
|
мас. % |
МЭА |
1488 |
1510 |
|
1920 |
8–30 |
10–20 |
ДГА |
918 |
1570 |
|
1980 |
15–52 |
50–65 |
ДЭА |
1207 |
1190 |
|
1520 |
22–75 |
20–40 |
ДИПА |
773 |
1220 |
|
1630 |
15–60 |
20–40 |
ТЭА |
964 |
930 |
|
1470 |
– |
– |
МДЭА |
– |
1050 |
|
1340 |
– |
– |
Согласно схеме исходный газ в абсорбере 1 контактирует с этано- ламином во 2 ступени – сначала со слаборегенерированным, а затем – с полностью регенерированным потоком. Абсорбент с низа абсорбера поступает в десорбер 3, где отделяется углеводородный газ, а насыщенный кислыми компонентами поглотитель через теплообмен- ники 6 поступает в регенерационную колонну 2, в которой комплекс- ные соединения Н2S и CО2 с амином разлагаются, а выделяющиеся кислые газы выходят сверху колонны 2. С низа колонны 2 регенериро-
138
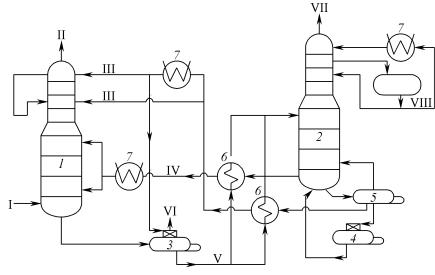
ванный поглотитель через ребойлер 5 и охладительные аппараты 6 и 7 направляются в абсорбер. Часть абсорбента при этом циркулирует че- рез очиститель 4, где отделяются накапливаемые в растворе неразла- гающиеся соединения этаноламина с СОS и СS2, которые снижают по- глотительную способность абсорбента по Н2S и CО2.
Рис. 4.2. Технологическая схема хемосорбционной очистки газа МЭА:
1 – абсорбер; 2 – десорбер (регенератор МЭА); 3 – промежуточный десорбер; 4 – очиститель; 5 – ребойлер; 6 – теплообменники; 7 – холодильники.
I – исходный газ; II – очищенный газ; III – регенерированный МЭА;
IV – слаборегенерированный МЭА; V – насыщенный МЭА; VI – топливный газ;
VII – смесь кислых газов; VIII – циркуляционное орошение
Технологические параметры процесса:
абсорбер: t = 35–40 °C, |
Р = 3–5 МПа; |
десорбер: t = 125 °С, |
Р = 0,3–0,8 МПа. |
Однако использование МЭА имеет ряд недостатков. Лучшие ре- зультаты дает использование ДЭА, т.к. он не дает неразлагающихся соединений с СОS и СS2, имеет меньшие потери от испарения, более высокую селективность к Н2S по сравнению с МЭА и др.
139
Технологическая схема аналогична приведенной на рис. 4.2, только отсутствует очиститель 4. Концентрация ДЭА в зависимости от разновидности процесса от 20–25 до 25–35 % (поглотительная спо- собность более концентрированного раствора выше). В настоящее время на установках очистки газа от Н2S в качестве хемосорбента по- лучил применение МДЭА (метилдиэтаноламин). Его эффективность максимальна при концентрации 30–50 мас. %. На реальных техноло- гических установках используется концентрация около 70 мас. %, т.к. повышенная концентрация позволяет существенно снизить цир- куляцию раствора.
Процессы очистки УГ растворами солей щелочных металлов
Эти процессы основаны на хемосорбционной активности вод- ных растворов карбонатов Na и К по отношению к основным серосо- держащим соединениям газа (исключая меркаптаны). Для повышения активности растворов в них вводят активаторы. Основные протекаю- щие реакции:
К2СО3 + Н2S ↔ |
КНСО3 + КНS, |
(4.3) |
СОS + Н2О ↔ |
СО2 + Н2S, |
(4.4) |
К2СО3 + СО2 + Н2О ↔ 2КНСО3. |
(4.5) |
|
Технологическая схема аналогична схеме очистки аминами. Наи- более распространен поташ-процесс, в котором в качестве поглотителя используются 25–35 %-й раствор К2СО3, очищающий газ от Н2S, СО2, СОS и СS2. Абсорбция идет при t = 110–115 °С, Р = 2–8 МПа. Регене- рация поглотителя протекает при t = 115–120 °С, давлении, близком к атмосферному, или под вакуумом.
Процесс применяют для очистки УГ с высоким содержанием СО2 и общей концентрацией кислых газов 5–8 %.
К недостаткам процесса можно отнести:
–трудность удаления меркаптанов;
–коррозию оборудования;
– необходимость иметь низкое соотношение количеств Н2S и CО2 в УГ.
140
