
- •Предметы и задачи микробиологии. Разделы микробиологии
- •История развития микробиологии и вирусологии
- •Систематика, классификация микроорганизмов
- •Морфология микроорганизмов
- •Строение бактериальной клетки. Обязательные и необязательные компоненты
- •Движение бактерий. Типы жгутикования.
- •Общая характеристика вирусов и фагов
- •Взаимодействие вирусной и бактериальной клетки: механизмы, исход, взаимодействия
- •Общая характерстика грибов
- •Систематика грибов. Зигомицеты
- •12. Систематика грибов. Базидиомицеты: характеристика, представители.
- •13. Систематика грибов. Дейтеромицеты: характеристика, представители.
- •Значение дейтеромицетов
- •14. Дрожжи: характеристика, систематика, применение.
- •15. Понятие об обмене веществ. Энергетический и пластический обмены.
- •16. Химический состав организмов. Органические и неорганические вещества
- •17. Ферменты: классификация, свойства, механизмы действия.
- •По своему составу ферменты делятся на:
- •Виды кофакторов:
- •18. Применение микробных ферментов в практической деятельности.
- •19. Поступление веществ в клетку.
- •20. Типы питания микроорганизмов. Потребность микроорганизмов в
- •21. Энергетический обмен. Гликолиз.
- •Подготовительный этап
- •Бескислородное окисление, или гликолиз
21. Энергетический обмен. Гликолиз.
Энергетический обмен (катаболизм, диссимиляция) — совокупность реакций расщепления органических веществ, сопровождающихся выделением энергии. Энергия, освобождающаяся при распаде органических веществ, не сразу используется клеткой, а запасается в форме АТФ и других высокоэнергетических соединений. АТФ — универсальный источник энергообеспечения клетки. Синтез АТФ происходит в клетках всех организмов в процессе фосфорилирования — присоединения неорганического фосфата к АДФ.
У аэробных организмов (живущих в кислородной среде) выделяют три этапа энергетического обмена: подготовительный, бескислородное окисление и кислородное окисление; у анаэробных организмов (живущих в бескислородной среде) и аэробных при недостатке кислорода — два этапа: подготовительный, бескислородное окисление.
Подготовительный этап
Заключается в ферментативном расщеплении сложных органических веществ до простых: белковые молекулы — до аминокислот, жиры — до глицерина и карбоновых кислот, углеводы — до глюкозы, нуклеиновые кислоты — до нуклеотидов. Распад высокомолекулярных органических соединений осуществляется или ферментами желудочно-кишечного тракта или ферментами лизосом. Вся высвобождающаяся при этом энергия рассеивается в виде тепла. Образовавшиеся небольшие органические молекулы могут быть использованы в качестве «строительного материала» или могут подвергаться дальнейшему расщеплению
Бескислородное окисление, или гликолиз
Этот этап заключается в дальнейшем расщеплении органических веществ, образовавшихся во время подготовительного этапа, происходит в цитоплазме клетки и в присутствии кислорода не нуждается. Главным источником энергии в клетке является глюкоза. Процесс бескислородного неполного расщепления глюкозы — гликолиз.
Потеря электронов называется окислением, приобретение — восстановлением, при этом донор электронов окисляется, акцептор восстанавливается.
Следует отметить, что биологическое окисление в клетках может происходить как с участием кислорода:
А + О2 → АО2,
так и без его участия, за счет переноса атомов водорода от одного вещества к другому. Например, вещество «А» окисляется за счет вещества «В»:
АН2 + В → А + ВН2
или за счет переноса электронов, например, двухвалентное железо окисляется до трехвалентного:
Fe2+ → Fe3+ + e—.
Гликолиз — сложный многоступенчатый процесс, включающий в себя десять реакций. Во время этого процесса происходит дегидрирование глюкозы, акцептором водорода служит кофермент НАД+ (никотинамидадениндинуклеотид). Глюкоза в результате цепочки ферментативных реакций превращается в две молекулы пировиноградной кислоты (ПВК), при этом суммарно образуются 2 молекулы АТФ и восстановленная форма переносчика водорода НАД·Н2:
С6Н12О6 + 2АДФ + 2Н3РО4 + 2НАД+ → 2С3Н4О3 + 2АТФ + 2Н2О + 2НАД·Н2.
Дальнейшая судьба ПВК зависит от присутствия кислорода в клетке. Если кислорода нет, у дрожжей и растений происходит спиртовое брожение, при котором сначала происходит образование уксусного альдегида, а затем этилового спирта:
С3Н4О3 → СО2 + СН3СОН,
СН3СОН + НАД·Н2 → С2Н5ОН + НАД+.
У животных и некоторых бактерий при недостатке кислорода происходит молочнокислое брожение с образованием молочной кислоты:
С3Н4О3 + НАД·Н2 → С3Н6О3 + НАД+.
В результате гликолиза одной молекулы глюкозы высвобождается 200 кДж, из которых 120 кДж рассеивается в виде тепла, а 80% запасается в связях АТФ.


22. Источники энергии у микроорганизмов разнообразны.
У фотоавтотрофов источником энергии служит видимый свет. Световая энергия, улавливаемая фотоактивными пигментами клетки в процессе фотосинтеза, трансформируется в химическую энергию, обеспечивающую энергетические потребности клетки.
Источником энергии для биосинтеза клеточных веществ из СО2 у хемоавтотрофов является химическая энергия, высвобождаемая в результате окисления кислородом воздуха неорганических соединений (NH3, H2S и др.).
Хемоорганотрофы (хемогетеротрофы) получают энергию в процессах окисления органических соединений.
Любое природное органическое вещество и многие синтетические могут быть использованы гетеротрофами, но не всеми. Одни окисляют многие органические вещества, другие – лишь небольшой набор их, имеются и такие, которые проявляют большую специфичность по отношению к энергетическому материалу.
Поскольку возбудители порчи пищевых продуктов и используемые при переработке пищевого сырья обносят к хемоорганотрофам, их энергодающие процессы и рассматриваются ниже.
Окисление органических веществ может происходить различными путями:
1. Прямым, т. е. присоединением к веществу кислорода.
2. Непрямым, т. е. дегидрогенерированием (отнятием водорода). Отнятый от окисляемого вещества водород переносится на другое вещество, которое при этом восстанавливается.
3. Путем переноса электронов (е~) от одного вещества к другому. Вещество, теряющее электроны, окисляется, а присоединяющее их – восстанавливается.
Вещество, отдающее водород (электроны), называется донором, а вещество, присоединяющее их, – акцептором.
Биологическое окисление (в клетках) органических веществ происходит чаще путем дегидрогенерирования. Так как атом водорода состоит из протона (Н+) и электрона (е~), перенос водорода с одного вещества на другое включает и перенос электрона.
Перенос водорода (электрона) от подвергающегося окислению вещества к акцептору осуществляется различными окислительно-восстановительными ферментами.
Реакцию окисления – восстановления можно изобразить следующим образом:

Конечным акцептором водорода может быть кислород воздуха или другое вещество, способное восстанавливаться.
В зависимости от конечного акцептора водорода хемоорганотрофные микроорганизмы делят на две группы:
Аэробы, окисляющие органические вещества с использованием молекулярного кислорода, который и является конечным акцептором водорода;
Анаэробы, которые в энергетических процессах не используют кислород. Конечными акцепторами водорода служат органические или неорганические соединения.
Аэробные: Многие аэробные микроорганизмы, к которым относят грибы, некоторые дрожжи и многие бактерии, подобно высшим организмам (растениям, животным), окисляют органические вещества полностью до минеральных веществ – углекислого газа и воды. Процесс этот называется дыханием.
В качестве энергетического материала в процессе дыхания микроорганизмы часто используют углеводы. При этом сложные (ди-, три- и полисахариды) ферментативным путем гидролизу-ются до моносахаров, которые и подвергаются окислению.
Этот
процесс в общем виде может быть представлен
следующим уравнением: ![]()
Гликолитический распад глюкозы происходит следующим образом:
1. Первым этапом является активирование глюкозы путем фосфорилирования при участии АТФ и фермента фосфотрансферазы (гексокиназы). К молекуле глюкозы от молекулы аденозинтрифосфорной кислоты (АТФ) присоединяется концевой фосфатный остаток, обладающий макроэргической (со) связью. Образуется глюкозо-6-фосфат, а АТФ превращается в аденозиндифосфорную кислоту (АДФ).
2. Глюкозо-6-фосфат путем изомеризации при участии фермента глюкозофосфатизомеразы переходит во фруктозо-6-фосфат.
3. Фруктозо-6-фосфат затем фосфорилируется за счет АТФ при участии соответствующей фосфотрансферазы (фосфофруктокиназы). Образуется фруктозо-1,6-дифосфат, а АТФ превращается в АДФ. Вторичное фос-форилирование молекулы гексозы приводит к ее дальнейшему активированию.
4. Фруктозо-1,6-дифосфат расщепляется при участии фермента альдолазы на две молекулы фосфотриоз. Одна из них — фосфодиоксиацетон, другая — фосфат глицеринового альдегида. Оба эти вещества легко могут превращаться друг в друга.
Дальнейшему превращению подвергаются две молекулы 3-фосфоглицеринового альдегида, так как фосфат диоксиацетона под действием фермента триозофосфатизомеразы превращается в 3-фосфоглицериновый альдегид.
5. Следующим этапом является окисление 3-фосфоглицеринового альдегида. Эта реакция катализируется дегидрогеназой, коферментом которой является НАД (см. с. 53). В окислении участвует фосфорная кислота.
Молекула 3-фосфоглицеринового альдегида присоединяет фосфат, а водород переносится на кофермент НАД, который восстанавливается в НАД·Н2. Освобождающаяся при окислении фосфоглицеринового альдегида энергия сосредоточивается в, макроэргической связи (∞) образующейся 1,3-дифосфоглицериновой кислоты.
6. В дальнейшем фосфатная группа 1,3-дифосфоглицериновой кислоты, имеющая макроэргическую связь, при участии фермента фосфоглицератки-назы переносится на молекулу аденозиндифосфорной кислоты. Образуется 3-фосфоглицериновая кислота, а АДФ превращается в АТФ. Таким образом свободная энергия окисления альдегидной группы запасается в молекуле
7. З-Фосфоглицериновая кислота под влиянием фермента фосфоглицеромутазы превращается в 2-фосфоглицериновую кислоту.
8. Под действием фермента энолазы 2-фосфоглицериновая кислота, теряя воду, переходит в энольную форму фвсфопировиноградной кислоты. При этом происходит перераспределение внутримолекулярной энергии, большая часть которой сосредоточивается в форме макроэргической фосфатной связи фосфоэнолпировиноградной кислоты.
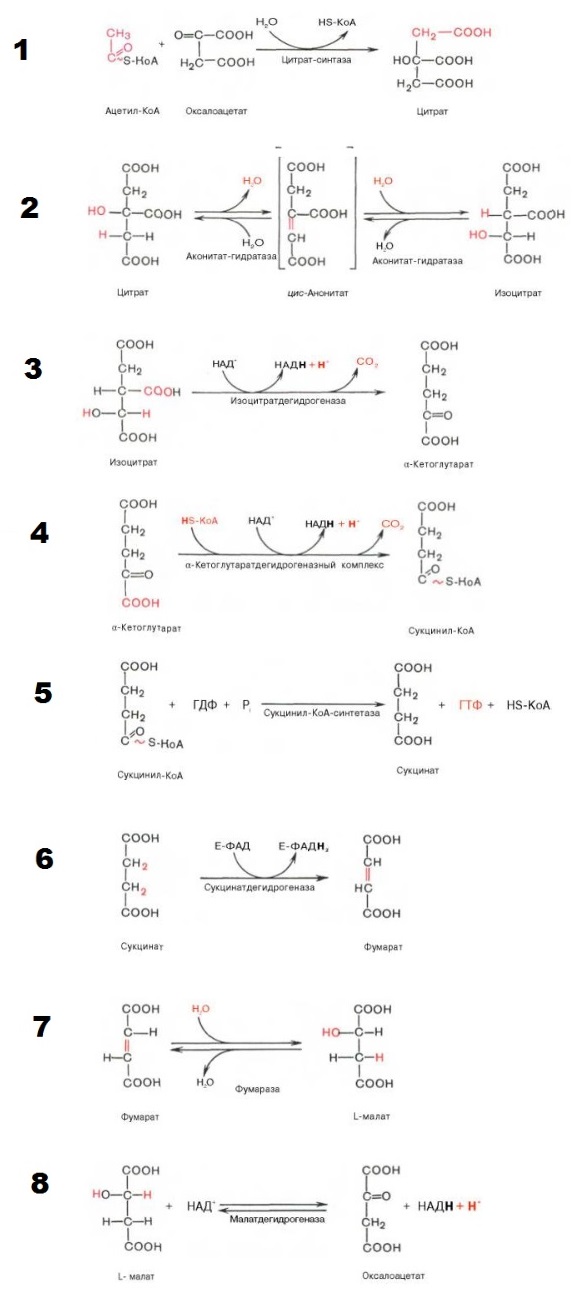
В процессе дыхания аэробных микроорганизмов пировиноградная кислота в дальнейшем подвергается полному окислению до СO2 и Н2O, вступая в сложный цикл превращений (цикл Кребса) с образованием три- и дикарбоновых кислот, последовательно окисляющихся (отщепляется Н2) и декарбоксилирующихся (отщепляется СO2).

Этапы:
Конденсация ацетил-КоА и оксалоацетата с образованием цитрата. Происходит реакция отщепление карбоксильной группы аминокислот, в процессе которой образуется ацетил-КоА (он выполняет функцию транспортировки углерода в различных обменных процессах). При соединении с молекулой щавелевой кислоты получается цитрат (фигурирует в буферных обменах). На данном этапе кофермент А полностью высвобождается, и получаем молекулу воды. Данная реакция необратима.
Превращение цитрата в изоцитрат. Дегидрирование (отщепление молекул воды) от цитрата, в результате которого получается цис-аконитат. И присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат).
Превращение изоцитрата в а-кетоглутарат. Изолимонная кислота(изоцитрат) дегидрируется в присутствии НАД- зависимой изо-цитратдегидрогеназы.На выходе получаем альфа-кетоглутарат. (Альфа-кетоглутарат участвует в регуляции всасывания аминокислот, нормализует метаболизм и положительно влияет на антистрессорные процессы). Также образуется NADH (аллостерический фермент).
Окисление α-кетоглутарата до сукцинил-КоА. Окислительное декарбоксилирование а-кетоглутарата с образованием сукцинил-КоА - тиоэфира, содержащего высокоэнергетическую фосфатную связь.
Превращение сукцинил-КоА в сукцинат. Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Так же происходит образование высокоэргической фосфатной связи ГТФ за счет тиоэфирной связи сукцинил-КоА.
Дегидрогенирование сукцината. Образование фумарата. Образовавшийся сукцинат превращается в фумарат под действием фермента сукцинат-дегидрогеназы. Единственная дегидрогеназная реакция цикла Кребса, в ходе которой осуществляется прямой перенос водорода с субстрата на флавопротеин без участия НАД+.
Образование малата из фумарата. Под влиянием фермента фумаратгидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является L-яблочная кислота (L-малат).
Превращение малата в оксалоацетат. Под влиянием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат. Происходит полное «сгорание» одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА. А коферменты (НАД+ и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться.
Формулы реакций цикла:
Некоторые аэробные гетеротрофные микроорганизмы получают энергию за счет неполного окисления органических веществ; при этом в среде накапливаются промежуточные недоокисленные продукты, преимущественно органические кислоты.
При неполном окислении энергетического материала высвобождается соответственно меньшее количество энергии. Часть потенциальной энергии окисляемого вещества остается в продуктах неполного окисления. Например, некоторые плесневые грибы в определенных условиях окисляют сахар с образованием воды и различных органических кислот – глюконовой, лимонной, яблочной, щавелевой, янтарной и др. Уксуснокислые бактерии окисляют этиловый спирт до уксусной кислоты и воды:
Дальнейшее превращение образующихся пировиноградной кислоты и восстановленного промежуточного переносчика водорода НАД · Н2 у анаэробов иное, чем у аэробов. Пировиноград-ная кислота в бродильных процессах является исходным материалом для разнообразных продуктов брожения (спиртов, органических кислот).
У одних анаэробов она непосредственно служит конечным акцептором водорода от НАД · Н2 и восстанавливается в продукт брожения – молочную кислоту; НАД · Н2 при этом окисляется в НАД.
У других анаэробов из пировиноградной кислоты образуются различные промежуточные продукты, которые служат затем акцепторами водорода от НАД · Н2. Последний регенерируется, а акцептировавшие водород восстановленные органические соединения, являющиеся конечными продуктами брожения, выделяются в окружающую среду. В зависимости от того, какой основной продукт накапливается в среде, процесс брожения имеет соответствующее название.
Примерами такого типа получения энергии могут служить следующие виды брожения.
Спиртовое брожение осуществляется многими дрожжами в анаэробных условиях. Молекула глюкозы (энергетический материал) в этом процессе превращается в две молекулы этилового спирта и две молекулы углекислого газа с выделением энергии:
![]()
В молекуле спирта заключено энергии 1,37-106 Дж. Как видно из уравнения, освобождается только часть энергии, много ее остается в уксусной кислоте.
Некоторые из этих окислительных процессов используют в промышленности, например, при производстве уксуса, лимонной и глюконовой кислот.
23. Анаэробы. Анаэробные микроорганизмы, к которым относят многие бактерии и некоторые дрожжи, получают необходимую для жизнедеятельности энергию в процессе брожения. Этот энергодающий процесс протекает также путем сопряженного окисления-восстановления, но без участия кислорода воздуха.
Конечным акцептором водорода, отнятого от окисляемого органического вещества, служат органические вещества – промежуточные продукты распада используемого субстрата.
Анаэробные микроорганизмы подразделяют на:
Облигатные или безусловные, для которых кислород не только не нужен, но и вреден
Факультативные или условные, которые могут жить как при доступе воздуха, так и без него.
Степень анаэробности у факультативных анаэробов различна. Одни из них лучше развиваются в анаэробных условиях или при ничтожно малом содержании кислорода в среде (микроаэрофилы), другие – при доступе воздуха. Известны факультативные анаэробы (например, некоторые дрожжи), способные в зависимости от условий развития переключаться с анаэробного на аэробный тип получения энергии.
Энергетическим материалом при брожении чаще служат углеводы, из них наиболее используемый – глюкоза.
Превращение глюкозы до образования пировиноградной кислоты протекает так же, как и у аэробов по гликолитическому пути:
![]()
Молочнокислое брожение – это процесс получения энергии молочнокислыми бактериями, заключающийся в превращении молекулы сахара в две молекулы молочной кислоты с выделением энергии:
![]()
Как видно из уравнений, среди конечных продуктов брожения всегда имеются продукты неполного окисления – органические вещества, заключающие в себе значительное количество потенциальной энергии.
Известно много других брожений, отдельные типы которых различаются составом конечных продуктов, что зависит от комплекса ферментов возбудителя брожения.
Многие бродильные процессы применяют в промышленности; они могут являться причиной порчи пищевых продуктов.
Маслянокислое брожение вызывается облигатно анаэробными маслянокислыми бактериями. Глюкоза в этом энергодающем процессе превращается в масляную кислоту, водород и углекислый газ:
![]()
В анаэробных условиях некоторые микроорганизмы могут при окислении органических веществ использовать неорганические акцепторы водорода (электроны), которые при этом восстанавливаются. Эти микроорганизмы используют, следовательно, в качестве окислителя не свободный, а связанный кислород неорганических веществ, богатых этим элементом.
Такой способностью обладают, например, денитрифицирующие бактерии, восстанавливающие нитраты до свободного азота. Этот способ получения энергии называют нитратным дыханием.
Десульфатирующие бактерии используют в качестве конечного акцептора электронов (водорода) сульфаты, восстанавливая их до сероводорода, – сульфатное дыхание.
Таким образом, различие между аэробным и анаэробным процессом получения энергии у гетеротрофов заключается в природе конечного акцептора водорода (окислителя).
Рассмотренные процессы (дыхание, брожение) следует расценивать не только как процессы, обеспечивающие организм энергией. Многие промежуточные продукты распада углеводов служат исходным материалом для синтеза важнейших компонентов клетки (белков, нуклеиновых кислот, липидов и др.).
Важным поставщиком промежуточных продуктов для биосинтетических процессов является цикл Кребса. Многие кетокислоты, образующиеся в этом цикле превращений ди- и трикарбоновых кислот, путем аминирования и переаминирования превращаются в различные аминокислоты, из которых далее синтезируются белки.
24. Влияние влажности. Жизнедеятельность микроорганизмов возможна только при наличии в среде свободной влаги, связанная вода недоступна для микроорганизмов. Сама клетка на 70–80% состоит из воды, поэтому обезвоживание, высушивание субстрата и клеток микроорганизмов оказывает на них губительное действие.
Для развития микроорганизмов важна не абсолютная величина влажности, а ее доступность, которая обусловлена активностью воды (аw). Этот показатель выражает отношение давления паров над субстратом (Рс) к давлению паров над чистой водой (Р) при одной и той же температуре: аw =Рс / Р
Активность воды лежит в интервале от 0 до 1 и характеризует относительную влажность. Микроорганизмы могут осуществлять жизнедеятельность при активности воды от 0,999 до 0,62 и не растут в аэрозолях и во льду.
Микроорганизмы обладают различной устойчивостью к высушиванию. Устойчивы к высушиванию сапрофиты, молочнокислые бактерии, дрожжи. Особенно устойчивы к высушиванию споры бактерий и плесневых грибов, способные сохраняться в высушенном состоянии сотни и тысячи лет.
Нитрифицирующие, клубеньковые бактерии, наоборот, весьма чувствительны к высушиванию и быстро погибают при понижении влажности почвы ниже 40 %. В высушенном состоянии микроорганизмы не проявляют биологической активности, но сохраняют свои свойства; при увеличении влажности жизнедеятельность их полностью восстанавливается.
Микроорганизмы в зависимости от отношения к влажности делятся на следующие группы: гидрофиты (влаголюбивые); ксерофиты (сухолюбивые); мезофиты (средневлаголюбивые).
Для большинства бактерий минимальная влажность субстрата должна составлять 20–30 %, а для грибов – 11–13 %. Развитие микроорганизмов в субстрате, в частности на пищевых продуктах, возможно только при определенной влажности. Влажность продуктов изменяется в зависимости от относительной влажности воздуха, между ними устанавливается определенное подвижное равновесие. Однако различные продукты при одной и той же влажности воздуха могут иметь разную равновесную или активную влажность.
Влажность воздуха может значительно колебаться при уменьшении температуры. Так, с понижением температуры влагоудерживающая способность воздуха понижается, и избыточная влага конденсируется в виде капелек на поверхности продукта. В этом случае микроорганизмы могут быстро перейти в активное состояние, размножиться и вызвать порчу продукта.
Губительное действие высушивания на микроорганизмы широко используют для сохранения различных продуктов.
Сушке подвергают мясо, рыбу, овощи, фрукты, травы.
Методы лиофильной сушки – высушивания путем замораживания в вакууме, успешно применяют для длительного сохранения культур микроорганизмов.
25. Влияние высокой температуры. Температурные условия в биосфере достаточно разнообразны. Свыше 80% ее принадлежит к постоянно холодным областям. Значительная часть поверхности суши, включающая и континент Антарктиду, имеет низкую температуру. Средняя температура почвы в умеренной климатической зоне составляет 12 °С.
Три температурные точки, имеющие решающее значение для развития того или другого микроорганизма, называются кардинальными:
1. Максимальная температурная точка, при которой происходит замедление и остановка развития.
2. Оптимальной называют температуру, при которой микроорганизмы развиваются наиболее интенсивно.
3. Минимальная температурная точка, при которой происходит замедление и остановка развития.
По отношению к температуре все микроорганизмы условно разделяют:
1. Психрофилы (опт 15–20 °С, min 8… –1 °С, max 30–35 °С)
А) Облигатные: приспособились к устойчивым холодным условиям.
Б) Факультативные: приспособились к устойчивым холодным условиям; более широкий температурный диапазон.
2. Мезофиллы (наиболее распространенная группа микроорганизмов. Опт 28…35 °С, min 5…10 °С, max 40…50 °С. Гнилостные бактерии; патогенные бактерии; токсигенные бактерии; промышленные культуры)
3. Термофилы (опт 35…40 °С, min 10… 15 °С, max 55…60 °С)
А) Термотолерантные (опт 35…40 °С, min 10… 15 °С, max 55…60 °С. Способны расти при повышенных температурах)
Б) Облигатные (опт 55…60 °С, min 40…45 °С, max 65…70 °С. эубактерии Bacillus acidocaldarius, Synechococcus lividus, археи Methanobacterium thermoautotrophicum, Thermoplasma acidophilum)
В) Факультативные (опт 20…40 °С, min 20…25 °С,max 50…65 °С. Способность расти в большом диапазоне)
Г) Экстримальные (опт 80…105 °С, min 60…65 °С, max 110 °С. Thermoproteus, Pyrococcus, Pyrodictium)
Встречаются термофилы в почве, навозе, кишечнике животных и человека.
Термофилы в большинстве своем споровые формы, причем споры их отличаются особой термоустойчивостью (Вас. stearothermophilus, Вас. aerothermophilus).
Переносят стерилизацию (особенно при большом начальном обсеменении) и вызывают плоско-кислую порчу консервов, причиняя большой вред производству пищевых консервов.
Механизмы термоустойчивости:
Роль мембранных липидов. Насыщенные жирные кислоты, входящие в состав липидов, имеют более высокую точку плавления по сравнению с ненасыщенными.
Роль ферментных белков. Температурные точки термофилов зависят от конформации одного или нескольких ключевых ферментов. При минимальной температуре роста происходит переход от жесткой неактивной конформации белковых молекул к конформации с ограниченной гибкостью; оптимальная температура роста определяет наиболее благоприятное конформационное состояние ферментных белков; при максимальной температуре начинаются нарушения конформации белков и снижение их ферментативной активности, а выше этой температуры рост прекращается вследствие тепловой денатурации белков.
Термостабильность структурных компонентов клетки термофилов. Клеточная стенка, мембраны, рибосомы термофилов значительно более термостабильны, чем соответствующие структуры мезофилов.
Отмирание клеток при нагревании наступает вследствие необратимых изменений в протоплазме: инактивации ферментов, денатурации белков. Большинство вегетативных клеток погибает уже при 60–70 °С в течение 15–30 мин, а при 100 °С в течение нескольких секунд. Дрожжи и плесени также не переносят температуру 50–60 °С.
Споры бактерии вследствие своего строения, химического состава отличаются большой термоустойчивостью, многие из них выдерживают кипячение в течение 5–6 ч (споры Вас. subtilis, Cl. botulimim, Сl. sporogenes). Высокую термоустойчивость проявляют споры при воздействии сухого жара.
26. Влияние низкой температуры. По отношению к низкой температуре микроорганизмы проявляют большую устойчивость, несмотря на то, что размножение и биохимическая деятельность микроорганизмов ниже минимальной кардинальной температурной точки прекращаются, гибель самой клетки может не наступать, и в таком анабиотическом состоянии многие микроорганизмы, а особенно споры, остаются жизнеспособными длительное время.
Под воздействием низких температур, особенно ниже минус 3 – минус 8 °С, в протоплазме клетки происходит ряд необратимых изменений, нарушается обмен веществ, инактивируются ферменты, происходят структурные изменения протоплазмы. Отмечено токсичное действие ионов солей, концентрация которых увеличивается в результате вымораживания воды, имеет значение и механическое повреждение протоплазмы клеток в результате образования внутриклеточных кристаллов льда.
27. Влияние лучистой энергии. Существуют различные формы лучистой энергии, характеризующиеся различными свойствами, силой и характером действия на микроорганизмы.
Электромагнитные излучения с разной длиной волн: радиоволны, инфракрасные лучи, видимый свет, УФ, рентгеновское, гамма-излучение, корпускулярные излучения (альфа- и бета-частицы нейтрона, протона и другие ядерные частицы).
Рентгеновское, гамма- и корпускулярное относятся к ионизирующим излучениям.
СВЧ-энергия – электромагнитные ультракороткие волны и микроволны с длиной волны от 10 м до нескольких мм при прохождении через среду вызывают в ней возникновение токов высокой и сверхвысокой частоты. Причиной гибели при СВЧ-воздействии является повреждение клетки под влиянием высоких температур. СВЧ-энергия оказывает влияние на генетические признаки микроорганизмов, на изменение интенсивности деления клетки, активность некоторых ферментов, гемолитические свойства. Эффект воздействия сильно зависит от частоты колебаний и времени облучения. Метод нагрева с помощью СВЧ-энергии является перспективным способом тепловой обработки пищевых продуктов: варки, сушки, разогрева, выпечки, стерилизации и пастеризации.
Ультрафиолетовые лучи с короткой длиной волны являются наиболее активной частью солнечного спектра. Вследствие присущей им высокой химической и биологической активности, лучи с длиной волны менее 400 нм вызывают инактивацию ферментов, коагуляцию белков, в результате чего наступает гибель клетки. Губительное действие прямого солнечного света на большинство микроорганизмов обусловлено повреждающим воздействием ультрафиолетовых лучей на ДНК клетки.
Репарация после воздействия УФЛ. В молекуле ДНК возникают тиминовые димеры, ингибирующие репликацию. Эти повреждения могут быть устранены с помощью фотореактивации – исправления поврежденного участка ДНК особым ферментом, расщепляющим тиминовые димеры и активируемым лучами синего света. Также исправить поврежденные структуры ДНК может комплекс ферментов: эндонуклеаза, которая вырезает поврежденный участок; полимераза, синтезирующая правильную структуру по комплиментарной цепи; лигаза, сшивающая синтезированные последовательности. Такой механизм носит название темновой репарации
Особенно чувствительны к свету различные патогенные микроорганизмы и гнилостные бактерии рода Pseudomonas. Пигментные бактерии и дрожжи значительно устойчивее к ультрафиолетовому облучению. Наибольшей устойчивостью к действию ультрафиолетовых лучей обладают споры.
В природе существуют микроорганизмы, для жизнедеятельности которых ультрафиолетовые лучи необходимы, это фотосинтезирующие бактерии, которые, подобно зеленым растениям, используют солнечную энергию для синтеза веществ протоплазмы из углекислоты и воды.
Действие ультрафиолетовых лучей широко используют на практике для дезинфекции воздуха лечебных учреждений и заводских помещений, обеззараживания тары, поверхности оборудования, воды.
Ионизирующая радиация, и в первую очередь гамма-лучи, рентгеновские лучи и ускоренные электроны способны вызывать процесс ионизации, т. е. превращать отдельные атомы и молекулы веществ в электрически заряженные частицы – ионы.
Под действием ионизирующей радиации происходит радиолиз воды, образование свободных радикалов и перекисей, которые активно вступают в химическое взаимодействие с другими веществами, происходит распад существовавших и возникновение новых веществ, изменяется течение физико-химических процессов.
Микроорганизмы более устойчивы к воздействию радиации, чем более высокоразвитые существа. Большие дозы радиоактивного воздействия, несомненно, губительно воздействуют на микробные клетки. Маленькие дозы, наоборот, способны вызвать мутации в клетки, что может привести к появлению новых признаков, например, таких как устойчивость микроорганизма к воздействию антибиотиков.
Наибольшей устойчивостью к радиации обладают микроорганизмы родов Deinococcus radiodurans, Shizosaccharomyces pombe, Boda marina, которые были выделены из воды атомных реакторов.
Воздействие излучений:
РАДУРИЗАЦИЯ (лучевая пастеризация) частичное подавление микроорганизмов
РАДИСИДАЦИЯ уничтожение определенных видов патогенных или токсигенных микроорганизмов
РАДАППЕРТИЗАЦИЯ практически полное уничтожение м/о в облучаемом продукте (аналогично тепловой стерилизации)
28. Влияние радиации. Ионизирующее облучение воздействует на такие микроорганизмы, как бактерии, дрожжи, плесени, вызывая поражение генетического материала клеток, эфффективно предотвращая в них протекание биологических процессов, необходимых для продолжения существования.
Способ воздействия
Основные мишени радиации – нуклеиновые кислоты и мембранные липиды. Изменения в мембранных липидах, в частности, в полиненасыщенных липидах, ведет к изменению мембран и ухудшению их функций, на такие как проницаемость. Активность мембранных эффектов может быть нарушена как вторичный эффект разрушения мембранных липидов. Ионизирующее облучение вызывает изменения в структуре ДНК облучамых клеток, что предотвращает репродукцию и другие функции клетки. Используемый энергетический уровень достаточен для разрушения определенных связей в молекулах ДНК, что делает невозможным размножение клеток. Нуклеиновые кислоты из-за их большого размера являются главными мишенями свободных радикалов, образованных в результате радиации. Хромосомы бактерий по своей природе очень чувствительны и их смертельное повреждение является результатом облучения. Способность бактерий восстанавливать ограниченное количество таких повреждений дает им значительно большую устойчивость к таким облучениям.
Уровень дозы
Факторы, воздействующие на чувствительность микроорганизмов при облучении, это уровень радиационной дозы, температура, атмосфера (наличие или отсутствие кислорода), среда и тип организма (размер – чем меньше размер целевого микроорганизма, тем он более устойчив к ионизирующему облучению, характеристики стенок клеток и принадлежность к грамположительным или грамотрицательным бактериям, количество и возраст клеток). В целом, чем выше применяемая доза, тем ниже количество выживших микроорганизмов и ниже скорость таких реакций, как образование радикалов из молекул воды. Эти радикалы могут воздействовать косвенно, нарушая нормальные клеточные функции, такие как мембранный перенос.
Радиочувствительность микроорганизмов модифицируют различные факторы, как внутренние: генетическая природа самой клетки, жизненная фаза клетки и другие, так и внешние: температура, концентрация кислорода и других газов, состав и свойства среды в которой производится облучение, а также тип радиационного воздействия и его мощность и другие факторы. Радиочувствительность микроорганизмов значительно ниже, чем у растений и животных на 1-2 порядка.
Если продукт заморожен, образование радикалов практически затормаживается. В целом, бактерии становятся более устойчивыми к ионизирующему облучению в замороженном или сушеном состоянии. В обоих состояниях распространение косвенного эффекта из-за радиолиза воды значительно снижено. Появление постороннего привкуса у сушеных продуктов значительно ниже, чем у влажных. Это благодаря низкому образованию свободных радикалов при сниженном влагосодержании. Как правило, чем проще форма жизни, тем более он устойчив к воздействию облучения. Например, вирусы более устойчивы, чем бактерии, которые более устойчивы, чем плесени, которые, в свою очередь, более устойчивы чем человеческий организм. Споры бактерий более устойчивы их вегетативных клеток в 5-15 раз.
Чувствительность бактерий к радиации значительно изменяется внутри одного и того же вида и, даже, популяции бактериальных клеток. Популяция клеток состоит из бактерий, располагающихся по устойчивости к радиации в вариационный ряд, так же, как и по другим биологическим признакам. Поэтому в популяции всегда присутствуют особо радиорезистентные клетки, для того, чтобы их убить, нужно облучать более мощными дозами, чем те, при которых погибает основная масса клеток более радиочувствительных. Грамположительные бактерии менее чувствительны к облучению, чем грамотрицательные.
Споры бактерий обладают очень низкой радиочувствительностью, но и среди неспорообразующих микроорганизмов известны организмы, радиоустойчивость которых может превышать устойчивость спор. Чаще всего они принадлежат к кокам или сарцинам.
29. Влияние рН среды. Концентрация водородных ионов (рН) в среде обитания является важным фактором, определяющим возможность роста и размножения микроорганимов. Водородный показатель реакции среды рН показывает степень её кислотности (рН от 7 до 1) или щелочности (рН от 7 до 14). Нейтральная реакция среды соответствует рН 7.
В природных условиях прокариоты (бактерии) могут развиваться в диапазоне рН от 1 до 11. В зависимости от отношения к рН среды их можно разделить на:
Нейтрофилы предпочитают нейтральную реакцию среды, оптимальный рН для их роста составляет 6,8-7,3, минимальный -4, максимальный-9. Подавляющее большинство бактерий относятся к нейтрофилам (гнилостные бактерии, возбудители отравлений, бактерии группы кишечной палочки и др.)
Ацидофилы (кислотолюбивые) развиваются при оптимальном рН 4 и выше (уксуснокислые и другие бактерии, продуцирующие органические кислоты).
Алкалофилы (щелочелюбивые) развиваются при оптимальном рН 9 и выше (некоторые представители бактерий кишечной группы - холерный вибрион и др.).
Споры бактерий обычно более устойчивы к изменениям рН, чем вегетативные клетки.
Зная отношение различных микроорганизмов к реакции среды и регулируя рН, можно подавлять или стимулировать их развитие, что имеет большое практическое значение. Так, неблагоприятное действие кислой среды на гнилостные бактерии положено в основу хранения некоторых пищевых продуктов в маринованном и квашеном виде.
Окислительно-восстановительные условия среды
Молекулярный кислород является одним из важнейших факторов внешней среды, определяющим направление биохимических реакций, осуществляемых микроорганизмами в энергетическом обмене. Отношение микроорганизмов к содержанию кислорода в среде определяется наличием у тех или иных окислительно-восстановительных ферментов, ответственных за энергетический обмен. При консервировании, например, грибов в домашних условиях для предотвращения развития палочковидной спорообразующей анаэробной бактерии - возбудителя ботулизма - Clostridiumbotulinum, банки следует заполнять не полностью, а оставлять некоторое воздушное пространство. Тогда имеющийся О2 будет препятствовать прорастанию спор.
В виноделии для предотвращения развития аэробных микроорганизмов-вредителей (пленчатых дрожжей, уксуснокислых бактерий) необходимо следить за полным заполнением ёмкостей с вином с целью предотвратить поступление необходимого для их развития О2.
30. Влияние химических антисептиков. Все химические вещества могут оказывать на микроорганизмы 3 вида воздействий:
Стимулирующее действие – ускорять развитие микроорганизмов (питательные вещества);
Бактериостатическое – химические вещества, затормаживающие развитие микроорганизмов;
Бактерицидное – химические вещества, приводящие к гибели микроорганизмов.
Химические вещества, уничтожающие микроорганизмы в окружающей среде, называются дезинфицирующими. Антимикробные химические вещества могут обладать бактерицидным, вирулицидным, фунгицидным действием и т.д.
Вещества, обладающие бактерицидным действием называются антисептиками. Частным случаем антисептиков являются дезинфицирующие вещества (уничтожают только болезнетворные м/о). Антисептики нашли широкое применение в медицине, быту, с/х и довольно ограниченное в пищевой промышленности.
Химические вещества, используемые для дезинфекции, относятся к различным группам, среди которых наиболее широко представлены вещества, относящиеся к хлор-, йод- и бромсодержащим соединениям и окислителям.
Антимикробным действием обладают также кислоты и их соли (оксолиновая, салициловая, борная); щелочи (аммиак и его соли).
Стерилизация– предполагает полную инактивацию микробов в объектах, подвергшихся обработке.
Дезинфекция — процедура, предусматривающая обработку загрязненного микробами предмета с целью их уничтожения до такой степени, чтобы они не смогли вызвать инфекцию при использовании данного предмета. Как правило, при дезинфекции погибает большая часть микробов (в том числе все патогенные), однако споры и некоторые резистентные вирусы могут остаться в жизнеспособном состоянии.
Асептика– комплекс мер, направленных на предупреждение попадания возбудителя инфекции в рану, органы больного при операциях, лечебных и диагностических процедурах. Методы асептики применяют для борьбы с экзогенной инфекцией, источниками которой являются больные и бактерионосители.
Антисептика– совокупность мер, направленных на уничтожение микробов в ране, патологическом очаге или организме в целом, на предупреждение или ликвидацию воспалительного процесса.
31. Влияние биотических факторов. Биологические факторы, обладающие свойством воздействовать на микроорганизмы, весьма разнообразны. Все живые существа объединены в устойчивые экологические системы – биоценозы. Взаимоотношения между отдельными видами микроорганизмов в пределах одного сообщества могут быть различными и проявляться в форме синергизма, сателлизма, антагонизма и др.
Синергизм. Для такого типа взаимоотношений между особями микробной ассоциации характерны одинаковые физиологические процессы у различных микроорганизмов, в результате чего имеет место увеличение количества веществ, синтезируемых микробной ассоциацией.
Сателлизм. При таком типе взаимоотношений происходит стимуляция роста одного вида микроорганизма продуктами жизнедеятельности другого.
Антагонизм. Для этого типа взаимоотношений характерно угнетение жизнедеятельности (а иногда и полное уничтожение) одних микроорганизмов веществами, синтезируемыми другими микроорганизмами.
Паразитизм – это такое отношение между членами ассоциации, при котором один из организмов (паразит) получает необходимые вещества за счет другого организма (хозяина), нанося при этом вред, что приводит к гибели хозяина.
Кроме взаимного влияния микроорганизмов друг на друга существуют и другие биологические объекты и, следовательно, и другие виды воздействия. Особый интерес представляет фагия. Это одна из форм взаимодействия между фагами (по своей природе это вирусы) и другими микроорганизмами (бактериями, актиномицетами, синезелеными водорослями).
По степени специфичности действия фаги подразделяют на три группы:
Монофаги – способны лизировать бактерии одного вида;
Полифаги – способны лизировать бактерии разных видов (преимущественно родственных);
Фаговары – способны лизировать только определенные варианты данного вида бактерий.
Кроме перечисленных широко используется действие еще одной группы биологически активных веществ, способных избирательно подавлять рост, инактивировать микроорганизмы, грибы, риккетсии, простейших и др. Это обширная группа антибиотиков, в настоящее время насчитывающая около 2000 соединений различного происхождения.
По происхождению антибиотики подразделяют на шесть групп:
1. Антибиотики, образуемые грибами и лишайниками. К этой группе относят пенициллин, гризеофульвин, цефалоспорин, усниновая кислота.
2. Антибиотики, продуцируемые актиномицетами. К этой группе относят стрептомицин, неомицин, канамицин, хлортетрациклин, хлорамфеникол, эритромицин, тилозин, нистатин.
3. Антибиотики, продуцируемые бактериями. Эта группа менее обширна, чем группа антибиотиков грибного и актиномицетного происхождения. Способностью продуцировать антибиотики обладают в большинстве своем сапрофитные бактерии, обитающие в почве. К этой группе относят колицин, грамицидин, пиоционин, субтилин, полимиксин. Некоторые из этих антибиотиков токсичны при парэнтеральном введении и применяются местно.
4. Антибиотики животного происхождения. К этой группе относят вещества, образуемые тканями животных: эритрин, выделяемый из эритроцитов некоторых животных; экмолин, полученный из тканей рыб; лизоцим, интерферон.
5. Антибиотики растительного происхождения. Многие растения способны синтезировать летучие и нелетучие вещества, обладающие бактерицидным и бактериостатическим действием на микроорганизмы. Такие соединения называют фитонцидами. Фитонциды призваны обеспечить защиту растений от возбудителей различных заболеваний. Некоторые фитонциды выделены в чистом виде. Например, аллицин – из чеснока, рафанин – из семян редиса, иманин – из зверобоя.
6. Синтетические антибиотики, полученные искусственно путем биосинтеза.
По механизму действия выделяют четыре основные группы антибиотиков:
1. Антибиотики, ингибирующие синтез пептидогликана клеточной стенки (пенициллины, цефалоспорины).
2. Антибиотики, нарушающие фенкцию цитоплазматической мембраны (грамицидин, полиены).
3. Антибиотики, разрушающие рибосомальные субчастицы и сдерживающие синтез белка (тетрациклины, амино-гликозиды, макролиды).
4. Антибиотики, избирательно подавляющие синтез нуклеиновых кислот (гризеофульвин, неомицин, новобиоцин).
32. Антибиотики – это химиотерапевтические препараты из химических соединений биологического происхождения (природные), а также их полусинтетические производные и синтетические аналоги, которые в низких концентрациях оказывают избирательное повреждающее или губительное действие на микроорганизмы и опухоли. Антибиотики, применяемые в медицинской практике, продуцируются актиномицетами (лучистыми грибами), плесневыми грибами, а также некоторыми бактериями. Как уже было сказано, противомикробное действие антибиотиков имеет избирательный характер: на одни организмы они действуют сильнее, на другие – слабее или вообще не действуют. Избирательно и воздействие антибиотиков и на животные клетки, вследствие чего они различаются по степени токсичности и влиянию на кровь и другие биологические жидкости. Некоторые антибиотики представляют значительный интерес для химиотерапии и могут применяться для лечения различных микробных инфекций у человека и животных.
Проблема лечения инфекционных заболеваний имеет такую же долгую историю, как и изучение самих болезней. С точки зрения современного человека, первые попытки в этом направлении были наивны и примитивны, хотя некоторые из них и не были лишены здравого смысла (например, прижигание ран или изоляция больных). Тот факт, что одни микробы могут каким-то образом задерживать рост других, был хорошо известен издавна. В народной медицине для обработки ран и лечения туберкулеза издавна применяли экстракты лишайников. Позднее в состав мазей для обработки поверхностных ран стали включать экстракты бактерий Pseudomonas aeruginosa. Опыт, накопленный тяжёлым путём проб и ошибок, вооружил знахарей знаниями целебных свойств вытяжек из трав и тканей животных, а также различных минералов. Изготовление настоев и отваров из растительного сырья было широко распространено в античном мире, их пропагандировал Клавдий Галён. В средневековье репутацию препаратов из лекарственного сырья значительно уменьшили всевозможные зелья, «изыскания» алхимиков и, конечно, убеждённость в неизлечимости «кар Господних». В этой связи следует упомянуть верование в целительное действие рук «помазанников Божьих», через прикосновение царствующей особы проходили толпы больных. Например, Людовик XIV возложил руки на 10 000 больных, а Карл II Стюарт — на 90 000. По мере понимания врачами правильности концепции лечение болезней принимало всё более «этиотропный» характер. Основателем химиотерапии с полным правом должен считаться Парацельс, названный А. И. Герценым «первым профессором химии от сотворения мира». Парацельс не без успеха применял для лечения инфекций человека и животных различные неорганические вещества (например, соли ртути и мышьяка). После открытия Нового Света стало известно о свойствах коры дерева «кина - кина», использовавшейся индейцами для лечения малярии. Популярности этого средства способствовало чудесное излечение жены вице-короля Америки, графини Цинхон, и в Европу кора прибыла уже под названием «порошок графини», а позднее её имя присвоили и самому хинному дереву.
Еще в 1871-1872 гг. российские ученые В.А. Манассеин и А.Г. Полотебнов наблюдали эффект при лечении зараженных ран прикладыванием плесени, хотя почему они помогают, никто не знал, и феномен антибиоза был неизвестен.
Однако некоторые из первых ученых-микробиологов сумели обнаружить и описать антибиоз (угнетение одними организмами роста других). Дело в том, что антагонистические отношения между разными микроорганизмами проявляются при их росте в смешанной культуре. До разработки методов чистого культивирования разные бактерии и плесени выращивались вместе, т.е. в оптимальных для проявления антибиоза условиях. Луи Пастер еще в 1877 при изучении сибирской язвы заметил, что заражение животного смесью возбудителя и других бактерий часто мешает развитию заболевания, что позволило ему предположить, что конкуренция между микробами может блокировать патогенные свойства возбудителя. Он описал антибиоз между бактериями почвы и патогенными бактериями – возбудителями сибирской язвы и даже предположил, что антибиоз может стать основой методов лечения. Наблюдения Л. Пастера (1887) подтвердили, что антагонизм в мире микробов – это распространенное явление, однако природа его была неясна.
Первые антибиотики были выделены еще до того, как стала известной их способность угнетать рост микроорганизмов. Так, в 1860 был получен в кристаллической форме синий пигмент пиоцианин, вырабатываемый небольшими подвижными палочковидными бактериями рода Pseudomonas, но его антибиотические свойства были обнаружены лишь через много лет. В 1899г. – Р. Эммерих и О. Лоу сообщили об антибиотическом соединении, образуемом бактериями Pseudomonas pyocyanea, и назвали его пиоцианазой; препарат использовался как местный антисептик. В 1896 Б. Гозио из жидкости, содержащей культуру грибка из рода Penicillium (Penicillium brevicompactum), удалось кристаллизовать еще одно химическое вещество, получившее название микофеноловая кислота, подавляющая рост бактерий сибирской язвы.
Но ни одно лекарство не спасло столько жизней, сколько пенициллин. С открытием этого вещества началась новая эра в лечении инфекционных болезней – эра антибиотиков. Открытие лекарств антибиотиков, к которым мы уже так привыкли в наше время, сильнейшим образом изменило человеческое общество. Отступили заболевания еще не давно считавшиеся безнадежными. Еще удивительнее история самого открытия.
Каждый день, поднимаясь на чердак госпиталя, где разместилась лаборатория, Флеминг проходил через госпитальные палаты, где лежали раненые на Первой мировой. Ежедневно прибывали всё новые и новые их группы. Здесь, в госпитале, они сотнями умирали от инфекции. Переломы, разрывы внутренних тканей... Кусочки земли и одежды, попавшие в раны, довершали работу бомб. Лицо раненого приобретало серый цвет, дыхание затруднялось — начиналось заражение крови. Результат — неизбежная смерть.
Флеминг стал исследовать эту инфекцию. Он рассказывал:
«Мне советовали обязательно накладывать повязки с антисептиками: карболовой, борной кислотами или перекисью водорода. Я видел, что антисептики убивают не все микробы, но мне говорили, что они убивают некоторые из них, и лечение проходит успешнее, чем в том случае, когда не применяют антисептики».
Флеминг решил поставить простой опыт, чтобы проверить, насколько антисептики помогают бороться с инфекцией.
Края большинства ран были неровными, со многими изгибами и извилинами. Микробы скапливались в этих изгибах. Флеминг сделал муляж раны из стекла: раскалил пробирку и изогнул её конец наподобие извилин раны. Затем он наполнил эту пробирку сывороткой, загрязнённой навозом. Это была как бы общая схема обычного боевого ранения. На следующий день сыворотка стала мутной и издавала неприятный запах. В ней размножилось огромное количество микробов. Затем Флеминг вылил сыворотку и наполнил пробирку раствором обычного сильного антисептика, после чего снова заполнил промытую таким образом пробирку чистой, незаражённой сывороткой. И что же? Сколько бы раз Флеминг ни промывал пробирку антисептиками, чистая сыворотка через день становилась такой же зловонной и мутной.
В изгибах пробирки микробы сохранялись, несмотря ни на что. Из этого опыта Флеминг сделал вывод, что обычные антисептики нисколько не помогают при фронтовых ранениях. Его совет военным врачам был следующим: удалять все омертвевшие ткани, где легко могут развиваться микробы, и помогать организму самому бороться с инфекцией посредством выделения белых кровяных телец, из которых образуется гной. Белые кровяные клетки (свежий гной) уничтожают колонии микробов.
Флеминг писал о своих чувствах в те дни:
«Глядя на заражённые раны, на людей, которые мучились и умирали и которым мы не в силах были помочь, я сгорал от желания найти, наконец, какое-нибудь средство, которое способно было бы убить эти микробы, нечто вроде сальварсана...»
Как-то раз в 1922 г., страдая насморком, Флеминг посеял в лабораторной посуде — чашке Петри — собственную носовую слизь. В той части чашки Петри, куда попала слизь, колонии бактерий погибли. Флеминг стал исследовать это явление и выяснил, что такое же действие оказывают слёзы, обрезки ногтя, слюна, кусочки живой ткани. Когда капля слезы попадала в пробирку с раствором, мутным от множества бактерий, он за несколько секунд становился совершенно прозрачным!
Сотрудникам Флеминга пришлось перенести немало «мучений», добывая слёзы для опытов. Они срезали цедру с лимона, выжимали её себе в глаза и собирали выступавшие слёзы. В больничной газете был даже помещён юмористический рисунок, на котором дети за небольшую плату дают лаборанту себя высечь, а другой лаборант собирает у них слёзы в сосуд с надписью «антисептики».
Флеминг назвал открытое им вещество «лизоцим» — от греческих слов «растворение» и «закваска» (имелось в виду растворение бактерий). К сожалению, лизоцим убивал далеко не все вредные, болезнетворные бактерии.
Совершить самое важное открытие в его жизни Флемингу также помогли случай и творческий беспорядок в лаборатории. Как-то в 1928 г. Флеминга навестил его коллега Прайс. Флеминг перебирал чашки Петри со старыми культурами. Во многие из них залетела плесень, что бывает довольно часто. Флеминг говорил Прайсу: «Как только вы открываете чашку с культурой, вас ждут неприятности: обязательно что-нибудь попадёт из воздуха...» Вдруг он замолчал и сказал, как всегда, спокойно: «Странно...»
В чашке Петри, которую он держал в руках, тоже выросла плесень, но здесь колонии бактерий вокруг неё погибли, растворились.
С этого момента Флеминг стал исследовать смертоносную для бактерий плесень, а чашку Петри, в которую она залетела, он сохранил до самой смерти.
Александр Флеминг наблюдая антагонизм Penicillium notatum и стафилококка в смешанной культуре открыл штамм плесневого гриба пеницилла (Penicillium notatum), выделяющего химическое вещество, которое задерживает рост стафилококка. Вещество было названо «пенициллин». Правда, впереди было самое важное испытание: не окажется ли это вещество таким же вредным для человека и животных, как для бактерий? Если бы это было так, пенициллин ничем бы не отличался от множества известных и до того антисептиков. Его нельзя было бы вводить в кровь. К величайшей радости Флеминга и его сотрудников, пенициллиновый бульон, смертоносный для бактерий, был не более опасен для подопытных кроликов и мышей, чем обычный бульон.
Но чтобы применять пенициллин для лечения, его нужно было получить в чистом виде, выделить его из бульона. Бульон, содержащий чужеродные для организма белки, нельзя было вводить в кровь человека.
В феврале 1929 г. Флеминг сделал сообщение о своём открытии в медицинском обществе. Ему не было задано ни одного вопроса! Учёные встретили открытие абсолютно равнодушно, без малейшего интереса. Ещё в 1952 г. Флеминг вспоминал об этой «ужасной минуте».
Так прошло одиннадцать лет! Те немногие химики, которые заинтересовались пенициллином, так и не смогли выделить его в чистом виде. Флеминг, впрочем, не терял надежды и верил, что у открытого им вещества большое будущее.
В 1940 г. неожиданно произошло одно из самых счастливых событий в жизни Флеминга. Из медицинского журнала он узнал, что оксфордским учёным Флори и Чейну удалось получить стабильный препарат пенициллин в очищенном виде. Флеминг ничем не выдал своей радости и только позже заметил, что о работе с такими химиками он и мечтал уже 11 лет.
Таким образом, к моменту получения пенициллина в очищенном виде было известно пять антибиотических средств (микофеноловая кислота, пиоцианаза, актиномицетин, мицетин и тиротрицин).
Так начиналась эра антибиотиков. В нашей стране большой вклад в учение об антибиотиках внесли З. В Ермольева и Г.Ф. Гаузе. Зинаида Виссарионовна Ермольева (1898 – 1974) – автор первого советского пенициллина (крустозин), полученного из P. Crustosum
Сам термин «антибиотики» (от греч. Anti, bios – против жизни) был предложен С. Ваксманом в 1942 году для обозначения природных веществ, продуцируемых микроорганизмами и в низких концентрациях антагонистичных к росту других бактерий.
В последующем число антибиотиков быстро росло. После 1940 было получено множество клинически важных антибиотиков, в их числе бацитрацин, хлорамфеникол (левомицетин), хлортетрациклин, окситетрациклин, амфотерицин В, циклосерин, эритромицин, гризеофульвин, канамицин, неомицин, нистатин, полимиксин, ванкомицин, виомицин, цефалоспорины, ампициллин, карбенициллин, аминогликозиды, стрептомицин, гентамицин.
Открытие левомицетина дает возможность бороться с сыпным тифом и трахомой — заболеванием глаз, приводившим к слепоте. Это же лекарство излечивает и дизентерию.
Другой антибиотик — тетрациклин губительно действует сразу на многих болезнетворных микробов. При этом, в отличие от пенициллина и стрептомицина, тетрациклин, так же как и левомицетин, принимается внутрь. Он быстро всасывается из желудка в кровь, с нею попадает ко всем тканям организма и поражает микробов.
В распоряжении врачей уже много надежных лекарств против микробов. Исследователи непрерывно ищут такие антибиотики, которые будут излечивать еще не побежденные болезни, вызывать меньше осложнений, дольше действовать.
В настоящее время открывают все новые и новые антибиотики. В середине 1980-х годов в США антибиотики прописывались чаще, чем любые другие лекарства, за исключением седативных средств и транквилизаторов. Антибиотики представляют собой самую многочисленную группу лекарственных средств. В настоящее время описано почти 7000 антибиотиков (образуемых лишь микроорганизмами); при этом только около 160 из них используется в медицинской практике. Так, в России в настоящее время используется 30 различных групп антибиотиков, а число препаратов приближается к 200.
Вероятно, в конце концов удастся найти антибиотики и против рака: уже сейчас обнаружены антибиотики, которые могут если не излечивать, то задерживать развитие раковых опухолей у человека и животных.
В руках врачей антибиотики стали могучим средством борьбы со многими тяжелыми болезнями. Однако их нельзя применять без назначения врача, так как это может привести к вредным последствиям, например вызвать так называемую лекарственную болезнь. Поэтому только врач может решить, какой антибиотик и в какой дозе следует принимать больному.
Классификация антибиотиков по происхождению:
Антибиотики микробного происхождения
А) антибиотики, образуемые бактериями:
Актиномицетами: Стрептомицин, канамицин, гентамицин, тетрациклин, эритромицин, циклосерин, леворин
Палочковидными бактериями: грамицидин С, полимиксин, продигиозин
Б) Антибиотики, образуемые плесневыми грибами: Пенициллины, цефалоспорины, гризеофульвин, микроцид
2) Антибиотики растительного происхождения (фитонциды): Новоиманин (трава зверобоя), алилчеп (лук), хлорофиллипт (листья эвкалипта), гассипол (семена хлопка или корень хлопчатника)
3) Антибиотики животного происхождения - лизоцим (яичный белок)
Классификация антибиотиков по химической структуре:
Класс |
Название класса |
Состав |
Некоторые представители |
I |
β-лактамы (основные группы: пенициллины, цефалоспорины, монобактамы, карбапенемы) |
Азотосодержащие гетероциклические соединения, имеющие β-лактамное кольцо |
Бензилпенициллин Цефазолин Имипенем |
II |
Гликопептиды |
Гликозилированные циклические или полициклические нерибосомные пептиды |
Ванкомицин Тейкопланин |
III |
Аминогликозиды |
В состав молекулы входят аминосахара |
Стрептомицин Гентамицин Тобрамицин Канамицин |
IV |
Тетрациклины |
Состоят из 4 конденсированных бензольных колец с различными радикалами |
Доксициклин Тетрациклин |
V |
Макролиды и Азалиды |
Содержат лактонное кольцо, связанное с аминосахарами |
Эритромицин Азитромицин Кларитромицин |
VI |
Линкозамиды |
Содержат в составе молекулы несколько колец |
Линкомицин Клиндамицин |
VII |
Левомицетин (хлорамфеникол) |
Содержат в составе молекулы нитробензеновое ядро |
Левомицетин Хлорамфеникол |
VIII |
Рифамицины |
Ароматические соединения, производные диокси-аминофенилпропана |
Рифампицин |
IX |
Полипептиды |
Полимеры, построенные из остатков аминокислот |
Полимиксин Грамицидин |
X |
Полиены |
Содержат несколько сопряженных двойных связей в молекулах |
Амфотерицин В Нистатин Леворин |
Антибиотики в медицине. Открытие антибиотиков вызвало переворот в медицине. Многие антибиотические вещества оказались незаменимыми лечебными препаратами. Они нашли широкое применение при лечении многих инфекционных заболеваний, которые ранее считались неизлечимыми или сопровождались высоким летальным исходом. К числу таких заболеваний необходимо отнести некоторые формы туберкулеза и, прежде всего туберкулез менингитный, который до применения антибиотиков вызывал 100%-ный летальный исход, чуму, азиатскую холеру, брюшной тиф, бруцеллез, пневмонию, различные септические процессы и др.
Антибиотики в сельском хозяйстве. Наряду с медицинским использованием антибиотики находят широкое применение в сельском хозяйстве. Прежде всего, антибиотики используются в качестве препаратов в ветеринарии для лечения различных заболеваний сельскохозяйственных животных. В этом случае они, как и в медицине, оказались весьма эффективными средствами.
Антибиотические вещества находят все возрастающее применение в борьбе с фитопатогенными организмами - возбудителями заболеваний растений, наносящими ощутимый урон сельскохозяйственному производству.
При выборе антибиотиков, используемых в растениеводстве, необходимо руководствоваться следующими основными требованиями к препарату:
1) антибиотик должен обладать специфической биологической активностью к возбудителю заболевания растений;
2) он должен легко проникать в ткани растений и проявлять внутри них биологическую активность;
3) лечебные дозы антибиотика должны быть безвредными для растения;
4) антибиотик, находясь на поверхности и внутри тканей растения, должен относительно длительное время проявлять биологическую активность, но должен также легко и быстро инактивироваться, попадая в почву.
Одним из самых главных требований к антибиотикам, используемым в сельском хозяйстве, должно быть то, чтобы эти препараты не применялись в медицинской практике. Это принципиальное условие обеспечивает снижение уровня появления резистентных форм микроорганизмов, патогенных для человека.
Антибиотики в пищевой и консервной промышленности. При борьбе с микроорганизмами, вызывающими порчу продуктов питания, наряду с физическими и химическими методами применяются и антибиотики. Однако для этих целей не могут быть использованы антибиотики, применяемые в медицине. Это правило введено в нашей стране и ряде других государств и связано оно с предупреждением процесса возникновения и распространения устойчивых к антибиотикам форм микробов.
Среди антибиотиков, применяемых в пищевой и консервной промышленности, можно назвать субтилин, низин и некоторые другие.
33. Особенности обмена веществ микроорганизмов. Спиртовое брожение: возбудители, химизм, энергетическая эффективность, применение.
Спиртовое брожение - микробиологический процесс превращения углеводов в спирт и углекислый газ. Вызывается аскомицетовыми дрожжами рода Saccharomyces, некоторыми бактериями и отдельными представителями мукоровых грибов.
Суммарное уравнение реакции:
С6 H12 O6 → 2 СНзCH2 ОН + 2 СО2 + Е
Основными возбудителями спиртового брожения являются дрожжи - сахаромицеты.
Это факультативно-анаэробные микроорганизмы. В аэробных условиях дрожжи получают энергию путем полного окисления моно- и дисахаридов до углекислого газа и воды, т.е. путем аэробного дыхания. При этом интенсивно накапливается биомасса (эффект Пастера). Поэтому производство хлебопекарных дрожжей ведут в аэробных условиях.
С энергетической точки зрения брожение – процесс малоэкономичный; выше указывалось, что при использовании грамм-молекулы глюкозы в процессе брожения синтезируется всего 2 моля АТФ.
Любое брожение – процесс многоэтапный, протекающий как бы в две стадии:
первая – окислительная – включает превращение глюкозы до пировиноградной кислоты с образованием двух молекул восстановленного НАД-Н2 – промежуточного акцептора- водорода.
во второй стадии – восстановительной ■–НАД-Н2 передает водород конечному акцептору, который превращается в основной конечный продукт брожения.
Недостаточность выделяющейся при брожении энергии дрожжи возмещают переработкой значительно большего количества сахара, чем при дыхании. Некоторые дрожжи вообще не способны к сбраживанию сахара и являются аэробами.
Спиртовое брожение лежит в основе производства этилового спирта, пива, вина, используется в хлебопечении. Совместно с молочнокислым брожением оно используется при производстве кваса, кефира, кумыса. Основными потребителями этилового спирта являются пищевая и химическая промышленность, а также медицина.
34. Особенности обмена веществ микроорганизмов. Молочнокислое брожение: возбудители, химизм, энергетическая эффективность, применение.
Молочнокислое брожение - процесс превращения углеводов молочнокислыми бактериями в молочную кислоту.
Возбудители молочнокислого брожения подразделяются на 2 группы: гомоферментативные и гетероферментативные, которые в свою очередь вызывают гомоферментативное и гетероферментативное молочнокислое брожение. В основу этого деления положены конечные продукты, образуемые при гомо- и гетероферментативном молочнокислом брожении.
Гомоферментативное молочнокислое брожение и его возбудители.
При гомоферментативном молочнокислом брожении образуется преимущественно молочная кислота.
Химизм процесса:
С6H12О6 → 2 СНзСНОНСООН + Е
глюкоза → молочная кислота
К гомоферментативным молочнокислым бактериям относятся молочнокислые стрептококки: Streptococcus lactis, Streptococcus cremoris, Streptococcus thermophilus, а также молочнокислые палочки: Lactobacillus delbrueckii, Lactobacillus acidophilus, Lactobacilus bulgaricus, Lactobacillus ptantarum.
Гетероферментативное молочнокислое брожение и его возбудители. Конечными продуктами при этом брожении являются не только молочная кислота, но и побочные продукты: уксусная кислота, этиловый спирт, янтарная кислота, диоксид углерода, водород. Суммарное уравнение процесса имеет вид:
С6H12О6 → СНзСНОНСООН + СООНСН2СН2СООН + СНзСООН +
глюкоза →молочная кислота +янтарная кислота +уксусная кислота
СНзСН2ОН + C02+Н2 +Е
этиловый спирт
К гетероферментативным молочнокислым бактериям относятся бактерии рода Streptococcus: Streptococcus diacetilactis, Streptococcus acetoinicus; бактерии рода Lactobacillus: Lactobacillus brevis, Lactobacillus helveticus, а также бактерии рода Leuconostoc: Leuconostoc mesenteroides, Leuconostoc cremoris.
Энергетическая эффективность молочнокислого брожения составляет две молекулыАТФ, образованные в процессе окисления глюкозы до пирувата. Для многих микроорганизмов брожение является единственным способом ассимиляции энергии. Большинство таких организмов живет в анаэробных условиях и погибает в присутствии кислорода, но есть и такие, которые нормально существуют и в присутствии кислорода, и без него.
Практическое значение молочнокислого брожения
Оно находит широкое применение при изготовлении кисломолочных продуктов, сливочного масла, маргарина, используется в хлебопечении, при квашении овощей, силосовании кормов и производстве молочной кислоты.
Многие мезофильные гетероферментативные молочнокислые бактерии и лейконосток являются вредителями в производстве спирта, пива, вина, безалкогольных напитков, сахара и др.
35. Особенности обмена веществ микроорганизмов. Маслянокислое брожение: возбудители, химизм, энергетическая эффективность, применение.
Маслянокислое брожение – это процесс превращения бактериями в анаэробных условиях углеводов, спиртов и других органических веществ в масляную кислоту (бутират).
Маслянокислые бактерии относятся к роду Clostridium. Это крупные, подвижные грамположительные палочки, образующие устойчивые споры. Широко распространены в природе. Быстро разлагают органическое вещество.Обитают там, где много органических веществ и нет доступа воздуха - в иловых отложениях водоемов, навозе, почве и т.д.
Суммарное уравнение процесса: С6Н12О6 → СН3СН2СН2СООН + 2 СО2 + Н2 + Эн.( глюкоза - масляная кислота)
Маслянокислое брожение используется в промышленности для получения масляной кислоты (продуцент Clostridiumbutyricum). Хотя масляная кислота обладает резким, неприятным запахом прогорклого масла, ее эфиры отличаются приятным ароматом: метиловый эфир имеет яблочный запах, этиловый - грушевый, амиловый - ананасный. Эфиры масляной кислоты используют в кондитерской, безалкогольной, парфюмерной промышленности.
Маслянокислые бактерии участвуют в круговороте веществ в природе. С другой стороны, маслянокислые бактерии могут вызвать массовую гибель картофеля и овощей, вспучивание сыров, порчу консервов, прогоркание масла и маргарина, увлажненной муки и других продуктов, чем наносят большой урон народному хозяйству. Борьба с маслянокислыми бактериями затруднена из-за высокой устойчивости спор.
36. Особенности обмена веществ микроорганизмов. Уксуснокислое брожение: возбудители, химизм, энергетическая эффективность, применение.
Уксуснокислое брожение – аэробное окисление углеводов и спирта уксуснокислыми бактериями в уксусную кислоту. Таким образом, это брожение относится к неполным окислениям или окислительным брожениям. Суммарное уравнение процесса имеет вид:
С6H12O6 + 2 02 → 2СНзСООН + 2CO2 + 2Н20 + Е или
глюкоза → уксусная кислота
СНзСН2ОН + O2 → СНзСООН + Н2О + Е
этиловый спирт → уксусная кислота
возбудителями уксуснокислого брожения являются уксуснокислые бактерии, относящиеся к двум родам: Gluconobacter и Acetobacter. Это короткие, подвижные грамотрицательные палочки, не образующие спор. Оптимальная температура развития - 30˚ С. Бактерии кислотоустойчивы, оптимальное значение рН для развития 5,4-6,3. Обитают на цветах, зрелых фруктах, ягодах, овощах, в прокисших соках, пиве, вине, квашенных овощах.
Практическое значение уксуснокислого брожения
Используется в промышленности для получения натурального спиртового уксуса (продуцент Acetobacter aceti). Кроме того, производят также винный уксус (из вина) и яблочный уксус (из яблочного сока).
С другой стороны, уксуснокислые бактерии являются вредителями спиртового, пивоваренного, консервного производств, виноделия, производства безалкогольных напитков
37. Особенности обмена веществ микроорганизмов. Лимоннокислое брожение: возбудители, химизм, энергетическая эффективность, применение.
Лимоннокислое брожение, окисление плесневыми грибами из родов Aspergillus и Penicillum углеводов, некоторых спиртов и органических кислот до лимонной кислоты.
Лимоннокислым брожением называется окисление глюкозы грибами в лимонную кислоту. Конечный результат брожения можно представить следующим суммарным уравнением:
2С6Н1206 +302 -> 2С6Н807 + 4Н20.
Химизм образования лимонной кислоты из сахара до настоящего времени окончательно не установлен. Большинство исследователей считает, что это брожение до образования пировино-градной кислоты протекает, как и другие брожения. Далее превращение пировиноградной кислоты в лимонную через ряд кислот (уксусную, янтарную, фумаровую, яблочную, щевелево-уксусную) сходно с превращениями в цикле Кребса.
Лимонная кислота используется в кондитерской промышленности, производстве безалкогольных напитков, сиропов, в кулинарной практике и медицине.
38. Особенности обмена веществ микроорганизмов. Разложение клетчатки и пектиновых веществ: возбудители, химизм, энергетическая эффективность, применение.
Целлюлозоразлагающие бактерии (цитофаги, миксобактерии, ак- тиномицеты) и пектинразлагающие (многие виды рода Bacillus) обитают в почве.
Разложение клетчатки и пектиновых веществ в аэробных условиях происходит под действием микроорганизмов, которые обладают пектолитическими ферментами и целлюлазой.

Продукты распада пектиновой кислоты (сахара) окисляются или сбраживаются разнообразной микрофлорой. В анаэробных условиях - это маслянокислое брожение. Пектиновое брожение используется при мочке волокнистых растений (лен, конопля, кенаф и т. д.). Разложение пектиновых веществ в аэробных условиях – это "гнили" плодов и овощей. Размягчение консервированных огурцов вызывают возбудители Bacillus.
39. Круговорот азота в природе. Процессы аммонификаци, нитрификации и иммобилизации азота.
Аммонификация
Микробиологическое превращение азотсодержащих органических соединений (белка, мочевины, нуклеиновых кислот, хитина и других веществ) сопровождается освобождением аммиака, вследствие чего данный процесс получил название аммонификации
Этот процесс называют также гниением, поскольку при этом происходит накопление продуктов, обладающих неприятным специфическим запахом
Аммонификация – один из важнейших процессов, определяющих плодородие почвы, поскольку при этом азот из недоступной для растений формы переходит в аммиак
В разложении белков участвуют многочисленные грибы и бактерии, в том числе представители родов Bacillus, Pseudomonas, Proteus и др.
Нитрификация Высвобождающийся аммиак образует с различными кислотами аммонийные соли, которые являются источниками азотного питания для растений и микроорганизмов Высвобождающийся аммиак окисляется нитрифицирующими бактериями до нитритов и нитратов в процессе нитрификации Процесс нитрификации осуществляют нитрифицирующие бактерии, которые являются хемолитотрофами К хемолитотрофным относятся бактерии, которые используют в качестве источника энергии процессы окисления неорганических веществ
Нитрификация является двухфазным процессом
Все нитрифицирующие бактерии выделены в семейство Nitrobacteriaceae и разделены на две группы, в зависимости от того, какую фазу процесса они осуществляют:
Первую фазу - окисление солей аммония до солей азотистой кислоты (нитритов) осуществляют так называемые аммонийокисляющие бактерии - представители родов Nitrosomonas, Nitrosococcus и Nitrosolobus и др
Вторую фазу нитрификации – окисление нитритов до нитратов – осуществляют нитритокисляющие бактерии, которые относятся к родам Nitrobacter, Nitrococcus и др.
Все нитрифицирующие бактерии грамотрицательные облигатные аэробы и автотрофы
Иммобилизации азота
При определенных условиях имеющиеся в почве минеральные формы азота переходят в недоступные для растений соединения. Один из таких процессов возникает вследствие бурного развития микроорганизмов, которые потребляют азот и переводят его в белок цитоплазмы. Подобный процесс называют иммобилизацией азота.
Биологически закрепленный азот не теряется из почвы. После отмирания микроорганизмов белковые вещества минерализуются и превращаются в аммиак.
Иммобилизация азота наблюдается, например, при внесении в почву значительной массы соломы или соломистых удобрений. В результате иммобилизации использование азота растениями заметно снижается, что приводит к уменьшению урожая. Таким образом, иммобилизация представляет собой процесс, обратный минерализации.
Скорость и размеры ассимилируемого микробами азота связаны и с типом углеродсодержащего соединения. Так, глюкоза, легко используемая микроорганизмами, может вызвать значительно более быстрое закрепление азота, чем целлюлоза или, тем более лигнин. В общем можно считать, что органические соединения с соотношением С : N, близким к 20—25 : 1 и менее, способствуют накоплению минеральных форм азота в почве, а вещества с более широким соотношением этих элементов вызывают иммобилизацию азотных запасов.
Зная условия иммобилизации неорганического азота, можно сделать важные агротехнические выводы. Так, удобрять почву, предназначенную под зерновые культуры, растительными остатками, бедными азотом, опытный агроном не станет, так как это ухудшает азотное питание растений. Соломистые удобрения он будет вносить в почву лишь с добавлением соответствующих доз азотных удобрений.
В осеннее время года иммобилизация полезна, так как нитраты и аммиак связываются и не теряются в результате выщелачивания зимой. Весной азот, входящий в состав микробной клетки, частично минерализуется и превращается в аммиак и нитраты, которые затем используют растения. Интересно, что бобовые растения, которые существуют в симбиозе с бактериями, фиксирующими атмосферный азот, не испытывают депрессии от внесения соломистых удобрений. Наоборот, последние увеличивают их урожай и способствуют лучшему азотонакоплению.
40. Круговорот Азота в природе. Процесс азотфиксации. Свободноживущие и симбиотические азотфиксирующие микроорганизмы.
Основными микробиологическими процессами, связанными с превращением азотистых веществ, являются аммонификация, нитрификация, денитрификация и фиксация молекулярного азота

Считают, что этапом, ограничивающим скорость круговорота азота, является процесс азотфиксации
Это в основном биологический процесс, и единственными организмами, способными его осуществлять, являются бактерии
Способность к азотфиксации широко распространена среди бактерий
Биологическая фиксация азота в природе осуществляется частично свободноживущими, а частично симбиотическими азотфиксирующими бактериями
К азотфиксаторам относятся как аэробные, так и анаэробные бактерии
К свободноживущим азотфиксирующим бактериям относятся аэробные бактерии родов Azotobacter и Beijerinckia
К свободноживущим анаэробным азотфиксаторам относится бактерия Clostridium pasteurianum, которая была выделена из почвы еще С.Н.Виноградским
К симбиотическим азотфиксирующим бактериям относятся представители рода Rhizobium (клубеньковые бактерии)
В род Rhizobium объединены бактерии, вызывающие образование клубеньков на корнях бобовых растений и способные фиксировать азот в условиях симбиоза с ними
Конечным продуктом азотфиксации является ион аммония, который далее включается в азотсодержащие органические вещества (белки, нуклеиновые кислоты и др.)
Азотсодержащие органические вещества могут либо находится в составе клеток микроорганизмов, либо, при симбиотической азотфиксации, они находятся в составе растений, а при поедании растений животными попадают в тело животных
41. Круговорот серы. Микроорганизмы в нем участвующие, химизм обмена серы.
Микроорганизмы играют ключевую роль в осуществлении следующих важнейших этапов в превращении серы: минерализации органической серы, окислении минеральной серы и восстановлении минеральной серы
Микроорганизмы также участвуют в этапе ассимиляции сульфатов По морфологическим и физиологическим признакам бактерии, объединенные в группу сульфатвосстанавливающих бактерий, разнообразны
Среди них есть одноклеточные и нитчатые формы, неподвижные или передвигающиеся с помощью жгутиков или скольжением
Большинство имеют клеточную стенку грамотрицательного типа
Все они облигатные анаэробы
К сульфатвосстанавливающим бактериям относятся бактерии родов Desulfovibrio, Desulfotomaculum, Desulfobacter, Desulfococcus и другие
42. Питательные среды и методы стерилизации оборудования и сред.
Классификация питательных сред по составу:
1. Простые среды (МПБ, МПА, желатин, пептонная вода). Мясо-пептонный бульон (МПБ) является белковой основой всех сред. Существует несколько способов приготовления МПБ:
а) на мясной воде с добавлением готового пептона (продукт неполного переваривания белка) – это так называемый мясопептонный бульон;
б) на переварах продуктов гидролиза исходного сырья при помощи ферментов (трипсина – бульон Хоттингера, пепсина – бульон Мартена).
2. Сложные среды готовятся на основе простых с определенными добавками (углеводы, кровь, желчь, яйца, сыворотка, молоко, соли, факторы роста и т.п.)
Классификация питательных сред по исходным компонентам:
1.Естественные питательные среды — это натуральный продукт животного или растительного происхождения. Могут быть:
Растительные (исходные продукты – соя, горох, картофель, морковь и т.п.)
Животные (исходные продукты – мясо, рыба, яйца, молоко, животные ткани, желчь, сыворотка крови.и т.п.)
Смешанные (МПА, среда Левенштейна – Йенсена и т.п.)
2. Искусственные среды содержат переработанные естественные продукты (мясную воду, перевар), вещества, полученные из этих продуктов (пептон, дрожжевой и кукурузный экстракты) и различные добавки. Это самая большая и разнообразная по составу наиболее часто применяемая группа сред. Их готовят по определенным рецептам из различных настоев или отваров животного или растительного происхождения с добавлением неорганических солей, углеводов и азотистых веществ.
3. Синтетические среды (известного химического состава) состоят из химически чистых соединений в точно установленных концентрациях (с добавлением углеводов, солей, аминокислот, витаминов и т.п.). На основе этих сред, добавляя к ним естественные или искусственные среды получают полусинтетические среды.
Стерилизация питательных сред. Все питательные среды независимо от их назначения разливают в чистую посуду и стерилизуют. Большинство сред стерилизуют автоклавированием, но при различных режимах в зависимости от их состава.
1. Синтетические среды и все агаровые среды, не содержащие в своем составе нативного белка и углеводов, стерилизуют 15—20 мин в автоклаве при температуре 115—120°С и давлении 1-1,5 атмосферы.
2. Среды с углеводами и молоком (в состав которого входит лактоза), питательный желатин стерилизуют текучим паром при температуре 100°С дробно или в автоклаве при 112°С и давлении до 1 атмосферы.
3. Среды, в состав которых входят белковые вещества (сыворотка крови, асцитическая жидкость), обеспложиваются тиндализацией или фильтрованием.
4. Для стерилизации питательных сред, содержащих в своем составе нативные белки, пользуются фильтрацией через мембранные фильтры Зейтца
Для контроля стерильности среды после стерилизации помещают в термостат при 37°С на 3-5 сут. Жидкие среды должны оставаться прозрачными, а на поверхности и в толще плотных питательных сред не должны появляться признаки роста. Кроме контроля стерильности, производят химический контроль готовых сред, который заключается в том, что в нескольких образцах каждой серии определяют рН, количество общего и аминного азота и хлоридов.
Существует также биологический контроль сред. В этом случае несколько образцов среды засевают лабораторной культурой того микроба, для которого приготовлена среда, и изучают характер его роста. Только после того, как среды выдержали контроль, их можно использовать по назначению.
Метод |
Краткая характеристика |
Область применения |
Термический: |
Нагревание объекта стерилизации |
Основной метод стерилизации реакторов, сред, оборудования |
а) острым паром |
Пропускание струи пара в агрегат со средой |
Стерилизация аппаратов и сред |
б) глухим паром |
Пар изолирован от стерилизуемых сред металлическими стена-ми (например, в змеевиках) |
Стерилизация питательных сред и их компонентов |
в) паром генерируемым в сосуде |
Используются электро-нагреватели, которые вводят в стерилизуемый объект |
Стерилизация реакторов и сред |
г) в автоклаве |
Паром под давлением |
Стерилизация сред, мелкого оборудования |
2. Химический |
С применением дезинфицирующих агентов (окиси этилена или пропилена, ß-пропио-лактона) |
Стерилизация питательных сред |
3.Фильтрационный |
Пропускание газов или жидкостей через мелкопористые или волокнистые фильтры, задерживающие микроорганизмы |
Стерилизация воздуха (газа), жидких сред |
4.Радиационный |
Обработка УФ- и ионизирующими излучениями |
Не распространен |
