
- •Введение
- •1. Спектральные и оптические методы анализа
- •1.1. Эмиссионный спектральный анализ. Фотометрия пламени
- •Контрольные вопросы
- •1.2. Молекулярно-абсорбционный анализ
- •Контрольные вопросы
- •1.3. Дифференциальная фотометрия
- •Контрольные вопросы
- •1.4. Фотометрическое титрование
- •Контрольные вопросы
- •1.5. Кинетический метод анализа
- •Контрольные вопросы
- •1.6. Фотометрия светорассеивающих систем
- •Контрольные вопросы
- •1.7. Люминесцентный анализ
- •Контрольные вопросы
- •1.8. Рефрактометрический метод анализа
- •Контрольные вопросы
- •1.9. Метрологические характеристики и статистическая обработка результатов анализа
- •2. Электрохимические методы анализа
- •2.1. Электрогравиметрия
- •Контрольные вопросы
- •2.2. Потенциометрия
- •Контрольные вопросы
- •2.3. Кондуктометрия
- •Контрольные вопросы
- •2.4. Полярографический анализ
- •Контрольные вопросы
- •2.5. Амперометрическое титрование
- •Контрольные вопросы
- •3. Хроматографические методы
- •3.1. Характеристика основных конструктивных узлов (блоков) хроматографа
- •3.2. Принцип работы газового хроматографа на примере chrom 5
- •3.3. Генератор водорода. Устройство и принцип работы
- •3.4. Методика выполнения работы Отбор пробы
- •Подготовка хроматографов к выполнению измерения
- •Выполнение измерений
- •Вычисление результатов анализа
- •3.5. Методы расчета хроматограмм
- •3.6. Методы расчета концентраций
- •Контрольные вопросы
- •4. Титриметрические методы анализа
- •Правила титрования
- •4.1. Кислотно-основное титрование в водном растворе
- •Контрольные вопросы
- •4.2. Осадительное титрование
- •Контрольные вопросы
- •4.3. Методы комплексообразования. Комплексонометрическое титрование
- •Контрольные вопросы
- •4.4. Окислительно-восстановительное титрование
- •Контрольные вопросы
- •Заключение
- •Библиографический список
- •Оглавление
- •394026 Воронеж, Московский просп., 14
Контрольные вопросы
1. Отличие турбидиметрии от нефелометрия.
2. Факторы, влияющие на условия измерения и их учет.
3. Напишите формулы коллоидных мицелл оксалата кальция до и после точки эквивалентности.
4. Применимость методов сравнения калибровочного графика, титрования для анализа. Преимущества и недостатки.
5 Точность измерений в фотометрии светорассеивающих систем.
1.7. Люминесцентный анализ
Люминесценция – избыточное по сравнению с тепловым излучение, возникающее через некоторое время ( > 10–8 с) после поглощения веществом энергии извне. Если излучение возникает в результате поглощения ультрафиолетового света, его называют флуоресценцией. Энергетическая схема флуоресценции представлена на рис. 7. Линиями изображены колебательные подуровни нормального (синглетного) и возбужденного (тоже синглетного) состояния молекулы; V – колебательные квантовые числа.
Из-за потерь энергии на внутреннюю конверсию в возбужденном состоянии (переход на нижний колебательный подуровень, с которого происходит излучательный переход молекулы в нормальное состояние) спектр флуоресценции смещен в область больших длин волн в сравнении со спектром поглощения.

Рис. 7. Схема, иллюстрирующая явление флуоресценции
Зависимость интенсивности флуоресценции от концентрации I = f(С) проходит через максимум, но для очень малых значений С она является линейной и характеризуется высокой чувствительностью.
Флуориметрические измерения проводят на приборах, позволяющих выделить в падающем на кювету световом потоке при помощи светофильтра длину волны ультрафиолетового диапазона, соответствующую максимуму поглощения молекулами или ионами анализируемого вещества. Второй светофильтр выделяет в световом потоке флуоресцентного излучения длину волны, соответствующую максимуму излучения. Принципиальная схема флуориметра изображена на рис. 8.
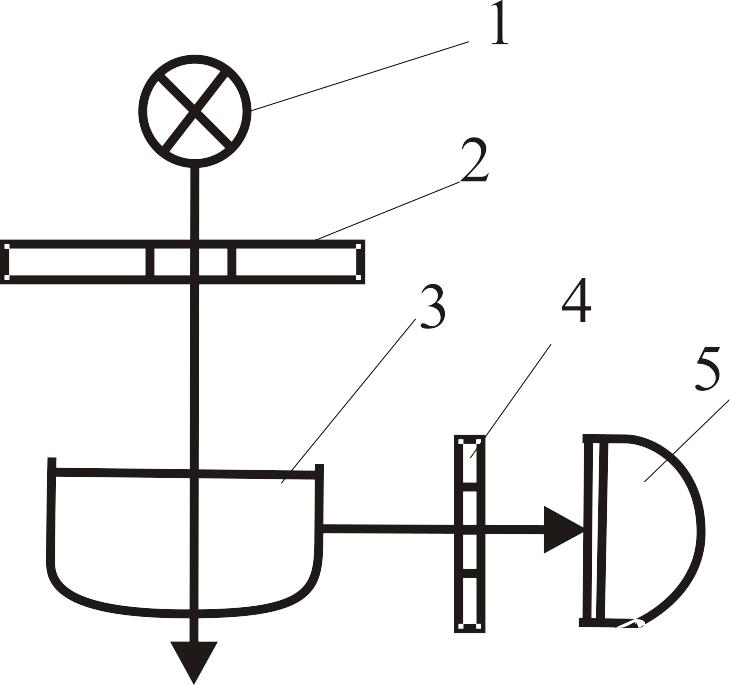
Рис. 8. Схема флуориметра: 1– источник света, 2 – светофильтр, 3 – кювета, 4 – светофильтр, 5 – приемник света
Пример. Количественное определение бора флуориметрическим методом.
Флуоресценция (разновидность люминесценции) представляет собой вторичное излучение молекул в короткий период времени непосредственно после поглощения инициирующего ультрафиолетового излучения. Длина волны вторичного излучения больше, чем инициирующего.
Для очень разбавленных растворов наблюдается линейная зависимость интенсивности флуоресценции от концентрации. Бор образует с бензоином комплекс обладающей способностью к флуоресценции. При проведении реакции в щелочной водно-спиртовой среде облучаемый ультрафиолетовыми лучами раствор дает светло-голубое свечение с максимумом излучения около 480 нм.
В мерные колбы на 25 мл помещают 1, 2, 3, 4 и 5 мл стандартного раствора бора. Добавляют по 15 мл этанола, 3 мл буферного раствора, 2 мл раствора бензоина и водой доводят объем до метки. Одновременно аналогично готовят задачу и нулевой раствор, содержащий все компоненты, кроме бора. Через 5 мин после сливания и перемешивания реагентов измеряют интенсивность флуоресценции эталонных растворов и задачи. По полученным данным строят калибровочный график в координатах “деления шкалы прибора – концентрация бора в пробе”. Обрабатывают его по методу наименьших квадратов. Рассчитывают доверительный интервал для концентрации бора в пробе. Результат анализа определяют по графику.
