- •Растворы
- •100 г раствора – 4 г NaBr 1000г раствора – 40 г
- •Молярная концентрация эквивалента.
- •Количество вещества эквивалента равно отношению массы вещества Х к молярной массе эквивалента этого
- •Рассчитать мольные доли глюкозы С6H12O6 и воды в растворе с массовой долей глюкозы
- •.Расcчитать молярность и моляльность 15-% раствора серной кислоты (плотность 1,1 г/см3)
- •Задание
- •Растворы электролитов и неэлектролитов
- •Вещества
- •Почему растворы электролитов проводят электрический ток?
- •Строение молекулы воды
- •Электролитическая диссоциация – процесс распада электролита на ионы при растворении его в воде
- •Последовательность процессов, происходящих при электролитической диссоциации:
- •Уравнения диссоциации
- •Электролиты
- •Степень диссоциации – это отношение числа частиц, распавшихся на ионы (Nд),
- •Водородный показатель, рН среды, кислотность среды
- •Индикаторы
- •Принцип
- •Среди физиологических жидкостей организма наиболее кислым является желудочный сок, фактически он представляет собой
.Расcчитать молярность и моляльность 15-% раствора серной кислоты (плотность 1,1 г/см3)
Масса 1 л кислоты m = 1000*1,105 = 1105 г.
Кислоты в нем содержится 1105*0,15=165,75 г.
Эквивалентная масса кислоты 98/2=49 г/моль.
Нормальность (молярная концентрация эквивалента): Сэкв = 165,75/(49*1) = 3,38 н.
(моль-экв/дм3)
Молярность (молярная концентрация): С = 165,75/(98*1) = 1,69 М (моль/дм3) Моляльность: b = 165,75/(98*(1105-165,75)) = 1,8 моль/кг
Задание
1,33 г AlCl3 растворили в 200 мл воды.
Плотность полученного раствора - 1,05 г/см3.
Рассчитать: ω, С, Сэкв, b, χ

Растворы электролитов и неэлектролитов
Вещества
ЭЛЕКТРОЛИТЫ НЕЭЛЕКТРОЛИТЫ
Электролиты – вещества, растворы и расплавы которых проводят электрический ток
Неэлектролиты – вещества, растворы и расплавы которых не проводят электрический ток.
Почему растворы электролитов проводят электрический ток?
Сванте Аррениус (1859-1927)
Создал теорию электролитической диссоциации. За исследования в области электролитов был удостоен
Нобелевской премии в 1903 г.

Строение молекулы воды
O
104,5
H H
+
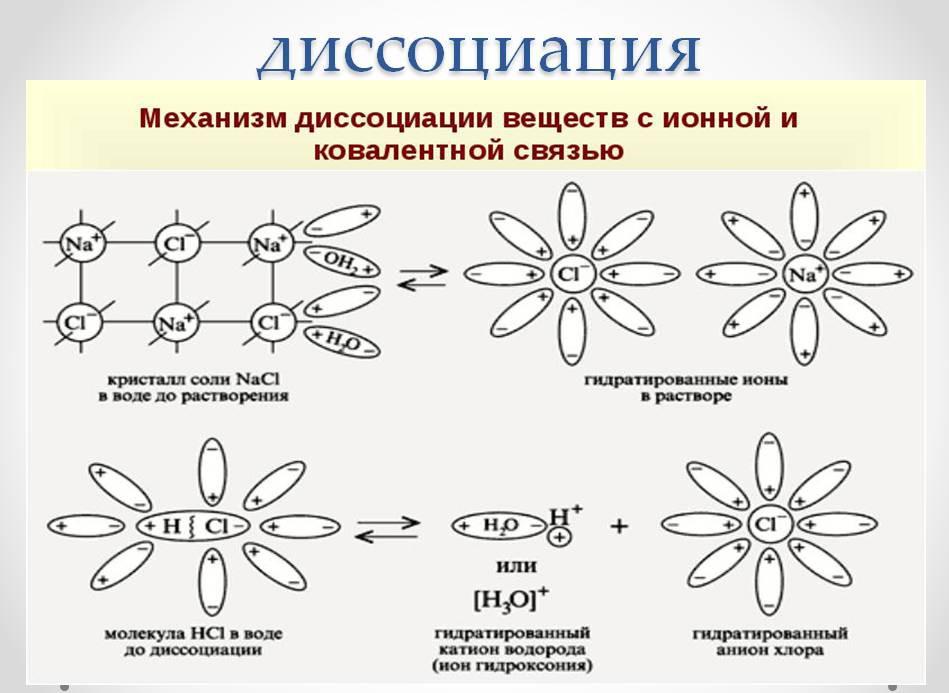
Электролитическая диссоциация – процесс распада электролита на ионы при растворении его в воде или расплавлении.
Легче всего диссоциируют вещества с ионной и ковалентной полярной связью:
 Кислоты : HCl, H2SO4, HF, HNO3
Кислоты : HCl, H2SO4, HF, HNO3
 Основания: NaOH, Ba(OH)2, KOH
Основания: NaOH, Ba(OH)2, KOH  Соли : NaCl, CuSO4, KNO3
Соли : NaCl, CuSO4, KNO3