
- •Контрольная работа №1
- •1. Параметры состояния.
- •2. Уравнение состояния идеального газа.
- •3. Смеси идеальных газов.
- •4. Теплоёмкость.
- •5. Первый закон термодинамики.
- •6. Термодинамические процессы идеальных газов.
- •7. Второй закон термодинамики.
- •8. Газовые циклы.
- •9. Теплопередача.
- •10. Тепловая защита зданий. Теплоснабжение и горячее водоснабжение.
- •12. Газоснабжение жилых и промышленных объектов. Принципиальные схемы и оборудование.
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО РЫБОЛОВСТВУ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«МУРМАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Кафедра энергетики и транспорта
Контрольная работа №1
по дисциплине: «Теплогазоснабжение и вентиляция».
Вариант №37.
Выполнил: Кушнир В. Н.
Группа Ст(б) – 391.01
Факультет ЕТФ
Проверил: Пантелеев С. П.
доцент кафедры энергетики
и транспорта.
Мурманск
2012
1. Параметры состояния.
1.16. В лекциях Чаплина В.М. по отоплению и вентиляции для 3-го курса Императорского Московского Технического Училища (1903 г.) приводятся следующие значения нормальных температур внутри помещений.
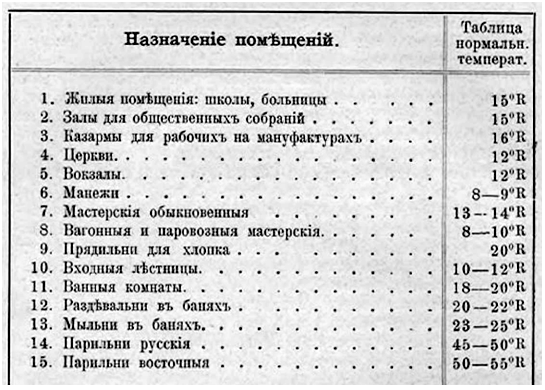
Выразить данные температуры в градусах Цельсия.
Решение:
t°С =5 t°R/4.
5*15/4=18,75 °С.
16*5/4=20 °С.
12*5/4=15 °С.
8*5/4=10 °С.
9*5/4=11,25 °С.
13*5/4=16,25 °С.
14*5/4=17,5 °С.
8*5/4=10 °С.
10*5/4=12,5 °С.
20*5/4=25 °С.
18*5/4=22,5 °С.
22*5/4=27,5 °С.
23*5/4=28,75 °С.
25*5/4=31,25 °С.
45*5/4=56,25 °С.
50*5/4=62,5 °С.
55*5/4=68,75 °С.
15 °R=18,75 °С.
16 °R=20 °С.
12 °R=15 °С.
8 - 9 °R=10 - 11,25 °С.
13 - 14 °R=16,25 - 17,5
8 - 10 °R=10 - 12,5 °С.
20 °R=25 °С.
10 - 12 °R=12,5 - 15 °С.
18 - 20 °R=22,5 - 25 °С.
20 - 22 °R=25 - 27,5 °С.
23 - 25 °R=28,75 - 31,25 °С.
45 - 50 °R=56,25 - 62,5 °С.
50 - 55 °R=62,5 - 68,75 °С.
Общая задача №2. Масса 5 м3 метана при определенных условиях составляет 4,2 кг. Определить плотность и удельный объем метана при этих условиях.
Решение:
v= V/М - удельный объем.
В системе СИ единица удельного объема 1 м3/кг. Между удельным объемом вещества и его плотность существует очевидное соотношение:
v = 1/ρ, от сюда
ρ= 1/ v.
v=5/4,2=1,19
(кг/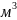 ).
).
ρ=1/1,19=0,84 ( /кг).
2. Уравнение состояния идеального газа.
Общая задача №2. Определить массу газа в сосуде с объемом 6 при температуре 63 оС. Давление газа по манометру равно 0,45 бар. Барометрическое давление 750 мм.рт.ст.
Решение:
B=750
мм.рт.ст=750*133.322=99991.5=0.1*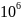 Па
- по табл. П.1.2 "Соотношение между
различными единицами давления".
Па
- по табл. П.1.2 "Соотношение между
различными единицами давления".
Рм =0,45 бар=0,045* Па.
PV= R0T - уравнение Клайперона.
Если газ содержит v молей, то уравнение Клапейрона примет вид:
pV = vR0 T.
В свою очередь v=M/μ.
pV = (M/μ) R0T,
Обозначим через R отношение R = R0 / μ - удельная газовая постоянная.
M=PV/(RT).
P=(0.045+0.1)* =0.145* (Па).
R(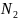 )=297
Дж/(кг*К).
)=297
Дж/(кг*К).
M=(0.145* *6)/(297*336)=8,72 (кг).
2.13. Масса пустого баллона для кислорода емкостью 50 л равна 80 кг. Определить массу баллона после заполнения его кислородом при температуре t = 20 °С до давления 100 бар.
Решение:
PV= R0 T - формула Клайперона.
m=PV/RT - масса кислорода.
R(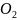 )=260
Дж/кгK.
)=260
Дж/кгK.
m=0,05*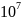 /(260*293)=6,56
(кг).
/(260*293)=6,56
(кг).
М=80+6,56=86,56 (кг).
3. Смеси идеальных газов.
3.13. Газовая смесь имеет следующий массовый состав: СО2 = 12,0 %; О2 = 8,0 %; N2 = 80,0 %. До какого давления нужно сжать эту смесь, находящуюся при нормальных условиях, чтобы плотность её составляла р= =1,6 кг/м3.
Решение:
PV=R○T - уравнение Клайперона.
PV=MRT.
ρ=M/V.
P= ρRT - давление.
T=273 К - т. к. смесь находится в нормальных условиях.
P=1.6*(189*0.12+260*0.08+297*0.8)*273=0.12*106 (Па).
Общая задача №1. Какое давление нужно создать, чтобы газовая смесь массой 8 кг при температуре 220 ○С занимала объем, равный 11 м3? Состав газа : Н2=20 %, О2=31 %, СО2=21 %, N2=28 %.
Решение:
PV=R○T - уравнение Клайперона.
Зная, что R = R0 / μ - удельная газовая постоянная, а
v=M/μ М - удельный объем, получаем:
PV=MRT.
P=MRT/V.
R(Н2)=4125 Дж/кг*К.
R(О2)=260 Дж/кг*К.
R(СО2)=189 Дж/кг*К.
R(N2)=297 Дж/кг*К.
Р=8*(4125*0,2+260*0,31+189*0,21+297*0,28)/11=0,37*106 (Па).
