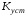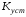- •C.М. Дрюцкая
- •Введение
- •Тема 1. Введение. Классы и номенклатура неорганических соединений. Основные законы и понятия химии. Закон эквивалентов.
- •1.1. Теоретические сведения
- •Химические свойства оксидов
- •Получение кислот
- •Химические свойства кислот
- •Получение оснований
- •Химические свойства оснований
- •Получение солей
- •Химические свойства средних солей
- •Числовые приставки
- •Систематические и тривиальные названия некоторых веществ
- •Систематические и международные названия некоторых сложных веществ
- •Названия наиболее распространенных кислот и их анионов
- •1.2. Контрольные вопросы и задания
- •1.3. Примеры решения задач
- •1.4. Индивидуальные задания
- •Варианты контрольного задания
- •Варианты контрольного задания
- •1.5. Тестовые задания
- •Тема 2. Способы выражения концентрации (состава) раствора.
- •2.1. Теоретические сведения
- •2.2. Контрольные вопросы и задания
- •2.3. Примеры решения задач
- •2.4. Индивидуальные задания
- •Варианты контрольного задания
- •2.5. Тестовые задания
- •Тема 3. Химическая термодинамика.
- •3.1. Теоретические сведения
- •3.2. Контрольные вопросы и задания
- •3.3. Примеры решения задач
- •Стандартные термодинамические функции
- •3.4. Индивидуальные задания
- •Варианты контрольного задания
- •Варианты контрольного задания
- •3.5. Тестовые задания
- •Тема 4. Химическая кинетика. Термодинамика химического равновесия
- •4.1.Теоретические сведения
- •4.2. Контрольные вопросы и задания
- •4.3. Примеры решения задач
- •4.4. Индивидуальные задания
- •Варианты контрольного задания
- •4.5. Тестовые задания
- •Тема 5. Строение атома. Периодический закон и периодическая система элементов д.И. Менделеева. Химическая связь и строение соединений. Межмолекулярные взаимодействия.
- •5.1. Теоретические сведения
- •Основные характеристики протона, нейтрона и электрона
- •Корпускулярно-волновые свойства частиц
- •Число подуровней на энергетических уровнях
- •Число орбиталей на энергетических подуровнях
- •Последовательность заполнение атомных орбиталей
- •Электронные формулы элементов
- •Потенциалы (энергии) ионизации i1, эВ
- •Потенциалы (энергии) ионизации i1, эВ элементов V группы
- •Значение энергии (Eср) сродства к электрону для некоторых атомов.
- •Относительная электроотрицательность элементов
- •Свойства веществ в разных агрегатных состояниях
- •Сравнительная характеристика аморфных и кристаллических веществ
- •Свойства кристаллических решеток
- •5.2. Контрольные вопросы и задания
- •5.3. Примеры решения задач
- •План характеристики элемента по положению в Периодической системе д.И. Менделеева
- •5.4. Индивидуальные задания
- •Варианты контрольного задания
- •Исходные данные
- •5.5. Тестовые задания
- •Тема 6. Реакции с переносом электронов. Окислительно-восстановительные равновесия и процессы
- •6.1. Теоретические сведения
- •Характеристика элементов и их соединений в овр
- •Типы овр
- •Составление уравнений окислительно-восстановительных реакций
- •Участие ионов в различных средах
- •Стандартные электродные потенциалы металлов
- •6.2. Контрольные вопросы и задания
- •6.3. Примеры решения задач
- •6.4. Индивидуальные задания
- •Варианты контрольного задания
- •Исходные данные
- •6.5. Тестовые задания
- •Тема 7. Лигандообменные равновесия и процессы. Комплексные соединения
- •Координационные числа ионов - комплексообразователей
- •Основные комплексообразователи в кс
- •Среднее поле
- •Слабое поле
- •Геометрическая структура кс и тип гибридизации
- •Видимый спектр длин волн (нм) и окраска кс при их поглощении
- •Варианты контрольного задания
- •Тема 8. Осмотические свойства растворов. Протолитические равновесия и процессы. Электролитическая ионизация. Степень и константа ионизации
- •Теория электролитической ионизации (диссоциации).
- •Варианты контрольного задания
- •Тема 9. Гетерогенные равновесия и процессы. Произведение растворимости, условия образования и растворения осадков
- •Условия смещения гетерогенного равновесия:
- •Варианты контрольного задания
- •Тема 10. Ионное произведение воды. РН. Гидролиз солей
- •Изменение окраски некоторых индикаторов
- •Примеры буферных растворов.
- •Уравнения Гендерсона – Гассельбаха
- •Варианты контрольного задания
- •Объем учебной дисциплины «Общая и неорганическая химия» и виды учебной работы для студентов очного отделения фармацевтического факультета
- •Календарный план лабораторных занятий по общей и неорганической химии для студентов дневного отделения фармацевтического факультета
- •I семестр (продолжительность - 5 часов)
- •Календарный план лекций по общей и неорганической химии для студентов дневного отделения фармацевтического факультета
- •I семестр (продолжительность - 2 часа)
- •Название важнейших кислот и солей.
- •Значения некоторых фундаментальных физческих постоянных
- •Термодинамические свойства веществ.
- •Стандартные электродные потенциалы (е0) некоторых систем
- •Константы устойчивости комплексных ионов
- •Константы нестойкости некоторых комплексных ионов
- •Константы ионизации кислот и оснований (Ки)
- •Коэффициенты активности (f) ионов при ионных силах раствора
- •Растворимость кислот, оснований и солей в воде
- •Константы растворимости
- •Ответы тестовых заданий
- •Оглавление
Константы устойчивости комплексных ионов

|
Комплексный ион |
|
lg
|
|
Аммиачные | ||
|
Au(NH3)+2 |
11027 |
27 |
|
Ag(NH3)+2 |
1,74107 |
7,24 |
|
Cd(NH3)2+4 |
3,63106 |
6,56 |
|
Co(NH3)2+6 |
2,45104 |
4,39 |
|
Co(NH3)3+6 |
1,991035 |
35,3 |
|
Cu(NH3)+2 |
7,251010 |
10,86 |
|
Cu(NH3)2+4 |
1,071012 |
12,03 |
|
Hg(NH3)2+4 |
1,991019 |
19,3 |
|
Ni(NH3)2+6 |
1,02108 |
8,01 |
|
Zn(NH3)2+4 |
5,01108 |
8,7 |
|
Бромидные | ||
|
AgBr–2 |
2,19107 |
7,34 |
|
AuBr–2 |
2,881012 |
12,46 |
|
BiBr–4 |
6,92107 |
7,84 |
|
CdBr2–4 |
5,01103 |
3,7 |
|
HgBr2–4 |
1,001021 |
21,00 |
|
ZnBr2–4 |
3,1610–3 |
–2,5 |
|
Гидроксидные | ||
|
Ag(OH)–2 |
1,00104 |
4,0 |
|
Al(OH)–4 |
1,001033 |
33,0 |
|
Cd(OH)2–4 |
2,63108 |
8,42 |
|
Cr(OH)–4 |
7,941029 |
29,9 |
|
Cu(OH)2–4 |
3,631014 |
14,56 |
|
Fe(OH)2–4 |
3,63108 |
8,56 |
|
Zn(OH)2–4 |
5,021017 |
17,70 |
|
Иодидные | ||
|
AgJ–2 |
5,51011 |
11,74 |
|
Комплексный ион |
|
lg
|
|
BiJ–4 |
8,911014 |
14,95 |
|
CdJ2–4 |
2,24105 |
5,35 |
|
HgJ2–4 |
6,761029 |
29,83 |
|
PbJ2–4 |
8,32103 |
3,92 |
|
ZnJ2–4 |
3,110–1 |
–0,51 |
|
Нитритные | ||
|
Ag(NO2)–2 |
6,76102 |
2,83 |
|
Тиоцианатные (роданидные) | ||
|
Ag(NCS)–2 |
1,7108 |
8,23 |
|
Co(NCS)2–4 |
5,1210–1 |
–0,309 |
|
Fe(NCS)3–6 |
1,70103 |
3,23 |
|
Fe(NCS)–4 |
3,39104 |
4,53 |
|
Hg(NCS)2–4 |
1,71021 |
21,23 |
|
Тиосульфатные | ||
|
Ag(S2O3)3–2 |
2,881013 |
13,46 |
|
Cu(S2O3)3–2 |
1,861012 |
12,27 |
|
Фторидные | ||
|
AlF3–6 |
4,681020 |
20,67 |
|
FeF3–6 |
1,261016 |
16,10 |
|
Хлоридные | ||
|
AgCl–2 |
1,1105 |
5,04 |
|
AuCl–3 |
2,63109 |
9,42 |
|
AuCl–4 |
2,01021 |
21,30 |
|
BiCl3–6 |
2,63106 |
6,42 |
|
CdCl2–4 |
5,0110 |
1,7 |
|
CuCl–2 |
2,24105 |
5,35 |
|
HgCl2–4 |
1,661015 |
15,22 |
|
SnCl2–4 |
30,2 |
1,48 |
|
SnCl2–6 |
6,61106 |
6,82 |
|
ZnCl2–4 |
10–1 |
–1,0 |
|
Цианидные | ||
|
Ag(CN)–2 |
7,081019 |
19,85 |
|
Au(CN)–2 |
2,01038 |
38,3 |
|
Au(CN)–4 |
1056 |
56 |
|
Комплексный ион |
|
lg
|
|
Cd(CN)2–4 |
1,291017 |
17,11 |
|
Co(CN)4–6 |
1,231019 |
19,09 |
|
Co(CN)3–6 |
11064 |
64 |
|
Cu(CN)–2 |
1,001024 |
24 |
|
Fe(CN)4–6 |
7,941036 |
36,9 |
|
Fe(CN)3–6 |
7,941043 |
43,9 |
|
Hg(CN)2–4 |
9,331038 |
38,97 |
|
Ni(CN)2–4 |
1,01031 |
31,0 |
|
Этилендиаминовые | ||
|
Co(en)3+3 |
4,91048 |
48,69 |
|
Cu(en)2+2 |
1,351020 |
20,13 |
|
Ni(en)2+3 |
1,291019 |
19,11 |
Константы нестойкости некоторых комплексных ионов
|
Схема диссоциации комплексного иона |
Константа нестойкости |
|
[Ag(NH3)2]+ ↔ Ag+ + 2NH3 [Ag(NO2)2]- ↔ Ag+ + 2NO2- [Ag(S2O3)2]3- ↔ Ag+ + 2S2O32- [Ag(CN)2]- ↔ Ag+ + 2CN- [HgCl4]2- ↔ Hg2+ + 4Cl- [HgBr4]2- ↔ Hg2+ + 4Br- [HgI4]2- ↔ Hg2+ + 4I- [Hg(CN)4]2- ↔ Hg2+ + 4CN- [Cd(NH3)4]2+ ↔ Cd2+ + 4NH3 [Cd(CN)4]2- ↔ Cd2+ + 4CN- [Cu(NH3)4]2+ ↔ Cu2+ + 4NH3 [Cu(CN)4]3- ↔ Cu+ + 4CN- [Ni(NH3)6]2+ ↔ Ni2+ + 6NH3 |
9,3 · 10-8 1,8 · 10-3 1,1 · 10-13 1,1 · 10-21 8,5 · 10-16 1,0 · 10-21 1,5 · 10-30 4,0 · 10-42 7,6 · 10-8 7,8 · 10-18 2,1 · 10-13 5,0 · 10-31 1,9 · 10-9 |
ПРИЛОЖЕНИЕ 7