
- •Дисциплина: Инженерная химия
- •2. Технологические критерии эффективности химико-технологических процесса (производительность, интенсивность, степень превращения для различных видов реакций, селективность, выход продукта).
- •3. Принципы составления материальных и тепловых балансов химических реакций.
- •4. Эмпирические методы расчета тепловых эффектов.
- •Рассмотрим, например простую обратимую химическую реакцию:
- •7. Исследование кинетики гомогенных химических реакций. Реакторы периодического действия с постоянным и переменным объемом реакционной массы, реакторы идеального вытеснения.
- •8. Особенности исследования кинетики гомогенных каталитических процессов.
- •9. Кинетика гетерогенно - каталитических процессов.
- •10. Основные стадии и кинетические особенности гетерогенно- каталитических процессов.
- •12. Кинетика гетерофазных химических. Процессов в системах газ-жидкость, жидкость-жидкость (несмешивающиеся). Диффузионная, кинетическая и переходная области гетерофазного процесса.
- •14. Общие положения, понятие о химических реакторах, классификация химических реакторов: периодические, непрерывнодействующие и полупериодические реакторы.
- •15. Общие положения, понятие о химических реакторах, классификация химических реакторов: изотермические, адиабатические и политропные реакторы, реакторы смешения и вытеснения.
- •18. Расчет изотермических реакторов для проведения процессов в системах г-ж, ж-ж(н), аппараты колонного типа, система смеситель-сепаратор, модели смещения фаз в реакторах полупериодического действия.
- •20. Основы расчета реакторов с неидеальным потоком движения реакционной среды, использование ячеечной и диффузионной модели для расчета реальных реакторов.
- •Проектные уравнения реакторов, работающих в политропном режиме
- •Проектные уравнения реакторов, работающих в адиабатическом режиме
- •Проектные уравнения реакторов, работающих в изотермическом режиме
- •Оптимальный температурный режим и способы его осуществления в промышленных реакторах
- •1) Простые необратимые реакции
- •2) Обратимые химические реакции
- •Тепловая устойчивость химических реакторов
3. Принципы составления материальных и тепловых балансов химических реакций.
В основе расчета любого процесса лежит уравнение материального баланса.
Уравнение материального баланса базируется на законе сохранения массы вещества.

I II III
I – сумма всех входящих материальных потоков в элемент ХТС;
II – сумма всех выходящих материальных потоков из элемента ХТС;
III – суммарные материальные потери в элементе ХТС.
Различают теоретический и практический материальные балансы.
Теорерический материальный баланс составляется на заданную производительность с учетом только стехиометрии реакции.
А+В=С+Д
GA+GB=GC+GД
Практический материальный баланс рассчитывают на основе теоретического материального баланса с учетом степени превращения, селективности, выхода, соотношения исходных реагентов, степени чистоты сырья, количество растворителя или инертного газа.
Уравнения практического материального баланса:
1.


2.


3.



4.


5.
 (консекутивная
схема)
(консекутивная
схема)


Отклонения практического от теоретического баланса обусловлены тремя основными факторами:
Термодинамический (реакции не идут до конца вследствие их обратимости);
Кинетический (реакции идут не до конца из-за падения скорости);
Механизмы реакции (обуславливает образование побочных продуктов и как следствие снижает селективность реакции).
Материальный баланс может быть записан в виде уравнения, таблицы или диаграммы.
Тепловой баланс составляется с целью определения теплового режима работы реактора.
Реактор может работать в следующих тепловых режимах:
Изотермический (температура на входе в реактор и на выходе одинакова);
Адиабатический (отсутствует теплообмен с окружающей средой);
Смешанный или политропный тепловой режим.
В основе теплового баланса лежит закон сохранения энергии, согласно которому
åQприх. = åQрасх. +åQпот
åQприх – характеризует сумму всех входящих тепловых потоков;
åQрасх – сумма всех выходящих тепловых потоков;
±åQпот – суммарные тепловые потери.
Для изотермического режима уравнение теплового баланса:
Qреаг ± Qr. ± Qф ± QF = Qпрод,+ Qнагр. + Qпот.
где Qреаг – количество тепла, поступающего с исходными реагентами;
Qr – тепло химических реакций;
Qф – тепло фазовых переходов;
Qнагр – количество тепла, необходимое для нагрева сырья до температуры реакции.
Qпот не должно превышать 5%.
В отличие от материального баланса, тепловой баланс не всегда сходится.
Приход тепла:
Qреаг – тепло, входящее в реактор с исходными реагентами;
Qреаг=∑ Qi
Qреаг, i = Gi×Cpi×Ti
где Gi – мольный поток i-го реагента;
Cpi – теплоемкость i-го реагента, (Дж·моль)/К;
 -
тепло, выделяющееся (или поглощающееся)
в результате химических превращений:
-
тепло, выделяющееся (или поглощающееся)
в результате химических превращений:
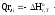 Gi(j)
Gi(j)
где
 -
тепловой эффект химической реакции,
(Дж·моль)/К;
-
тепловой эффект химической реакции,
(Дж·моль)/К;
Gi(j) – мольный поток i-го реагента, участвующего в реакции (или полученного j-го продукта реакции);
 -
тепло, выделяющееся (или поглощающееся)
в результате фазовых превращений
(испарение, конденсация, кристаллизация,
плавление, возгонка, растворение):
-
тепло, выделяющееся (или поглощающееся)
в результате фазовых превращений
(испарение, конденсация, кристаллизация,
плавление, возгонка, растворение):
 Gi(j)ф
Gi(j)ф
где Gi(j)ф – мольный поток i-го реагента (j-го продукта), претерпевающегося фазовый переход;
 -
энтальпия фазового перехода, кДж/моль
(справочная величина).
-
энтальпия фазового перехода, кДж/моль
(справочная величина).
Расход тепла:
Qпрод – тепло, выходящее из реактора с продуктами реакции;
Qпрод
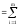 Qпрод,
j
Qпрод,
j
Qпрод, j = Gj×Cpj×Tj
где Gj – мольный поток j-го продукта реакции;
Cpj – теплоемкость j-го продукта реакции, Дж/(моль·К);
Tj – температура j-го продукта реакции, К.
Qнагр – количество тепла, расходуемое на нагревание исходных реагентов до температуры реакции:
Qнагр,i = ∑[Gi×Cpi× (Ti,r – Ti)]
где Gi – мольный поток i - реагента, подвергаемый нагреву;
Cpi – теплоемкость i- реагента, Дж/(моль·К);
Ti – температура i- реагента на входе в реактор;
Ti,r – температура i- реагента на выходе из реактора.
Qпот – тепловые потери (1 – 5% от прихода тепла);
Qпот = (0,01– 0,05)∙Qприх ,
±QF – количество тепла, отводимое (подводимое) от реактора при помощи теплоносителя (хладоагента). Тепловая нагрузка на реактор.
Исходя из тепловой нагрузки на реактор, рассчитывают необходимую поверхность теплообмена F.
QF рассчитывают по уравнению:
±QF = Qрасх. - Qприх
 ,
м2
,
,
м2
,
где Кt – коэффициент теплопередачи; ∆Т – движущая сила теплопередачи (разность между температурой реакции и температурой теплоносителя).
После нахождения поверхности теплообмена F осуществляют ее анализ, сравнивая с поверхностью теплообмена, имеющемся у реактора.
F<Fr (поверхность реактора) – справочная величина;
F>Fr – интенсифицируют процесс теплообмена (изменяют К и ∆T) или вводят дополнительные теплообменные устройства.
F≈Fr – неустойчивый тепловой режим, но интенсифицировать его проще.
Тепловой баланс записывается в виде уравнения, диаграммы или таблицы.
