
- •Дисциплина: Инженерная химия
- •2. Технологические критерии эффективности химико-технологических процесса (производительность, интенсивность, степень превращения для различных видов реакций, селективность, выход продукта).
- •3. Принципы составления материальных и тепловых балансов химических реакций.
- •4. Эмпирические методы расчета тепловых эффектов.
- •Рассмотрим, например простую обратимую химическую реакцию:
- •7. Исследование кинетики гомогенных химических реакций. Реакторы периодического действия с постоянным и переменным объемом реакционной массы, реакторы идеального вытеснения.
- •8. Особенности исследования кинетики гомогенных каталитических процессов.
- •9. Кинетика гетерогенно - каталитических процессов.
- •10. Основные стадии и кинетические особенности гетерогенно- каталитических процессов.
- •12. Кинетика гетерофазных химических. Процессов в системах газ-жидкость, жидкость-жидкость (несмешивающиеся). Диффузионная, кинетическая и переходная области гетерофазного процесса.
- •14. Общие положения, понятие о химических реакторах, классификация химических реакторов: периодические, непрерывнодействующие и полупериодические реакторы.
- •15. Общие положения, понятие о химических реакторах, классификация химических реакторов: изотермические, адиабатические и политропные реакторы, реакторы смешения и вытеснения.
- •18. Расчет изотермических реакторов для проведения процессов в системах г-ж, ж-ж(н), аппараты колонного типа, система смеситель-сепаратор, модели смещения фаз в реакторах полупериодического действия.
- •20. Основы расчета реакторов с неидеальным потоком движения реакционной среды, использование ячеечной и диффузионной модели для расчета реальных реакторов.
- •Проектные уравнения реакторов, работающих в политропном режиме
- •Проектные уравнения реакторов, работающих в адиабатическом режиме
- •Проектные уравнения реакторов, работающих в изотермическом режиме
- •Оптимальный температурный режим и способы его осуществления в промышленных реакторах
- •1) Простые необратимые реакции
- •2) Обратимые химические реакции
- •Тепловая устойчивость химических реакторов
Проектные уравнения реакторов, работающих в политропном режиме
1) РИС-П-П
Для этого реактора конвективный перенос отсутствует, т. е. части II=0 и III=0
 (1)
(1)
 -
скорость химической реакции. Для РИС-П-П:
-
скорость химической реакции. Для РИС-П-П:
 (2)
(2)
Подставив (2) в (1) и проведя сокращения, получаем:

Умножим левую и правую части на объем реакционной смеси, получим окончательное выражение для теплового баланса РИС-П-П:

 -общая
поверхность тепообмена.
-общая
поверхность тепообмена.
2) РИВ
В РИВ изменение температуры происходит в одном направлении – по длине реактора.
Изменение температуры за счет молекулярной теплопроводности мало и его можно не учитывать (III=0).
С учетом этого общее уравнение теплового баланса для РИВ при стационарном режиме, когда накопление в реакторе тепла =0 :
 (3)
(3)
Скорость
химического процесса в РИВ может быть
выражена тем же уравнением, что и в
случае РИС-П ( ),
а линейная скорость и движение теплового
потока:
),
а линейная скорость и движение теплового
потока:
 (4).
(4).
Подставим (4) в (3) и, сокращая, получим:

 -
на единицу длины реактора.
-
на единицу длины реактора.
3) РИС-Н
Для РИС-Н можно считать, что отсутствует градиент параметров, как во ремени, так и в объеме, поэтому уравнение теплового баланса составляют в целом для реактора.
При стационарном режиме работы запишем уравнение теплового баланса:




Исходя из полученных общих уравнений, Отражающих политропный режим можно найти проектные уравнения для адиабатического и изотермического режимов.
Проектные уравнения реакторов, работающих в адиабатическом режиме
Реактор, работающий в адиабатическом режиме представляет собой аппарат, стенки которого изолированы от окружающей среды.
Т. к. при адиабатическом режиме отвод тепла отсутствует, то V=0
1) РИС-П
 (5)
(5)
Если
принять, что значения ΔHr,
Cp
– постоянные, то после интегрирования
уравнения (5):

или
 (6)
(6)
T – температура на выходе, T0 – температура на входе в реактор.
 .
.
При проведении реакции до конца, т. е. xi=1 из уравнения (6) получим уравнение:
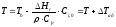
T
– температура реакционной массы в
адиабатическом процессе;
 -
адиабатическое изменение температуры.
-
адиабатическое изменение температуры.
2) В проточных реакторах вытеснения и смещения также отсутствует теплообмен, поэтому для проточного вытеснения РИВ получаем:
 (7)
(7)
Если
принять, что
 и
и не зависят от температуры, то из (7)
следует:
не зависят от температуры, то из (7)
следует:
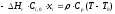
3) Для проточного реактора смешения РИС-Н:

Таким
образом, для всех реакторов при
адиабатическом режиме и постоянных
значениях
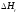 и
и тепловой баланс выражается в виде
одинаковых уравнений.
тепловой баланс выражается в виде
одинаковых уравнений.
Проектные уравнения реакторов, работающих в изотермическом режиме
Химические процессы при постоянных температурах можно провести в непрерывно действующих реакторах, т. е. для РИС-П такой режим невозможен, а возможен только для РИС или РИС-Н.
Для
них можно принять, что


1) С учетом этих замечаний получим для РИВ обобщенное уравнение:

2) Для проточного реактора смешения РИС-Н можно записать, что

Оптимальный температурный режим и способы его осуществления в промышленных реакторах
Температурный режим проведения химического процесса, обеспечивающий экономически целесообразную максимальную производительность едины объема реактора по целевому продукту называется оптимальным.
Подход к разработке оптимального температурного режима может быть различным, в зависимости от типа химической реакции. Рассмотрим влияние кинетического уравнения на выбор температурного режима:
