
Билет № 4
1.Опишите химическое строение, физико-химические свойства, классификацию и биологическую роль жирных кислот.
Ответ-Жирные кислоты (ЖК) – это монокарбоновые кислоты с одной алифатической цепью, т.е. состоящие из одной карбоксильной группы и длинного неполярного хвоста. Жирные кислоты природных липидов, как правило, содержат четное количество атомов углерода.Жирные кислоты подразделяются на предельные (или насыщенные) и непредельные (ненасыщенные). Предельные кислоты не содержат двойных связей. Непредельные кислоты содержат одну (мононенасыщенные) или несколько (полиненасыщенные) двойных связей:
СН3(СН2)nСН=СН(СН2)nСООН – мононенасыщенные;
СН3(СН2)n(СН=СНСН2)m(СН2)kСООН – полиненасыщенные
Двойные связи в природных полиненасыщенных жирных кислотах изолированные (несопряженные). Как правило, связи имеют цис-конфигурацию, что придает таким молекулам дополнительную жесткость.Это имеет биологический смысл, т.к. такие молекулы входят в состав клеточных мембран.Приведем их классификацию.Из ненасыщенных ЖК чаще всего встречаются пальмитиновая и стеариновая.
С16:0 – сокращенное обозначение пальмитиновой кислоты – означает,что у нее 16 атомов углерода и нет двойных связей.СН3(СН2)14СООН – другое обозначение пальмитиновой кислоты С18:0 – стеариновая, СН3(СН2)16СООН
Кроме того, выделяются следующие насыщенные жирные кислоты:
С12:0 – лауриновая;
С14:0 – миристиновая;
С20:0 – арахиновая;
С22:0 – бегеновая;
С24:0 – лигноцериновая.
Моноеновые:
С 16 : 1 – пальмитоолеиновая
СН3(СН2)5СН=СН(СН2)7СООН;
С18:1 – олеиновая
СН3(СН2)7СН=СН(СН2)7СООН.
Положение двойной связи относительно карбоксильной группы обозначают знаком Δ9, где число показывает порядковый номер атома углерода,возле которого находится двойная связь. Таким образом, названные кислоты могуть быть обозначены соответственно С16:1, Δ9 и С18:1, Δ9. Полиеновые кислоты чаще всего бывают с двумя и тремя двойными связями:
С18:2, Δ9 – линолевая, СН3(СН2)4(СН=СНСН2)2(СН2)6СООН;
С18:3, Δ9 – линоленовая, СН3СН2(СН=СНСН2)3(СН2)6СООН.
Иногда встречаются жирные кислоты (т.н. необычные), в алифатических цепях которых есть заместители: СН3-, -ОН, С=О и др.:
СН3
СН3(СН2)7-СН-(СН2)8СООН – туберкулостеариновая, С19:0, из туберку-
лезных палочек
С Н2
СН3(СН2)5-СН - СН(СН2)9СООН – лактобацилловая С19:0.
Жирные кислоты нерастворимы в воде, температура плавления понижается с увеличением числа двойных связей и укорочением цепи.Такие жирные кислоты, как линолевая, линоленовая и им подобные (с двумя и тремя двойными связями), не синтезируются внутри организма человека и называются незаменимыми. Поэтому их необходимо получать с пищей.При этом полиеновые кислоты делят на две группы: ω-3 и ω-6 (в зависимости от положения двойной связи от углеродного атома последней, метильной группы). Эти кислоты являются предшественниками разных групп гормонов местного действия – эйкозаноидов. Так, линолевая кислота является примером ω-6 кислот. В качестве примера ω-3 кислот можно привести тимнодоновую (эйкозапентановую) кислоту, С20:5 (ω-3). Она содержится в жире морских рыб, хотя имеет растительное происхождение, синтезируется фитопланктоном. Кроме того, такие рыбы как лосось, макрель, сельдь, сардина и др., поедая планктон, накапливают эту кислоту в своем жире. При употреблении человеком в пищу этой кислоты у него понижается свертываемость крови, что используется для профилактики сердечно-сосудистых заболеваний.
2.Объясните значение образование кетоновых тел для метаболизма клеток. Опишите реакции окисления ацетоацетата до CO2 и H2O, подсчитайте баланс энергии(количество АТФ).
Ответ-Кетоновые тела ворастворимые соединения, поэтому легко транспортируются через внутреннюю мембрану митохондрий, также как и через гемато-энцефалический барьер и клеточные мембраны. В связи с этим они могут использоваться в качестве источника энергии различными тканями,включая ЦНС (рис. 6.).
• D-β-гидроксибутират окисляется до ацетоацетата при участии
NAD+-зависимой β-гидроксибутиратдегидрогеназы, при этом продуцируется
молекула NADH (1).
• Следующая стадия присоединение HSCoA. Синтез ацетоацетил-
СоА происходит путем реакции ацил-тиоэфирного обмена с участием сукци-
нил-СоА ферментом СоА-трансферазой (2). Сукцинил-СоА интермедиат
цикла лимонной кислоты.
• При участии тиолазы (3) и еще одной молекулы HSСоА ацетоаце-
тил-СоА расщепляется на 2 молекулы ацетил-СоА.

Рис.6. Кетоновые тела клеточное топливо
Кетоновые тела являются предпочтительными субстратами для аэробных мышц и сердца, чем глюкоза, когда они доступны. В периферических тканях кетоновые тела должны вновь превратиться в ацетил-СоА в митохондриях.
Реакцию катализирует сукцинил-КоА-аце-тоацетат-КоА-трансфераза. Этот фермент не синтезируется в печени, поэтому печень не использует кетоновые тела как источники энергии, а производит их «на экспорт». Кетоновые тела – хорошие топливные молекулы; окисление одной молекулы β-гидроксибутирата до СО2 и Н2О обеспечивает синтез 27 молекул АТФ. Эквивалент одной макроэргической связи АТФ (в молекуле сукцинил-КоА) используется на активацию ацетоацетата, поэтому суммарный выход АТФ при окислении одной молекулы β-гидроксибутирата - 26 молекул.
3.Поясните схемы биосинтеза фосфатидилхолина двумя возможными способами(экстренным и de novo). В чем отличия этих путей?Что такое липотропные факторы?
Ответ-
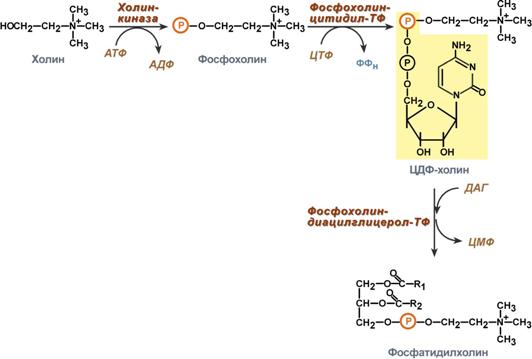
Другой путь синтеза фосфатидилхолина получил название «спасательного» (salvage) пути, поскольку холин, образовавшийся при распаде фосфатидилхолина в процессе метаболизма, как бы спасается от разрушения и вновь используется в готовом виде для построения фосфатидилхолина. Этот путь очень похож на путь синтеза фосфатидилэтаноламина На первом этапе синтеза свободный холин активируется при помощи АТР под действием холинкиназы с образованием фосфохолина:
Фосфохолин реагирует затем с СТР, образуя цитидиндифосфатхолин:
CDP-холин взаимодействует с 1,2-диацилглицеролом, в результате чего образуется фосфатидилхолин:
Спасательный» путь синтеза фосфатидилхолина необходим многим животным, так как их способность синтезировать это соединение de novo ограниченна. Это обусловлено тем, что метальные группы в форме S-аденозилметионина. необходимые для такого синтеза, образуются из незаменимой аминокислоты метионина. При недостаточном содержавши метионина в пище возможность метилирования фосфатидилэтаноламина и других акцепторов метальных групп становится ограниченной. В этих условиях организм старается «спасти» и повторно использовать
уже метилированный свободный холин. Фактически при недостатке метионина в рационе животных его можно хотя бы частично компенсировать за счет содержащегося в пище холина.
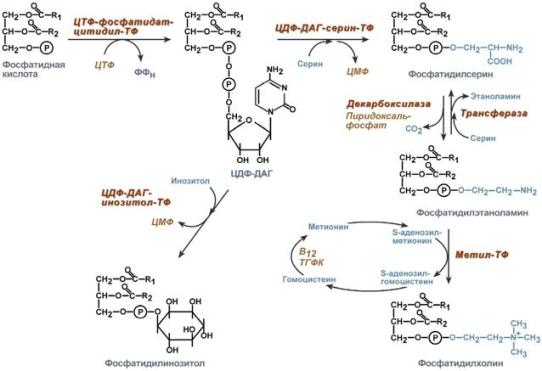
При синтезе de novo холиновая голова молекулы фосфатидилхолина не встраивается в молекулу в готовом виде, а образуется из этаноламина, входящего в состав фосфатидилэтаноламина, путем трехкратного метилирования. Донором метальных групп служит S-аденозилметионин - активированная форма метионина, в которой метальная группа обладает повышенной реакционной способностью.
Липотро́пные вещества́ являются важными факторами, способствующими нормализации обмена липидов и холестерина в организме, стимулируют мобилизации жира из печени и его окисление, что ведёт к уменьшению степени выраженности жировой инфильтрации печени. По анатомо-терапевтическо-химической классификации относятся к группе A05 — препараты для лечения заболеваний печени и желчевыводящих путей, поэтому их можно считать гепатопротекторами. В настоящее время современной фармацевтической индустрией синтезируются препараты, обладающие липотропным эффектом.
Липотропное действие оказывают (карнитин,холин,метионин,инозит,лецитин,тиоктовая кислота,бетаин)
4.Объясните взаимосвязь обмена углеводов и липидов(какие метаболиты углеводного обмена и как используются для биосинтеза липидов)?
Ответ- Биосинтез липидов из углеводов. L-Глицерофосфат, необходимый для биосинтеза ТГ (нейтральных жиров) и ФЛ (фосфатидов) образуется при восстановлении диоксиацетонфосфата (ДГАФ), который является продуктом расщепления фруктозо-1,6-бисфосфата в процессе фруктозобисфосфат-альдолазной реакции. Биосинтез высокомолекулярных карбоновых (жирных) кислот происходит из ацетил-СоА, который может образовываться в результате окислительного декарбоксилирования пирувата под действием пируватдегидрогеназного комплекса. Пируват является центральным промежуточным продуктом обмена углеводов.
Транспорт ацетил-СоА из митохондрий в цитоапазму тесно связан с обменом углеводов. Перенос ацетил-СоА из митохондрий в цитоплазму происходит в основном в виде цитрата. Цитрат, как известно, образуется в реакции конденсации ацетил-СоА с оксалоацетатом (ОАА), катализируемой цитратсинтазой. Оксалоацетат представляет собой продукт карбоксилирования пирувата.
Кроме того, окислительный пентозофосфатный путь метаболизма углеводов является одним из источников восстановительных эквивалентов при биосинтезе кислот. Так, например, для синтеза пальмитата требуется 14 молекул NAДФH, шесть из которых поставляет окислительный пентозофосфатный путь метаболизма углеводов. а восемь молекул NADPH образуется в процессе переноса 8 молекул ацетил-СоА в цитоплазму с участием пирувата и мататлегидрогеназной системы, перенос атомов водорода из разных субстратов сопровождается образованием кетокистот (предшественников глюконеогенеза) без участия атмосферного кислорода. кетокистоты в процессе карбоксилирования выделяют С02. Таким образом, образование и выделение С02 при биосинтезе жиров из углеводов происходит при меньших количествах 02,, потому что водород восстановленных коферментов идет не в дыхательную цепь, а на восстановительные биосинтетические процессы.
Биосинтез углеводов из жиров в организме животных ограничен, т. к. у них нет ферментов, способных превращать жирные кислоты в метаболиты глюконеогенеза, и только глицерол, как компонент жиров, может использоваться для биосинтеза углеводов. Растения и некоторые бактерии, благодаря наличию глиоксилатного цикла, способны использовать ацетил-СоА для биосинтеза углеводов. В результате одного оборота глиоксилатного цикла образуется две молекулы оксалоацетата, одна из которых поддерживает цикличность процесса, а вторая может быть субстратом глюконеогенеза.
5.Определение содержание бета-липопротеинов в плазме крови: принцип метода, диагностическое значение.
Ответ-Диагностическое значение: в сыворотке крови практически здоровых лиц содержание бета-липопротеидов колеблется в пределах 3,0-4,5 г/л. С повышением в плазме крови содержания пре-бета-ЛП и бета-ЛП (гиперлипопротеинемия) и изменением соотношения отдельных классов ЛП(понижением альфа-ЛП), т.е. дислипопротеинемией, в настоящее время связывают развитие атеросклероза и ИБС.
Принцип метода- определения бета-липопротеидов основан на их способности в присутствии полиэлектролитов и гепарина объединяться в комплексы, которые повышают мутность исследуемого раствора. Степень мутности раствора прямо пропорциональна концентрации бета-липопротеидов в сыворотке крови и измеряется на фэке.
6. Тесты NN: 192,201,219,228. Ситуационные задачи NN: 89,99,105
