
Руководство по факультетской терапии (Болдуева)
.pdf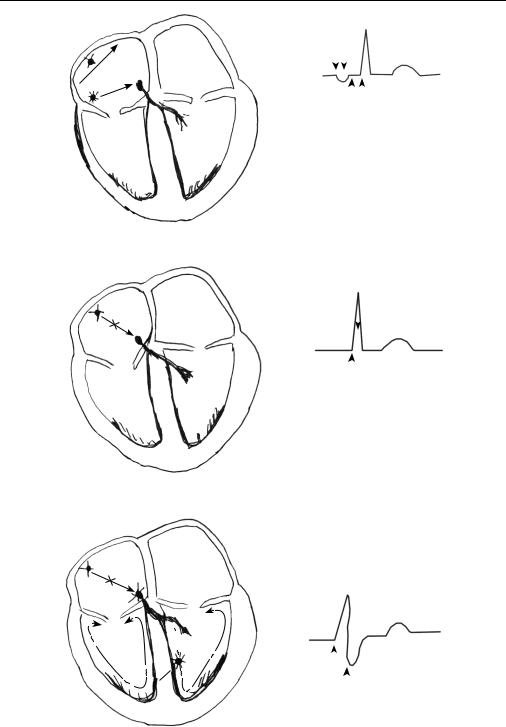
101
|
|
|
|
|
|
|
QRS |
|
|
|
1 2 |
|
T |
||||
|
2 |
3 |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
||
1 |
|
|
P |
|
|
|||
|
|
|
|
|||||
|
|
3 4 |
||||||
4
4
Рис. 5.6, а. Ретроградное распространение импульса
|
4 |
||
|
|
|
QRS |
1, 2, 3 |
|
|
T |
|
|
||
|
|
||
|
|
|
|
|
1, 2, 3 |
||
44
Рис. 5.6, б. Антероградное распространение импульса
QRS
T
 1, 2, 3
1, 2, 3
4 |
|
|
|
1, 2, 3 |
|||
|
|||
|
|
||
|
4 |
||
Рис. 5.6, в. Ретроградное распространение импульса

102
(1, 2, 3) по ножкам пучка Гиса обычным образом — антероградно. Комплекс QRS
(4) обычного вида и ширины.
На рис. 5.6, в изображено ретроградное распространение импульса, возникшего в водителе ритма 3-го порядка (ножки пучка Гиса) в ситуации, когда блокированы СА- и АВ-узлы. Зубец Р отсутствует, так как нет возбуждения предсердий (1, 2, 3). Импульс распространяется по желудочкам «снизу вверх» — ретроградно, поэтому комплекс QRS (4) широкий, деформированный.
Механизмы развития аритмий:
–аритмии вследствие нарушения образования импульса:
•повышенный автоматизм;
•триггерная активность;
–аритмии вследствие нарушения проведения импульса:
•механизм re-entry;
–аритмии вследствие комбинированного нарушения образования и проведения импульса.
Повышенный автоматизм:
–возможно повышение/понижение автоматизма синусового узла под влиянием вегетативной нервной системы (физиологические реакции, воздействие лекарственных препаратов);
–автоматизм латентных водителей ритма:
•замещающий (выскальзывающий) ритм — защитная функция, предотвращающая асистолию сердца. Он появляется тогда, когда снижается импульсация основного (СА) водителя ритма. Частота сердечных сокращений зависит от частоты импульсов, возникающих в этих очагах. В зависимости от уровня поражения частота импульсов равна (но не выше) или ниже, чем частота СА-ритма;
•повышение автоматизма латентных водителей ритма проводящей системы происходит в том случае, когда вследствие каких-либо причин (симпатическая стимуляция, ишемия, гипоксия, отек, электролитные нарушения) скорость их деполяризации выше скорости деполяризации клеток синусового узла. Появляется эктопический импульс — преждевременное возникновение электрического импульса (т. е. раньше, чем должно быть при нормальном ритме сердечных сокращений). Последовательность эктопических импульсов называется эктопическим ритмом, его частота обычно выше синусового;
•при поражении миокарда некоторые кардиомиоциты, не принадлежащие к проводящей системе сердца, могут приобретать патологическую
способность к автоматизму и спонтанной деполяризации, возникают патологические очаги автоматизма.
Триггерная активность
В некоторых случаях нормальный потенциал действия может вызывать некоторые дополнительные деполяризации (постдеполяризации), которые могут быть ранними и поздними.
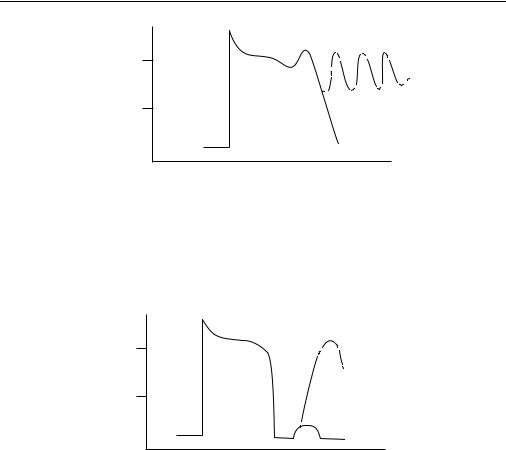
Ранние постдеполяризации — это быстрые колебания мембранного потенциала в сторону положительных значений во время фазы реполяризации (рис. 5.7). Они чаще всего возникают при состояниях, сопровождающихся увеличением потенциала действия — удлинения QT, снижения внутриклеточной концентрации калия.
103
Мембранный потенциал, мВ
0
–50
–100
ПД
Ранняя постдеполяризация
Рис. 5.7. Схематическое изображение ранней постдеполяризации
Поздние постдеполяризации — возникают вскоре после завершения фазы реполяризаци (рис. 5.8) и чаще их причиной служит повышение концентрации внутриклеточного кальция (например, дигиталисная интоксикация), воздействие катехоламинов, ишемия миокарда.
Мембранный потенциал, мВ
0
–50
–100
ПД
Поздняя постдеполяризация
Рис. 5.8. Схематическое изображение поздней постдеполяризации
Механизм re-entry
Повторный вход волны возбуждения (re-entry) лежит в основе большинства тахиаритмий. Происходит циркуляция электрического тока в участке миокарда, приводящая к периодической деполяризации мембраны кардиомиоцитов.
Внорме импульсы из синусового узла строго упорядоченно распространяются по миокарду, после чего затухают. Каждый участок проводящей системы деполяризуется под действием одного импульса только один раз (из-за обсуждавшейся выше рефрактерности). Для существования же петли re-entry необходимо несколько условий:
Первое условие — наличие двух каналов проведения импульса (дихотомическое деление на два функциональных пути) с общим началом и концом.
Внорме (рис. 5.9, а) импульс достигает точки 1, откуда параллельно следует по путям а) и б) в нижележащие отделы, где затухает; поскольку скорость проведения и рефрактерность обоих путей одинаковая, если две волны возбуждения
встречаются, то они гасят друг друга (x).

104
импульс
а) 1 б)
x
а — норма |
Рис. 5.9, а. Механизм re-entry |
Второе условие — однонаправленный блок (блокада проведения импульса по одному из путей в антероградном направлении — «сверху вниз»).
В этом случае (рис. 5.9, б) антероградное проведение возможно только по одному пути (путь а)). Распространяясь дистально, импульс достигает конечной части пути — (у). Здесь импульс может распространиться дальше дистально, а также вернуться по пути б) «снизу вверх» — ретроградно. Сохранение ретроградного проведения импульса — это важная часть данного условия.
1 а) б)
y
б — однонаправленный блок |
Рис. 5.9, б. Механизм re-entry |
Третье условие — замедление скорости проведения импульса.
Если импульс, распространяющийся ретроградно с обычной скоростью по пути б), достигнет точки 1, а путь а) будет находиться в периоде рефрактерности, то импульс здесь затухнет (рис. 5.10, а). Если же импульс по пути б) будет распространяться медленнее, чем в норме, то путь а) успеет выйти из состояния рефрактерности (рис. 5.10, б). Таким образом, импульс, идущий ретроградно по
1 |
б) |
|
1 |
а) |
|
||
|
|
а) |
б) |
|
y |
|
y |
|
|
|
|
а — нормальная скорость ретроградно- |
б — замедление ретроградного проведения |
||
го проведения импульса |
|
импульса |
|
Рис. 5.10. Механизм re-entry

105
пути б), дойдет до точки 1, а затем попадет в путь а) — «петля» замкнулась — начинается круговое движение импульса, которое активирует другие части проводящей системы.
Образование «петли» re-entry возможно в любом месте миокарда, т. е. там, где возникают условия его образования. Это случается вследствие ишемии миокарда, воспаления, образования соединительной ткани (кардиосклероз), когда формируется «негомогенность проведения импульса». Чем тяжелее морфологические изменения миокарда, тем чаще и дольше функционирует механизм повторного входа, вызывая жизнеопасные аритмии. Иногда механизм повторного входа возникает в проводящей системе без морфологических изменений миокарда (врожденные, идиопатические изменения в проводящей системе сердца). Данный вид аритмии обычно прогностически более благоприятный.
Взависимости от размеров петли повторного входа различают macro-re-entry
иmicro-re-entry. Формирование macro-re-entry, в частности, лежит в основе возникновения трепетания предсердий. При формировании петли micro-re-entry движение импульса происходит по малому замкнутому кольцу, не связанному с каким-либо анатомическим препятствием. Формирование множества петель micro-re-entry в предсердиях или желудочках ведет к возникновению фибрилляции предсердий или желудочков. В этих случаях передние фронты циркулирующих волн возбуждения постоянно наталкиваются на ограниченные участки невозбудимой ткани, находящейся в рефрактерном периоде. В связи с этим волны micro-re- entry постоянно меняют свое направление, возникают завихрения и хаотическое случайное возбуждение отдельных участков предсердий или желудочков.
Этиология аритмий
1. Заболевания сердца (врожденные и приобретенные), приводящие к поражению клеточных мембран кардиомиоцитов: ишемическая болезнь сердца, артериальная гипертензия, миокардиты, кардиомиопатии, пороки сердца и др.
2. Нарушения регуляции сердечно-сосудистой системы (симпатические
ипарасимпатические влияния).
3.Нарушения кислотно-основного и электролитного равновесия; гормональные нарушения.
4.Физические и химические воздействия: кофеин, никотин, алкоголь, лекарственные вещества (проаритмогенное действие антиаритмических средств, сердечные гликозиды, симпатомиметики, холинолитики и др.).
5.Врожденные (в том числе наследственные) нарушения проводящей системы.
Нарушения ритма и проводимости более неблагоприятны для прогноза у лиц
с органическим поражением сердца, в то время как аритмии, обусловленные нарушением регуляции сердечно-сосудистой системы, обычно более благоприятны.
Определения
Брадикардия — снижение частоты ритма сердечных сокращений менее 60 уд./мин, возникающее в результате нарушения образования и проведения импульса возбуждения.
Брадикардия может возникать у совершенно здоровых людей, например синусовая брадикардия у спортсменов. Также синусовая брадикардия может

106
наблюдаться при активации парасимпатической нервной системы, воздействии лекарственных препаратов, нарушении гормонального, электролитного баланса. В норме ночью происходит урежение ЧСС, поэтому нужно оценивать циркадные колебания ЧСС в течение суток. Патологическое уменьшение ЧСС ночью с эпизодами асистолии в несколько секунд может определяться у лиц с синдромом обструктивного апноэ сна (sleep-apnoe). Возникновение синусовой брадикардии у пожилых лиц, у которых ранее наблюдалась нормальная ЧСС, может свидетельствовать о дисфункции синусового узла.
Брадикардия может возникать при нарушении/прекращении проведения импульса на любом уровне, тогда частота сердечных сокращений будет определяться частотой работы водителей ритма более низкого порядка (АВ-соединение, ножки пучка Гиса и т. д.).
Тахикардия диагностируется в том случае, когда частота трех или более последовательных сокращений сердца превышает 90 уд./мин. Тахикардия также может быть физиологической (при физической, эмоциональной нагрузке)
ипатологической. Тахикардия у здоровых людей может быть свидетельством детренированности — неадекватное увеличение ЧСС в ответ на небольшую физическую нагрузку. Синусовая тахикардия возникает при увеличении активности симпатической нервной системы любого генеза, воздействии лекарственных препаратов, электролитном дисбалансе, эндокринной патологии, анемии, лихорадке, периферической вазодилатации. Источником несинусовой тахикардии может служить любой эктопический очаг предсердий
ижелудочков.
Прежде чем разбирать конкретные нозологии, необходимо обсудить понятия о регулярности сердечных сокращений и о синусовом ритме.
Регулярность сердечных сокращений оценивается при сравнении продолжительности интервалов R–R между последовательно зарегистрированными сердечными циклами. Регулярный, или правильный, ритм сердца определяется тогда, когда продолжительность измеренных интервалов R–R одинакова и разброс полученных величин не превышает ±10% от средней продолжительности интервалов R–R. В остальных случаях диагностируется неправильный (нерегулярный) сердечный ритм.
ЧСС правильного ритма определяется по формуле
ЧСС = 60 / R–R (с).
При неправильном ритме подсчитывают число комплексов QRS, зарегистрированных за какой-то определенный отрезок времени (например, за 3 с). Умножая этот результат в данном случае на 20 (60 с/3 с = 20), подсчитывают ЧСС.
Ритм синусовый, если:
–за каждым зубцом Р следует комплекс QRS
–каждому комплексу QRS предшествует зубец Р
–зубец Р направлен вверх (положительный) в отведениях I, II, III
Если зубец Р присутствует на ЭКГ, но не соблюдаются все указанные правила, это означает, что возбуждение предсердий происходит, но источником импульса в данном случае является не синусовый узел.

107
ФИБРИЛЛЯЦИЯ И ТРЕПЕТАНИЕ ПРЕДСЕРДИЙ
Фибрилляция предсердий (ФП) (мерцательная аритмия — в отечественной литературе) — хаотические, нерегулярные возбуждения отдельных групп предсердных мышечных волокон с частотой 400–700 импульсов в минуту с утратой механической систолы предсердий и нерегулярными возбуждениями и сокращениями желудочков.
Трепетание предсердий (ТП) — наджелудочковая тахикардия, характеризующаяся организованным возбуждением и сокращениями предсердий с частотой 250–400 импульсов в минуту с регулярным или нерегулярным (после задержки в АВ-узле) проведением импульсов к желудочкам.
Распространенность ФП в общей популяции составляет ~2%, в возрасте старше 80 лет — до 15%. В Европе ФП страдают около 6 млн человек; прогнозируется, что в связи со старением населения в ближайшие 50 лет частота ее возникновения удвоится. ФП увеличивает риск развития инсульта в 5 раз и обусловливает возникновение каждого 5-го инсульта, риск смерти при наличии ФП увеличивается вдвое. ФП является одной из самых частых причин сердечной недостаточности.
Этиология
1.Органическое поражение миокарда.
2.Идиопатические (врожденные) формы ФП.
Органическое поражение миокарда. Считается, что одной из основных причин ФП является ремоделирование (изменение структуры и геометрии) левого предсердия. Ремоделирование/дилатация левого предсердия происходит при различных заболеваниях:
–артериальная гипертензия (вследствие диастолической дисфункции левого желудочка — см. главу «Сердечная недостаточность»). В настоящее время артериальная гипертензия рассматривается как один из основных этиологических факторов ФП;
–ишемическая болезнь сердца: хроническая ишемия миокарда и постинфарктное ремоделирование; острая ишемия при инфаркте миокарда;
–митральные пороки сердца любого генеза (ревматический митральный стеноз, являвшийся основной причиной ФП в середине прошлого века, в настоящее время уступает свое место другим порокам);
–аортальные пороки в фазу «митрализации» порока;
–различные врожденные пороки сердца (чаще дефект межпредсердной перегородки);
–различные кардиомиопатии, в том числе «спортивное сердце»;
–миокардиты;
–синдром обструктивного апноэ сна;
–ожирение и сахарный диабет;
–бронхолегочная патология;
–заболевания перикарда;
–перенесенные операции на сердце;

108
–электролитный дисбаланс;
–гормональные воздействия (тиреотоксикоз);
–алкогольная и иная острая интоксикация;
–лекарственные препараты (симпатомиметики/холинолитики и др.).
«Идиопатическая фибрилляция предсердий» (фокусная) (ФП), развивающаяся
вмолодом возрасте, может быть частично объяснена наследственной предрасположенностью. Более подробно эта форма будет обсуждена ниже.
Впоследние годы были выделены определенные геномные мутации, связанные с риском возникновения ФП.
Необходимо помнить, что возраст сам по себе при отсутствии исходного заболевания сердца может служить фактором риска ФП, так как с возрастом
впредсердиях происходит разрастание соединительной ткани, фиброз, что создает предпосылки к формированию и поддержанию механизмов ФП, которые будут описаны далее.
Трепетание предсердий (ТП) возникает при тех же патологических состояниях, что и ФП. Однако причиной этого нарушения ритма сердца несколько чаще
бывают заболевания, характеризующиеся перегрузкой правого предсердия, в том числе тромбоэмболии легочной артерии, хроническая обструктивная болезнь легких и др.
Патофизиологические изменения, способствующие возникновению фибрилляции
итрепетания предсердий
Внастоящее время обсуждаются два механизма фибрилляции предсердий. 1. «Гипотеза множественных волн возбуждения». Как уже было отмечено,
любые органические поражения миокарда могут вызвать ремоделирование левого предсердия. В предсердии происходит пролиферация и дифференцировка фибробластов в миофибробласты, разрастание соединительной ткани и фиброз. Возникает негомогенность (неоднородность) проведения импульса, что, как обсуждалось ранее, является предпосылкой к формированию механизма re-entry. Согласно этой теории ФП сохраняется из-за хаотичного проведения по сократительной мускулатуре предсердий множества независимых мелких волн механизма micro-re-entry. Начало и окончание волн ФП постоянно взаимодействуют, что приводит к их разрушению и образованию новых волновых фронтов (рис. 5.11).
2. «Фокусная», «изолированная», «идиопатическая» или первичная (так как нет заболевания миокарда) ФП. Считается, что к пациентам с идиопатической формой ФП следует относить лиц без органического поражения миокарда; причиной аритмии у них являются очаги эктопической активности, расположенные в устьях легочных вен, впадающих в левое предсердие. Ткань легочных вен характеризуется более коротким рефрактерным периодом, а также быстрыми изменениями ориентации миофибрилл. В середине XX века у больных с ФП были обнаружены муфты мышечной ткани, распространяющиеся на легочные вены, которые являются остатками эмбриональной ткани. Мышечные муфты легочных вен — это важный источник фокальной активности, который может запускать и поддерживать ФП. В качестве основного механизма фокальной активности в легочных венах было выявлено нарушение регуляции кальциевого потока и натриево-кальциевого обмена.
109
ЛП
ЛП
|
ВПВ |
|
|
|
|
|
ВПВ |
ЛВ |
ПП |
ЛВ |
ПП |
а |
НПВ |
б |
НПВ |
|
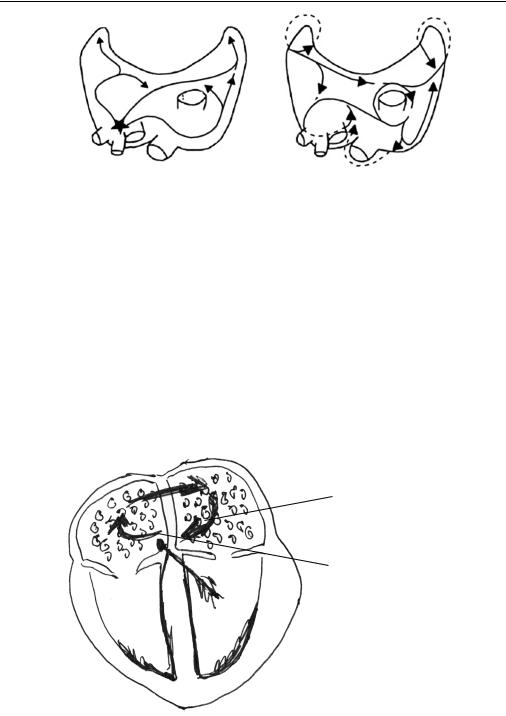
Рис. 5.11. Механизм фибрилляции предсердий: а — патологический очаг возбуждения. Эктопический очаг (обозначен звездочкой) часто находится в области легочных вен. Это приводит к небольшим волнам фибрилляторного проведения, как при множественных волнах re-entry; б — множественные волны re-entry. Небольшие волны (обозначены стрелками) беспорядочно повторно входят в области (re-entry), предварительно активизированные ими или другой небольшой волной. Их маршруты изменяются. ЛП — левое предсердие; ЛВ — легочные вены; НПВ — нижняя полая вена; ВПВ — верхняя полая вена; ПП — правое
предсердие
Запомните!
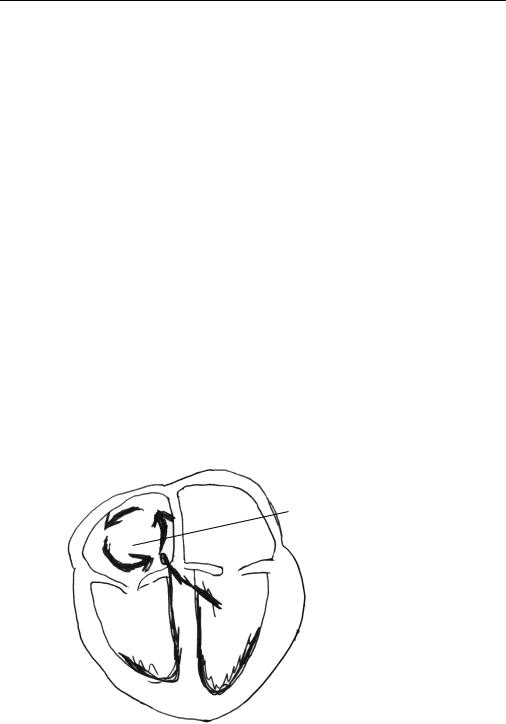
В основе развития фибрилляции предсердий в большинстве случаев лежит механизм micro-re-entry (рис. 5.12) с формированием хаотичного сокращения кардиомиоцитов предсердий с частотой 400–700 импульсов в минуту.
micro re-entry при фибрилляции предсердий
Волны micro re-entry
Распространение фронта возбуждения
Рис. 5.12. Механизм формирования фибрилляции предсердий
110
В основе ТП лежит ритмичная циркуляция круговой волны возбуждения (macro-re-entry) в предсердиях, например, вокруг кольца трехстворчатого клапана или у основания правого предсердия, между трикуспидальным клапаном и устьем полых вен (кава-трикуспидальный перешеек — рис. 5.12). Поскольку расстояние между началом и окончанием «петли повторного входа» достаточно большое, количество импульсов, которые могут пройти по этому пути за одну минуту, меньше, чем при фибрилляции предсердий, поэтому и скорость сокращения предсердий при данном виде аритмии меньше, чем при ФП, а именно, 250–400 в минуту.
Запомните!
В основе развития трепетания предсердий в большинстве случаев лежит механизм mаcro-re-entry (рис. 5.13) с формированием регулярного сокращения предсердий с частотой 250–400 импульсов в минуту и регулярным или нерегулярным проведением к желудочкам (после задержки части импульсов в AВ-узле).
Как при ФП, так и при ТП АВ-узел не может пропустить к желудочкам столь большое количество предсердных импульсов, так как часть импульсов из предсердий достигает АВ-узла, когда тот находится в состоянии рефрактерности.
Поэтому при ФП наблюдается неправильный хаотичный желудочковый ритм, причем число сокращений желудочков зависит от продолжительности абсолютного рефрактерного периода АВ-узла. Большое количество импульсов из множества очагов re-entry несогласованно пытается пройти через АВ-узел, но проходят не все, а только те, которые достигли АВ-узла в тот момент, когда он вышел из состояния рефрактерности. Возбуждение с предсердий на желудочки,
macro re-entry при фибрилляции предсердий
Петля macro-re-entry в районе кава-трикуспидального перешейка
Рис. 5.13. Механизм формирования трепетания предсердий
