
Фармакология (Пособие для резидентуры)
.pdf
ОБЩАЯ ФАРМАКОЛОГИЯ
ния), используют плацебо – лекарственные формы, которые по внешнему виду, запаху, вкусу и прочим свойствам имитируют принимаемый препарат, но не содержат лекарственного вещества (состоят лишь из индифферентных формообразующих веществ).
При «слепом контроле» в неизвестной для больного последовательности чередуют лекарственное вещество и плацебо. Только лечащий врач знает, когда больной принимает плацебо.
При «двойном слепом контроле» об этом информировано третье лицо (заведующий отделением или другой врач). Такой принцип исследования веществ позволяет особенно объективно оценить их действие, так как при ряде патологических состояний плацебо может давать положительный эффект у значительной части больных. Ц
Достоверность полученных данных подтверждается статистически.
В большинстве стран клиническое испытание новых лекарственных веществ обычно проходит 4
фазы /1, 4/.
1-я фаза. Проводится на небольшой группе здоровых добровольцев. Устанавливаются оптимальные дозировки, которые вызывают желаемый эффект. елесообразны также фармакокинетические исследования, касающиеся всасывания веществ, периода их «полужизни», метаболизма. Рекомендуется, чтобы такие исследования выполняли клинические фармакологи.
2-я фаза. Проводится на Энебольшом количестве больных (обычно до 100–200) с заболеванием, для лечения которого предлагается данный препарат. Детально исследуются фармакодинамика (включая плацебо) и фармакокинетика веществ, регистрируются возникающие побочные эффекты. Эту фазу апробации рекомендуется проводить в специализированных клинических центрах.
3-я фаза. Клиническое (рандомизированное контролируемое) испытание на большом контингенте больных (до нескольких тысяч). Подробно изучаются эффективность (включая «двойной слепой контроль») и безопасность веществ. Специальное внимание обращают на побочные эффекты, в том числе аллергические реакции и токсичность препарата. Проводится сопоставление с другими препаратами этой группы. Если результаты проведенного исследования положительные, материалы представляютсяГв официальную организацию, которая дает разрешение на регистрацию и выпуск препарата для практического применения.
4-я фаза. Широкое исследование препарата на максимально большом количестве больных. Наиболее важны данные о побочных эффектах и токсичности, которые требуют особенно длительного, тщательного и масштабного наблюдения. Кроме того, оцениваются отдаленные результаты лечения. Полученные данные оформляются в виде специального отчета, который направляется в ту организацию, которая давала разрешение на выпуск препарата. ти сведения важны для дальнейшей судьбы препарата (его применения в широкой медицинской практике).
Качество препаратов оценивают с помощью химических и физико-химических методов, указанных в осударственной Фармакопее. В отдельных случаях, если строение действующих веществ неизвестно или химические методики недостаточно чувствительны, прибегают к биологической стандартизации. Имеется в виду определение активности лекарственных средств на биологических объектах. Таким путем оценивают препараты ряда гормонов, сердечных гликозидов и др. Выражается активность в условных единицах действия (ЕД). Для сравнения используют стандарт, имеющий постоянную активность. Методы биологической стандартизации и вещества, для которых они обязательны, указаны в Государственной фармакопее.
12

ФАРМАКОКИНЕТИКА 2
ГЛАВА 2. ФАРМАКОКИНЕТИКА
Фармакокинетика1 – «это то, что организм делает с лекарством». Изучение кинетики препарата во время процессов абсорбции (всасывание), распределения, депонирования, метаболизма и экскреции в
совокупности описывается как фармакокинетика. |
Ц |
|
2.1. ПУТИ ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Применение лекарственных средств начинается с их введения в организм или нанесения на поверхность тела /3/.
От пути введения зависят:
скорость развития эффекта;
выраженность эффекта;
продолжительность действия;
характер действия.
Существующие пути введения обычно подразделяют на:
энтеральные – через пищеварительный тракт;
парентеральные – минуя пищеварительный тракт.
Энтеральные пути:
|
пероральный (введение через рот); |
|
сублингвальный (под язык); |
трансбуккальный (защечный); |
|
|
дуоденальный (в двенадцатиперстную кишку); |
|
ректальный (в прямую кишку). |
Самый распространенный пероральный (внутрь; per os) путь введения обладает рядом свойств: |
|
|
медленное наступление эффекта с относительно долгой продолжительностью; |
|
развитие умеренного по силе эффекта (вследствие феномена первого прохождения лекарства |
|
через печень и частичной инактивации лекарственного вещества); |
|
удобство и простота введения; |
|
отсутствие требования стерильности; |
|
отсутствие необходимостиЭв помощи медицинского персонала; |
|
оптимальность применения для хронического лечения; |
|
усвоение может зависеть от пищи. |
Для сублингвального введения характерно: |
|
|
быстрое всасывание; |
|
быстрое наступление мощного, короткого эффекта; |
|
развитие общего действия (резорбтивного); |
|
Г |
отсутствие прохождения через печеночный барьер при первом пассаже;
1 От греч. «pharmacon» – лекарство, «kinetiсos» – движение.
13
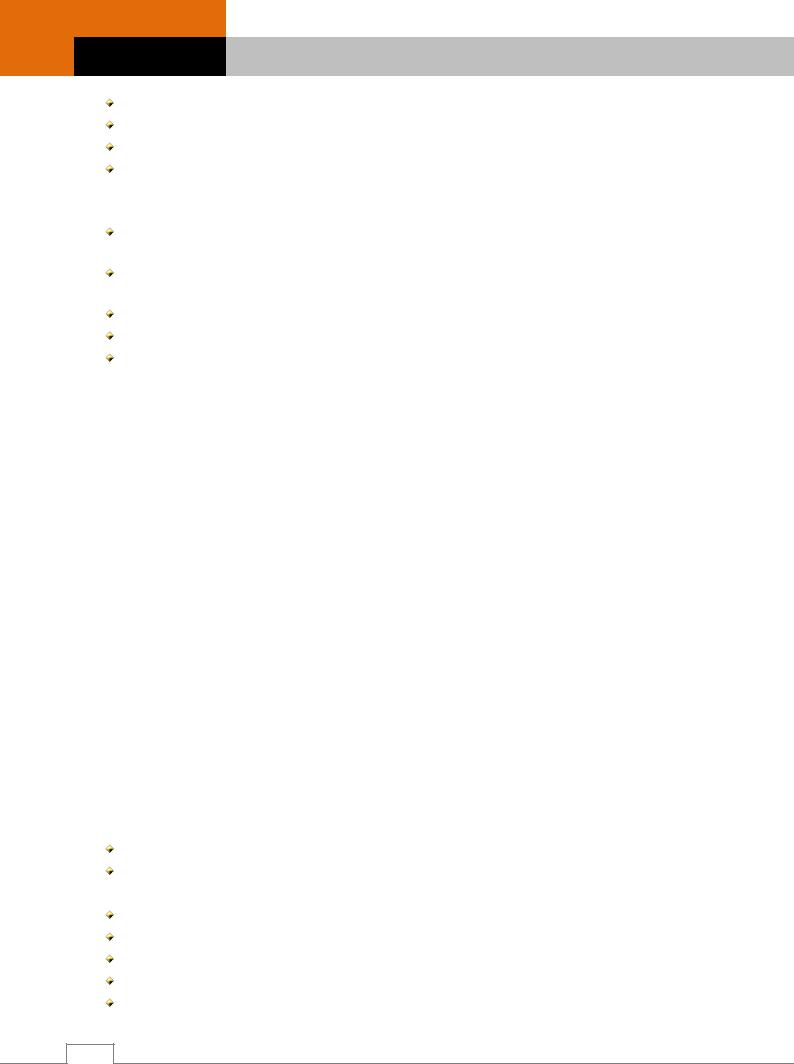
ОБЩАЯ ФАРМАКОЛОГИЯ
отсутствие контакта с ферментами и средой желудочно-кишечного тракта (ЖКТ);
отсутствие соблюдения правил стерильности и помощи медперсонала;
оптимальность для оказания скорой помощи;
применение некоторых веществ с высокой активностью в малых дозах (некоторые гормональные средства, нитроглицерин).
К свойствам трансбуккального (от лат. «buccalis» – щечный) пути введения относится:
прием определенного лекарства путем размещения его между щекой и десной или в полости
рта до полного рассасывания; |
Ц |
|
развитие местного действия на слизистую оболочку полости рта и верхних дыхательных путей;
отсутствие соблюдения стерильности и помощи медперсонала;
применение в основном для хронического лечения;
отличие от сублингвального пути (подъязычная область богато васкуляризированна) заключается в более медленном всасывании (через слизистые оболочки ротовой полости) и, в результате, оказании преимущественно местного действия.
введения характерно:
Иногда препараты вводят дуоденально через зонд в двенадцатиперстную кишку. Для этого пути  Э
Э
быстрое создание высоких концентраций вещества в кишечнике;
местное действие вводимого лекарства;
отсутствие соблюдения стерильности;
необходимость в помощи медперсонала;
возможность применения для хронического лечения и для оказания скорой помощи.
Так, например, наносится солкосерил на язвенные поверхности в ЖКТ для ускорения процессов репарацииГ.
Характеристики для ректального пути введения (per rectum):
всасывание путем простой диффузии;
поступление в кровоток значительной части вещества (около 50%) минуя печень;
отсутствия воздействие ферментов ЖКТ на лекарство;
высокая биодоступность введенного лекарства в сравнении с пероральным приемом;
применение для введения суппозиториев или лекарственных клизм (объем 50 мл);
отсутствие всасывания в толстой кишке лекарств, имеющие структуру белков, жиров и полисахаридов;
комбинирование веществ с раздражающим влиянием со слизями;
отсутствие соблюдения стерильности;
необходимость помощи медперсонала при введении лекарственных клизм;
использование для создания местного и резорбтивного действия;
применение как для хронического лечения, так и для оказания скорой помощи.
К парентеральным путям введения относят:
внутривенный;
внутримышечный;
подкожный;
внутриартериальный;
интрастернальный;
14

ФАРМАКОКИНЕТИКА |
2 |
|
|
внутрибрюшинный;
ингаляционный;
субарахноидальный;
субокципитальный и другие.
Инъекционные способы введения обеспечивают быстроту действия, максимальную биодоступность лекарства и не зависят от состояния больного.
Особенно быстро наступает эффект при внутривенном введении. Поэтому его часто используют в практике неотложных состояний, в случаях, когда невозможно ввести лекарство другим способом. Вводят обычно медленно в виде однократного, дробного, капельного введения (инстилляционно, от лат. instillatio – вкапывание, что обеспечивает постоянную его концентрацию в крови) и инфузии. Внутривенно можно вводить только стерильные, прозрачные растворы, нельзя вводить нерастворимые соединения, масляные растворы (возможность эмболии), средства с выраженным раздражающим действием (могут привести к развитию тромбоза, тромбофлебита), препараты, вызывающие свертывание крови или гемолиз. Однако внутривенно можно вводить ряд веществ, обладающих раздражающими свойствами, которые нельзя вводить подкожно или внутримышечно – раствор кальция хлорида.
При внутримышечном и подкожном введении эффект наступает несколько медленнее. Для пролонгирования фармакотерапевтического эффекта лекарства вводять в мышцу в малорастворимом виде (взвесь) в масле или других основах, задерживающих всасывание веществ из места введения. Внутримышечно и подкожно не следует вводить вещества, оказывающие выраженное раздражающее действие, так как это может быть причиной воспалительных реакций, инфильтратов и даже некроза.
Недостатками указанных путей введения являются их относительная сложность, а также болезненность, необходимость стерильности препаратов и участия медицинского персонала.
Внутриартериальное введение более локально доводит высокие концентрации лекарства до
ДляГгазообразных и летучих соединений основным является ингаляционный путь введения. Этим путем можно вводить газы, пары летучих веществ, аэрозоли, мелкодисперсные порошки. Стенки легочных альвеол имеют очень густую сеть кровеносных капилляров и в своей совокупности представляют большую поверхность (~90 м2), поэтому всасывание действующих веществ через легкие происходит очень быстро. Выраженностью эффекта легко управлять, изменяя концентрацию вещества во вдыхаемом воздухе. Скорость всасывания зависит также от объема дыхания, активной поверхности альвеол и их проницаемости, растворимости веществ в крови и скорости тока крови. Особое значение имеет размер частичек действующего вещества, степень дисперсности (от лат. «disperses» – рассыпанный, степень раздробленности вещества на частицы). Частицы размером 20 мкм проникают в терминальные бронхиолы, размером 6 мкм – в респираторные бронхиолы, 2 мкм – в
области-мишени, кровоснабжаемой данной артерией. Таким путем иногда вводят некоторые
противомикробные и противоопухолевые средства. Для уменьшения общего токсического действия
лекарства отток крови может быть перекрыт путем пережатия вен. Этим путем вводят
рентгеноконтрастные препараты с целью диагностики локализацию опухоли, тромба, сужения |
|
сосудов, аневризмы. |
Ц |
Интрастернальный (от лат. «sternum» – грудина) путь является альтернативой внутривенного
введения при технической невозможности введения в вену (у детей, пожилых пациентов).
Иногда инъекции применяются для локального введения препаратов в определенные полости, где развиваются патологический процесс или патологические очаги в тканях (полости брюшины, плевры, гайморовых полостях, мочевом пузыре, матке, суставе, спинномозговом канале и т.п.). Такой путь введения называется внутриполостной, к нему относятся конъюнктивальное, интраназальное, внутриплевральное, внутривагинальное, интратрахеальное, интравентрикулярное и др. пути
введения. |
Э |
|
15

ОБЩАЯ ФАРМАКОЛОГИЯ
предальвеолярный жом и менее 1 мкм – в альвеолы. Очень сильно измельченное лекарственное средство, проникая в альвеолы, может повредить структуру мембраны и нарушить дыхательную функцию. Ингаляционный способ введения позволяет создать высокую концентрацию лекарственного вещества на месте введения, что наиболее удобно для лечения бронхолегочных заболеваний и купирования приступов при бронхиальной астме. Этим способом вводят и некоторые общие анестетики (средства для ингаляционного наркоза).
Лекарственные средства, плохо проникающие через гематоэнцефалический барьер, могут быть введены под оболочки мозга: субарахноидально, субдурально или субокципитально. Например, так применяют некоторые антибиотики при инфекционном поражении тканей и оболочек мозга. Субарахноидально вводят местные анестетики с целью спинномозговой анестезии.
Высоколипофильные препараты всасываются и оказывают резорбтивное действие при их трансдермальном нанесении. Преимуществом этой формы является длительное поддержание стабильной концентрации веществ в плазме крови. В виде трансдермальных форм лекарства применяют как однократно, так и для длительного лечения.
Иногда пользуются ионофоретическим введением ионизированных веществ (с кожи или со слизистых оболочек). Их всасывание обеспечивается слабым электрическим полем.
Интраназально применяют некоторые пептиды, например, десмопрессин, кальцитонин. Многие из них при этом пути введения всасываются лучше, если в состав препарата включены «промотеры», т.е. вещества, способные изменять свойства слизи или ослаблять тесные межклеточные контакты эпителия слизистой оболочки носовой полости. Всасывание в данном случае происходит со слизистой оболочки полости носа.
2.2. ВСАСЫВАНИЕ
Всасывание ряда веществ преимущественно, имеющих кислый характер, происходит частично из желудка. Однако преобладающее большинство лекарственных средств всасывается, главным образом,
в тонкой кишке вследствие интенсивного кровоснабжения и значительной всасывающей поверхности |
||||||||
слизистой оболочки кишечника /3/. |
|
|
Ц |
|||||
Известны следующие основные механизмы всасывания через мембрану клеток: |
||||||||
1. Пассивная диффузия (рис. 2.1): |
|
|
|
|
||||
определяется градиентом концентрации веществ; |
Внешняя среда |
|||||||
перенос |
веществ |
|
|
из |
области |
высокой |
||
|
|
|
||||||
концентрации в область низкой (по градиенту |
|
|||||||
концентрации) осуществляется без затрат энергии; |
|
|||||||
высокая |
степень |
|
липофильности |
облегчает |
|
|||
прохождения через клеточную мембрану; |
|
|
||||||
|
|
Э |
|
Плазматическая |
||||
проникают гидрофобные вещества, липофильные |
||||||||
неполярные и полярные маленькие |
молекулы |
мембрана |
||||||
|
||||||||
(углекислый газ, оксид азота, вода, мочевина); |
|
|
||||||
не проникают полярные крупные молекулы, |
|
|||||||
заряженные частицы |
|
(ионы) |
и макромолекулы |
Внутренняя среда |
||||
(ДНК, белки); |
|
|
|
|
|
|
|
|
является |
основным |
|
механизмом |
всасывания |
Рис. 2.1. Пассивная диффузия /8/. |
|||
Г |
|
|
|
|
|
|||
лекарственных средств в тонкой кишке. |
|
|
|
|||||
16
ФАРМАКОКИНЕТИКА |
2 |
|
|
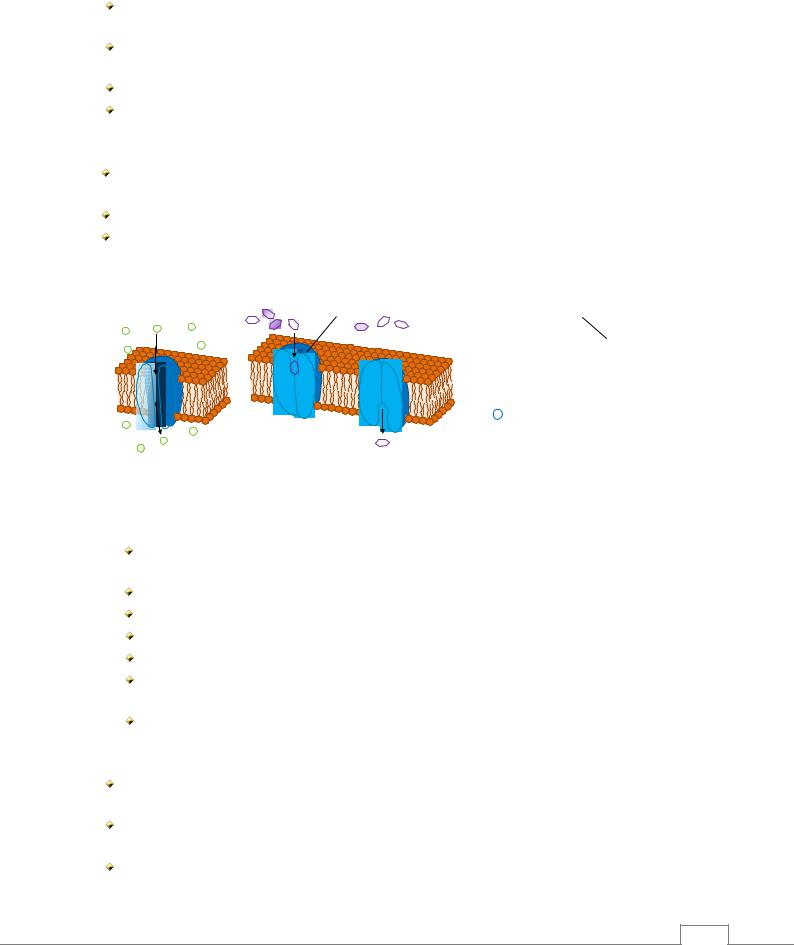
2. Облегченная диффузия (рис. 2.2): |
|
|
|
|
||
перенос веществ осуществляется с помощью транспортных белков (белков каналов или белков- |
|
|||||
переносчиков); |
|
|
|
|
|
|
участие белков обеспечивает более высокую скорость по сравнению с простой пассивной |
|
|||||
диффузией; |
|
|
|
|
|
|
не требует специальных энергетических затрат; |
|
|
|
|||
этим путем проходят полярные вещества (аминокислоты, моносахариды) и заряженные |
|
|||||
частицы (ионы). |
|
Ц |
|
|
||
|
|
|
|
|
||
3. Фильтрация (рис. 2.3): |
|
|
|
|
|
|
представляет собой проникновение через поры мембран (диаметр пор в мембране эпителия |
|
|||||
кишечника невелик – примерно 0,4 нм, или 4 Å) |
|
|
|
|
||
интенсивность зависит от гидростатического и осмотического давления; |
|
W |
||||
|
|
|||||
диффундируют вода, некоторые ионы, а также мелкие гидрофильные молекулы (например, |
|
|||||
|
|
|
|
|
Pore |
|
мочевина). |
|
|
|
|
|
|
|
|
Белок-переносчик |
|
|
|
|
Са2+ |
Э |
|
Водные молекулы |
|
|
|
|
|
|
|
|
||
|
|
Глюкоза |
|
|
|
|
Облегченная диффузия |
Облегченная диффузия с помощью |
|
Пора |
|
|
|
|
|
|
|
|||
Г |
|
|
Рис. 2.3. Фильтрация /8/. |
|
|
|
через канал |
|
белков-переносчиков |
|
|
|
|
Рис. 2.2. Облегченная диффузия /8/. |
|
|
|
|
||
4. Активный транспорт (рис. 2.4): |
|
|
|
|
||
участвуют транспортные системы клеточных мембран (белки-переносчики или белки- |
|
|||||
насосы); |
|
|
|
|
|
|
осуществляется против градиента концентрации переносимого вещества; |
|
|
||||
перенос происходит с затратами энергии (за счет гидролиза АТФ); |
|
|
||||
характеризуется избирательностью к определенным соединениям; |
|
|
||||
обладает возможностью конкуренции двух веществ за один транспортный механизм; |
|
|
||||
характеризуется насыщаемостью (при высоких концентрациях лекарственного вещества |
|
|||||
возможен феномен «насыщения белков-переносчиков»); |
|
|
|
|||
обеспечивает всасывание гидрофильных полярных молекул, ряда неорганических ионов, |
|
|||||
сахаров, аминокислот, пиримидинов. |
|
|
|
|
||
В зависимости от количества и направления перемещения веществ различают /3/: |
|
|
||||
унипорт – транспорт одного вещества в одном направлении в зависимости от градиента |
|
|||||
(потенциал-зависимый Na+-канал); |
|
|
|
|
||
симпорт – транспорт двух веществ в одном направлении через один переносчик (например, |
|
|||||
одновременный перенос молекулы глюкозы и иона Na+); |
|
|
|
|||
антипорт – |
перемещение двух веществ в разных направлениях через один переносчик |
|
||||
(например, Na+,K+-АТФаза).
17

ОБЩАЯ ФАРМАКОЛОГИЯ
Внеклеточная жидкость |
|
|
|
|
Цитоплазмати- |
|
Ц |
||
ческая мембрана |
|
|||
АТФ |
||||
|
АТФ |
|||
АТФ |
|
|
||
|
|
|
||
АДФ + Ф |
|
АДФ + Ф |
||
АДФ + Ф |
|
|
||
|
|
|
||
Цитоплазма |
|
|
|
|
а) Унипорт |
б) Антипорт |
в) Унипорт, связанный |
||
с симпортом |
||||
|
|
|
||
Рис. 2.4. Активный транспорт /8/. |
||||
5. Пиноцитоз (рис. 2.5): |
|
|
|
|
является везикулярным типом транспорта; |
|
|
||
Э |
|
|
||
происходит инвагинация клеточной |
мембраны с последующим образованием пузырька |
|||
(пиносомы) с захваченными крупными молекулами вещества;
пиносома мигрирует по цитоплазме к противоположной стороне клетки, где путем экзоцитоза содержимое выводится наружу.
|
|
Внеклеточная |
|
|
|
|
жидкость |
|
|
|
Рецептор |
|
|
|
|
|
Плазматическая |
|
|
|
Рецептор- |
мембрана |
|
|
|
|
|
|
|
|
опосредованный |
|
|
|
|
|
|
|
|
|
эндоцитоз |
|
|
Рис. 2.5. Механизм эндоцитоза, |
|
|
Пиноцитоз |
||
|
|
опосредованного рецепторами и |
||
|
|
|
|
|
Участок |
Белки, |
|
|
пиноцитоза /8/. |
инвагинации, пок- |
|
|
||
обеспечивающие |
|
|
|
|
рытый белками |
образование |
|
|
|
|
|
|
|
|
|
везикулы |
|
|
|
|
Везикула, |
|
|
|
|
покрытая |
Везикула |
|
|
|
белками |
|
|
|
6. ЭндоцитозГ, опосредуемый рецепторами (рис. 2.5):
везикулярный тип транспорта;
происходит инвагинация клеточной мембраны с последующим образованием окаймленных ямок (эндосом);
внутриклеточная сторона окаймленной ямки содержит набор адаптивных белков, внешняя сторона мембраны включает специфические рецепторы (например, ЛПНП-рецептор).
макромолекулы проходят внутрь со значительно большей скоростью, чем вещества, поступающие в клетки за счет пиноцитоза;
представляет собой избирательный механизм;
18

|
|
|
|
|
|
|
|
ФАРМАКОКИНЕТИКА |
2 |
|
|
|
позволяет захват большого количества специфических лигандов2 без поглощения большего |
||||||||||
|
объема внеклеточной жидкости. |
|
|
|
|
|
|
|
|||
|
Всасывание лекарственных средств зависит от различных факторов: |
|
|
|
|||||||
|
1. Физико-химические свойства лекарства и лекарственной формы: |
|
|
|
|
||||||
|
длительность расщепления таблетки или капсулы; |
|
|
|
|
||||||
|
время растворения в содержимом желудка и кишечника; |
|
|
|
|
||||||
|
присутствие эксципиентов (высушивающих веществ) в таблетке или капсуле; |
|
|
||||||||
|
стабильность в ЖКТ; |
|
|
|
|
|
|
|
|||
|
физико-химические свойства лекарственного средства (степени ионизации, липофильность, |
||||||||||
|
гидрофильность). |
|
|
|
|
|
|
|
|
|
|
|
2. Состояние ЖКТ пациента (табл. 2.1): |
|
|
|
|
|
|
|
|||
|
рН содержимого ЖКТ (при снижении рН лучше всасываются слабые кислоты, так как |
||||||||||
|
становятся менее ионизированными, а повышение рН облегчает всасывание слабых оснований |
||||||||||
|
и задерживает всасывание слабых кислот); |
|
|
|
|
|
|
||||
|
скорость опорожнения желудка; |
|
|
|
|
|
|
|
|||
|
время прохождения лекарства по тонкой кишке; |
|
|
|
|
||||||
|
|
|
Э |
|
|
|
|
|
|||
|
наличие заболеваний ЖКТ; |
|
|
|
|
|
|
|
|||
|
интенсивность кровоснабжения ЖКТ; |
|
|
|
|
|
|
|
|||
|
активность ферментов. |
|
|
|
|
|
|
|
|||
|
Таблица 2.1. Влияние факторов на особенность всасывания в зависимости от природы |
|
|
||||||||
|
лекарственных средств и среды. |
|
|
|
|
|
|
|
|||
|
Факторы |
|
|
|
Всасывание лекарственных средств |
|
|
||||
|
|
|
|
|
Слабые кислоты |
Слабые основания |
|
||||
2 |
Г |
|
|
|
↓ |
|
|
|
|
||
|
Изменение рН |
Щелочная |
|
|
|
|
|
|
|||
|
|
Кислая |
|
|
|
|
|
↓ |
|
|
|
|
Степень |
Низкая |
|
|
|
↓ |
|
|
|
|
|
|
ионизации |
|
|
|
|
|
Ц |
|
|
|
|
|
|
Высокая |
|
|
|
|
|
↓ |
|
|
|
|
Липофильность |
Низкая |
|
|
|
↓ |
|
↓ |
|
|
|
3. Взаимодействие лекарства с содержимым желудка и кишечника:
взаимодействие с другими лекарствами;
взаимодействие с пищей.
4. Фармакокинетические характеристики препарата:
метаболизм в стенке кишечника;
метаболизм под действием кишечной микрофлоры.
Важную роль в активном транспорте и абсорбции веществ через клеточные мембраны, играет мембранный транспортер Р-гликопротеин3 (MDR1)4. Это мембранный белок – гликопротеин из семейства ABC-переносчиков (ATP-binding cassette), продукция которого регулируется специальным геном. Р-гликопротеин является АТФ-зависимым выкачивающим насосом (efflux transporter), обеспечивающий перенос липидов, стероидов, пептидов, билирубина и др. через мембрану клетки, а
От лат. «ligare» – связывать; химическое соединение, которое образует комплекс с той или иной биомолекулой (например, с клеточным рецептором, с ДНК) и вызывает биохимические, физиологические или фармакологические эффекты.
3 P – от англ. permeability.
4 Multi-Drug Resistance Protein 1 – Белок Множественной Лекарственной Устойчивости 1.
19

ОБЩАЯ ФАРМАКОЛОГИЯ
также выведении из клеток лекарственных веществ и других ксенобиотиков /3, 8/.
Он локализуется в тонкой кишке, печени, почках, гистогематических барьерах, поджелудочной железе, коре надпочечников, в некоторых гемопоэтических и иммунокомпетентных клетках, а также в ряде опухолевых клеток, участвуя в регуляции абсорбции, распределении, экскреции, а также эффективности и токсичности многих веществ (рис. 2.6).
|
) |
|
Плотный |
P-gp |
контакт |
|
Апикальнаямембраначеловек)( |
|
Базолатеральнаямембранакровь( |
Плотный |
|
|
|
|
|
|||
|
контакт |
|
|||
Энтероцит |
Почечная |
P-gp |
|||
|
|||||
эпителиальная |
|
||||
|
|
||||
|
клетка |
Просвет |
|||
|
|
|
|||
|
|
|
нефрона |
||
P-gp |
|
Базолатеральная |
|
|
P-gp |
|
|
мембрана |
|
|
|
А |
|
|
|
Б |
|
|
|
|
|
|
|
|
Плотный |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
контакт |
||
|
|
|
Базолатеральная |
|
P-gp |
||
|
|
|
|
||||
|
|
|
мембрана |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
Гепатоцит |
|
Желчный |
|
|
|
|
|
|
каналец |
||
|
|
|
|
|
|
||
|
|
|
|
|
P-gp |
||
|
|
|
|
|
Мембрана |
||
|
|
|
|
|
канальца |
||
|
|
|
|
|
|
Кровь |
|
|
В |
|
|
|
Ц |
||
|
|
|
|
|
|||
|
Рис. 2.6. Действие Р-гликопротеина на просвет кишечника (А), активную секрецию в первичную |
||||||
|
|
|
мочу (Б) и желчь (В) /8/. |
||||
|
Р-гликопротеин является функциональным барьером, препятствующим накоплению токсических |
||||||
НапримерГ, в энтероцитахЭтонкой кишки Р-гликопротеин ограничивает абсорбцию дигоксина, паклитаксела и др., снижая их биодоступность. В гематоэнцефалическом барьере – препятствует накоплению винбластина, циклоспорина А, антрациклинов и др. в головном мозге.
веществ, способствующим выведению ксенобиотиков и их метаболитов из организма с мочой, желчью, кишечником.
Также Р-гликопротеин может являться причиной резистентности некоторых препаратов. Известно, что в опухолевых клетках повышается продукция Р-гликопротеина, который активно выводит из клетки опухоли противоопухолевые препараты.
Ингибируя активность Р-гликопротеина, можно повысить концентрацию лекарственного средства и эффективность лечения. Например, при ингибировании Р-гликопротеина опухолевых клеток подавляется развитие их резистентности к противоопухолевым препаратам, при применении верапамила (ингибитор Р-гликопротеина в кишечнике, печени и почках) повышается концентрация дигоксина в плазме крови, индуктор рифампицин снижает концентрацию дигоксина соответственно
(рис. 2.7).
20
ФАРМАКОКИНЕТИКА 2
|
|
Блокада |
|
|
|
Ядро |
|
||
|
|
|
|
|
|
|
|
||
|
Pgp |
эффлюкс-насоса |
|
|
|
|
|
||
|
Повышение |
|
|
|
|
||||
|
|
|
|
|
|
||||
|
|
внутриклеточной |
|
|
|
||||
|
|
концентрации |
|
|
|
|
|||
|
|
|
лекарства |
|
|
|
|
||
Эффект |
|
|
|
|
|
|
|
|
|
ППУ |
|
|
100 |
|
|
|
|
|
|
ГЭЦ |
|
|
|
|
|||||
|
|
|
80 |
|
|
|
|
|
|
Эндоцитоз |
|
(%) |
60 |
|
|
|
|
|
|
|
|
Выживание |
40 |
|
Pgp-Р121(Д) |
|
|
|
|
|
|
|
|
|
Pgp-Д/Pgp-Р121 |
|
|
|
|
Доксорубицин |
|
|
20 |
|
Pgp-Д |
|
|
|
|
|
|
|
0 |
|
Контроль |
|
|
|
|
Реверсин 121 |
|
|
0 |
20 |
40 |
60 |
80 |
100 |
|
Время (дни)
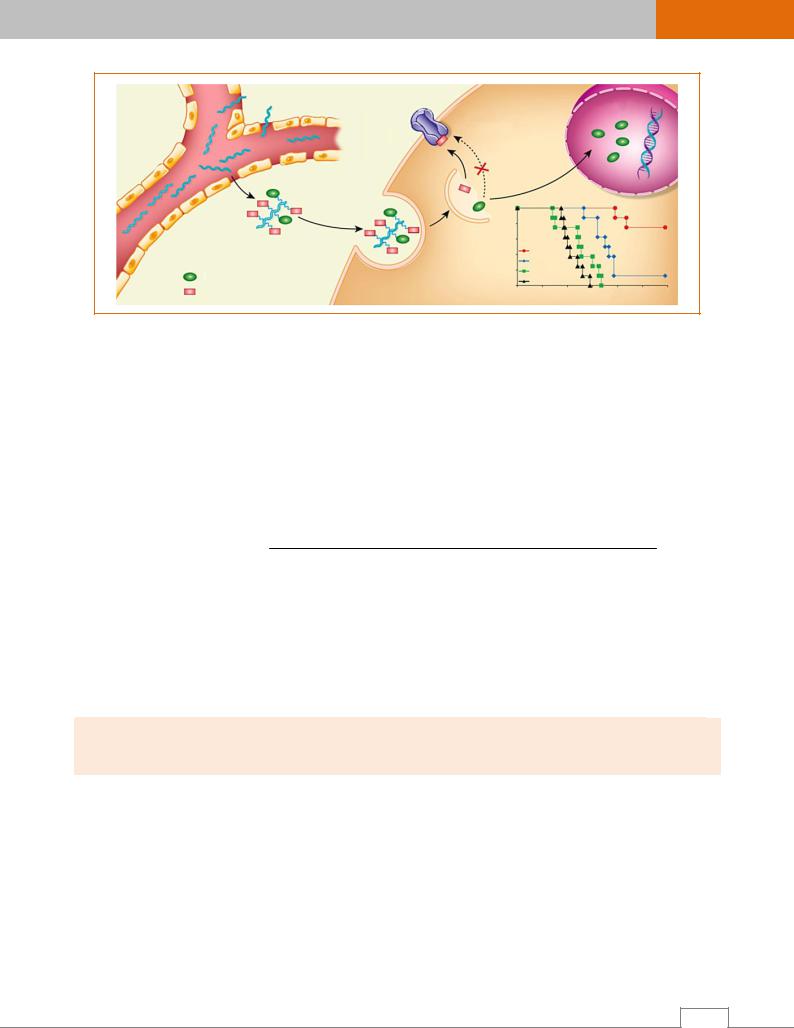
Рис. 2.7. Совместное применение субстрата Р-гликопротеина с его ингибитором для предупреждения развития резистентности: ППУ – повышенная проницаемость и удерживание; Pgp – Р-гликопротеин; Д – доксорубицин; Р121 – Реверсин 121 /8/.
При некоторых заболеваниях происходит изменение функции или снижение экспрессии Р-гли- копротеина (в мозге при болезни Альцгеймера, в кишечнике при энтероколитах и др.).
Существуют не только субстраты (вещества, подверженные транспортированию Р-гликопро-
теином), но и его ингибиторы и индукторы (рис. 2.8).
Биодоступность – характеристика, определяющая количество потерь лекарственного средства: чем выше биодоступность лекарственного вещества, тем меньше его потерь, тем выше эффективность.
количество неизмененного вещества, достигшее плазмы крови
Биодоступность =
исходная доза препарата
При энтеральном введении потери лекарства связаны с его всасыванием из ЖКТ и первом прохождении через печеночный барьер (пресистемный метаболизм). При внутривенном введении биодоступность принимают за 100%.
О биодоступности можно судить и по выделению препарата с мочой (если он не подвергается биотрансформации). В отдельных случаях критерием биодоступности может служить величина фармакологического эффекта, если возможно его точное количественное измерение.
2.3. РАСПРЕДЕЛЕНИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ В ОРГАНИЗМЕ. БИОЛО ИЧЕСКИЕ БАРЬЕРЫ. ДЕПОНИРОВАНИЕ
Распределение лекарства начинается после абсорбции, однако подавляющее большинство лекарственных средств распределяется в организме неравномерно. Для достижения клеток-мишеней лекарственное средство должно покинуть кровоток, пройдя через гистогематические барьеры (от греч. «histos» – ткань, «haima» – кровь) – «фильтры» между кровью и клетками-мишенями.
В организме несколько гистогематических барьеров: гематоэнцефалический барьер – барьер между кровью и тканями мозга; плацентарный барьер – барьер между кровью матери и организмом плода; гематоофтальмический барьер – барьер между кровью и водянистой влагой глаза; гематолимфатический барьер – барьер между кровью и лимфой; аэрогематический барьер – барьер между кровью и воздухом в альвеолах; энтерогематический барьер – барьер между кровью и ЖКТ и многие другие.
21
