
Задачи и упражнения / Авдеенко А.П. Сборник задач по неорганической химии
.pdf
Задача № 5. Составить уравнения следующих химических реакций:
Na2O + SO3 |
; |
CaO + H2O |
; |
CuO + P2O5 ; |
ZnO + K2O |
; |
ZnO + HCl |
; |
ZnO + Ca(OH)2 . |
SO2 + H2O |
; |
SO3 + Ba(OH)2 |
; |
|
Решение. Na2O + SO3 |
Na2SO4; |
CaO + H2O Ca(OH)2; |
|
ZnO + K2O |
K2ZnO2; |
ZnO + 2HCl |
ZnCl2 + H2O; |
SO2 + H2O |
H2SO3; |
SO3 + Ba(OH)2 |
BaSO4 + H2O; |
3CuO + P2O5 |
Cu3(PO4)2; |
ZnO + Ca(OH)2 |
CaZnO2 + H2O/ |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 6. Какие из перечисленных оксидов будут взаимодействовать с водой: CaO, Na2O, SiO2, CuO, P2O5, CrO3 ?
Решение. С водой взаимодействуют кислотные оксиды, за исключением SiO2, и оксиды щелочных и щелочно-земельных металлов:
оксид щелочного или щелочно-земельного металла + Н2О щелочь;
кислотный оксид + Н2О |
кислота. |
|
CaO + H2O = Ca(OH)2; |
CuO + H2O ; |
SiO2 + H2O ; |
P2O5 + 3H2O = 2H3PO4; |
Na2O + H2O = 2NaOH; |
CrO3 + H2O = H2CrO4. |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 7. Какие из оксидов будут реагировать попарно: CaO, K2O,
Al2O3, SO3 ? |
|
|
|
|
|
Решение. Известно: |
|
|
|
||
основной оксид |
+ кислотный оксид |
соль; |
|||
амфотерный оксид + кислотный оксид |
соль; |
||||
амфотерный оксид + оснóвный оксид |
соль. |
|
|||
CaO + Al2O3 |
|
Ca(AlO2)2 ; |
K2O + SO3 |
K2SO4; |
|
CaO + SO3 |
CaSO4; |
Al2O3 + 3SO3 |
Al2(SO4)3; |
||
K2O + Al2O3 |
|
2KAlO2. |
|
|
|
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 8. Как можно получить следующие оксиды: P2O5, CuO ?
41
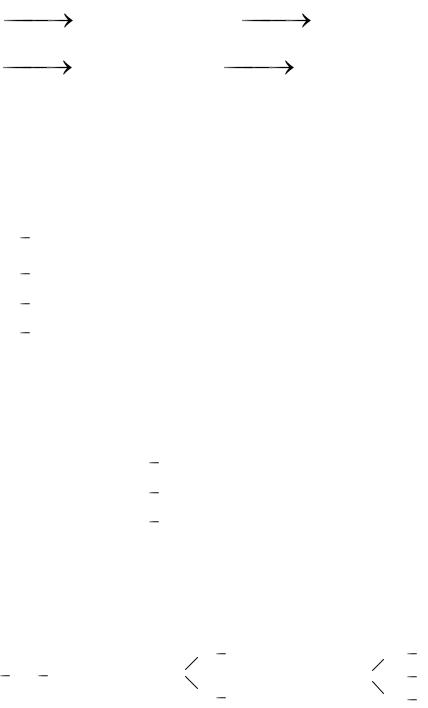
to |
2P2O5; |
Cu(OH)2 |
|
to |
CuO + H2O; |
Решение: 4P + 5O2 |
|
|
|||
to |
2CuO; |
CuCO3 |
to |
|
CuO + CO2. |
2Cu + O2 |
|
|
1.9.2. Типовые задачи с решениями по основаниям
Задача № 1. Назвать следующие основания по международной номен-
клатуре: KOH, Al(OH)3, CuOH, Cu(OH)2.
Решение. |
KOH |
гидроксид калия; |
|
|
|
|
Al(OH)3 |
гидроксид алюминия; |
|
CuOH |
гидроксид меди (I); |
|
Cu(OH)2 |
гидроксид меди (II). |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 2. Найти эмпирические формулы следующих оснований: гидроксид железа (III), гидроксид бария, гидроксид аммония.
Решение. |
Гидроксид железа (III) |
Fe(OH)3; |
|
гидроксид бария |
Ba(OH)2; |
|
гидроксид аммония |
NH4OH. |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 3. Привести графические формулы следующих оснований:
LiOH, Zn(OH)2, Fe(OH)3.
O |
H |
|
|
O |
H |
Решение. LiOH: Li O H; Zn(OH)2: Zn |
|
; Fe(OH)3: Fe |
|
O |
H . |
|
|
||||
O |
H |
|
|
O |
H |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 4. К каким типам относятся следующие основания: LiOH, KOH, Ca(OH)2, Ba(OH)2, Al(OH)3, Zn(OH)2, Cr(OH)2, Fe(OH)2, Ni(OH)2 ?
Решение. К щелочам относятся растворимые основания 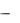 основания щелочных, щелочно-земельных металлов и NH4OH: LiOH, KOH, Ca(OH)2, Ba(OH)2. К амфотерным основаниям относятся основания тех металлов, кото-
основания щелочных, щелочно-земельных металлов и NH4OH: LiOH, KOH, Ca(OH)2, Ba(OH)2. К амфотерным основаниям относятся основания тех металлов, кото-
42

рые образуют амфотерные оксиды: Al(OH)3, Zn(OH)2. К нерастворимым основаниям все остальные основания: Cr(OH)2, Fe(OH)2, Ni(OH)2.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 5. По формулам оксидов Na2O и CrO составить формулы соответствующих гидроксидов.
Решение. Так как оксиды Na2O и CrO обладают оснóвными свойствами, то их гидроксиды также должны проявлять оснóвные свойства и должны относиться к основаниям.
Определив валентность элемента и зная формульную валентность груп-
пы ОН, равную 1, составляем формулы оснований: |
|
||
Na2O NaOH; CrO Cr(OH)2. |
|
|
|
Рекомендуем самостоятельно составить подобную задачу и решить ее. |
|||
Задача № 6. Составить уравнения следующих химических реакций: |
|||
NaOH + H2SO4 |
; |
t o |
; |
|
|
Fe(OH)2 |
|
NaOH + NiCl2 |
; |
Ni(OH)2 + HCl |
; |
Ca(OH)2 + P2O5 |
; |
Zn(OH)2 + KOH |
; |
NaOH + Al + H2O ; |
Zn(OH)2 + HNO3 . |
Решение. 2NaOH + H2SO4 = Na2SO4 + 2H2O; |
|
NaOH + NiCl2 = Ni(OH)2 |
+ 2NaCl; |
3Ca(OH)2 + P2O5 = Ca3(PO4)2 + 3H2O;
2NaOH + Al + 2H2O = 2NaAlO2 + 3H2 ;
to
Fe(OH)2 = FeO + H2O; Ni(OH)2 + 2HCl = NiCl2 + 2H2O;
Zn(OH)2 + 2KOH = K2ZnO2 + 2H2O; Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2H2O.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 7. Какие из перечисленных оснований будут взаимодейство-
вать с NaOH; HCl: Ca(OH)2, Al(OH)3, Be(OH)2, Cu(OH)2 ?
Решение. Со щелочью будут реагировать только амфотерные основания:
NaOH + Al(OH)3 = NaAlO2 + 2H2O; 2NaOH + Be(OH)2 = Na2BeO2 + 2H2O.
43
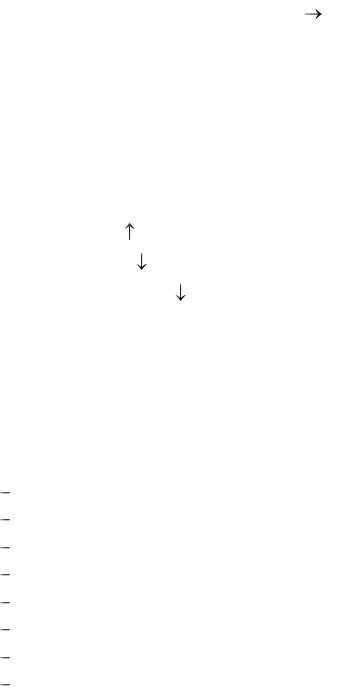
С кислотами реагируют все типы оснований:
Ca(OH)2, + 2HCl = CaCl2 + 2H2O;
Al(OH)3 + 3HCl = AlCl3 + 3H2O;
Be(OH)2 + 2HCl = BeCl2 + 2H2O;
Cu(OH)2 + 2HCl = CuCl2 + 2H2O.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 8. Какие из перечисленных оснований будут реагировать по-
парно: LiOH, Ba(OH)2, Be(OH)2, Cu(OH)2 ?
Решение. Известно, что амфотерное основание + щелочь соль + Н2О:
2LiOH + Be(OH)2 = Li2BeO2 + 2H2O; Ba(OH)2 + Be(OH)2 = BaBeO2 + 2H2O.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 9. Как можно получить следующие основания: KOH и
Fe(OH)3 ?
Решение. K2O + H2O = 2KOH;
2K + 2H2O = 2KOH + H2 ;
K2SO4 + Ba(OH)2 = BaSO4 + 2KOH; Fe2(SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
1.9.3. Типовые задачи с решениями по кислотам
Задача № 1. Назвать следующие кислоты: HCl, H2S, H2SO4, H2SO3, H3PO4, HNO3, HNO2, H2CO3.
Решение. HCl |
кислота хлороводородная; |
H2S |
кислота сероводородная; |
кислота серная; кислота сернистая; кислота фосфорная; кислота азотная; кислота азотистая; кислота угольная.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
44

Задача № 2. Найти эмпирические формулы следующих кислот: бромоводородная кислота, хромовая кислота, селеновая кислота.
Решение. Бромоводородная кислота |
HBr; |
хромовая кислота |
H2CrO4; |
селеновая кислота |
H2SeO4. |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 3. Привести графические формулы следующих кислот: HCl,
H2S, HNO3, H3PO4. |
|
|
|
|
|
Решение. |
|
|
|
|
|
H |
O |
H |
O |
||
HCl: H Cl; H2S: S ; HNO3: H O N |
; |
H3PO4: H |
O |
|
P = O. |
|
|||||
H |
O |
H |
O |
||
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 4. К каким типам относятся следующие кислоты: HCl, HNO3, H2S, H2SO4, H2CrO4, HVO3, HF, H3PO4 ?
Решение. Бескислородные кислоты: HCl, H2S, HF. Кислородсодержащие кислоты: HNO3, H2SO4, H2CrO4, HVO3, H3PO4.
Классифицировать кислоты можно также по числу атомов водорода, способных замещаться в молекуле кислоты:
одноосновные HCl, HNO3, HVO3, HF;
двухосновные H2S, H2SO4, H2CrO4; трехосновные H3PO4.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 5. По формулам Al2O3, MnO2, CO2, CrO3 составить формулы соответствующих гидроксидов.
Решение. Гидроксиды кислотных оксидов являются кислотами, а гидроксиды амфотерных оксидов проявляют также амфотерные свойства и могут выступать в роли как кислот, так и оснований.
СО2 |
кислотный оксид; Н2СО3 |
кислота; |
СO2 |
H2O |
|
H2CO3. |
|
|
СrО3 |
кислотный оксид; Н2СrО4 |
кислота; |
СrO3 |
H2O |
|
H2CrO4. |
|
|
|
45 |
|

Al2O3 амфотерный оксид, Al(OH)3 амфотерный гидроксид; Al(OH)3 может выступать в роли как основания Al(OH)3, так и кислоты H3AlO3 или HAlO2;
H3AlO3 |
H2O |
HAlO2. |
|
MnO2 |
амфотерный оксид, Mn(OH)4 амфотерный гидроксид, Mn(OH)4 |
может выступать в роли как основания Mn(OH)4, так и кислоты H2MnO3, полученной в результате отщепления 1 молекулы H2O от H4MnO4;
H4MnO4 H2O H2MnO3.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача 6. Составить уравнения следующих химических реакций: |
|
||||
H2SO4 |
+ Zn ; |
HNO3 + Cu |
; |
HNO3 + Cu |
; |
разб. |
|
разб. |
|
конц. |
|
H2SO4 |
+ NaOH ; |
HNO3 + Fe(OH)3 ; |
HBr + Al2O3 |
; |
|
H2SO4 |
+ NaCl . |
|
|
|
|
конц. |
|
|
|
|
|
Решение. H2SO4 |
+ Zn = ZnSO4 + H2 ; |
|
|
|
|
разб. |
|
|
|
|
|
4HNO3 + Cu = Cu(NO3)2 + 2NO2 |
+ 2H2O ; |
|
|
||
конц. |
|
|
|
|
|
8HNO3 + 3Cu = 3Cu(NO3)2 + 2NO |
+ 4H2O ; |
|
|
||
разб. |
|
|
|
|
|
3HNO3 + Fe(OH)3 = Fe(NO3)3 + 3H2O ; |
|
|
|||
2HF + CaO = CaF2 + H2O; |
|
|
|
||
H2SO3 |
+ 2NaOH = Na2SO3 + 2H2O ; |
|
|
||
6HBr + Al2O3 = 2AlBr3 + 3H2O ; |
|
|
|
||
H2SO4 |
+ 2NaCl = Na2SO4 + 2HCl . |
|
|
|
|
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 7. С какими из перечисленных веществ будет реагировать
HCl: Na2O, ZnO, CrO3, SO2, Mg(OH)2, Zn, Cu ?
Решение. Na2O + 2HCl = 2NaCl + H2O; ZnO + 2HCl = ZnCl2 + H2O;
CrO3 + HCl ;
46

SO2 + HCl ;
Mg(OH)2 + 2HCl = MgCl2 + 2H2O; Zn + 2HCl = ZnCl2 + H2O;
Cu + HCl .
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 8. Как можно получить следующие кислоты: HBr и H3PO4 ? Решение. HBr 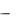 бескислородная кислота, ее получают следующими
бескислородная кислота, ее получают следующими
способами:
H2 + Br2 = 2HBr;
2NaBr + H2SO4 = Na2SO4 + 2HBr .
H3PO4 |
кислородсодержащая кислота, ее получают следующими |
способами:
P2O5 + 3H2O = 2H3PO4;
Ca3(PO4)2 + 3H2SO4 = 3CaSO4 + 2H3PO4.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
1.9.4. Типовые задачи с решениями по солям
Задача № 1. Назвать следующие соли по международной номенклатуре:
CaCl2, Na2S, K2SO3, Li2SO4, Fe(NO3)3, Fe(NO2)2, Ca3(PO4)2, NaHPO4, Na2HPO4, Fe(OH)2Cl, (FeOH)2SO4.
Решение. |
CaCl2 |
хлорид кальция; |
сульфид натрия; сульфит калия; сульфат лития; нитрат железа (III); нитрит железа (II); фосфат кальция;
дигидрофосфат натрия; гидрофосфат натрия;
Fe(OH)2Cl дигидроксохлорид железа (III); (FeOH)2SO4 гидроксосульфат железа (II).
Рекомендуем самостоятельно составить подобную задачу и решить ее.
47
Задача № 2. Найти эмпирические формулы следующих солей: гидрокарбонат кальция, гидроксосульфат магния, хромат калия.
Решение. Гидрокарбонат кальция |
Ca(HCO3)2; |
гидроксосульфат магния |
(MgOH)2SO4; |
хромат калия |
K2CrO4. |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 3. Привести графические формулы следующих солей: CaCl2, Zn3(PO4)2, MgCO3, Na2HPO4, Fe(NO3)3, (FeOH)2SO4.
Решение.
|
Cl |
CaCl2: Ca |
; |
|
Cl |
|
|
O |
|
Zn |
P = O |
|
|
O |
|
|
O |
Zn (PO ) : Zn |
; |
|
3 |
4 2 |
O |
|
|
|
|
|
O |
|
Zn |
P = O |
|
|
O |
Na – O
Na2HPO4: Na – O  P = O;
P = O;
H – O
|
O |
MgCO3: Mg |
C = O; |
|
O |
|
|
|
|
|
O |
|
|
|
O |
N |
|
|
|
|
|
|
O |
|
|
|
|
|
O |
Fe(NO3)3 Fe |
|
|
O |
N |
O |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
N |
|
|
|
|
|
|
O |
|
|
|
O – H |
|
|
|
Fe |
|
O |
||
|
|
|
O |
|
|
(FeOH)2SO4: |
|
|
S |
. |
|
|
|
O |
|||
|
|
|
|
O |
|
|
Fe |
|
|||
|
|
|
|||
O – H
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 4. К каким типам относятся следующие соли: Mn(NO3)2, CuSO4, (ZnOH)2SO4, NaHSO3, FeOHCl2, MgOHCl, K2HPO4 ?
Решение. Средние соли |
Mn(NO3)2, CuSO4; |
оснóвные соли |
(ZnOH)2SO4, FeOHCl2, MgOHCl; |
кислые соли |
NaHSO3, K2HPO4. |
Рекомендуем самостоятельно составить подобную задачу и решить ее.
48
Задача № 5. Составить уравнения следующих химических реакций:
Fe2(SO4)3 + NaOH |
; |
CaCl2 + Na2CO3 |
; |
|
NaHSO4 + NaOH |
; |
Zn + CuSO4 ; |
|
|
Ba(NO3)2 + H2SO4 |
; |
AlOHCl2 + HCl |
; |
|
to |
; |
|
to |
|
FeCO3 |
|
Ca(HCO3)2 |
|
|
Решение. Fe2(SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4 ; |
|
|||
NaHSO4 + NaOH = Na2SO4 + H2O; |
|
|||
Ba(NO3)2 + H2SO4 = BaSO4 |
+ 2HNO3 ; |
|
||
to |
FeO + CO2; |
|
|
|
FeCO3 |
|
|
||
CaCl2 + Na2CO3 = CaCO3 |
+ 2NaCl; |
|
||
Zn + CuSO4 = Cu + ZnSO4; |
|
|
||
AlOHCl2 + HCl = AlCl3 + H2O ; |
|
|||
Ca(HCO3)2 |
to |
CaO + 2CO2 + H2O. |
|
|
|
|
|||
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 6. Предложить все возможные методы получения соли K2SO4.
Решение. 1. 2KOH + H2SO4 = K2SO4.+ 2H2O;
2.K2O + H2SO4 = K2SO4.+ 2H2O;
3.2K + H2SO4 = K2SO4.+ H2 ;
4.K2O + SO3 = K2SO4;
5.2KOH + SO3 = K2SO4.+ H2O;
6. Ag2SO4 + 2KCl = 2AgCl + K2SO4;
7. 2KCl + H2SO4 = K2SO4.+ 2HCl .
1.9.5. Типовые задачи с решениями по взаимосвязи между классами неорганических веществ
Задача № 1. Исходя из Р, О2 и Са получить Са3(РО4)2.
Решение. 1) 4P + 5O2 = 2P2O5;
2)2Ca + O2 = 2CaO;
3)3CaO + P2O5 = Са3(РО4)2.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
49
Задача № 2. Исходя из Zn, Na, H2O и CuSO4 получить Na2ZnO2.
Решение. 1) 2Na + 2H2O = 2NaOH + H2 ;
2)CuSO4 + Zn = ZnSO4 + Cu;
3)ZnSO4 + 2NaOH = Zn(OH)2 + Na2SO4;
4)Zn(OH)2 + 2NaOH = Na2ZnO2 + 2H2O.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
Задача № 3. Осуществить следующие цепочки химических превраще-
ний: |
|
|
|
|
1) |
Cl2 |
NaCl |
HCl |
ZnCl2 MgCl2 AgCl; |
2) |
Na |
Na2O |
NaOH |
Na2SO4 NaOH NaNO3. |
Решение. 1) Сl2 + 2Na = 2NaCl;
2NaCl + H2SO4 = Na2SO4 + 2HCl; 2HCl + Zn = ZnCl2 + H2 ;
ZnCl2 + Mg = MgCl2 + Zn;
MgCl2 + 2AgNO3 = 2AgCl + Mg(NO3)2. 2) 4Na + O2 = 2Na2O;
Na2O + H2O = 2NaOH;
2NaOH + SO3 = Na2SO4 + H2O;
Na2SO4 + Ba(OH)2 = BaSO4 + 2NaOH; NaOH + HNO3 = NaNO3 + H2O.
Рекомендуем самостоятельно составить подобную задачу и решить ее.
1.10.Упражнения и задачи для самостоятельного решения
1.Написать формулы оксидов K, Ba, Al, Si, P, S, Cl, Os, зная, что валентность элемента соответствует номеру группы периодической системы.
2.Назвать следующие оксиды по международной номенклатуре: Cu2O, CuO, ZnO, Al2O3, Mn2O3, MnO2, CO2, P2O5, SO3, Mn2O7, RuO4.
3.К каким типам относятся следующие оксиды: N2O3, Na2O, BaO, Cl2O, Al2O3, WO3, SnO, PbO2, MnO, FeO ?
4.Карбонат магния MgCO3 при нагревании разлагается на два оксида. Рассчитать, какое количество каждого оксида образуется при разложении 210 кг
MgCO3.
50
