
- •Харківський національний університет імені В.Н.Каразіна Медичний факультет
- •План лекції:
- •Функції і властивості посмугованих м’язів
- •Скелетні м’язи
- •Схема будови відрізка м'язового волокна:
- •саркомер
- •Електронна мікроскопія
- •ОСНОВНІ БІЛКИ МІОФІБРІЛ
- •АКТИН
- •МІОЗИН
- •Молекулярні механізми м’язового скорочення:
- •Молекулярні механізми м’язового скорочення:
- •Роль енергії АТФ у механізмі м’язового скорочення:
- •Схема ковзання ниток актину і міозину в ході скорочення
- •Процеси енергозабезпечення м’язової діяльності:
- •Етапи м’язового скорочення
- •Поняття про рухову одиницю
- •Класифікація рухових одиниць:
- •Фізіологічні характеристики скорочення м’язів
- •Типи скорочення м’язів залежно від зміни їх довжини і напруження: ізометричні, ізотонічні
- •Залежність між довжиною м’язового волокна та його напруженням
- •Три фази м’язового скорочення:
- •Максимальна сила в ізотонічному режимі
- •Типи скорочення м’язів залежно від частоти подразнення: одиночні, тетанічні
- •Робота м’язів:
- •ВТОМА М'ЯЗІВ - це тимчасове зниження або втрата їхньої працездатності, що виникають у
- •Значення м’язів у спорті
- •Значення м’язів у спорті
- •Порівняльна характеристика скелетних та гладеньких м’язів:

ОСНОВНІ БІЛКИ МІОФІБРІЛ
Білок |
Доля білка % |
Функції |
|
|
|
|
|
Міозин |
|
Головний компонент товстих філаментів. Утворює |
|
44 |
зв’язки з актином. Рухається по актину за рахунок |
||
|
|
гідролізу АТФ |
|
|
|
|
|
Актин |
22 |
Головний компонент тонких філаментів. Під час |
|
скорочення вздовж нього рухається міозин |
|||
|
|
||
|
|
|
|
Тропонін(С,І,Т) |
5 |
Комплекс з 3 білків, який регулює скорочення при |
|
зв’язуванні з іонами Ca2+ |
|||
|
|
||
|
|
|
|
Тропоміозин |
5 |
Зв’язаний з актином білок, який блокує рух |
|
міозину |
|||
|
|
||
|
|
|

АКТИН
Актинова Тропоміозин глобула
Тропоніновий Тропонін С
комплекс |
Тропонін І |
|
|
|
Тропонін Т |
Спіральний
фрагмент із актинових глобул
Переплетені |
Актинова |
Глобулярні |
спіральні |
головки |
|
Філаменти |
нитка |
міозину |
Міозинові |
Межі |
-актинін |
|
Нитки |
Саркомеру |
||
|

МІОЗИН
Голівка міозину може приєднуватися до актину й володіти ферментативною спроможністю (розщеплювати АТФ)
МІОЗИН - мономер
МІОЗИН - полімер

Молекулярні механізми м’язового скорочення:
Під час скорочення м’язів під світловим мікроскопом спостерігаються такі зміни:
зменшується довжина саркомера;
зменшується довжина І-дисків;
зменшується довжина Н-зони;
довжина А дисків не змінюється.
Під час розслаблення м’язів відбуваються протилежні зміни :
збільшується довжина саркомера;
збільшується довжина І-дисків;
збільшується довжина Н-зони;
довжина А дисків не змінюється.
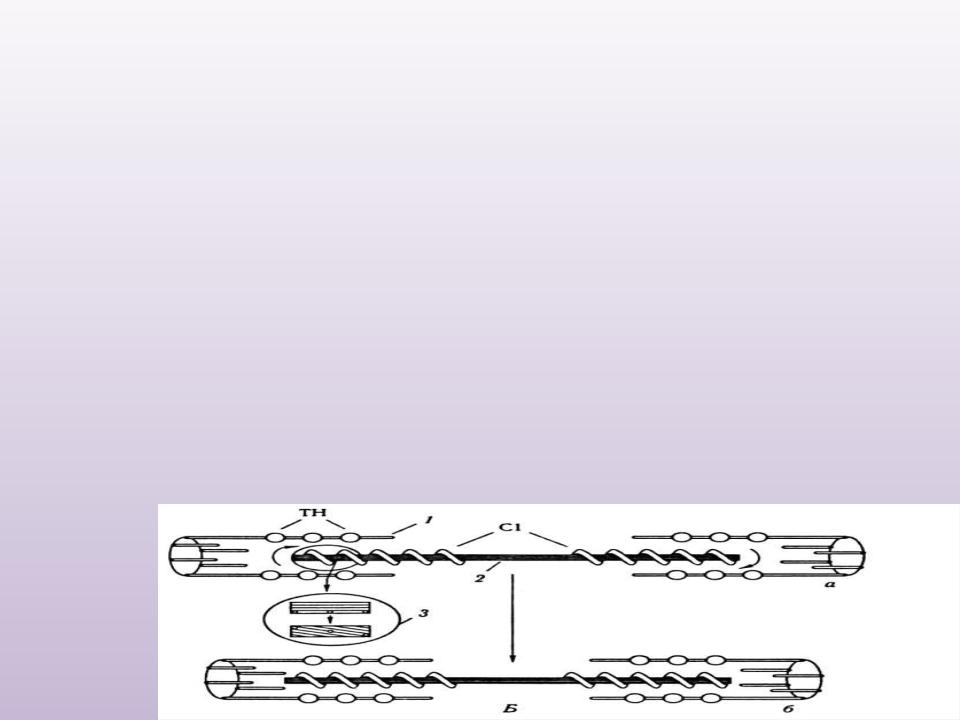
Молекулярні механізми м’язового скорочення:
основні положення теорія Хакслі-Хансона – теорія «ковзання» міофібрил (Huxley H.E., Hanson J., 1954)
1.Скорочення міофібрил відбувається внаслідок скорочення великої кількості саркомерів.
2.Під час скорочення довжина «тонких» актинових і «товстих» міозинових філаментів не змінюється.
3.Процес скорочення відбувається в результаті ковзання актинових філаментів вздовж міозинових.
4.Процес м’язового скорочення потребує енергії АТФ.

Роль енергії АТФ у механізмі м’язового скорочення:

Коли концентрація іонів Са2+ у цитоплазмі низька.
Розміщення тропоніну таке, що тропоміозин блокує активні центри актину. Скорочення неможливе
При зростанні концентрації іонів Са2+ в саркоплазмі м’язового волокна, ці іони взаємодіють з тропоніном С.
Конформація тропоніну змінюється.
Тропоміозин занурюється вглиб актинової філаменти. Активні центри актину звільнюються.
Скорочення стає можливим

Схема ковзання ниток актину і міозину в ході скорочення


