
- •1. Железоуглеродистые сплавы
- •Механические свойства стали обыкновенного качества группы а (гост 380-88)*
- •Механические свойства качественных конструкционных углеродистых сталей (после нормализации) (гост 1050-74)
- •Применение качественных углеродистых конструкционных сталей
- •Конструкционные углеродистые стали выпускаются в виде разнообразных профилей большого количества типоразмеров. Приведены наиболее применяемые в конструкциях рэс сортаменты сталей.
- •Механические свойства хромистых нержавеющих сталей
- •Механические свойства аустенитных сталей в закаленном состоянии
- •Механические свойства криогенных сталей
- •Вопросы для самопроверки
- •2. Титановые сплавы
- •Механические свойства технического титана (отожженный)
- •2.2. Титановые сплавы
- •Механические свойства и псевдо- титановых сплавов в отожженном состоянии
- •Необходима высокая прочность и малый вес. Замена конструкционной углеродистой стали на титановые сплавы позволяет снизить массу деталей примерно в два раза.
- •Вопросы для самопроверки
- •3. Магниевые сплавы
- •Литейные магниевые сплавы, их состав и свойства
- •Продолжение табл.3.1
- •Вопросы для самопроверки
- •Алюминиевые сплавы
- •Химический состав деформируемых неупрочняемых сплавов
- •Вопросы для самопроверки
- •5. Конструкционные сплавы на основе меди
- •Вопросы для самопроверки
- •6. Материалы упругих элементов
- •Допустимая скорость охлаждения при этом виде отжига зависит от массы изделия, его формы и теплопроводности и лежит в пределах 20-200 °с/ч.
- •9. Химико-термическая обработка металлов
- •Вопросы для самопроверки
- •Библиографический список
- •Чернышов Александр Васильевич
- •394026 Воронеж, Московский просп. , 14
А.В.Чернышов
КОНСТРУКЦИОННЫЕ МЕТАЛЛЫ И СПЛАВЫ РЭС
Учебное пособие
Воронеж 2002
УДК 621.396.66
Чернышов А.В.; Конструкционные металлы и сплавы РЭС: Учеб. пособие. Воронеж: Воронеж. гос.техн. ун-т, 2002. 96 с.
В учебном пособии рассматриваются основные сведения о конструкционных материалах, применяемых при изготовлении деталей и узлов радиоэлектронных средств: корпусов, механизмов, пружины, элементов несущих конструкций.
Издание предназначено для студентов специальности 200800 «Проектирование и технология радиоэлектронных средств» по направлению 654300 «Проектирование и технология электронных средств» и может быть использовано при самостоятельном изучении курса «Материаловедение и материалы РЭС», при выполнении курсового проекта по дисциплине «Технология деталей РЭС».
Учебное пособие подготовлено в электронном виде в текстовом редакторе MS WORD; содержbтся в файле УП М&М Конструкционные металлы и сплавы в РЭС.doc, объем файла 900 Кбайт
Табл. 29/ Ил.16/ Библиогр.: 9 назв.
Научный редактор д-р физ. - мат. наук Ю.С. Балашов
Рецензенты: технол.отдел ВНИИС; д.ф.-м.наук Санин В.Н.
Издается по решению редакционно-издательского совета Воронежского государственного технического университета
© Чернышов А.В., 2002
© Оформление. Воронежский
государственный
технический университет, 2002
ОГЛАВЛЕНИЕ
|
Введение |
5 |
|
|
1. |
Железоуглеродистые сплавы |
6 |
|
1.1. |
Фазовый состав сплава железо-углерод |
6 |
|
1.2. |
Влияние углерода, примесей и легирующих элементов |
10 |
|
|
на свойства сталей |
|
|
1.3. |
Конструкционные стали общего назначения |
15 |
|
1.3.1. |
Классификация сталей и общие требования, предъявляемые к ним |
15 |
|
1.3.2. |
Углеродистые стали обыкновенного качества |
16 |
|
1.3.3. |
Углеродистые качественные стали |
18 |
|
1.4 |
Легированные конструкционные стали |
21 |
|
1.4.1. |
Классификация и маркировка легированных сталей |
21 |
|
1.4.2. |
Конструкционные легированные стали |
22 |
|
1.4.3. |
Коррозионно-стойкие стали (нержавеющие стали) |
23 |
|
1.4.4. |
Инструментальные стали |
27 |
|
2. |
Титановые сплавы |
30 |
|
2.1. |
Титан |
30 |
|
2.2. |
Титановые сплавы |
32 |
|
2.3. |
Литейные титановые сплавы |
39 |
|
3. |
Магниевые сплавы |
40 |
|
4. |
Алюминиевые сплавы |
47 |
|
4.1. |
Алюминий |
47 |
|
4.2. |
Конструкционные деформируемые сплавы, не упрочняемые термической обработкой |
50 |
|
4.3. |
Конструкционные деформируемые алюминиевые сплавы, упрочняемые термической обработкой |
54 |
|
4.4. |
Литейные алюминиевые сплавы |
58 |
|
5. |
Конструкционные сплавы на основе меди |
61 |
|
5.1. |
Медь |
61 |
|
5.2. |
Латунь |
63 |
|
5.3. |
Бронзы |
67 |
|
6. |
Материалы упругих элементов |
72 |
|
7. |
Металлы и сплавы для электронновакуумных Приборов |
75 |
|
8. |
Термическая обработка металлов и сплавов |
79 |
|
8.1. |
Общие положения. Классификация видов термической Обработки |
79 |
|
8.2. |
Отжиг металлов |
80 |
|
8.3. |
Закалка, отпуск и старение сплавов |
83 |
|
|
|
|
|
9. |
Химико-термическая обработка металлов и сплавов |
87 |
|
9.1. |
Общие сведения |
87 |
|
9.2. |
Цементация, азотирование и цианирование стали |
88 |
|
Заключение |
90 |
|
|
Библиографический список |
91 |
|
ВВЕДЕНИЕ
При изготовлении элементов несущих конструкций, корпусов, механизмов радиоэлектронных средств используется большая номенклатура конструкционных материалов, в большой степени определяющих габариты, вес, жесткость аппаратуры различного назначения - носимой, возимой, бортовой. Это выдвигает перед студентами задачу изучения конструкционных материалов для осознанного, рационального выбора их в процессе разработки конструкций и изготовления изделий.
Раздел "Конструкционные металлы и сплавы РЭС", рассмотренный в данном учебном пособии, является составной частью дисциплины "Материаловедение и материалы радиоэлектронных средств". По учебному плану на изучение этой дисциплины отводится ограниченное аудиторное время, поэтому студенты определенную часть курса должны проработать самостоятельно. Кроме того, в имеющихся пособиях и учебниках по радиоматериалам, предназначенных для обучения студентов по специальности 200800 "Проектирование и технология радиоэлектронных средств" сведения по конструкционным металлам и сплавам или отсутствуют, или освещены недостаточно полно. Цель данного пособия - восполнить пробелы в учебниках и обеспечить студентов дополнительным материалом для самостоятельной работы над курсом.
Пособие содержит 9 глав, в которых рассматриваются конструкционные сплавы на основе железа, титана, магния, алюминия, меди, сплавы для изготовления пружин и материалы для электронновакуумных приборов излагаются сведения о термической и химико-термической обработке. Рассматриваются состав и строение сплавов, влияние различных легирующих элементов на физико-механические свойства, взаимосвязь между структурой и конструкционно-технологическими параметрами, область применения сплавов в конструкциях РЭС. В пособии приведены таблицы, содержащие марки сплавов, наиболее применяемых в изделиях радиоэлектронных средств, их составы и основные механические и технологические параметры. Эти данные могут быть полезными при выполнении курсовых и дипломных проектов.
1. Железоуглеродистые сплавы
Фазовый состав сплава железо-углерод
Диаграмма состояния сплава железо-углерод отображает фазовый состав и структуру сплава в зависимости от температуры и от соотношения компонентов Fe и C.
Чистое железо металла серебристого цвета с температурой плавления 1539 °С, плотностью 7,86 г/м3. Оно известно в двух полиморфных модификациях и : -железо с ОЦК решеткой существует в двух температурных интервалах - от 1392 до 1539 °С (иногда эту ОЦК модификацию обозначают - железом) и при температуре ниже 911 °С. До температуры 768 °С - железо - ферромагнитно, а при температуре 768 °С, которую называют точкой Кюри, происходит магнитное превращение, т.е. железо переходит из ферромагнитного состояния в парамагнитное. - железо существует при температурах 911-1392 °С; оно парамагнитно. Кристаллическая решетка - железа - гранецентрированная кубическая решетка (ГЦК). Железо обладает большим сродством к кислороду, углероду, азоту, сере, фосфору и другим элементам. С металлами железо образует твердые растворы замещения, с углеродом, азотом, водородом - твердые растворы внедрения.
Углерод является неметаллическим элементом. Температура плавления 3500 °С. Углерод полиморфен. В обычных условиях он находится в виде модификации графита, но может существовать и в виде мета стабильной модификации алмаза.
Растворимость углерода в и модификациях железа различна: в -железе его растворяется не более 0,023 %, в -железе значительно больше (до 2,14 %). Сплав железа с углеродом образует твердые растворы, химические соединения и механические смеси. Максимальная растворимость углерода в железе, когда образуются твердые растворы, составляет 2,14 %. Эти сплавы называют сталью, а при содержании выше 2,14 % С - чугуном. При затвердевании чугун имеет в своей структуре хрупкую эвтектику, плохо обрабатываемую давлением, но обладающую хорошими литейными свойствами. Из большого количества сплавов в системе Fe - C в радиоэлектронных средствах находят применение стали. Поэтому мы будем в основном рассматривать те сплавы, в которых содержание углерода менее 2,14 %.
В сплаве Fe – C существуют твердые растворы – феррит, аустенит и химическое соединение - цементит Fe3C.
Феррит (от латинского слова Ferrum - железо) - твердый раствор внедрения С в -железе. Обозначается обычно Ф, или Fe. Атом углерода располагается в решетке феррита в центре грани куба, где помещается сфера радиусом 0,29 атомного радиуса железа R, а также в вакансиях, на дислокациях и т.д. Различают высокотемпературный -феррит с предельной растворимостью углерода 0,1 % и низкотемпературный -феррит с растворимостью углерода 0,02 %. Феррит имеет невысокую прочность (в = 250 МПа) и твердость (НВ =80 - 90), 0,2 =120 МПа, высокую пластичность (=40 %), магнитен, тепло- и электропроводен. На диаграмме состояния Fe – C (рис. 1.1) область чистого высоко- и низкотемпературного феррита ограничена линиями AHN и GPQ соответственно.
Аустенит - твердый раствор внедрения С в -железо. Обозначается аустенит A или Fe (С). Атом углерода в решетке -железа располагается в центре элементарный ячейки, в которой может разместить ся сфера радиусом 0,41 R (R - радиус атома железа) и в дефектных областях кристалла. Предельная растворимость углерода в аустените 2,14 %. Аустенит - немагнитен, имеет большую твердость и прочность, чем феррит, обладает пониженной упругостью и хорошей вязкостью. На диаграмме состояния Fe - C аустенит ограничен линией NJESG.
Цементит - это химическое соединение железа с углеродом - карбид железа Fe3C. Имеет очень сложную ромбоэдрическую кристаллическую решетку с плотной упаковкой атомов. Температура плавления около 1250 °С. Аллотропических превращений не испытывает, но при низких температурах слабо ферромагнитен. Магнитные свойства цементит теряет при 217 °С. К характерным особенностям цементита относятся очень высокая твердость (>800 НВ) и чрезвычайно низкая, практически нулевая, пластичность, что обусловлено, вероятно, сложностью строения кристаллической решетки.
Цементит способен образовывать твердые растворы замещения. Неметаллические элементы, например азот, кислород, могут замещать в цементите углерод; металлы - марганец, хром, вольфрам и др., могут замещать атомы железа. Такой твердый раствор на базе решетки цементита называется легированным цементитом. Обычное обозначение легированного цементита M3C (под М подразумевается железо или другие металлы, замещающие Fe в решетке Fe3C).
Цементит является неустойчивым соединением и может распадаться на железо и углерод в виде графита. Переход цементита в графит играет важную роль при формировании высокоуглеродистых сплавов - чугунов. Состав цементита - 75 % (атомн.) Fe и 25 % (атомн.) С или 6,67 % (по массе) С - остальное железо.
На диаграмме количество С принимается равным содержанию его в цементите (6,67 %), а поскольку цементит представляет собой химическое соединение, то при рассмотрении состояния сплава он принимается самостоятельным компонентом. Поэтому ось абсцисс двойная, на ней отложено со держание С от 0 до 6,67 % и Fe3C от 0 до 100 %. По оси ординат отложены температуры. Если умножить содержание углерода (по верхней оси) на 15, то получим процентное содержание цементита в сплаве по массе.
На диаграмме существуют три горизонтальные линии (HJB, ECF, PSK), указывающие на протекание нонвариантных реакций. При 1499 °С (линия HJB) протекает перитектическая реакция Жв + Фн Аj, в результате которой образуется аустенит. Реакция эта наблюдается у сплавов, содержащих от 0,1 до 0,5 % С.
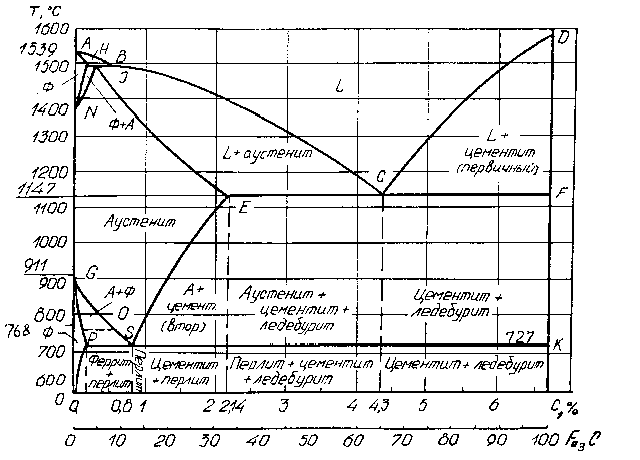
Рис. 1.1. Диаграмма состояния сплава Fe-C
При 1147 °С (линия ЕСF) протекает эвтектическая реакция ЖеАе+Ц, в результате которой образуется эвтектическая смесь из аустенита и цементита, называемая ледебуритом. Реакция протекает у всех сплавов, систем, содержащих углерода более 2,14 %.
При 727 °С (горизонталь РSK) протекает эвтектоидная реакция АsФр + Ц, в результате которой образуется эвтектоидная смесь из феррита и цементита, которая называется перлитом.
Различают пластинчатый и зернистый перлит, т.е. структуру стали, состоящую из феррита и чередующихся пластинок цементита, или структуру, состоящую из феррита и цементита в виде зерен.
Укажем на характерные точки на диаграмме сплава Fe - С. Точка А (1539 °С) на диаграмме соответствует температуре плавления чистого железа, а точка Д (1250 °С) - температуре плавления цементита Fe3c. Точки N (1392 °С) и G (911 °С) соответствуют полиморфному превращению -железа в -железо. Точка Е (1147 °С) характеризует предельную растворимость углерода в - железе (2,14 % С).
Процесс кристаллизации сплавов начинается по достижении температур, соответствующих линии АВСД (линия ликвидус), а конец затвердевания - температурам соответствующих линии AHJE (линия солидус).
Верхний левый угол диаграммы характеризует превращения, связанные с аллотропическим превращением () при высоких температурах. При температурах, соответствующих линии АВ, из жидкости выделяются кристаллы твердого раствора углерода в -железе (-раствор) - феррит (Ф).
В сплавах с содержанием до 0,1 % С кристаллизация заканчивается при температурах, соответствующих линии АН образованием -твердого раствора.
Как указывалось выше, линия HJB - линия перитектического превращения, протекающего при постоянной температуре, в результате которого образуется твердый раствор углерода в - железе, т.е. аустенит (А).
Сплавы, содержащие от 0,1 до 0,16 % С (точки Н и J соответственно), испытывают перитектическое превращение Жв + Фн()Фн + Ад, в результате которого образуется двухфазная структура Ф (-раствор)+А (-раствор). В сплаве, содержащем 0,16 % С (точка J), исходные кристаллы твердого раствора Ф и вся жидкая фаза при перитектичеоком превращении полностью расходуются на образование аустенита: Жв + Фн Аj.
В сплавах, содержащих 0,16 0,5% С, при перитектичеоком превращении Фн расходуется полностью, а жидкая фаза остается в избытке: Жв + Фн Жв + Аj (аустенит). Поэтому при температурах ниже линии JВ сплав будет двухфазным: аустенит ( - твердый раствор) + жидкость. Процесс кристаллизации закончится по достижении температур, соответствующих линии солидус JE. После затвердевания эти сплавы приобретают однофазную структуру - аустенит (А).
Рассмотрим теперь превращения, протекающие в твердом состоянии. Они связаны с переходом при охлаждении - железа в - железо и распадом аустенита. Линия GS на диаграмме соответствует температурам начала превращения - . Ниже этой линии из аустенита выделяется феррит. В области температур, заключенной между линиями GS и GP, существуют кристаллы феррита и аустенита.
Линия ES показывает изменение растворимости углерода в аустените с изменением температуры, а при охлаждении соответствует температурам начала распада аустенита с выделением из него цементита. Цементит, выделяющийся из аустенита, называется вторичным, в отличие от цементита, кристаллизующегося из жидкой фазы при температурах ниже линии СД.
Точка S при температуре 727 °С и концентрации 0,8 % С показывает минимальную температуру равновесного существования аустенита при охлаждении. При достижении 727 °С происходит распад аустенита с образованием эвтектоидной смеси - перлита, представляющего из себя механическую смесь двух фаз – феррита и цементита. Таким образом, перлит содержит 0,8 % углерода. Точка Р характеризует предельную растворимость углерода (0,023 % С) в - железе при эвтектоидной температуре. Линия РQ, на диаграмме показывает изменение растворимости углерода в - железе и выделение избыточного углерода из феррита в виде высокоуглеродистой фазы - цементита, называемого третичным цементитом. Сплавы, концентрация углерода в которых находится в пределах от Q до Р, имеют двухфазную структуру: феррит + третичный цементит, а сплавы левее линии РQ, состоят только из феррита.
Сплавы, содержащие не более 0,02 % С называют техническим железом. Сплавы, содержащие углерод до 0,8 %, называют доэвтектоидными сталями. Сплав с содержанием 0,8 % С называется эвтектоидной сталью. Сплавы, содержащие углерод от 0,8 % до 2,14 %, называются заэвтектоидными сталями.
Доэвтектоидные стали имеют структуру феррита, выделяющегося из аустенита ниже температуры, определяемой линиями Gs и РS, и перлита, образующегося из аустенита при достижении температуры 727 °С (линия РSК). Необходимо отметить, что количество перлитов в доэвтектоидной стали возрастает по мере увеличения углерода, что обусловливает повышение прочности и твердости сплава и снижение пластичности.
Заэвтектоидные стали имеют структуру, состоящую из вторичного цементита, выделившегося из аустенита при температурах ниже линии ЕS, и перлита, образовавшегося в результате распада аустенита при эвтектоидной температуре 727 °С (линия РSК). Выделение цементита в заэвтектоидных сталях существенно повышает прочность заэвтектоидной стали, но одновременно снижает пластичность.
Представленные на диаграмме состояния сплава Fe - C линии и соответствующие им превращения часто обозначаются буквами с присвоенным им номером. Так превращение, происходящее при 727 °С в процессе охлаждения обозначают Ar1; в тех случаях, когда превращение происходит в процессе нагрева, его обозначают Ас1. Точке Ас2 соответствует магнитное превращение при Т = 768 °С в процессе нагрева; точке Аr2 соответствует магнитное превращение, происходящее при охлаждении сплава. Точка Аc3 соответствует определенной температуре при заданном составе при переходе. Обратный переход обозначается точкой Аrз. Точка Ас4 соответствует переходу от кристаллической решетки -аустенита к решетке -феррита. Обратное превращение обозначается точкой Аr4. Критические точки, образующие линию ЕS, обозначают Аcm.
Влияние углерода, примесей и легирующих элементов на
свойства сталей
Промышленные стали не являются бинарными сплавами Fe - C. Помимо основных двух элементов в сталях присутствует ряд постоянных или неизбежных примесей Mn, Si, Al, S, P, O, N, H и др., которые оказывают влияние на ее свойства. Содержание этих примесей колеблется от десятых и сотых до тысячных долей процента и зависит от способа выплавки стали.
Структура стали после медленного охлаждения состоит из двух фаз: феррита и цементита. Количество цементита возрастает в стали прямо пропорционально содержанию углерода. Твердые и хрупкие частицы цементита повышают сопротивление движению дислокаций, т.е. повышают сопротивление деформации и уменьшают пластичность и вязкость. Вследствие этого увеличение содержания углерода приводит к возрастанию твердости (НВ), предела прочности на разрыв (и), предела текучести (0,2) и уменьшению относительного удлинения (), сужения и ударной вязкости (ан) (рис. 1.2).

Рис. 1.2. Влияние углерода на механические свойства стали
С увеличением содержания углерода в стали снижается плотность, растут удельное электрическое сопротивление и коэрцитивная сила, понижаются теплопроводность, остаточная индукция и магнитная проницаемость.
Содержание углерода определяет и технологические свойства сталей: обрабатываемость резанием, давлением и свариваемость. Увеличение углерода в стали вследствие упрочнения и ухудшения теплопроводности ведет к снижению обрабатываемости резанием, увеличивается количество теплоты, которое вызывает отпуск и снижает стойкость инструмента. Низкоуглеродистые вязкие стали также плохо обрабатываются резанием из-за плохой поверхности и трудноудаляемой стружки. Лучше всего обрабатываются резанием стали с содержанием углерода 0,3 0,4 %.
С увеличением углерода снижается технологическая пластичность - способность деформироваться в холодном состоянии. Обычно способность стали к штампуемости оценивается отношением о, 2/в. Для сталей глубокой вытяжки это отношение должно находиться в пределах 0,65 0,7. Такими свойствами обладают стали с содержанием 0,08 0,1 % С (до 0,4 % Мn и не более 0,03 % Si).
Хорошо свариваются стали с содержанием углерода до 0,3 %. Стали с большим содержанием С требуют применения специального подогрева и замедленного охлаждения.
Сера является вредной примесью в стали. С железом она образует химическое соединение FeS, которое практически нерастворимо в Fe в твердом состоянии, но растворимо в жидком металле. Соединение FeS образует с железом легкоплавкую эвтектику (температура плавления 988 °С), которая образуется при очень малом содержании серы. При нагревании стали до температуры прокатки, эвтектика расплавляется, нарушается связь между зернами металла, и вследствие этого при деформации стали в местах расположения эвтектики возникают надрывы и трещины. Это явление носит название красноломкости. Сернистые включения сильно снижают механические свойства, особенно пластичность (, ) (в поперечном направлении вытяжки при прокатке), ударную вязкость (ан), а также предел выносливости. Кроме того, сернистые включения ухудшают свариваемость и коррозийную стойкость. Поэтому содержание серы в стали в зависимости от качества не должно превышать 0,035 + 0,06 %.
Фосфор может растворяться в и - железе и при высоком содержании (более 1,0 %) образует фосфид железа Fe3P. Растворяясь в феррите, фосфор искажает кристаллическую решетку, увеличивая предел прочности на растяжение и предел текучести, но сильно снижает пластичность и вязкость. Фосфор повышает порог хладоломкости и уменьшает работу развития трещины. Каждые 0,01 % Р повышают порог хладоломкости примерно на 25 °С. Фосфор, как и сера, является вредной примесью для большинства сталей и содержание Р не должно превышать в сталях 0,025 0,08 %. Однако допускается содержание S и Р до 0,1 0,2 % в сталях, обрабатываемых на токарных станках-автоматах.
Азот и кислород присутствуют в стали в виде хрупких неметаллических включений (FeO, Fe4N др.), твердых растворов, которые располагаются в раковинах, трещинах и других дефектных участках. Концентрируясь по границам зерен, кислород и азот повышают порог хладоломкооти, понижают сопротивление хрупкому разрушению и снижают предел выносливости стали. Водород при повышенных количествах скапливается в микрообъемах внутри стальных изделий, создает высокие давления и вызывает внутренние трещины, резко ухудшает свойства стали, а при сварке способствует образованию холодных трещин.
Для нейтрализации вредных примесей при производстве сталей вводят добавки. Марганец вводят в любую сталь для нейтрализации кислорода и серы (кипящая сталь), в результате улучшается пластичность сталей. Такие стали называют кипящими и при маркировке обозначают кп.
Сталь спокойная получается при введении раскислителей Mn, Si, Al в определенных пределах. Она является наиболее качественной и обозначается при маркировке сп. Полуспокойная сталь (пс) по качеству занимает промежуточное положение между кипящей и спокойной и для раскисления ее вводят Mn и Al.
Все химические элементы, содержащиеся в стали, разделяют на 4 вида:
постоянные, примеси Mn, Al, Si применяемые в качестве раскислителей при производстве стали, а также сера и фосфор, полностью освободиться от которых при массовом производстве невозможно;
скрытые примеси (0, N, Н), присутствующие в любой стали в очень малых количествах;
случайные примеси, попадающие в сталь из шихты (Cu, As и др.), содержание и вид этих примесей зависит от вида руды, из которой выплавляют сталь;
легирующие элементы, специально вводимые в сталь в определенных концентрациях с целью изменения ее строения и свойств.
Стали, в которые вводят легирующие элементы для придания определенных свойств, называют легированными сталями.
В промышленных легированных сталях, которые являются многокомпонентными системами, легирующие элементы могут находиться:
в свободном состоянии и в форме интерметаллических соединений с железом или между собой;
в виде оксидов, сульфидов и других неметаллических включений;
в карбидной фазе – в виде раствора в цементите или в виде самостоятельных соединений с углеродом – специальных карбидов;
в форме раствора в железе.
В любом случае легирующие элементы растворяются во всех основных фазах сплава Fe - C: в феррите, аустените, цементите, или образуют специальные карбиды, имеющие отличную от цементита формулу и кристаллическую решетку.
Легирующие элементы по влиянию на температурную область существования полиморфных модификаций железа разделяют на две группы.
К элементам первой группы относят Ni и Mn. Они понижают температуру превращения и повышают температуру превращения (точки А3 и А4 соответственно), (рис. 1.3, а). При повышенной концентрации легирующих элементов Ni и Mn стали не испытывают фазовых превращений и при всех температурах представляют твердый раствор легирующего элемента в - железе. Такие сплавы называют аустенитными. Сплавы с легирующими элементами Ni и Mn, частично претерпевающие превращения называют полуаустенитными
Элементы второй группы (Cr, W, Mo, V, Si, Al) понижают точку превращения А4 и повышают точку А3. Это приводит к тому, что при определенной концентрации легирующих элементов критические точки (точнее их интервалы А4 и А3) сливаются, и область -фазы полностью замыкается (рис.1.3, б). Сплавы при всех температурах состоят из твердого раствора легирующего элемента в - железе. Такие сплавы называют ферритными, а сплавы, имеющие лишь частичное превращение, называют полуферритными.
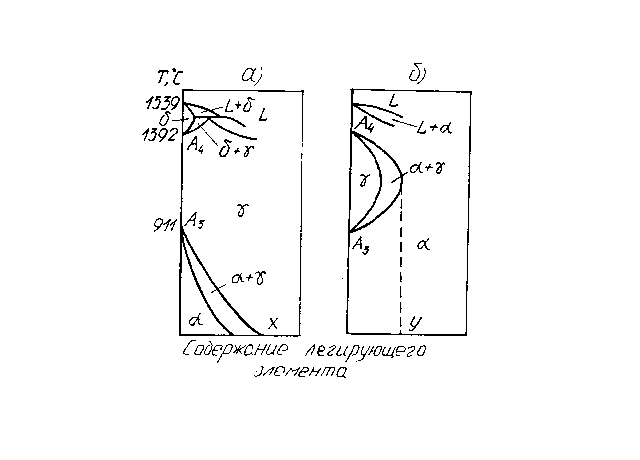
Рис. 1.3. Влияние легирующих элементов на полиморфизм железа
Легирующие элементы, растворимые в феррите, повышают его временное сопротивление (в), не изменяя существенно относительное удлинение (), за исключением марганца и кремния, которые при содержании их > 2,5 3,0 %, снижают пластичность. Легирующие элементы при введении их в сталь около 1 2 % снижают ударную вязкость, а при более высоком содержании повышают порог хладоломкости. Исключение составляет Ni, который упрочняет феррит, одновременно увеличивает его ударную вязкость и понижает порог хладоломкости. Этим объясняются высокие вязкие свойства сталей, содержащих Ni.
Легирующие элементы, растворяясь в -железе, повышают прочность аустенита при нормальной и повышенной температурах. Для аустенита характерны низкий предел текучести при сравнительно высоком значении предела прочности на разрыв. Упрочнение аустенитных сталей легко достигается также в результате пластической деформации.
Как указывалось выше, легирующие элементы в сплаве Fe - C образуют карбидные фазы. Карбиды, образующиеся в легированных сталях, делятся на две группы.
К первой группе относятся карбиды типа Me3C, Me7C3, Me23C6, Me6C (Mn3C, Cr7C3, Cr23C6, Fe3W3C, и др.), имеющие сложные кристаллические решетки. Карбиды этой группы хорошо растворяются в аустените при нагреве.
Ко второй группе относятся карбиды типа MeC, Me2C (TiC, NGC, TaC, ZrC, Mo2C, W2C, Ta2C), имеющие более простую кристаллическую решетку (объемно-центрированную кубическую или гексагональную). Эти карбиды относятся к фазам внедрения.
Фазы внедрения трудно растворимы в аустените при нагреве в отличие от карбидов первой группы. Это значит, что при нагреве они могут не перейти в твердый раствор. Фазы внедрения обладают наиболее высокой твердостью и высокой температурой плавления. Чем выше дисперсность частиц карбидов в стали, тем выше ее прочность и твердость.
Если количество легирующих элементов в стали очень велико, то они образуют с железом или один с другим интерметаллические соединения, например, Fe7Mo6, Fe7W6, Fe3Nb2, Fe3Ti и др. Многие из интерметаллических соединений оказывают благоприятное воздействие на упрочнение стали, когда они выделяются в процессе старения. Но некоторые из интерметаллических соединений, например FeCr, FeV, являются нежелательными, так как вызывают охрупчивание стали.
Конструкционные стали общего назначения
Классификация сталей и общие требования, предъявляемые к ним
Стали классифицируют по химическому составу, качеству, способу производства, структуре, назначению.
В зависимости от химического состава конструкционные стали общего назначения разделяются на углеродистые и легированные. К углеродистым сталям относятся сплавы системы Fe - C, у которых содержание постоянных (Mn, Si, P, S) и случайных примесей (Cr, Ni, Cu) незначительно, а легирующие элементы отсутствуют. Легированными сталями называют такие, в которые вводятся легирующие компоненты Cr, Mo, W, Ni, Mn, V, Ti и др.
По содержанию легирующих элементов легированные стали подразделяются на низколегированные (содержание легирующих элементов 5 %), среднелегированные (5 10 %), высоколегированные (блее 10 % ).
Как углеродистые, так и легированные стали делятся на низкоуглеродистые (менее 0,25 % С), среднеуглеродистые (0,25 0,6 % С) и высокоуглеродистые (более 0,6 % С).
По способу производства стали разделяют на мартеновские, конверторные, бессемеровские и электростали. Наиболее качественной сталью, содержащей наименьшее количество вредных примесей Р и 3, является сталь, полученная в электропечах и мартеновских печах. Сталь, полученная бессемеровским способом, содержит не удаляемые примеси 0, N, Н, вносимые воздухом. По характеру раскисления стали делят на спокойные (сп), полуспокойные (пс) и кипящие (кп). По структуре, формирующейся в условиях равновесия, как нелегированные, так и легированные стали делятся на доэвтектоидные, эвтектоидные и заэвтектоидные. Доэвтектоидные стали имеют в структуре стали избыточный феррит. Эвтектоидные стали имеют перлитную структуру. Заэвтектоидные стали имеют в структуре избыточные (вторичные) карбиды.
По назначению (применению) стали подразделяют на конструкционные, инструментальные и стали со специальными свойствами, например, коррозионно-стойкие, жаропрочные, износостойкие и др.
В свою очередь, конструкционные стали разделяют на углеродистые обыкновенного качества, качественные углеродистые и легированные конструкционные.
При производстве радиоэлектронных средств применение сталей в элементах несущих конструкций достаточно большое, особенно там, где необходима высокая прочность и не предъявляются жесткие требования по весу.
К конструкционным сталям предъявляется комплекс механических и технологических требований. Стали должны иметь высокие механические свойства: предел прочности на растяжение в, предел текучести 0,2, относительные удлинение и сужение , , твердость НВ. Конструкционные стали должны обладать и хорошими технологическими свойствами: легко обрабатываться резанием, давлением (штамповка, прокатка и т.д.), хорошо свариваться; иметь малую склонность к деформациям и трещинообразованию при закалке и т.д. Следует напомнить, что предел прочности в и текучести 0,2 характеризуют прочность; относительное сужение и относительное удлинение характеризуют пластичность; ударная вязкость ан и порог хладоломкости Т50 (температура полухрупкости) показывают значение вязкости и характеризуют надежность конструкционного материала.
Износостойкость, коррозионная стойкость, выносливость (усталостная прочность), жаропрочность характеризуют долговечность.
1.3.2. Углеродистые стали обыкновенного качества
Углеродистые стали обыкновенного качества имеют свойства, гарантируемые ГОСТ 380-88. При выплавке они меньше очищаются от вредных примесей и содержат больше серы и фосфора, чем качественные углеродистые стали. Их отливают в крупные слитки, вследствие чего в них значительно развита ликвация и они часто содержат большое количество неметаллических включений.
ГОСТ 380-88 предусматривает поставку стали трех групп.
Группа А - с гарантируемыми механическими свойствами. Эта сталь используется в том случае, если при изготовлении изделия не подвергают горячей обработке (сварке, ковке и т.д.). Структура и свойства, которые сталь получила при изготовлении на металлургическом заводе, сохраняются и у потребителя.
Группа Б - с гарантируемым химическим составом. Эта сталь используется в том случае, если будет подвергаться горячей обработке (сварке, горячей штамповке и т.д.). В данном случае исходная структура и механические свойства не сохраняются. Для потребителя основное значение приобретает химический состав стали, который определяет режим горячей обработки и конечные механические свойства.
Группа В - с гарантируемыми механическими свойствами и химическим составом. Применяется в том случае, если сталь подвергается сварке. В зоне теплового влияния шва свойства металла изменяются и потребителю важно знать химический состав, который определяет свойства стали в зоне нагрева и режим сварки. Кроме того, потребителю необходимо знать исходные механические свойства металла, не подвергаемые тепловому нагреву при сварке, которые при этом не меняются.
Углеродистые стали обыкновенного качества обозначаются при маркировке буквой Ст (сталь) и цифрами 1,2,3,...,6, указывающими на номер стали. Чем больше цифра, тем больше содержание углерода в стали, тем выше прочность (в, 0,2,) и ниже пластичность (). Если после марки стали стоит кп - значит сталь кипящая, если сп - спокойная, если пс - полуспокойная. В табл.1.1 приведены механические свойства сталей группы А, а в табл.1.2 - химический состав стали группы Б (Гост 380-88). При маркировке сталей группы Б и В перед Ст ставятся соответственно буквы Б и В; при маркировке сталей группы А буква А не указывается. Стали группы В имеют гарантированные механические свойства такие же, как в табл.1.1, а химический состав, как сталь группы Б (табл.1.2).
Из углеродистой стали обыкновенного качества изготавливают несущие конструкции РЭС, работающие при относительно невысоких напряжениях, а также малоответственные детали (оси, валы, шестерни, втулки, болты, гайки и т.д.), не подвергающиеся термической обработке.
Таблица 1.1
