
- •1. Исследование лекарственных средств, стерилизуемых в процессе производства.
- •2. Как производится посев на стерильность: в каких количествах, на какие питательные среды, условия и время инкубации, оценка результатов.
- •3. Что такое пирогенность воды и лекарственных средств, отчего она может возникнуть?
- •4. Почему наличие пирогенности инъекционных растворов недопустимо?
- •5. Каким способом определяют пирогенность воды и лс?
- •6. Исследование лекарственных средств, не стерилизуемых в процессе производства: какие показатели определяются?
- •7. Методика определения общего количества бактерий, общего количества грибов.
- •8. Наличие, каких микробов не допускается в лекарственных средствах? Методика их выявления и идентификации.
Занятие 10 Тема: «Санитарно-микробиологический контроль в фармацевтических учреждениях. Микробиологический контроль лекарственного сырья и готовых лекарственных средств (окончание)»
1. Исследование лекарственных средств, стерилизуемых в процессе производства.
Л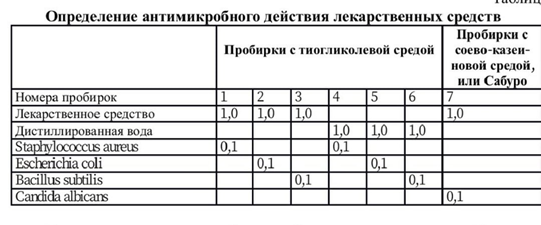 С
для инъекций, глазные капли, мази, плёнки,
другие ЛС, в отношении которых имеются
соответствующие указания в
нормативно-технической документации
(НТД), д.б. стерильными. Отбор
образцов для анализа.
Число образцов из каждой серии от 3 до
40, в зависимости от метода стерилизации,
для автоклавированных средств - 10. Для
исследования ЛС д. б. приготовлены в
виде растворов, суспензий или эмульсий.
Определение
антимикробного действия ЛС.
Во избежание неправильной оценки
результатов анализа необходимо определить
однократно для каждого наименования
ЛС обладает ли оно антимикробным
действием. Для определения антимикробного
действия из ампулы с ЛС следует внести
по 1 мл в 3 пробирки с 10 мл тиогликолевой
среды и в 1 пробирку с 10 мл жидкой
соево-казеиновой среды или среды Сабуро.
Для контроля в 3 пробирки с тиогликолевой
средой и в пробирку с 10 мл жидкой
соево-казеиновой среды или среды Сабуро
вносится по 1 мл стерильной дистиллированной
воды (табл.). Затем во все пробирки следует
внести по 0,1 мл взвеси тест-штамма,
содержащего 1000 клеток в 1 мл. В пробирки
с тиогликолевой средой вносятся штаммы
Staphylococcus aureus; Bacillus subtilis; Escherichia coli; в
пробирки с соево-казеиновой средой или
средой Сабуро - Candida albicans.
С
для инъекций, глазные капли, мази, плёнки,
другие ЛС, в отношении которых имеются
соответствующие указания в
нормативно-технической документации
(НТД), д.б. стерильными. Отбор
образцов для анализа.
Число образцов из каждой серии от 3 до
40, в зависимости от метода стерилизации,
для автоклавированных средств - 10. Для
исследования ЛС д. б. приготовлены в
виде растворов, суспензий или эмульсий.
Определение
антимикробного действия ЛС.
Во избежание неправильной оценки
результатов анализа необходимо определить
однократно для каждого наименования
ЛС обладает ли оно антимикробным
действием. Для определения антимикробного
действия из ампулы с ЛС следует внести
по 1 мл в 3 пробирки с 10 мл тиогликолевой
среды и в 1 пробирку с 10 мл жидкой
соево-казеиновой среды или среды Сабуро.
Для контроля в 3 пробирки с тиогликолевой
средой и в пробирку с 10 мл жидкой
соево-казеиновой среды или среды Сабуро
вносится по 1 мл стерильной дистиллированной
воды (табл.). Затем во все пробирки следует
внести по 0,1 мл взвеси тест-штамма,
содержащего 1000 клеток в 1 мл. В пробирки
с тиогликолевой средой вносятся штаммы
Staphylococcus aureus; Bacillus subtilis; Escherichia coli; в
пробирки с соево-казеиновой средой или
средой Сабуро - Candida albicans.
Посевы в тиогликолевой среде инкубируют при 30-35ºС в течение 2 сут., а на соевоказеиновой среде, или среде Сабуро, - при 20-25ºС в течение 3 сут. При отсутствии антимикробного действия ЛС в опытных и контрольных пробирках должен наблюдаться рост перечисленных тест-микробов. В этом случае можно продолжать исследование и провести прямой посев данного ЛС на стерильность.
2. Как производится посев на стерильность: в каких количествах, на какие питательные среды, условия и время инкубации, оценка результатов.
Методы испытания стерильности. Испытание на стерильность проводят 2мя методами: методом прямого посева или методом мембранной фильтрации. Метод мембранной фильтрации используют во всех случаях, когда природа препарата, его физико-химические свойства позволяют фильтровать его через мембранные фильтры. Метод прямого посева используют для испытания на стерильность ЛС, не обладающих антимикробным действием или антимикробное действие которых можно устранить разведением или инактивированием, а также для препаратов, испытание которых невозможно выполнить методом мембранной фильтрации.
При испытании на стерильность параллельно проводятся соответствующие отрицательные контроли.
П осев
ЛС на стерильность (метод прямого
посева).
Испытуемый препарат, если необходимо,
растворяют в соответствующем растворителе
и высевают в количествах, указанных в
табл. Количество испытуемого препарата
для посева в зависимости от объёма
содержимого одной единицы (ампул,
флаконов), составляющих серию. Посевы
с тиогликолевой средой инкубируют при
т. от 30 до 35°C, а в соево-казеиновой среде,
или среде Сабуро, - от 20 до 25°С. Продолж.
инкубации посевов в обеих питательных
средах составляет 14 суток. Если во всех
посевах роста нет, Лп стерилен.
осев
ЛС на стерильность (метод прямого
посева).
Испытуемый препарат, если необходимо,
растворяют в соответствующем растворителе
и высевают в количествах, указанных в
табл. Количество испытуемого препарата
для посева в зависимости от объёма
содержимого одной единицы (ампул,
флаконов), составляющих серию. Посевы
с тиогликолевой средой инкубируют при
т. от 30 до 35°C, а в соево-казеиновой среде,
или среде Сабуро, - от 20 до 25°С. Продолж.
инкубации посевов в обеих питательных
средах составляет 14 суток. Если во всех
посевах роста нет, Лп стерилен.
Метод мембранной фильтрации. При определении стерильности ЛС, обладающих антимикробным действием, и ЛС, разлитых в ёмкости больше 100 мл, используют метод мембранной фильтрации. ЛС фильтруют в асептических условиях через 2 стерильных мембранных фильтра, затем смывают 3-4 порциями по 100 мл физ. раствора. Каждую мембрану стерильными ножницами разрезают пополам, половину помещают в тиогликолевую среду, половину - в жидкую соево-казеиновую среду, или среду Сабуро. Посевы выдерживают в термостате при тех же температурах в течение 7 суток при ежедневном просмотре. Для контроля полноты смывания другую мембрану разрезают пополам и по половине мембраны помещают в питательные среды, куда засевают тест-микробы: Staphylococcus aureus и Candida albicans. Наличие роста этих микробов после инкубации в термостате указывает на полноту смывания. Для контроля стерильности условий фильтрования производят фильтрование растворителя, и фильтры засевают в те же питательные среды.
В отношении ЛС, не стерилизуемых в процессе производства, проводится испытание на микробиологическую чистоту. Это испытание включает в себя количественное определение жизнеспособных бактерий и грибов, а также выявление определённых видов микроорганизмов, наличие которых недопустимо в нестерильных ЛС. Испытание проводят в асептических условиях. ЛС, обладающие антимикробным действием, и консерванты, входящие в состав некоторых лс, могут подавлять рост отдельных видов микроорганизмов при проведении испытаний. Во избежание неправильной оценки результатов испытания определяют действие ЛС в отношении тест-микробов. Для испытания антимикробного действия ЛС, не стерилизуемого в процессе производства, применяют тест-микробы: B. subtilis, B. cereus, E. coli, S. aureus, Salmonella abony, Candida albicans, Aspergillus. Предварительно готовят разведения ЛС: 1:10, 1:50, 1:100, 1:500, 1:1000. В пробирки с питательными средами вносят по 1 мл каждого разведения, в контрольные пробирки - по 1 мл стерильной дистиллированной воды. Затем во все пробирки вносят по 0,1 мл микробной взвеси тест-штамма. При обнаружении антимикробного действия ЛС устраняют его и после этого производят посев на микробиологическую чистоту. При отсутствии антимикробного действия производят прямой посев. Количественное определение бактерий и грибов проводят двухслойным агаровым методом в чашках Петри.
Определение общего числа бактерий. Испытуемый раствор вносят по 1 мл в каждую из 2 пробирок с 4 мл расплавленного и охлаждённого до 45-50°C МПА. Быстро перемешивают содержимое каждой пробирки и переносят в чашку Петри, содержащую 15-20 мл застывшего агара. Быстрым, осторожным покачиванием чашки Петри равномерно распределяют верхний слой агара.
