
- •1. Какие объекты в аптеках подвергаются микробиологическому исследованию?
- •2. Кто проводит эти исследования?
- •3. Расскажите обо всех исследуемых объектах: отбор проб, методика исследования, какие показатели определяются, какие требования предъявляются?
- •4. Каковы источники и пути загрязнения микробами растительного лекарственного сырья?
- •5. Правила хранения лекарственного сырья. Чем опасно микробное обсеменение лекарств?
- •6. На какие категории делятся лекарственное сырьё в зависимости от требований к их микробной чистоте?
- •7. Исследования лекарственных средств, стерилизуемых в процессе производства: какие показатели определяются?
- •8. Для чего проводится предварительное определение антимикробной активности лекарственных средств? Как оно проводится, с какими тест-микробами, на каких питательных средах, как оценивается результат?
- •9. Что нужно сделать при наличии антимикробного действия, какими способами?
2. Кто проводит эти исследования?
Микробиологический контроль проводится 2 раза в квартал сертифицированными бактериологическими лабораториями Территориального Управления Роспотребнадзора и бактериологическими лабораториями инспекции по контролю за качеством лекарств.
3. Расскажите обо всех исследуемых объектах: отбор проб, методика исследования, какие показатели определяются, какие требования предъявляются?
Лекарственные средства для инъекций, глазные капли, мази, плёнки, другие лекарственные средства, в отношении которых имеются соответствующие указания в нормативно-технической документации (НТД), должны быть стерильными.
Отбор образцов для анализа. Число образцов из каждой серии от 3 до 40, в зависимости от метода стерилизации, для автоклавированных средств - 10. Для исследования лекарственные средства должны быть приготовлены в виде растворов, суспензий или эмульсий.
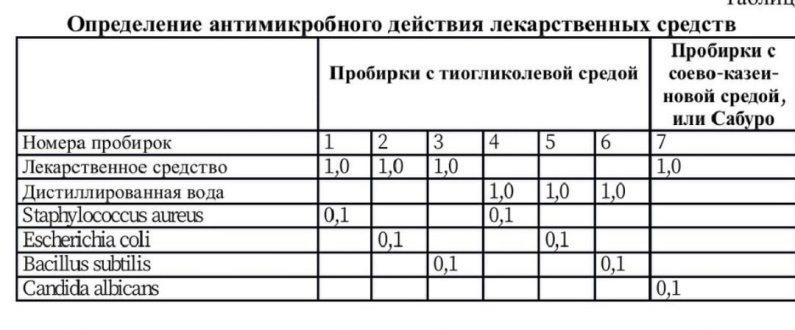
Определение антимикробного действия лекарственного средства. Во избежание неправильной оценки результатов анализа необходимо определить однократно для каждого наименования лекарственного средства обладает ли оно антимикробным действием. Для определения антимикробного действия из ампулы с лекарственным средством следует внести по 1 мл в 3 пробирки с 10 мл тиогликолевой среды и в 1 пробирку с 10 мл жидкой соево-казеиновой среды или среды Сабуро. Для контроля в 3 пробирки с тиогликолевой средой и в пробирку с 10 мл жидкой соево-казеиновой среды или среды Сабуро вносится по 1 мл стерильной дистиллированной воды (табл.). Затем во все пробирки следует внести по 0,1 мл взвеси тест-штамма, содержащего 1000 клеток в 1 мл. В пробирки с тиогликолевой средой вносятся штаммы Staphylococcus aureus; Bacillus subtilis; Escherichia coli; в пробирки с соево-казеиновой средой или средой Сабуро - Candida albicans. Посевы в тиогликолевой среде инкубируют при 30-35ºС в течение 2 суток, а на соевоказеиновой среде, или среде Сабуро, - при 20-25ºС в течение 3 суток. При отсутствии антимикробного действия лекарственного средства в опытных и контрольных пробирках должен наблюдаться рост перечисленных тест-микробов. В этом случае можно продолжать исследование и провести прямой посев данного лекарственного средства на стерильность.
 ??????
??????
4. Каковы источники и пути загрязнения микробами растительного лекарственного сырья?
Источники микробного загрязнения: • воздух помещений. Известно, что 1 л воздуха в большом городе содержит от 1 тыс. до 1 млн. разных частиц, которые являются носителями микрофлоры – один микроорганизм приходится на 1000 взвешенных частиц; • исходные лекарственные и вспомогательные вещества животного, растительного и синтетического происхождения (например, сильно контаминированы – панкреатин, пепсин, глюкоза, тальк, крахмал, агар и др.); • дисперсионные среды, в том числе вода очищенная, микробная контаминация которой происходит при транспортировке, хранении; • вспомогательные материалы (фильтрующие – вата, бумага, марля; упаковочные – бумага, флаконы, банки, коробки, пробки); • человек. В спокойном состоянии человек в 1 мин выделяет до 200 тыс. разных частиц (чешуйки, клетки эпидермиса и др.), при движении – до 1 млн., поэтому присутствие в торговом зале аптеки значительного количества посетителей, занос извне пыли, грязи приводит к увеличению в воздухе микрофлоры, проникающей и в производственные помещения; • персонал аптеки. Даже в специальной одежде в чистых помещениях в окружающую среду сотрудники выделяют до 2 млн. частиц размером от 0,5 мкм до 5 мкм, 300 тыс. частиц размером 5 мкм и более 160 частиц, на которых находятся микроорганизмы. • Источники загрязнения в основном – рот и нос. При разговоре количество частиц, выделяемых человеком, возрастает; • технологический процесс (оборудование, приборы, аппараты).
