
- •1. Рабочая программа по дисциплине «Техническая термодинамика»
- •2. Рабочая программа, методическое обеспечение по дисциплине «Прикладная термодинамика»
- •3.Конспект лекций
- •4. Методические указания и пример расчета газового цикла теплового двигателя
- •5.Задачи с примерами решений
- •6. Варианты домашнего задания по расчету газового цикла теплового двигателя
- •1.4. Контрольные вопросы к зачету.
- •3.1. Термодинамика
- •3.1.1. Содержание и метод термодинамики
- •3.1.2. Основные понятия термодинамики
- •3.1.3. Газовые смеси
- •3.1.4. Законы идеальных газов
- •3.1.5. Первое начало термодинамики
- •3.1.5.1. Первое начало термодинамики как математическое
- •3.1.5.2. Первое начало термодинамики простого тела
- •3.1.6. Понятие теплоёмкости
- •3.1.7.Первое начало термодинамики для идеальных газов
- •3.1.7.1. Закон Майера
- •3.1.7.2. Принцип существования энтропии идеального газа
- •3.1.8. Термодинамические процессы
- •3.1.8.1. Классификация термодинамических процессов
- •3.1.8.2. Работа в термодинамических процессах
- •3.1.9. Круговые процессы (циклы)
- •3.1.9.1. Тепловые машины, понятие термического к.П.Д.,
- •3.1.9.2. Цикл Карно
- •3.1.10. Второе начало термодинамики
- •3.1.11. Термодинамические циклы двигателей внутреннего сгорания
- •3.1.11.1. Циклы поршневых двигателей внутреннего сгорания
- •3.1.11.2. Циклы газотурбинных установок
- •3.1.12.Водяной пар
- •3.1.13.Влажный воздух
- •3.1.14.Истечение сжимаемых и несжимаемых жидкостей
- •3.1.14.1. Истечение несжимаемых жидкостей
- •3.1.14.2.Истечение сжимаемых жидкостей (газов и паров)
- •4. Методические указания и пример расчета газового цикла теплового двигателя
- •3 .Рй цикл в координатах t-s цикл в координатах t-s
- •5.Задачи с примерами решений
- •5.1.Параметры состояния и основные газовые законы
- •Задачи для самостоятельного решения
- •5.2. Газовые смеси
- •Задачи для самостоятельного решения
- •5.3. Первое начало термодинамики
- •Задачи для самостоятельного решения
- •5.4. Процессы изменения состояния вещества Примеры решения задач
- •Задачи для самостоятельного решения
- •5.5. Пары Примеры решения задач
- •Задачи для самостоятельного решения
- •5.6. Циклы тепловых машин Примеры решения задач
- •Определение параметров пара в крайних точках цикла
- •Определение термического кпд цикла
- •Задачи для самостоятельного решения
- •5.7. Истечение газов и паров Примеры решения задач
- •Задачи для самостоятельного решения
- •6.Варианты домашнего задания по расчету газового цикла теплового двигателя Состав газовых смесей
- •Исходные данные к расчету газового цикла
- •625003, Г. Тюмень, ул.Семакова, 10.
5.2. Газовые смеси
Пример 5.2.1. По данным анализа установлен следующий объемный состав природного газа:
![]()
![]()
![]()
![]()
![]()
![]()
Определить среднюю молекулярную массу природного газа μт, плотность газа в нормальных условиях ρ, массовые концентрации компонентов тi, их парциальные давления Pi; средние теплоемкости Cpm, Cvm и показатель адиабаты k.
Решение
Молекулярные массы составляющих смесь газов равны (по данным физических характеристик компонентов газа из справочных таблиц):
![]()
Молекулярная масса природного газа определяется по уравнению
 ,
(3.1.13)
,
(3.1.13)
где μi — молекулярная масса компонентов смеси, CH4, C2H6, C3H8 и т. д.; ri — молярная (или объемная) концентрация компонентов смеси, определяемая как отношение объема компонента к объему смеси; тi -массовая концентрация компонентов смеси, определяемая как отношение массы данного компонента к массе смеси в целом.
Так как в условии задачи дан объемный состав газа, то удобнее воспользоваться первым уравнением соотношения (3.1.13)
![]()
![]() кг/кмоль.
кг/кмоль.
Плотность газа при нормальных условиях (0°С и 0,1 МПа) можно определить из уравнения Клапейрона Рυ=Р/ρ=R/T или из закона Авогадро, утверждающего, что удельный молярный объем газа в нормальных условиях величина постоянная и равна
![]() м3/кмоль,
м3/кмоль,
![]() кг/м3.
кг/м3.
По уравнению Клапейрона при t = 0°C и Р = 0,1 МПа
![]() кг/м3,
кг/м3,
![]() Дж/(кг∙К).
Дж/(кг∙К).
Массовые и объемные концентрации газа связаны между собой соотношением
![]() (3.1.14)
(3.1.14)
отсюда
![]() (3.1.15)
(3.1.15)
Следовательно, массовые концентрации отдельных компонентов смеси равны:
![]() ,
,
![]()
![]()
![]()
![]()
![]()
Так что массовый состав газа в процентах равен:
![]()
![]()
Сумма массовых концентраций, как и молярных (объемных), равна единице:
![]() (3.1.17)
(3.1.17)
Парциальные давления отдельных компонентов газа определяются по закону Дальтона из соотношения
![]() (3.1.18)
(3.1.18)
Так что давление метана CH4, этана C2H6 и т. д. в смеси равно:
![]() МПа,
МПа,
![]() МПа,
МПа,
![]() МПа,
МПа,
![]() МПа,
МПа,
![]() МПа,
МПа,
![]() МПа.
МПа.
Сумма парциальных давлений равна давлению смеси
![]() МПа.
МПа.
Средняя теплоемкость смеси определяется по уравнениям:
массовая теплоемкость смеси
![]() (3.1.19)
(3.1.19)
молярная теплоемкость смеси
![]() (3.1.20)
(3.1.20)
где
![]() — массовая
теплоемкость компонентов смеси при
данной температуре;
— массовая
теплоемкость компонентов смеси при
данной температуре;
![]() —
молярная теплоёмкость компонентов
смеси при данной температуре.
—
молярная теплоёмкость компонентов
смеси при данной температуре.
При
температуре 0 °С и давлении 0,1 МПа можно
принять, что теплоемкость метана
![]() =
2,17 кДж/кг∙К, этана
=
2,17 кДж/кг∙К, этана
![]() =
1,65 кДж/кг∙К, пропана
=
1,65 кДж/кг∙К, пропана
![]() =
1,56кДж/кг∙К, бутана
=
1,56кДж/кг∙К, бутана
![]() =
1,58 кДж/кг∙К, углекислого газа
=
1,58 кДж/кг∙К, углекислого газа
![]() =
0,815 кДж/кг∙К, азота
=
0,815 кДж/кг∙К, азота
![]() =1,039
кДж/кг∙К. Следовательно, массовая
теплоемкость смеси (при постоянном
давлении) равна
=1,039
кДж/кг∙К. Следовательно, массовая
теплоемкость смеси (при постоянном
давлении) равна
![]()
![]() кДж/кг∙К.
кДж/кг∙К.
Молярная теплоемкость смеси газов при постоянном давлении
![]() кДж/кмоль∙К.
кДж/кмоль∙К.
Из
уравнения Майера
![]() можно найти теплоемкости смеси при
постоянном объеме
можно найти теплоемкости смеси при
постоянном объеме
![]()
![]() кДж/кг∙К,
кДж/кг∙К,
![]() кДж/кг∙К.
кДж/кг∙К.
Из сопоставления численных значений теплоемкостей можно определить показатель адиабаты природного газа указанного состава (как идеального газа)
![]() .
.
Пример 5.2.2. Критическая температура н-бутана Ткр=425,2 К и критическое давление Ркр=37,5 атм. Определить удельный объем н-бутана при температуре 80 0С и давлении 10 кг/см2.
Решение
а) Определяем приведенную температуру и приведенное давление
![]() ,
,
![]() .
.
б) По графику рис. 3.1.2 определяем коэффициент сжимаемости z=0,825.
в)
удельный объем определяем из уравнения
![]() откуда
откуда
![]() м3/кг.
м3/кг.
Пример 5.2.3. Определить вязкость водорода и вязкость двуокиси углерода при температуре 200 0С и нормальном давлении.
Решение
Вязкость названных газов определяем по уравнению Сутерланда
![]()
Таблица 3.1.2
Значение коэффициента С в уравнении Сутерланда для различных газов
Наименование газов |
С |
Наименование газов |
С |
метан |
164 |
пентан |
382,8 |
ацетилен |
198,2 |
водород |
73 |
этилен |
225 |
азот |
103,9 |
этан |
252 |
кислород |
126,6 |
пропилен |
321,6 |
воздух |
106,8 |
пропан |
278 |
окись углерода |
101,2 |
1-бутилен |
328,9 |
двуокись углерода |
254 |
2-бутилен |
362,1 |
двуокись серы |
306 |
и-бутилен |
339 |
сероводород |
331 |
и-бутан |
368 |
водяной пар |
673 |
н-бутан |
377,4 |
|
|
Вязкость водорода и двуокиси углерода при нормальной температуре равна: водорода 84∙10-7н∙сек/м2 и двуокиси углерода 136,75∙10-7 н∙сек/м2, а из табл. 3.1.2 значение равно 73 и 254.
Вязкость Н2 при 2000С:
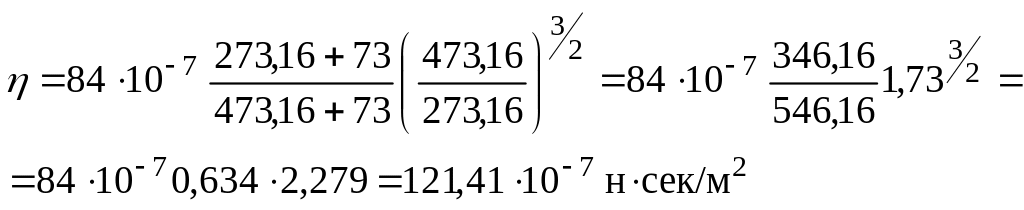
Тем же приемом определяем для СО2 η = 225,8∙10-7 н∙сек/м2.
Пример 5.2.4. Атмосферный воздух имеет примерно следующий массовый состав: тО2=23,2%; тN2=76,8%.
Определить объемный состав воздуха, его газовую постоянную, кажущуюся молекулярную массу и парциальные давления кислорода и азота, если давление воздуха по барометру р=101325 Па.
Решение
По уравнению получаем
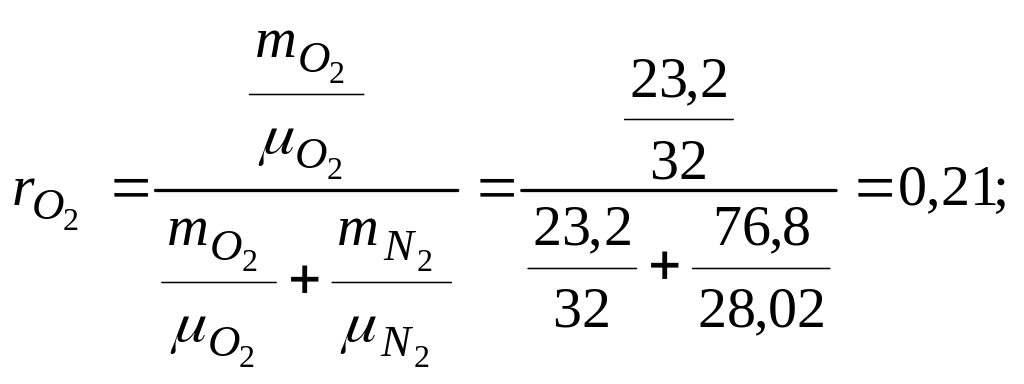
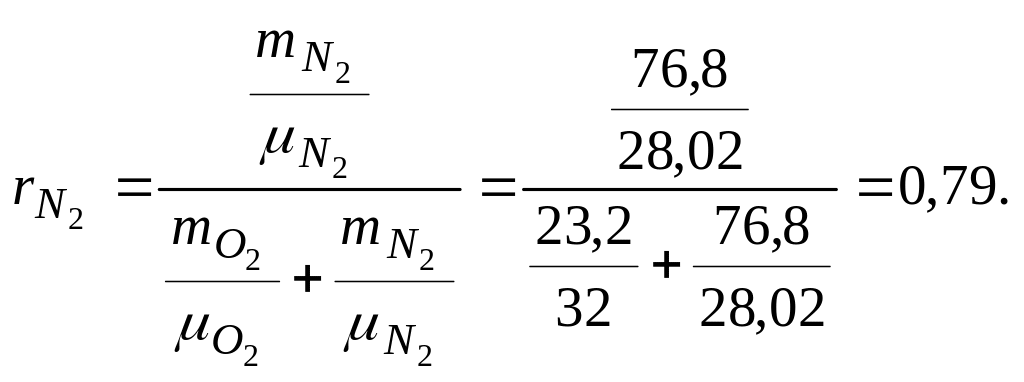
Газовую постоянную воздуха находим по уравнению
![]()
=0,232∙260+0,768∙295=287 Дж/(кг∙К).
Кажущуюся молекулярную массу смеси определяем из уравнения
![]()
=0,21∙32+0,79∙28,02=28,9,
или из уравнения
![]()
Отсюда
![]()
Парциальные давления получим из уравнения
рi=rip,
следовательно
рО2=rО2 p=0,21∙101325=21278 Па;
рN2=rN2 p=0,79∙101325=80047 Па.
