
- •Що таке еквівалентна електрична провідність?
- •Охарактеризуйте особливості коагуляції золів сумішами електролітів.
- •Що таке діаграма плавкості?
- •Що таке кінетична стійкість дисперсної системи?
- •Які властивості розчинів називають колігативними?
- •Що таке активні молекули?
- •Як можна виміряти електродний потенціал?
- •В чому полягає сутність методів хроматографічного аналізу?
- •Що таке буферна система?
- •Що таке гальванічний елемент?
- •Як орієнтуються молекули поверхнево-активної речовини в адсорбційному шарі?
- •В чому полягає суть методу потенціометричного титрування?
- •Сформулюйте закон Кольрауша, наведіть математичний вираз закону.
- •В чому полягає спільність та відмінність у властивостях розчинів високомолекулярних сполук та істинних розчинів; розчинів вмс та колоїдних розчинів?
- •Дайте визначення понять: фаза, компонент, ступінь свободи системи.
- •В чому полягає сутність методу кондуктометричного титрування?
-
В чому полягає спільність та відмінність у властивостях розчинів високомолекулярних сполук та істинних розчинів; розчинів вмс та колоїдних розчинів?
РОЗЧИНИ ВИСОКОМОЛЕКУЛЯРНИХ СПОЛУК — термодинамічно стійкі гомогенні зворотні системи, які утворюються спонтанно при змішуванні полімерів і низькомолекулярних рідин.
І́стинний ро́зчин — розчин, в якому частинки дисперсної фази представлені молекулами.
Колоїдні розчини — це високодисперсні двофазні системи, що складаються з дисперсійного середовища і дисперсної фази, причому лінійні розміри частинок останньої перебувають в межах від 1 до 100 нм.
Яке явище називають набрякання ВМС?
Однобічний процес проникнення молекул розчинника у фазу полімеру називається набуханням
Поясніть механізм набрякання.
При набуханні полімеру в умовах збереження сталого об’єму виникає тиск набухання, механізм виникнення якого подібний до механізму виникнення осмотичного тиску.
Що таке обмежене та необмежене набрякання?
Необмежене набухання — це набухання, яке спонтанно переходить у розчинення, при якому утворюється однофазна гомогенна система.
Обмеженим набуханням називається процес взаємодії полімеру з низькомолекулярною рідиною, обмежений стадією набухання.
Від яких факторів залежить ступінь набрякання?
Природа полумеру і розчинника , температура, розчинність полімеру
Як впливають електроліти на ступінь набрякання? (Ряди Гофмейстера).
Ряд іонiв, що розташованi в порядку пiдсилення чи послаблення їхнього впливу на властивостi розчинника (в'язкість, поверхневий натяг, розчинність i т. п.), а також на швидкiсть реакцiй у даному розчинниковi та iншi фiзико-хімiчнi процеси. Синонім — ряд Гофмейстера.
Білет 8
-
Дайте визначення понять: фаза, компонент, ступінь свободи системи.
Фаза - у фізичній хімії – однорідна складова частина фізико-хімічної системи, відмежована поверхнею розділу від інших частин цієї системи (напр., суміш льоду й води при 0°С являє собою фізико-хімічну систему, а окремо лід і вода – тверду й рідку її фази). Фаза - складова частина багатофазної системи, що відрізняється за своїм аґреґатним станом (газова, рідка, тверда фази).
Компонент — різновид, складова частина чогось.
Сту́пені ві́льності або ступені свободи — кількість незалежних змінних, які однозначно описують стан фізичної системи.
Назвіть умови фазових рівноваг.
Сформулюйте правило Гіббса та проаналізуйте його.
Прáвило фаз, або правило Гіббса — співвідношення, що пов'язує кількість різних речовин (компонентів), фаз і термодинамічних ступенів свободи у гетерогенній системі (у стані термодинамічної рівноваги). Цим правилом користуються для знаходження у певному пункті фазової діаграми найвищого значення кількості термодинамічних ступенів свободи.
Що таке діаграма стану системи?
Це діаграма яка показує в якому стані перебуває система
Який вигляд має діаграма стану води?
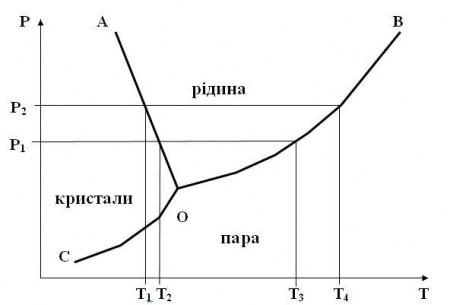
Застосуйте до неї правило фаз Гіббса.
Вода може перебувати в трьох фазах: у вигляді криги, рідини та (пари) газу. Стан, коли всі три фази співіснують, має
f=1-3+2=0
ступенів свободи. Тому на фазовій діаграмів він може позначатися лише одніїю точкою (це потрійна точка води).
Стан, коли співіснують 2 фази (наприклад, вода й газ) має
f=1-2+2=1
ступенів свободи, тобто зображається на фазовій діаграмі лінією. Справді, в залежності від тиску й температури вода й пара можуть існувати в різних співвідношеннях. Проте, при вибраній температурі тиск і співвідношення води в рідкому стані і парі у рівноважному стані фіксоване. Для заданого тиску існує єдина температура, при якій водяна пара над поверхнею рідини насичена (точка роси).
