
- •Оглавление
- •3. Химическая кинетика и равновесие
- •3.1 Скорость химических процессов
- •2.2 Химическое равновесие
- •4 Растворы электролитов
- •4.1 Концентрация растворов
- •4.2. Электролитическая диссоциация.
- •4.3. Гидролиз солей
- •5. Окислительно-восстановительные процессы.
- •5.1 Окислительно-восстановительные реакции
- •5.2 Гальванические элементы
- •5.3 Электрохимическая коррозия металлов
- •5.4 Электролиз растворов
- •6. Варианты заданий
- •620144, Г.Екатеринбург,ул.Куйбышева,30
4.2. Электролитическая диссоциация.
Ионно-молекулярные уравнения.
Электролитами называют вещества, растворы и расплавы которых проводят электрический ток. К электролитам относятся неорганические кислоты, основания, амфотерные гидроксиды и соли. Они распадаются в водных растворах и расплавах на катионы и анионы.
Процесс распада молекул электролитов на ионы в среде растворителя получил название электролитической диссоциации. Количественно диссоциация определяется степенью и константой диссоциации. Степень диссоциации – это число, показывающее какая часть молекул от общего их количества в растворе распадается на ионы:
=
![]()
По степени диссоциации электролиты условно разделяют на сильные ( ≈ 1) и слабые( < 1).
Сильные электролиты
К ним относятся минеральные кислоты: HNO3, H2SO4, HCl, HBr, HJ, HClO4; гидроксиды щелочных и щелочно-земельных металлов: LiOH, NaOH, KOH, Ba(OH)2 и др. ; соли – средние, кислые, основные – Fe2(SO4)3; NaHCO3; Al(OH)Cl2 и тп.
Сильные электролиты диссоциируют практически нацело:
Fe2(SO4)3 = 2Fe3+ + 3SO42-
HNO3 = H+ + NO3-
NaHCO3 = Na+ + HCO3-
Ba(OH)2 = Ba2+ + 2OH-
Слабые электролиты
К ним относятся кислоты: HNO2, H2CO3, H2S и др. а также все органические кислоты, в том числе уксусная CH3COOH; гидроксиды металлов основного характера Fe(OH)3, Cu(OH)2 и др. (кроме щелочных и щелочноземельных) и гидроксид аммония NH4OH, а также амфотерные гидроксиды Al(OH)3; Cr(OH)3; Zn(OH)2; Sn(OH)2 и др.
Для слабых электролитов диссоциация обратимый процесс, для которого справедливы общие законы равновесия. Например, для уксусной кислоты константа равновесия, называемая константой диссоциации имеет вид: CH3COOH ↔ CH3COO- + H+
Кд
=
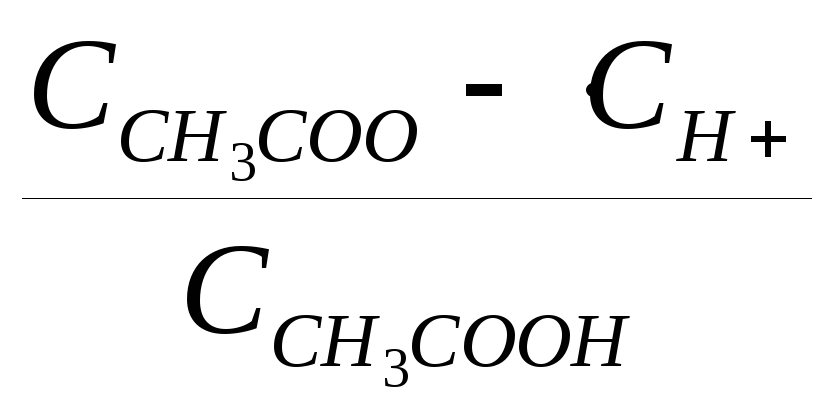
Многоосновные
кислоты и многокислотные основания
диссоциируют ступенчато, и каждую
ступень равновесного состояния
характеризует своя константа диссоциации
(причем К![]() всегда больше К
всегда больше К![]() и т.д.), например, при
и т.д.), например, при
диссоциации Н2S:
1-я ступень Н2S
↔ Н+
+ НS-
К![]() =
=![]() =
6∙10-8
=
6∙10-8
2- я ступень НS-
↔ Н+
+ S2-
К![]() =
=![]() =
1∙10-14,
=
1∙10-14,
где [ ] - равновесные концентрации ионов и молекул.
Диссоциация Сu(ОН)2:
1-я ступень Си(ОН)2 ↔ Си(ОН)+ + ОН-
2-я ступень Си(ОН)+ ↔ Си2+ + ОН-
Амфотерные гидроксиды, например Рb(ОН)2 диссоциируют по основному типу: Рb(ОН)2 ↔ РbОН+ + ОН-
РbОH+ ↔ Pb2+ + ОН-
и кислотному:
Н2РbО2 ↔ Н+ + НРbО2-
HPbO2- ↔ H+ + PbO22-
В растворах электролитов реакции протекают между ионами. Для записи ионных реакций применяют ионные уравнения. При составлении ионных уравнений реакций все слабые электролиты, газы и труднорастворимые электролиты записывают в молекулярной форме, все сильные электролиты (кроме труднорастворимых солей) в ионной форме. Примеры составления ионных уравнений реакций:
а) образование труднорастворимых соединений:
Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3
Cu2+ + 2NO3- + 2Na+ + 2OH- = Cu(OH)2 + 2Na+ + 2NO3-
Cu2+ + 2OH- = Cu(OH)2
б) образование газообразных веществ:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
2Na+ + CO32- + 2H+ + 2Cl- = 2Na+ + 2Cl- + H2O + CO2
CO32- + 2H+ = H2O + CO2
в) образование слабых электролитов:
CH3COONa + HNO3 = CH3COOH + NaNO3
CH3COO- + Na+ + H+ + NO3- = CH3COOH + Na+ + NO3-
CH3COO- + H+ = CH3COOH
Пример 1. Написать реакции для следующих превращений: KOH А KHSO3 В K2SO3
Решение:
А. KOH + H2SO3 = KHSO3 + H2O
K+ + OH- + H2SO3 = K+ + HSO3- + H2O
OH- + H2SO3 = HSO3- + H2O
В. KHSO3 + KOH = K2SO3 + H2O
K+ + HSO3- + K+ + OH- = 2K+ + SO32- + H2O
HSO3- + OH- = SO32- + H2O
Задания к разделу 4.2.
Задания 81-100. напишите для предложенных соединений уравнения диссоциации, а также в молекулярной и ионной формах уравнения возможных реакций взаимодействия их H2SO4 с и NaOH.
|
81. HCl; Cr(OH)3 |
91. Ca(OH)2; H3PO4 |
|
82. Cd(OH)2; H2S |
92. HNO3; Be(OH)2 |
|
83. Cu(OH)2; HBr |
93. H2Cr2O7; KOH |
|
84. H2SO3; Sn(OH)2 |
94. HCN; Ga(OH)3 |
|
85. H2SiO3; Pb(OH)2 |
95. KOH; H2CO3 |
|
86. CH3COOH; Fe(OH)3 |
96. HF; Be(OH)2 |
|
87. H2Se; Zn(OH)2 |
97. NH4OH; HClO4 |
|
88. Fe(OH)2; H3AsO3 |
98. Pb(OH)2; HNO2 |
|
89. LiOH; HJ |
99. Mg(OH)2; HClO |
|
90. H2Te; Al(OH)3 |
100. Ba(OH)2; HMnO4 |
Задания 101-120. Напишите в молекулярной и ионной формах уравнения реакций для следующих превращений:
101. Ni(OH)2 (NiOH)2SO4 NiSO4 Ni(OH)2
102. CuSO4 (CuOH)2SO4 Cu(OH)2 Cu(OH)NO3
103. Bi(NO3)3 Bi(OH)(NO3)2 Bi(OH)3 Bi2O3
104. Co(OH)2 Co(OH)Cl CoCl2 Co(NO3)2;
105. Pb(NO3)2 Pb(OH)NO3 Pb(OH)2 K2PbO2
106. NiCl2 Ni(OH)2 Ni(OH)Cl NiCl2
107. Cr(OH)Cl2 CrCl3 Cr(OH)3 Cr(OH)SO4
108. (SnOH)2SO4 SnSO4 Sn(OH)2 Na2SnO2;
109. NiBr2 Ni(OH)Br Ni(OH)2 NiSO4
110. CoSO4 Co(OH)2 (CoOH)2SO4 Co(NO3)2
111. Cr2(SO4)3 Cr(OH)SO4 Cr2(SO4)3 CrCl3;
112. NiSO4 (NiOH)2SO4 Ni(OH)2 NiBr2;
113. Fe(OH)SO4 Fe2(SO4)3 Fe(OH)3 FeCl3
114. Sn(OH)2 Sn(OH)Cl K2SnO2 Sn(OH)2
115. NiBr2 (NiOH)2 SO4 Ni(OH)2 NiBr2
116. Al(OH)3 Al(OH)2Cl AlCl3 Al(NO3)3;
117. CoCl2 Co(OH)2 (CoOH)2SO4 CoSO4,
118. Bi(OH)3 Bi(OH)2NO3 Bi(OH)3 Bi2O3
119. Cu(OH)2 Cu(OH)Cl CuCl2 Cu(NO3)2
120. CoSO4 (CoOH)2SO4 Co(OH)2 Co(NO3)2
